- Titelei
- Teil I
- Teil II
- Teil III
- Anhang

DR. PETER ATTIA hat Medizin an der Stanford-Universität studiert und als Chirurg am renommierten Johns-Hopkins-Krankenhaus in Baltimore gearbeitet. Er hat eine Weiterbildung zum onkologischen Chirurgen an den National Institutes of Health absolviert und dort zu Immuntherapien gegen Melanome geforscht. Er ist Gründer der digitalen Plattform »Early Medical«, bei der sich Patienten individuelle Maßnahmen zur Verlängerung ihrer Lebens- und Gesundheitsspanne maßschneidern lassen können. Attia hat den erfolgreichen Gesundheits-Podcast THE DRIVE ins Leben gerufen und ist ständiges Redaktionsmitglied der Zeitschrift AGING. Er lebt in Austin, Texas mit seiner Frau und drei Kindern.
Bill Gifford ist langjähriger Journalist und Autor. Seine Arbeiten erschienen in Magazinen wie SCIENTIFIC AMERICA und MEN‘S HEALTH.
DIE BIBEL FÜR EIN LANGES UND GESUNDES LEBEN
»Eines der wichtigsten Bücher, die Sie jemals lesen werden.«
STEVEN LEVITT, Bestsellerautor von FREAKONOMICS
»Peter Attia bündelt die neuesten wissenschaftlichen Erkenntnisse zum Thema Langlebigkeit und bietet Strategien, um ein langes und gesünderes Leben zu führen. Ein verblüffendes Buch – und ein Weckruf zum Handeln!«
DR. ANNE FLECK, Internistin und Bestsellerautorin von ENERGY! und ENERGY! in 5 Minuten
»Voller überraschender Einblicke in die Taktiken und Techniken, die uns helfen können, Krankheiten zu vermeiden und länger und bei besserer Gesundheit zu leben. Attias Texte sind bereichernd.«
SIDDHARTHA MUKHERJEE, Autor und Pulitzer-Preisträger von DER KÖNIG ALLER KRANKHEITEN
»OUTLIVE ist bereits jetzt DAS herausragende Standardwerk zum Thema Langlebigkeit – und wird es wohl die nächsten Jahre bleiben. Alles andere dazu sind Fußnoten.«
BAS KAST, Bestsellerautor von DER ERNÄHRUNGSKOMPASS und KOMPASS FÜR DIE SEELE
Peter Attia
OUTLIVE
Wie wir länger und besser leben können, als wir denken
Aus dem Amerikanischen
von Jorunn Wissmann, Susanne Warmuth und Martina Wiese
Ullstein
Besuchen Sie uns im Internet:
www.ullstein.de
© 2024 der deutschen Ausgabe: Ullstein Buchverlage GmbH, Berlin
© 2023 by Peter Attia
Alle Rechte vorbehalten
Wir behalten uns die Nutzung unserer Inhalte für Text und
Data Mining im Sinne von § 44b UrhG ausdrücklich vor.
Umschlaggestaltung: zero-media.net, München,
nach einer Vorlage von Rodrigo Corral Studio
Autorenfoto: © Early Medical
E-Book by pepyrus
ISBN 978-3-8437-3157-7
Upper: upped by @surgicalremnants
Das Hörbuch Version ist verfügbar bei Hoerbuch.us
Emojis werden bereitgestellt von openmoji.org unter der Lizenz CC BY-SA 4.0.
Auf einigen Lesegeräten erzeugt das Öffnen dieses E-Books in der aktuellen Formatversion EPUB3 einen Warnhinweis, der auf ein nicht unterstütztes Dateiformat hinweist und vor Darstellungs- und Systemfehlern warnt. Das Öffnen dieses E-Books stellt demgegenüber auf sämtlichen Lesegeräten keine Gefahr dar und ist unbedenklich. Bitte ignorieren Sie etwaige Warnhinweise und wenden sich bei Fragen vertrauensvoll an unseren Verlag! Wir wünschen viel Lesevergnügen.
Hinweis zu Urheberrechten
Sämtliche Inhalte dieses E-Books sind urheberrechtlich geschützt. Der Käufer erwirbt lediglich eine Lizenz für den persönlichen Gebrauch auf eigenen Endgeräten. Urheberrechtsverstöße schaden den Autoren und ihren Werken, deshalb ist die Weiterverbreitung, Vervielfältigung oder öffentliche Wiedergabe ausdrücklich untersagt und kann zivil- und/oder strafrechtliche Folgen haben.
In diesem E-Book befinden sich Verlinkungen zu Webseiten Dritter. Bitte haben Sie Verständnis dafür, dass sich die Ullstein Buchverlage GmbH die Inhalte Dritter nicht zu eigen macht, für die Inhalte nicht verantwortlich ist und keine Haftung übernimmt.
Inhalt
Kapitel 3
Ziel, Strategie, Taktik
Von evidenzbasiert zu evidenzinformiert
Kapitel 5
Weniger essen, länger leben?
Wie lässt sich das kardiovaskuläre Risiko senken?
Kapitel 8
Zellen außer Kontrolle
Der Stoffwechsel von Krebszellen
Die Verheißung der Immuntherapie
Kapitel 9
Die Jagd nach Erinnerungen
Was genau ist die Alzheimerkrankheit?
Kann man neurodegenerativen Erkrankungen vorbeugen?
Der Zehnkampf der Hundertjährigen
Maximale aerobe Leistung: VO2max
Kapitel 13
Das Hohelied der Stabilität
Was Sport bewirken kann: Barry
Das Wenige, was wir über die Biochemie der Ernährung wissen (und wie wir dazu kamen)
Kapitel 15
Die Biochemie der Ernährung in die Praxis umsetzen
DR: Diät à la Biochemie der Ernährung
TR: Argumente für (und gegen) Fasten
Schlaf und Herz-Kreislauf-Erkrankungen
Wie können wir unseren Schlaf bewerten?
Anhang
Anmerkung
Die in diesem Buch enthaltenen Informationen und Ratschläge ersparen keine Beratung durch einen kompetenten Facharzt. Alle die Gesundheit betreffenden Fragen sollen grundsätzlich mit einem Arzt besprochen werden. Autor und Verlag übernehmen keine Verantwortung für Verluste oder Schädigungen, die angeblich durch Informationen oder Empfehlungen aus diesem Buch entstanden sind.
Widmung
Für meine Patienten.
Und für Jill, Olivia, Reese und Ayrton – für eure Geduld.
Vorbemerkung des Autors
Ein populärwissenschaftliches Buch mit medizinischen Inhalten zu schreiben erfordert eine Gratwanderung zwischen Kürze und Detail, Genauigkeit und Lesbarkeit. Ich habe mein Bestes gegeben, um die optimale Balance zu finden, die Fakten korrekt darzustellen und zugleich die Zusammenhänge einem Laienpublikum zugänglich zu machen. Sie entscheiden, ob mir das gelungen ist.
Einleitung
Im Traum versuche ich, die fallenden Eier aufzufangen.
In einer großen, schmutzigen Stadt, die Baltimore ziemlich ähnlich sieht, stehe ich mit einem ausgepolsterten Korb in den Händen auf einem Bürgersteig und schaue nach oben. Alle paar Sekunden entdecke ich hoch über mir ein Ei, das Richtung Boden heruntersaust, und renne los, um es mit dem Korb aufzufangen.
Die Eier regnen auf mich herunter, und ich gebe alles, um sie zu erwischen, laufe hierhin und dorthin, während ich den Korb wie einen Baseballhandschuh den Eiern entgegenrecke. Aber ich kann sie nicht alle fangen. Einige – eine Menge – klatschen auf den Boden, und Eigelb spritzt mir auf die Schuhe und den Arztkittel. Verzweifelt hoffe ich, dass es endlich aufhört.
Woher kommen die Eier? Da oben auf dem Dach des Gebäudes oder auf einem Balkon muss irgendjemand stehen und sie zum Zeitvertreib über das Geländer werfen. Aber ich kann die Person nicht sehen und bin so im Stress, dass ich gar nicht dazu komme, weiter darüber nachzudenken. Ich renne bloß hin und her und versuche, so viele Eier wie möglich zu fangen. Und scheitere kläglich. Die Gefühle drohen mich zu übermannen, als mir klar wird, dass ich sie unmöglich alle erwischen kann, sosehr ich mich auch anstrenge. Ich fühle mich komplett überfordert und hilflos.
Und dann wache ich auf, und wieder ist die Chance auf kostbaren Schlaf dahin.
Wir vergessen fast alle unsere Träume, aber dieser scheint mich auch nach zwanzig Jahren immer noch nicht loszulassen. Während ich am Johns Hopkins Hospital Assistenzarzt in der Krebschirurgie war, hat er mich viele Male heimgesucht. Die Zeit damals war eine der besten meines Lebens, auch wenn ich manchmal das Gefühl hatte durchzudrehen. Für meine Kollegen und mich war es nicht ungewöhnlich, vierundzwanzig Stunden am Stück durchzuarbeiten. Ich lechzte nach Schlaf. Der Traum machte ihn immer wieder zunichte.
Die Oberärzte der Chirurgie am Hopkins waren auf schwierige Fälle wie Bauchspeicheldrüsenkrebs spezialisiert, was bedeutete, dass wir sehr häufig die einzigen Menschen waren, die die Patienten noch vor dem Tod bewahren konnten. Bauchspeicheldrüsenkrebs wächst symptomfrei im Stillen, und wenn man ihn entdeckt, ist er oft schon weit fortgeschritten. Eine Operation kam nur für etwa 20 bis 30 Prozent der Patienten infrage. Wir waren ihre letzte Hoffnung.
Im Kampf gegen den Krebs führten wir häufig die sogenannte Whipple-Operation durch, wobei der Pankreaskopf, also der obere Teil der Bauchspeicheldrüse, sowie der erste Abschnitt des Dünndarms, der Zwölffingerdarm, entfernt werden. Dieser schwierige und gefährliche Eingriff verlief zu Beginn fast immer tödlich. Trotzdem wagten sich Chirurgen an die Operation, was die Brisanz dieser Krebserkrankung unterstreicht. Zur Zeit meiner Ausbildung überlebten über 99 Prozent der Patienten den Eingriff für mindestens 30 Tage. Wir waren beim Eierfangen also schon ziemlich erfolgreich.
Damals war ich entschlossen, als Krebschirurg so gut zu werden, wie es nur ging. Ich hatte sehr hart gearbeitet, um so weit zu kommen. Die meisten meiner Lehrer an der Highschool und sogar meine Eltern hatten mir die Zulassung zum College nicht zugetraut und einen erfolgreichen Abschluss an der Stanford Medical School noch viel weniger. Doch nun fühlte ich mich zunehmend hin- und hergerissen. Einerseits liebte ich diese komplexen Operationen, und nach einem erfolgreichen Eingriff war ich immer in Hochstimmung. Wir hatten den Tumor entfernt – das Ei gefangen –, wenigstens glaubten wir das.
Andererseits fragte ich mich plötzlich, was diesen »Erfolg« ausmachte. In der Realität sah es so aus, dass diese Patienten trotzdem fast alle nach wenigen Jahren starben.[1] Das Ei würde unweigerlich am Boden zerschellen. Was erreichten wir also wirklich?
Als ich schließlich erkannte, wie fruchtlos dies alles war, frustrierte mich das dermaßen, dass ich die Medizin an den Nagel hängte und einen völlig anderen Beruf ergriff. Aber dann trafen mehrere Ereignisse zusammen, die bewirkten, dass ich komplett anders über Gesundheit und Krankheit dachte. Und so wandte ich mich mit einer neuen Herangehensweise und wiedererwachter Hoffnung erneut der Medizin zu.
Einen bedeutenden Anteil daran hatte mein Traum von den fallenden Eiern. Kurz gesagt: Mir dämmerte schließlich, dass sich das Problem nicht lösen ließ, indem man beim Fangen der Eier besser wurde. Vielmehr mussten wir versuchen, den Kerl aufzuhalten, der sie hinunterwarf. Wir mussten herausbekommen, wie man auf das Dach des Gebäudes gelangte, den Typ finden und ihn unschädlich machen.
Im wirklichen Leben hätte ich das liebend gern getan; als Boxer in jungen Jahren war mein linker Haken durchaus berüchtigt. Aber offensichtlich ist die Medizin ein wenig komplizierter als das. Letztlich erkannte ich, dass wir an die Sache – die fallenden Eier – ganz anders herangehen mussten, mit einer anderen Einstellung und anderen Werkzeugen.
Um genau das, ganz knapp gesagt, geht es in diesem Buch.
Teil I
Kapitel 1
Das lange Spiel
Vom schnellen Tod zum langsamen Sterben
Irgendwann müssen wir aufhören, Menschen einfach nur aus dem Fluss zu ziehen. Wir müssen flussaufwärts gehen und herausfinden, warum sie hineinfallen.
Bischof Desmond Tutu
Ich werde nie vergessen, wie ich zum ersten Mal eine Patientin sterben sah. Es war zu Beginn des zweiten Jahres meines Medizinstudiums. An einem Samstagabend war ich zum Hospitieren ins Krankenhaus gegangen, was uns von der Hochschule empfohlen wurde. Wir durften aber nur zusehen, weil wir damals gerade genug wussten, um die Patienten in Gefahr zu bringen.
Irgendwann kam eine Frau Mitte dreißig in die Notaufnahme, die über Kurzatmigkeit klagte. Sie stammte aus der Kleinstadt East Palo Alto, die im Gegensatz zum äußerst wohlhabenden Palo Alto von Armut geprägt ist. Während die Krankenschwestern sie ans EKG anschlossen und ihr eine Sauerstoffmaske anlegten, saß ich neben ihr und versuchte sie mit etwas Small-Talk abzulenken. Wie heißen Sie? Haben Sie Kinder? Wie lange haben Sie diese Symptome?
Ganz plötzlich verzerrte sich ihr Gesicht vor Angst, und sie begann nach Luft zu schnappen. Dann verdrehte sie die Augen und verlor das Bewusstsein.
Innerhalb von Sekunden wimmelte der Raum von Pflegepersonal und Ärzten, die ein Routineprogramm abspulten – sie führten einen Atemschlauch in die Luftröhre ein und pumpten die Frau in einem letzten verzweifelten Versuch, sie wiederzubeleben, mit hochwirksamen Medikamenten voll. Gleichzeitig begann ein Assistenzarzt mit einer Herzdruckmassage. Alle paar Minuten drückte ein Oberarzt Defibrillator-Paddles an ihren Brustkorb, und ihr Körper zuckte unter den heftigen Elektroschocks. Alles folgte einer präzisen Choreografie – jeder wusste, was zu tun war.
Ich zog mich in eine Ecke zurück, um niemandem im Weg zu stehen, doch der Assistenzarzt, der die Herzdruckmassage durchführte, fing meinen Blick auf und sagte: »Hey, kannst du mal herkommen und mich ablösen? Drück einfach genauso kräftig und im selben Rhythmus wie ich gerade, okay?«
Und so führte ich zum ersten Mal in meinem Leben eine Herzdruckmassage nicht an einer Puppe, sondern an einem Menschen durch. Doch es half alles nichts. Sie starb dort auf dem Tisch, während ich in rhythmischen Abständen auf ihren Brustkorb drückte. Wenige Minuten zuvor hatte ich sie noch nach ihrer Familie gefragt! Eine Krankenschwester zog das Laken über ihr Gesicht, und alle verschwanden so schnell, wie sie gekommen waren.
Die anderen hatten so etwas schon öfter erlebt, aber ich war entsetzt und zutiefst erschüttert. Was um alles in der Welt war da gerade passiert?
Ich sollte noch sehr viele Menschen sterben sehen, aber der Tod jener Frau verfolgte mich jahrelang. Wie ich heute vermute, starb sie wahrscheinlich an einer schweren Lungenembolie, doch immer wieder fragte ich mich, woran sie eigentlich gelitten hatte. Was war geschehen, bevor sie in die Notaufnahme kam? Und wäre alles anders gelaufen, wenn sie einen besseren Zugang zu ärztlicher Betreuung gehabt hätte? Hätte sich ihr trauriges Schicksal abwenden lassen?
Später, als Assistenzarzt am Johns Hopkins Hospital, lernte ich, dass der Tod auf zwei Arten kommt – schnell oder langsam. In den Straßen der Innenstadt von Baltimore regierte der schnelle Tod mit Schusswaffen, Messern und durch Raser verursachten Autounfällen. Es klingt vielleicht pervers, aber die in der Stadt herrschende Gewalt war ein wichtiger »Gegenstand« des Medizinstudiums. Ich hatte mich zwar für Hopkins entschieden, weil es einen ausgezeichneten Ruf für Leber- und Bauchspeicheldrüsenkrebs-OPs hatte, aber dass jeden Tag im Durchschnitt über zehn Fälle mit penetrierenden Traumata, meist Schuss- oder Stichverletzungen, eingeliefert wurden, hatte zur Folge, dass meine Kollegen und ich reichlich Gelegenheit hatten, unsere chirurgischen Fähigkeiten beim Flicken von Körpern zu trainieren, die allzu oft jung, arm, schwarz und männlich waren.
Während die Nächte von Patienten mit Verletzungen bestimmt wurden, ging es tagsüber um Patienten mit Gefäß- oder Magen-Darm-Krankheiten und vor allem Krebserkrankungen. Der Unterschied bestand darin, dass die »Wunden« dieser Menschen von langsam wachsenden, lange unentdeckt gebliebenen Tumoren verursacht wurden und auch nicht alle von ihnen überlebten – nicht einmal die Wohlhabenden, die von der Sonnenseite des Lebens. Krebs kümmert es nicht, wie reich wir sind. Nicht einmal, wer uns operiert. Wenn er dich töten will, wird es ihm gelingen. Letzten Endes belastete mich dieses langsame Sterben noch mehr als der schnelle Tod.
Doch dies ist kein Buch über den Tod. Eigentlich sogar das Gegenteil.
Mehr als fünfundzwanzig Jahre nachdem jene Frau in die Notaufnahme kam, bin ich immer noch praktizierender Arzt, aber ganz anders, als ich es mir vorgestellt hatte. Ich führe keine Krebsoperationen oder andere Eingriffe mehr durch. Wenn Sie mit einem Ausschlag oder einem gebrochenen Arm zu mir kommen, werde ich Ihnen vermutlich nicht allzu viel helfen können.
Was also mache ich?
Gute Frage. Würden Sie mir diese Frage auf einer Party stellen, so würde ich wahrscheinlich versuchen, mich davonzustehlen. Oder ich würde lügen und behaupten, ich sei Autorennfahrer, was ich tatsächlich werden möchte, wenn ich erwachsen bin. (Plan B: Schäfer.)
Mein Fokus als Arzt liegt auf Langlebigkeit. Das Problem ist nur, dass ich das Wort Langlebigkeit hasse. Es hat unter einer jahrhundertelangen Parade von Quacksalbern und Scharlatanen gelitten, die angeblich im Besitz eines geheimen Elixiers für ein längeres Leben waren. Mit diesen Leuten möchte ich nicht in Verbindung gebracht werden, und ich bin nicht so arrogant zu glauben, dass ich ein simples Rezept gegen dieses Problem hätte, über das sich die Menschheit bereits seit Jahrtausenden den Kopf zerbricht. Wäre es einfach, lange zu leben, dann bräuchte es dieses Buch nicht.
Beginnen wir mit dem, was Langlebigkeit nicht ist. Langlebigkeit bedeutet nicht, ewig zu leben. Nicht einmal, hundertzwanzig oder hundertfünfzig Jahre alt zu werden, was heutzutage einige selbst ernannte Experten ihren Anhängern routinemäßig versprechen. Sofern nicht irgendein revolutionärer Durchbruch erfolgt, der auf irgendeine Weise zwei Milliarden Jahre Evolutionsgeschichte ungeschehen macht und den gnadenlosen Pfeil der Zeit umkehrt, wird buchstäblich alles, was heute lebt, unweigerlich sterben. Es ist eine Einbahnstraße.
Ebenso wenig bedeutet Langlebigkeit, einfach nur einen Geburtstag nach dem anderen abzuhaken, während wir langsam dahinwelken. So widerfuhr es in der griechischen Mythologie dem unglückseligen Tithonos, für den Eos, die Göttin der Morgenröte, den Göttervater um ewiges Leben bat. Zu ihrer Freude gewährte er ihrem Liebhaber diese Bitte. Doch weil sie vergessen hatte, zugleich um ewige Jugend zu bitten, verfiel sein Körper mehr und mehr. Dumm gelaufen.
Die meisten meiner Patienten verstehen das intuitiv. Wenn sie das erste Mal zu mir kommen, erklären sie üblicherweise nachdrücklich, dass sie nicht länger leben wollen, wenn das bedeutet, dass sich ihre Gesundheit zugleich immer weiter verschlechtert. Viele haben miterlebt, dass es ihren Eltern oder Großeltern so ergangen ist – sie lebten zwar noch, aber körperliche Schwäche oder Demenz schränkten sie massiv ein. Dieses Schicksal möchten sich meine Patienten ersparen. Aber dann erkläre ich ihnen: Nur weil unsere Eltern im Alter leiden mussten oder früher starben als gedacht, muss es uns nicht genauso ergehen. Die Vergangenheit gibt nicht zwangsläufig die Zukunft vor. Unsere Langlebigkeit ist formbarer, als wir glauben.
Im Jahr 1900 betrug die Lebenserwartung etwa fünfzig Jahre, und die meisten Menschen starben meist »schnell« – an Unfällen, Verletzungen und verschiedenen Infektionskrankheiten.[2] Seitdem verdrängt das langsame Sterben nach und nach den schnellen Tod. Von den Personen, die dieses Buch lesen, werden die meisten vermutlich in den Siebzigern oder Achtzigern sterben und fast alle »langsam«. Vorausgesetzt, dass Sie nicht einer hochriskanten Beschäftigung wie Base-Jumping oder Motorradrennen nachgehen oder am Steuer Textnachrichten schreiben, stehen die Chancen ausgesprochen gut, dass Sie einer der chronischen Alterskrankheiten erliegen, die ich die vier apokalyptischen Reiter des Alterns nenne: Herz-Kreislauf-Erkrankungen, Krebs, neurodegenerative Erkrankungen oder Typ-2-Diabetes und damit einhergehende Stoffwechselstörungen. Für wahre Langlebigkeit – länger zu leben und länger besser zu leben – müssen wir diese Ursachen eines langsamen Sterbens verstehen und angehen.
Langlebigkeit hat zwei Komponenten. Die erste betrifft unsere chronologische Gesamtlebenszeit – wie lange wir leben –, doch die zweite und genauso wichtige betrifft die Qualität unserer Lebensjahre – wie gut wir leben. Letztere bezeichnen wir als gesunde Lebenszeit. Diese hatte Eos bei ihrem Bittgesuch für Tithonos vergessen. Die gesunde Lebenszeit wird gemeinhin als derjenige Lebensabschnitt definiert, in dem wir frei von Beeinträchtigung oder Krankheit sind, doch das finde ich zu stark vereinfacht. Ich bin heute genauso frei von »Beeinträchtigung und Krankheit« wie als fünfundzwanzigjähriger Medizinstudent, aber mein früheres Ich könnte mein jetziges etwa fünfzigjähriges Ich sowohl körperlich als auch geistig locker in die Tasche stecken. Das ist halt so. Der zweite Teil unseres Plans für Langlebigkeit besteht also darin, unsere körperlichen und geistigen Funktionen aufrechtzuerhalten und zu verbessern.
Die entscheidende Frage lautet: Wohin bin ich unterwegs? Wie sieht mein zukünftiger Weg aus? Schon in mittleren Jahren gibt es zahlreiche Warnsignale. Ich war bereits auf der Beerdigung von Schulfreunden, was mir den steilen Anstieg des Sterberisikos ab dem mittleren Alter vor Augen führt. Gleichzeitig erleben viele mit dreißig, vierzig oder fünfzig, wie ihre Eltern zunehmend von körperlichen Beeinträchtigungen, Demenz oder langwierigen Krankheiten beeinträchtigt werden. Das mit anzusehen ist immer traurig und bekräftigt einen meiner wichtigsten Grundsätze: Wir können uns nur dann eine bessere Zukunft schaffen und auf einen besseren Weg begeben, wenn wir uns ab sofort Gedanken darüber machen und jetzt aktiv werden.
Eines der größten Hindernisse auf der Suche nach Langlebigkeit ist die Tatsache, dass die Fertigkeiten, die meine Kollegen und ich während des Medizinstudiums erworben haben, den schnellen Tod sehr viel besser bekämpfen als langsames Sterben. Wir haben gelernt, gebrochene Knochen zu heilen, Entzündungen mit hochwirksamen Antibiotika den Garaus zu machen, geschädigte Organe zu unterstützen oder gar zu ersetzen und schwerwiegende Rückenmarks- oder Hirnverletzungen erfolgreich zu behandeln. Wir haben eine erstaunliche Fähigkeit entwickelt, Leben zu retten und beschädigten Körpern ihre volle Funktionsfähigkeit zurückzugeben, ja sogar Patienten, die fast tot waren, wiederzubeleben. Deutlich weniger erfolgreich waren wir jedoch dabei, unseren Patienten bei chronischen Leiden wie Krebs, Herz-Kreislauf-Erkrankungen oder neurologischen Krankheiten zu helfen, dem langsamen Sterben zu entgehen. Wir können ihre Symptome lindern und das Ende häufig kurzfristig hinauszögern, aber es sieht nicht so aus, als könnten wir die Uhr zurückdrehen, so wie es uns bei akuten Problemen gelingt. Beim Fangen der Eier sind wir besser geworden, aber nach wie vor fallen sie vom Dach.
Das Problem besteht darin, dass wir bei beiden Arten von Patienten – Menschen mit Traumata und Menschen mit chronischen Krankheiten – im Grunde den gleichen Ansatz verfolgen. Unsere Aufgabe war schon immer, den Patienten nicht sterben zu lassen, koste es, was es wolle. Mir ist vor allem ein Fall im Gedächtnis geblieben – ein vierzehnjähriger Junge, der eines Nachts dem Tode nah in die Notfallambulanz gebracht wurde. Ein Autofahrer hatte mit halsbrecherischem Tempo eine rote Ampel überfahren und den Honda, in dem der Junge saß, seitlich gerammt. Seine Vitalparameter waren schwach, seine Pupillen starr und geweitet, was auf ein schweres Hirntrauma schließen ließ. Als Leiter der Unfallchirurgie begann ich sofort mit den routinemäßigen Wiederbelebungsmaßnahmen, aber genau wie bei der Frau in der Notaufnahme in Stanford half alles nichts. Meine Kollegen bedeuteten mir aufzuhören, aber ich weigerte mich stur, ihn für tot zu erklären. Ich spulte weiter die Routineabläufe ab und pumpte Adrenalin und literweise Blut in seinen leblosen Körper, weil ich nicht akzeptieren wollte, dass das Leben eines unschuldigen Jungen auf diese Weise zu Ende ging. Später stand ich schluchzend im Treppenhaus und wünschte, ich hätte ihn retten können. Doch schon bei seiner Einlieferung war sein Schicksal besiegelt gewesen.
Dieses Berufsethos wird allen Medizinstudenten eingebläut: Niemand stirbt unter meiner Aufsicht. Die Behandlung unserer Krebspatienten gingen wir genauso an. Sehr oft war jedoch klar, dass wir zu spät hinzugezogen wurden, weil die Krankheit schon so weit fortgeschritten war, dass sich der Tod kaum noch abwenden ließ. So wie bei dem Jungen taten wir trotzdem alles, was in unserer Macht stand, um das Leben der Patienten zu verlängern, und unterzogen sie bis ganz zum Ende toxischen und oft qualvollen Behandlungen, um bestenfalls noch ein paar Wochen oder Monate Lebenszeit herauszuschinden.
Das Problem ist nicht, dass wir es nicht versuchen würden. Die moderne Medizin hat unglaublich viele Anstrengungen und Ressourcen in den Kampf gegen jede einzelne dieser Krankheiten gesteckt. Die Fortschritte sind jedoch alles andere als hervorragend. Die einzige Ausnahme sind vielleicht Herz-Kreislauf-Erkrankungen, bei denen die Sterblichkeitsrate in den Industrieländern im Lauf von rund sechzig Jahren um zwei Drittel gesenkt werden konnte (obwohl auch da noch immer einiges zu tun ist, wie wir sehen werden).[3] Dagegen ist die Sterberate bei Krebs in den mehr als fünfzig Jahren, seitdem Präsident Richard Nixon dem Krebs mit der Initiative »War on Cancer« buchstäblich den Krieg erklärte, kaum zurückgegangen.[4] Und das, obwohl Hunderte Milliarden Dollar öffentlicher und privater Spenden in die Forschung geflossen sind. Typ-2-Diabetes ist nach wie vor eine sehr ernste Bedrohung für das Gesundheitswesen, ohne irgendein Anzeichen abzuflauen, und Alzheimer sowie ähnliche neurodegenerative Erkrankungen suchen die prozentual zunehmende ältere Bevölkerung heim, wobei praktisch keine wirksame Behandlung in Sicht ist.
Auf jeden Fall greifen wir jeweils zum falschen Zeitpunkt ein, nämlich erst, nachdem die Krankheit weit fortgeschritten ist, und häufig, wenn schon nichts mehr hilft – wenn die Eier bereits herunterfallen. Mir drehte sich jedes Mal der Magen um, wenn ich einem Krebspatienten eröffnen musste, dass er nur noch sechs Monate zu leben habe, und wusste, dass sich die Krankheit wahrscheinlich schon mehrere Jahre, bevor sie überhaupt zu diagnostizieren war, im Körper eingenistet hatte. Wir hatten eine Menge Zeit vergeudet. Die Häufigkeit, mit der die apokalyptischen Reiter uns heimsuchen, nimmt im Alter zwar sprunghaft zu, doch üblicherweise entwickeln sich diese Krankheiten viel früher, als uns bewusst ist, und meistens dauert es sehr lange, bis sie zum Tode führen. Selbst wenn jemand »plötzlich« an einem Herzinfarkt stirbt, wurden die Herzkranzgefäße vermutlich schon über zwei Jahrzehnte hinweg fortschreitend geschädigt. Das langsame Sterben vollzieht sich sogar noch langsamer, als wir bemerken.
Daraus folgt der logische Schluss, dass wir früher einschreiten müssen, um den apokalyptischen Reitern Einhalt zu gebieten – oder, noch besser, sie gar nicht in unsere Nähe kommen zu lassen. Keine unserer Behandlungen von Lungenkrebs im Spätstadium hat die Sterberate auch nur annähernd so stark gesenkt wie der weltweite Rückgang des Rauchens im Verlauf der letzten zwanzig Jahre, was auch den weitverbreiteten Rauchverboten zu verdanken ist. Diese einfache präventive Maßnahme (nicht zu rauchen) hat mehr Leben gerettet als alle medizinischen Interventionen im Spätstadium. Trotzdem beharrt die Mainstream-Medizin darauf, eine Diagnose abzuwarten, bevor sie eingreift.
Typ-2-Diabetes ist ein Paradebeispiel. Die von der American Diabetes Association festgelegten Richtlinien der Regelversorgung sehen vor, dass bei einem Patienten Diabetes mellitus diagnostiziert wird, wenn er einen Hämoglobin-A1c-Wert (oder HbA1c-Wert)[5] von 6,5 Prozent oder höher aufweist, was einem durchschnittlichen Blutzuckerniveau von 140 mg/dl entspricht (normal wären eher 100 mg/dl oder ein HbA1c-Wert von 5,1 Prozent). Diese Patienten werden dann einer ausführlichen Behandlung unterzogen, unter anderem mit Medikamenten, die den Körper bei der Produktion von Insulin unterstützen, Medikamenten, die die Menge der vom Körper produzierten Glucose reduzieren, und schließlich direkt mit dem Hormon Insulin, um Glucose aus der Blutzirkulation heraus- und in ihre hochgradig insulinresistenten Körperzellen hineinzutransportieren.
Wenn aber der HbA1c-Test einen Wert von 6,4 Prozent aufweist, impliziert das einen durchschnittlichen Blutzuckerspiegel von 137 mg/dl – nur drei Punkte weniger –, was bedeutet, dass sie technisch betrachtet überhaupt keinen Typ-2-Diabetes haben. Stattdessen spricht man von Prädiabetes, wogegen die Richtlinien der Regelversorgung leichte sportliche Betätigung empfehlen sowie schwammig definierte Ernährungsumstellungen, die optionale Einnahme eines Wirkstoffs zur Glucose-Hemmung namens Metformin und »jährliche Kontrolluntersuchungen« – was im Grunde heißt, man soll abwarten, ob der Patient tatsächlich Diabetes entwickelt, bevor man ihn sodann dringend einer Behandlung unterzieht.
Ich würde behaupten, dass dies praktisch genau diejenige Vorgehensweise ist, die man zur Bekämpfung von Typ-2-Diabetes nicht verfolgen sollte. Wie wir in Kapitel 6 sehen werden, gehört Typ-2-Diabetes in ein Spektrum von Stoffwechselstörungen, die einsetzen, lange bevor jene magische Bluttestschwelle überschritten wird. Typ-2-Diabetes ist lediglich der Endpunkt der Strecke. Einschreiten sollte man bereits viel früher, wenn sich der Patient noch längst nicht in der Gefahrenzone befindet; selbst Prädiabetes kommt in diesem Prozess erst sehr spät ins Spiel. Es ist absurd und gefährlich, diese Erkrankung wie eine Erkältung oder Knochenbrüche zu behandeln, die man entweder hat oder nicht hat. Hier gibt es kein Entweder-oder. Doch allzu häufig beginnen die ärztlichen Interventionen erst mit der klinischen Diagnose. Warum wird das so hingenommen?
Ich glaube, dass wir anstreben sollten, so früh wie möglich einzuschreiten. Wir sollten versuchen, es gar nicht so weit kommen zu lassen, dass Menschen Typ-2-Diabetes und die anderen apokalyptischen Reiter entwickeln. Unsere Herangehensweise sollte nicht reaktiv, sondern proaktiv sein. Um langsames Sterben zu bekämpfen, müssen wir als Erstes unsere Einstellung ändern. Wir wollen diese Erkrankungen verzögern oder verhindern, sodass wir länger ohne Krankheiten leben können, statt mit Krankheiten dahinzuvegetieren. Das bedeutet: Bevor die Eier anfangen herunterzufallen, ist der beste Zeitpunkt, um einzugreifen – wie ich es auch in meinem eigenen Leben erfahren habe.
Am 8. September 2009, einem Tag, den ich nie vergessen werde, stand ich am Strand von Catalina Island, als meine Frau Jill plötzlich zu mir sagte: »Peter, ich finde, du solltest dich bemühen, etwas weniger vollschlank zu werden.«
Ich war so geschockt, dass ich beinahe meinen Cheeseburger fallen ließ. »Etwas weniger vollschlank zu werden?« Das hatte meine geliebte Frau gesagt?
Ich war durchaus der Meinung, dass ich den Burger und auch die Cola in meiner anderen Hand verdient hatte. Schließlich war ich soeben von Los Angeles aus zu dieser Insel rübergeschwommen – 34 Kilometer gegen die Strömung übers offene Meer, was 14 Stunden gedauert hatte. Noch vor einer Minute war ich darüber begeistert gewesen, diese Langstrecke erfolgreich von meiner Bucketlist streichen zu können.[6] Und auf einmal sollte ich ein kleines bisschen abnehmen!
Trotzdem wusste ich im gleichen Moment, dass Jill recht hatte. Ohne es wirklich zu registrieren, brachte ich mittlerweile stolze 210 Pfund auf die Waage, stramme 50 Pfund über meinem Kampfgewicht als jugendlicher Boxer. Wie so viele Männer in mittleren Jahren hielt ich mich nach wie vor für »athletisch«, auch wenn ich mich abmühen musste, meinen Körper in zu enge Hosen zu zwängen. Auf Fotos von damals ähnelt mein Bauch auffallend dem von Jill, als sie im sechsten Monat schwanger war. Ich hatte einen echten Dad Bod – eine prächtige Birnensilhouette – entwickelt und war noch nicht einmal vierzig.
Bluttests offenbarten größere Probleme, als ich im Spiegel sehen konnte. Obwohl ich exzessiv Sport trieb und mich meiner Meinung nach gesund ernährte (vom Cheeseburger nach dem Langstreckenschwimmen mal abgesehen), hatte ich eine Insulinresistenz entwickelt. Das war einer der ersten Schritte auf dem Weg zu Typ-2-Diabetes und vielen anderen schlimmen Dingen. Mein Testosteronlevel lag für einen Mann in meinem Alter unter dem 5. Perzentil. Es ist nicht übertrieben zu behaupten, dass mein Leben in Gefahr war – nicht unmittelbar, aber zweifellos auf längere Sicht. Ich wusste genau, wohin mich das führen konnte. Ich hatte die Füße von Menschen amputiert, die zwanzig Jahre zuvor so ausgesehen hatten wie ich. Noch bedrohlicher war, dass es in meiner eigenen Familie zahlreiche Männer gab, die in den Vierzigern an Herz-Kreislauf-Erkrankungen gestorben waren.
In diesem Moment am Strand erwachte mein Interesse an, ja, Langlebigkeit. Ich war sechsunddreißig und stand am Abgrund. Gerade erst war ich mit der Geburt unseres ersten Kindes, Olivia, Vater geworden. Als ich sie zum ersten Mal in ihrem weißen Wickeltuch im Arm hielt, verliebte ich mich auf der Stelle und wusste, dass mein Leben sich für immer verändert hatte. Doch bald erkannte ich, dass ich dank verschiedener Risikofaktoren und meiner Gene unter Umständen früh an einer Herz-Kreislauf-Krankheit sterben könnte. Was ich noch nicht begriff, war, dass sich dieses Problem restlos aus der Welt schaffen ließ.
Als ich mich in die wissenschaftliche Literatur vertiefte, wollte ich schon bald mit der gleichen Leidenschaft wie früher, als ich Krebschirurgie gelernt hatte, alles über Ernährung und Stoffwechselvorgänge erfahren. Weil meine Neugier schon immer unersättlich war, wandte ich mich an die führenden Experten in diesen Bereichen und überredete sie, meinen Wissensdurst zu stillen. Ich wollte verstehen, wie ich mich in diesen Zustand manövriert hatte und was das für meine Zukunft bedeutete. Und ich musste herausfinden, wie ich mich wieder auf Spur bringen konnte.
Meine nächste Aufgabe bestand darin, alles über die Natur und Ursachen von Atherosklerose oder Herz-Kreislauf-Erkrankungen herauszufinden, wovon die Männer in der Familie meines Vaters heimgesucht werden. Zwei von seinen Brüdern waren an einem Herzinfarkt gestorben, bevor sie fünfzig wurden, und einen dritten hatte der Tod in seinen Sechzigern ereilt. Das nächste naheliegende Thema war Krebs, der mich schon immer fasziniert hat, und danach kamen neurodegenerative Erkrankungen wie Alzheimer an die Reihe. Zum Schluss widmete ich mich dem sich rasant entwickelnden Feld der Gerontologie, die zu ergründen versucht, was den Alterungsprozess an sich antreibt und wie man ihn verlangsamen könnte.
Die wichtigste Erkenntnis war möglicherweise, dass die moderne Medizin nicht wirklich weiß, wann und wie sie die chronischen Alterskrankheiten in den Griff bekommen soll, denen wahrscheinlich die meisten Menschen in den Industrieländern zum Opfer fallen werden. Das liegt zum Teil daran, dass alle vier apokalyptischen Reiter komplexe Angelegenheiten sind – eher Krankheitsprozesse als akute Erkrankungen wie eine Erkältung. Überraschenderweise ist das gewissermaßen eine gute Nachricht. Jeder Reiter ist das Produkt mehrerer Risikofaktoren, die sich mit der Zeit addieren und anhäufen. Viele dieser Risikofaktoren sind für sich genommen jedoch leicht einzudämmen oder sogar zu eliminieren. Noch besser ist, dass sie bestimmte Merkmale oder Auslöser teilen, denen man allesamt mit einigen der Taktiken und Verhaltensänderungen, die wir in diesem Buch erörtern, beikommen kann.
Der größte Fehler der Medizin ist zu versuchen, alle diese Erkrankungen am falschen Ende der Zeitskala zu bekämpfen – sie wartet, bis sie sich eingenistet haben, statt es gar nicht erst so weit kommen zu lassen. Demzufolge ignorieren wir wichtige Warnsignale und verpassen die Gelegenheit, zu einem Zeitpunkt einzuschreiten, an dem wir noch die Chance haben, die Krankheiten abzuwehren, gesünder zu werden und die Gesamtlebenszeit vielleicht zu verlängern.
Hier sind einige Beispiele:
Statt Milliarden Dollar in die Erforschung der apokalyptischen Reiter zu stecken, verfolgt die Mainstream-Medizin völlig falsche Ansätze, um gegen die eigentlichen Ursachen vorzugehen. Wir werden einige vielversprechende neue Theorien über Ursprung und Ursachen der einzelnen Krankheiten sowie mögliche präventive Strategien untersuchen.
Die typische Auflistung Ihrer Cholesterinwerte, die Ihnen Ihr Arzt beim Gesundheitscheck mitteilt und erklärt, sowie zahlreiche Annahmen, die ihr zugrunde liegen (z. B. »gutes« und »schlechtes« Cholesterin), sind irreführend und zu stark vereinfacht, wenn nicht gar komplett nutzlos. Die Werte sagen so gut wie nichts über Ihr tatsächliches Risiko aus, an einer Herz-Kreislauf-Erkrankung zu sterben – und wir tun so gut wie nichts dafür, um diesen Killer zu stoppen.
Millionen Menschen leiden an einem kaum bekannten und zu selten diagnostizierten Leberleiden, das möglicherweise Typ-2-Diabetes vorausgeht. Trotzdem erhält man bei Personen in einem Frühstadium dieser Stoffwechselstörung häufig Blutwerte im »Normalbereich«. Doch leider sind »normale« oder »durchschnittliche« Werte in der ungesunden heutigen Zeit nicht gleichbedeutend mit »optimal«.
Die Stoffwechselstörung, die zu Typ-2-Diabetes führt, befördert auch Herz-Kreislauf-Erkrankungen, Krebs und Alzheimer. Wenn wir uns um einen gesunden Stoffwechsel bemühen, senkt dies auch das Risiko, an einem der apokalyptischen Reiter zu erkranken.
Fast alle »Diäten« ähneln einander: Manchen Menschen können sie helfen, aber bei den meisten erweisen sie sich als nutzlos. Statt über Diäten zu diskutieren, werden wir unser Augenmerk auf die Biochemie der Ernährung richten – wie sich die Kombination der Nährstoffe, die wir zu uns nehmen, auf unseren Stoffwechsel und unsere Physiologie auswirkt und wie wir aus Daten und Technologie das für uns optimale Ernährungsmuster herausfiltern können.
Ein spezieller Makronährstoff verdient mehr Aufmerksamkeit, als man gemeinhin vermutet: Nicht die Kohlenhydrate, nicht Fette, sondern Proteine gewinnen mit zunehmendem Alter entscheidend an Bedeutung.
Sportliche Betätigung ist das bei Weitem wirkungsvollste »Medikament«, um länger gesund zu leben. Mit keiner anderen Maßnahme tun wir auch nur annähernd so viel dafür, unsere Gesamtlebenszeit zu verlängern und unsere geistigen und körperlichen Funktionen in Schuss zu halten. Die meisten Menschen tun jedoch bei Weitem nicht genug – und auf die falsche Art Sport zu treiben kann mehr schaden als nützen.
Und schließlich musste ich mühsam lernen, dass das Ringen um körperliche Gesundheit und Langlebigkeit sinnlos ist, wenn wir unsere seelische Gesundheit vernachlässigen. Seelischer Schmerz kann unsere Gesundheit an allen Enden beeinträchtigen und muss behandelt werden.
Warum braucht die Welt noch ein weiteres Buch über Langlebigkeit? In den letzten Jahren habe ich mir diese Frage oft gestellt. Die meisten Autoren in diesem Themenbereich lassen sich in bestimmte Kategorien einteilen. Es gibt die wahren Gläubigen, die darauf beharren, dass man dem Tod ein Schnippchen schlagen und ewig leben kann, wenn man ihre ganz spezielle Diät befolgt (je restriktiver, desto besser) oder auf eine bestimmte Weise meditiert oder eine bestimmte Art von Superfood zu sich nimmt oder seine »Energie« auf die richtige Weise fließen lässt. Was sie an wissenschaftlicher Genauigkeit vermissen lassen, machen sie mit ihrer Leidenschaft wieder wett.
Am anderen Ende des Spektrums befinden sich diejenigen, die davon überzeugt sind, dass die Wissenschaft bald herausfinden wird, wie der Alterungsprozess an sich gestoppt werden kann, indem man irgendeinen mysteriösen zellulären Wirkmechanismus justiert, unsere Telomere verlängert oder unsere Zellen »umprogrammiert«, sodass wir gar nicht mehr altern müssen. Zu unseren Lebzeiten wird das höchstwahrscheinlich nicht mehr passieren, obwohl die Wissenschaft zweifellos Quantensprünge machen wird, was unser Verständnis des Alterungsprozesses und der apokalyptischen Reiter betrifft. Wir entdecken so vieles, aber kompliziert wird es, wenn es darum geht, wie wir dieses neu entdeckte Wissen außerhalb des Labors auf echte Menschen anwenden – oder zumindest, wie wir uns für den Fall absichern, dass diese hochtrabenden Forschungen doch daran scheitern, die Langlebigkeit in eine Pille zu gießen.
Meine eigene Rolle dabei sehe ich folgendermaßen: Ich bin weder Laborwissenschaftler noch klinischer Forscher, sondern vielmehr eine Art Übersetzer, der Ihnen beim Verstehen und Anwenden dieser Erkenntnisse helfen möchte. Dies erfordert ein gründliches Durchdringen der Wissenschaft, aber auch ein künstlerisches Geschick, so als würden wir ein Gedicht von Shakespeare in eine andere Sprache übertragen. Wir müssen die Bedeutung der Worte richtig vermitteln (die Wissenschaft) und zugleich den Ton, die Nuancen, das Gefühl und den Rhythmus erfassen (die Kunst). Entsprechend gründet mein Ansatz für Langlebigkeit fest auf wissenschaftlichen Erkenntnissen, doch es ist auch ein gut Teil Kunstfertigkeit gefragt, um Ihnen, den Patienten, mit Ihren ganz individuellen Genen, Ihrer Geschichte sowie Ihren Gewohnheiten und Zielen, das erforderliche Wissen auf die richtige Weise zum richtigen Zeitpunkt nahezubringen.
Ich glaube, dass wir schon heute mehr als genug wissen, um entscheidend voranzukommen. Aus diesem Grund heißt dieses Buch Outlive.[7] Darunter verstehe ich hier sowohl »länger leben« als auch »besser leben«. Im Gegensatz zu Tithonos können Sie Ihre Lebenserwartung verlängern und sich zugleich einer besseren Gesundheit erfreuen, womit Sie im doppelten Sinne mehr vom Leben haben.
Ich möchte Ihnen eine praktizierbare Gebrauchsanweisung für Langlebigkeit an die Hand geben – einen Führer, der Ihnen hilft, länger besser zu leben. Ich hoffe, Sie überzeugen zu können, dass Sie mit ausreichend Zeit und Mühe Ihre Gesamtlebenszeit um ein Jahrzehnt und Ihre gesunde Lebenszeit vielleicht um zwei Jahrzehnte erweitern können, sodass Sie sich bestenfalls so fit wie jemand fühlen, der zwanzig Jahre jünger ist als Sie.
Allerdings werde ich Ihnen nicht haarklein erzählen, was Sie zu tun haben. Ich möchte Ihnen nahebringen, wie Sie über diese Dinge denken sollten. Für mich war dies eine Reise, ein leidenschaftlicher Prozess des Lernens und geduldigen Übens, der an jenem Tag an der felsigen Küste von Catalina Island begann.
Im weiteren Sinne erfordert Langlebigkeit einen Paradigmenwechsel im medizinischen Ansatz, der den Fokus auf die Vorbeugung von chronischen Krankheiten legt und unsere gesunde Lebenszeit optimiert. Und wir sollten sofort aktiv werden und nicht warten, bis wir krank werden oder unsere geistigen und körperlichen Funktionen bereits merklich nachgelassen haben. Dies ist keine »präventive«, sondern proaktive Medizin. Ich glaube, sie hat das Potenzial, nicht nur das Leben Einzelner zu verändern, sondern unserer ganzen Gesellschaft enorm viel Leid und Leiden zu ersparen. Zudem geht dieser Wandel nicht vom medizinischen Establishment aus. Er wird sich nur dann vollziehen, wenn Patienten und Ärzte ihn gleichermaßen fordern.
Nur wenn wir anders an die Medizin herangehen, gelangen wir auf das Dach des Gebäudes, um zu verhindern, dass die Eier herunterfallen. Niemand sollte sich damit zufriedengeben, auf der Straße herumzurennen und zu versuchen, sie aufzufangen.
Kapitel 2
Medizin 3.0
Ein neuer Denkansatz für Medizin im Zeitalter chronischer Krankheiten
Man sollte das Dach reparieren, solange die Sonne scheint.
John F. Kennedy
Ich weiß nicht mehr, was der letzte Tropfen war, der das Fass meiner zunehmenden Frustration über das Medizinstudium zum Überlaufen brachte, aber ich weiß sehr wohl, dass der Anfang vom Ende mit dem Medikament Gentamicin zusammenhing. Gegen Ende des zweiten Jahres meiner Facharztausbildung lag ein Patient mit einer schweren Sepsis bei mir auf der Intensivstation. Im Grunde hielt ihn nur noch dieses Medikament, ein starkes Antibiotikum, am Leben. Gentamicin hat ein sehr enges therapeutisches Fenster, was die Sache verkompliziert. Gibt man dem Patienten zu wenig, hat es keine Wirkung, aber gibt man ihm zu viel, könnten Nieren und Gehör dauerhaft geschädigt werden. Die Dosierung hängt vom Gewicht des Patienten und der erwarteten Halbwertszeit des Wirkstoffs im Körper ab. Weil ich ein kleiner Mathefreak bin (genauer gesagt, nicht nur ein kleiner), entwickelte ich ein mathematisches Modell, das den genauen Zeitpunkt vorhersagte, wann dieser Patient seine nächste Dosis brauchen würde: um vier Uhr dreißig.
Als wir den Patienten um vier Uhr dreißig überprüften, stellte sich tatsächlich heraus, dass der Gentamicinspiegel im Blut auf exakt den Wert gefallen war, der eine weitere Dosis erforderlich machte. Ich bat die Krankenschwester, ihm das Medikament zu verabreichen, doch eine Kollegin, die sich ebenfalls noch in der Ausbildung befand, aber in der Klinik-Hackordnung eine Stufe über mir stand, widersprach. »Das würde ich nicht machen«, sagte sie. »Warten wir lieber bis zum Schichtwechsel um sieben Uhr.« Das verstand ich nicht – wir wussten, dass der Patient dann noch über zwei Stunden praktisch schutzlos einer massiven Infektion ausgeliefert wäre, die ihn töten konnte. Warum warten? Als die Kollegin gegangen war, wies ich die Schwester an, dem Patienten das Medikament trotzdem zu geben.
Später bei der Visite stellte ich den Patienten der behandelnden Ärztin vor und erläuterte, was ich getan hatte und warum. Ich glaubte, sie würde meine ärztliche Fürsorge – die richtige Dosierung des Medikaments – gutheißen, aber stattdessen hielt sie mir eine Standpauke, wie ich sie noch nie erlebt hatte. Ich war zwar seit mehr als 24 Stunden auf den Beinen, aber das war keine Halluzination. Sie schrie mich an und drohte sogar mit fristloser Entlassung, weil ich versucht hatte, den Zeitpunkt der Medikamentengabe für einen schwer kranken Patienten zu optimieren. Es stimmte, dass ich den Hinweis (keine direkte Anweisung) der Kollegin, meiner unmittelbaren Vorgesetzten, missachtet hatte und dass das nicht korrekt gewesen war, aber diese Tirade schockierte mich. Sollten wir uns nicht immer bemühen, Dinge zu verbessern?
Letztlich schluckte ich meinen Stolz hinunter und entschuldigte mich für meinen Ungehorsam. Das war aber nur ein Vorfall unter vielen. Im weiteren Verlauf meiner Facharztausbildung wuchsen die Zweifel, ob ich mich für den richtigen Beruf entschieden hatte. Immer wieder fanden meine Kollegen und ich uns im Konflikt mit einer Kultur, die sich gegen Wandel und Innovation sträubte. Dass Medizin an sich konservativ ist, hat natürlich gute Gründe. Doch mitunter hatte es den Anschein, als sei das gesamte Gefüge der modernen Medizin so stark in seinen Traditionen verwurzelt, dass es nicht in der Lage war, sich auch nur geringfügig zu verändern – selbst wenn es um Möglichkeiten ging, das Leben von Menschen zu retten, für deren Wohlergehen wir doch sorgen sollten.
Im fünften Jahr, gequält von Zweifeln und Frustration, teilte ich meinen Vorgesetzten mit, dass ich meine Ausbildung im Juni abbrechen würde. Meine Kollegen und Mentoren hielten mich für verrückt. Kaum jemand bricht die Facharztausbildung ab – schon gar nicht am Johns Hopkins Hospital, wenn man nur noch zwei Jahre vor sich hat. Aber mein Entschluss stand fest. Nach neun Jahren Medizinstudium für nichts und wieder nichts – so schien es wenigstens – trat ich eine Stelle bei der renommierten Unternehmensberatung McKinsey & Company an. Meine Frau und ich zogen quer durch die USA in die noble Gegend von Palo Alto und San Francisco, wo ich mich während meiner Zeit an der Stanford University so wohlgefühlt hatte. Nun war ich so weit von der Medizin (und Baltimore) entfernt, wie es nur ging, und ich war froh. Ich hatte das Gefühl, ein Jahrzehnt meines Lebens vergeudet zu haben. Doch letzten Endes führte dieser scheinbare Umweg dazu, dass sich mein Blick auf die Medizin – und, noch wichtiger, auf jeden einzelnen Patienten – grundlegend veränderte.
Wie sich herausstellte, lautete das Schlüsselwort Risiko.
Ursprünglich hatte mich McKinsey für Beratung in der Gesundheitsfürsorge vorgesehen, doch weil ich mich auch mit quantitativen Themen beschäftigt hatte (ich hatte Angewandte Mathematik und Maschinenbau studiert, weil ich in Luft- und Raumfahrttechnik promovieren wollte), steckten sie mich in die Abteilung Kreditrisiko. Das war 2006, als sich bereits die Weltfinanzkrise anbahnte, doch abgesehen von den Protagonisten in Michael Lewis’ Roman The Big Short hatte kaum jemand eine Ahnung von der Tragweite dessen, was da kommen sollte.
Wir sollten US-Banken mit einem neuen Regelwerk vertraut machen, das sie befolgen sollten, um genügend Reserven zur Deckung unerwarteter Verluste zu bilden. Beim Einschätzen ihrer erwarteten Verluste hatten die Banken einen guten Job gemacht, aber niemand wusste so richtig, wie mit den unerwarteten Verlusten umzugehen sei, die per definitionem sehr viel schwerer zu prognostizieren waren. Unsere Aufgabe bestand darin, die internen Daten der Banken zu analysieren und mathematische Modelle zur Vorhersage dieser unerwarteten Verluste auf Basis von Korrelationen zwischen Anlageklassen zu erstellen. Das war genauso kompliziert, wie es klingt – gewissermaßen ein blind abgefeuerter Schuss ins Blaue.
Was zunächst wie eine Hilfestellung für die größten US-Banken beim Überwinden einiger regulatorischer Hürden ausgesehen hatte, brachte zutage, dass sich eine Katastrophe rund um eine ihrer scheinbar sichersten und solidesten Geschäftsbereiche zusammenbraute: Prime-Hypotheken[8]. Gegen Ende des Sommers von 2007 gelangten wir zu dem erschreckenden, aber unausweichlichen Schluss, dass die Großbanken in den beiden kommenden Jahren durch Hypothekendarlehen mehr Geld verlieren würden, als sie in der letzten Dekade verdient hatten.
Ende 2007, nachdem wir sechs Monate rund um die Uhr gearbeitet hatten, fand ein Meeting mit den hohen Tieren unseres Kunden, einer großen US-Bank, statt. Normalerweise hätte mein Chef als Leiter des Projekts die Präsentation übernommen, doch stattdessen fiel seine Wahl auf mich. »Mit Blick auf Ihren bisherigen Werdegang«, sagte er, »gehe ich davon aus, dass Sie besser dazu geeignet sind, jemandem eine Horrornachricht zu überbringen.«
Tatsächlich war es fast so, als müsste ich einem Patienten mitteilen, dass er nicht mehr lange zu leben hatte. Ich stand in einem Tagungsraum der Chefetage und erläuterte der Geschäftsführung die Zahlen, die ihren Untergang prophezeiten. Im Laufe meiner Präsentation beobachtete ich, wie in den Gesichtern der Manager die fünf Phasen der Trauer aufschienen, die Elisabeth Kübler-Ross in ihrem Klassiker Interviews mit Sterbenden beschrieben hat: Nichtwahrhabenwollen, Zorn, Verhandeln, Depression, Zustimmung. Das hatte ich außerhalb einer Klinik noch nie erlebt.
Mein Abstecher in die Welt der Unternehmensberatung war bald wieder vorbei, aber er führte mir einen großen blinden Fleck der Medizin vor Augen – die Risikoeinschätzung. In der Finanz- und Bankenwelt ist es lebenswichtig, Risiken einschätzen zu können. Bedeutende Investoren gehen niemals unbedacht ein Risiko ein; sie informieren sich gründlich über mögliche Gefahren und Gewinne. Die Beschäftigung mit Kreditrisiken ist eine Wissenschaft, wenn auch eine unvollkommene, wie die Banken mich lehrten. In der Medizin sind Risiken offenkundig ebenfalls von Bedeutung, aber die Ärzteschaft geht an das Thema eher emotional als analytisch heran.
Der Ärger begann mit Hippokrates. Die meisten Leute kennen den Grundsatz des alten Griechen »Vor allem schade nicht«.[9] Er beschreibt prägnant die wichtigste Verantwortung des Arztes, die Patienten nicht zu töten oder irgendetwas zu tun, was ihr Befinden verschlechtert, statt es zu verbessern. Klingt plausibel. Doch da gibt es drei Probleme: (a) Hippokrates hat das nie so gesagt,[10] (b) es ist scheinheiliger Mist, und (c) in vielerlei Hinsicht ist es nicht hilfreich.
»Schade nicht«? Ernsthaft? Zahlreiche Behandlungen, die unsere medizinischen Vorgänger von Hippokrates’ Zeiten bis ins 20. Jahrhundert hinein ihren Patienten angedeihen ließen, waren weit eher angetan, ihnen zu schaden, als zu heilen. Haben Sie Kopfweh? Dann käme für Sie eine Trepanation infrage, wobei Ihnen ein Loch in den Schädel gebohrt wird. Merkwürdige wunde Stellen an den Geschlechtsteilen? Versuchen Sie bitte das Schreien zu unterdrücken, während der Doktor der Naturwissenschaft Ihre Genitalien mit giftigem Quecksilber betupft. Und dann gab es natürlich noch das seit Jahrtausenden bewährte Heilverfahren des Aderlasses, das gewöhnlich das Allerletzte war, was eine kranke oder verwundete Person benötigte.
Was mich an »Vor allem schade nicht« aber am meisten ärgert, ist die stillschweigende Voraussetzung, dass die beste Behandlung stets diejenige mit dem geringsten unmittelbaren Verlustrisiko ist – was sehr oft bedeutet, überhaupt nichts zu tun. Jeder Arzt, der seine Approbationsurkunde wert ist, kann mit einer Geschichte aufwarten, die diesen Unsinn widerlegt. Hier ist meine: Bei einem meiner letzten Trauma-Fälle als Assistenzarzt wurde ein siebzehnjähriger Junge eingeliefert. Er hatte eine Stichwunde im Oberbauch, direkt unterhalb des Schwertfortsatzes, dem kurzen knöchern-knorpeligen unteren Ende des Brustbeins. Als er hereingerollt wurde, schien er stabil zu sein, aber plötzlich zeigte er ein auffälliges Verhalten und bekam große Angst. Eine schnelle Ultraschalluntersuchung zeigte, dass sich in seinem Herzbeutel, dem Sack aus festem Bindegewebe, der das Herz umgibt, möglicherweise ein Erguss gebildet hatte. Mit einem Mal lag ein kritischer Notfall vor, denn wenn sich dort zu viel Flüssigkeit ansammelte, käme es zum Herzstillstand, der ihn innerhalb von ein oder zwei Minuten töten würde.
Es war keine Zeit mehr, ihn hinauf in den OP zu bringen – es war gut möglich, dass er die Fahrt im Aufzug nicht überleben würde. Als er das Bewusstsein verlor, musste ich in Sekundenschnelle eine Entscheidung treffen. Ich öffnete an Ort und Stelle seinen Brustkorb und schlitzte den Herzbeutel auf, um den Druck auf das Herz zu verringern. Es war stressig und blutig, aber es funktionierte, und kurz darauf hatten sich seine Vitalparameter wieder stabilisiert. Der Eingriff war zweifellos hochriskant gewesen und hatte ihm kurzfristig großen Schaden zugefügt, aber wenn ich es nicht getan hätte, wäre er beim Warten auf eine sicherere und sterilere Operation im OP vielleicht gestorben. Der schnelle Tod wartet auf niemanden.
Dieser dramatische Eingriff war nötig gewesen, weil das Risiko so asymmetrisch war: Nichts zu tun – um einen »Schaden« zu vermeiden – hätte vermutlich zu seinem Tod geführt. Umgekehrt war das hastige Öffnen des Brustkorbs, selbst wenn meine Diagnose falsch gewesen wäre, keineswegs lebensgefährlich, auch wenn man sich für einen Mittwochabend wahrscheinlich etwas anderes wünscht. Nachdem die akute Gefahr gebannt war, stellte sich heraus, dass die Spitze des Messers ganz leicht die Lungenarterie angeritzt hatte – eine kleine Wunde, die mit zwei Stichen vernäht wurde, nachdem er stabilisiert und in den OP gebracht worden war. Nach vier Übernachtungen konnte er nach Hause.
Risiken sollte man nicht um jeden Preis vermeiden. Wir müssen sie vielmehr verstehen, analysieren und mit ihnen arbeiten. Alles, was wir tun, sei es in der Medizin oder im täglichen Leben, beruht auf dem Abwägen von Risiken und Belohnungen. Haben Sie zum Mittagessen einen abgepackten Salat gegessen? Dann besteht eine geringe Wahrscheinlichkeit, dass sich im Grünzeug E. coli-Bakterien befanden. Sind Sie mit dem Auto zum Supermarkt gefahren? Ebenfalls riskant. Doch unter dem Strich ist der Salat vermutlich gut für Sie (oder zumindest nicht so schlecht wie andere Dinge, die Sie essen könnten).
Manchmal, wie bei dem Siebzehnjährigen mit der Stichwunde, muss man den Sprung ins Ungewisse wagen. In anderen, weniger akuten Situationen hat man vielleicht die Wahl, bei einem Patienten eine Darmspiegelung durchzuführen, bei der ein kleines, aber reales Verletzungsrisiko besteht, oder die Untersuchung zu unterlassen und dabei möglicherweise eine Krebserkrankung zu übersehen. Damit will ich sagen: Ein Arzt, der seinen Patienten noch nie irgendeinen Schaden zugefügt hat oder zumindest das Risiko einer Schädigung eingegangen ist, hat wahrscheinlich auch nicht viel unternommen, um ihnen zu helfen. Und in Fällen wie bei besagtem Teenager kann Nichtstun auch die riskanteste Entscheidung von allen bedeuten.
Eigentlich hätte ich es gut gefunden, wenn Hippokrates bei der Operation an dem Jungen mit der Stichwunde zugesehen hätte – oder bei einem beliebigen anderen Eingriff in einem modernen Krankenhaus. Alles hätte ihn umgehauen – von den Präzisionsinstrumenten aus Stahl über Antibiotika und Anästhesie bis zum hellen elektrischen Licht.
Es stimmt zwar, dass wir der Antike eine Menge verdanken – zum Beispiel die 20 000 meist aus dem Lateinischen oder Griechischen stammenden Wörter, die ich im Medizinstudium gepaukt habe. Dennoch ist die Vorstellung eines kontinuierlichen Fortschritts von der Zeit des Hippokrates bis in die Gegenwart eine Fiktion. Für mich sieht es so aus, als habe es in der Medizingeschichte zwei getrennte Zeitalter gegeben und wir ständen heute am Beginn eines dritten Zeitalters.
Die erste Ära, für die Hippokrates steht, die aber nach seinem Tod fast zweitausend Jahre angedauert hat, nenne ich Medizin 1.0. Ihre Schlussfolgerungen beruhten auf direkter Beobachtung, und ärztlicher Beistand stützte sich mehr oder weniger auf pure Vermutungen, die zum Teil ins Schwarze trafen, zum Teil aber auch nicht. So befürwortete Hippokrates Wandern als sportliche Betätigung und befand, dass »in Nahrung vorzügliche Medizin zu finden ist und in Nahrung schlechte Medizin zu finden ist«, was nach wie vor Gültigkeit hat. Für manches aus Medizin 1.0 trifft dies jedoch ganz und gar nicht zu, wie die Lehre von den »Körpersäften«, um nur ein Beispiel von vielen zu nennen. Hippokrates’ bedeutendste Leistung war die Erkenntnis, dass Krankheiten natürliche Ursachen haben und den Menschen nicht von den Göttern auferlegt werden, wie man vorher geglaubt hatte. Allein das war ein großer Schritt in die richtige Richtung. Mit ihm und seinen Zeitgenossen darf man daher nicht allzu kritisch ins Gericht gehen. Ohne Kenntnis von Naturwissenschaft oder der wissenschaftlichen Methode taten sie das Beste, was sie konnten. Man kann kein Werkzeug benutzen, das noch nicht erfunden wurde.
Die Ära der Medizin 2.0 brach Mitte des 19. Jahrhunderts mit dem Aufkommen der Keimtheorie zur Erklärung von Krankheitsursachen an, die an die Stelle der Idee trat, dass die meisten Krankheiten von »Miasmen«, giftigen Ausdünstungen, hervorgerufen werden. Das führte zu verbesserten Hygienemaßnahmen bei ärztlichen Behandlungen und letztlich zur Entwicklung von Antibiotika. Das heißt aber keineswegs, dass ein klarer Schnitt erfolgte – es war nicht so, dass Louis Pasteur, Joseph Lister und Robert Koch ihre bahnbrechenden Studien veröffentlichten[11] und sich die gesamte Ärzteschaft ihnen sogleich anschloss und über Nacht völlig anders praktizierte. Tatsächlich war der Übergang von Medizin 1.0 zu Medizin 2.0 ein langer, blutiger Gewaltmarsch, der sich durch vielerorts ausgetragene Grabenkämpfe gegen den Widerstand des Establishments auszeichnete.
Nehmen wir den Fall des armen Ignaz Semmelweis, eines ungarisch-österreichischen Chirurgen und Geburtshelfers, der mit Sorge beobachtete, dass so viele Mütter, die im Krankenhaus entbanden, am »Kindbettfieber« starben. Er kam zu dem Schluss, dass dies mit den Autopsien zusammenhing, die er und seine Kollegen morgens vornahmen, bevor sie am Nachmittag Geburtshilfe leisteten – ohne sich zwischendurch gründlich die Hände zu waschen. Obwohl die Existenz von Keimen noch nicht belegt war, glaubte Semmelweis, dass die Ärzte irgendetwas auf die Frauen übertrugen, was sie krank machte. Seine Beobachtungen stießen auf strikte Ablehnung. Semmelweis wurde von seinen Kollegen geächtet und starb 1865 in einer Irrenanstalt.
Genau im selben Jahr demonstrierte Joseph Lister erstmals erfolgreich das Prinzip der antiseptischen Chirurgie, indem er bei der Operation eines Jungen in einem Krankenhaus in Glasgow ein Sterilisierungsverfahren anwendete. Das war der erste praktische Nachweis, dass Krankheiten durch Keime verursacht werden können. Semmelweis hatte die ganze Zeit recht gehabt.
Der Übergang von Medizin 1.0 zu Medizin 2.0 wurde teilweise durch neue Technologien wie das Mikroskop angestoßen, aber der wichtigste Faktor war eine neue Denkweise. Die Grundlage dafür war schon um 1620 gelegt worden, als Sir Francis Bacon als Erster darlegte, was wir heute als die wissenschaftliche, oder empirische, Methode kennen. Dies markierte einen bedeutenden philosophischen Wandel, von Beobachten und Raten zum Beobachten und anschließendem Bilden einer Hypothese, auch wenn das, wie Richard Feynman hervorhob, im Grunde nur eine vornehme Bezeichnung für Raten ist.
Der nächste Schritt ist entscheidend: Man führt ein Experiment durch, um festzustellen, ob die Hypothese bzw. Vermutung zutrifft. Statt auf Behandlungen zurückzugreifen, von denen sie annahmen, dass sie wirkten – obwohl auch oft genug Gegenbeweise vorlagen –, konnten Forscher und Ärzte nun mögliche Heilverfahren systematisch testen und bewerten und sich anschließend für diejenigen entscheiden, die sich in Experimenten am besten bewährt hatten. Dennoch vergingen zweieinhalb Jahrhunderte zwischen Bacons Essay und der Entdeckung von Penicillin, die den letzten und entscheidenden Wendepunkt hin zu Medizin 2.0 markierte.
Medizin 2.0 war revolutionär. Sie ist ein bestimmendes Merkmal unserer Zivilisation, eine wissenschaftliche Kriegsmaschine, die tödliche Krankheiten wie die Pocken und zwei Typen von Polio ausgerottet hat. Ihre Erfolge setzten sich in den 1990er- und 2000er-Jahren mit der Eindämmung von HIV/Aids fort. Was eine Seuche zu sein schien, die die gesamte Menschheit bedrohte, wurde zu einer beherrschbaren chronischen Krankheit. Auch die seit Kurzem mögliche Heilung von Hepatitis C würde ich hier nennen wollen. Ich weiß noch, dass man uns im Medizinstudium erklärte, Hepatitis C werde eine unkontrollierbare Epidemie auslösen, die innerhalb von fünfundzwanzig Jahren die Infrastruktur für Lebertransplantationen in den USA völlig überfordern werde. Heute lassen sich die meisten Fälle durch eine kurze Behandlung mit (allerdings sehr teuren) Medikamenten heilen.
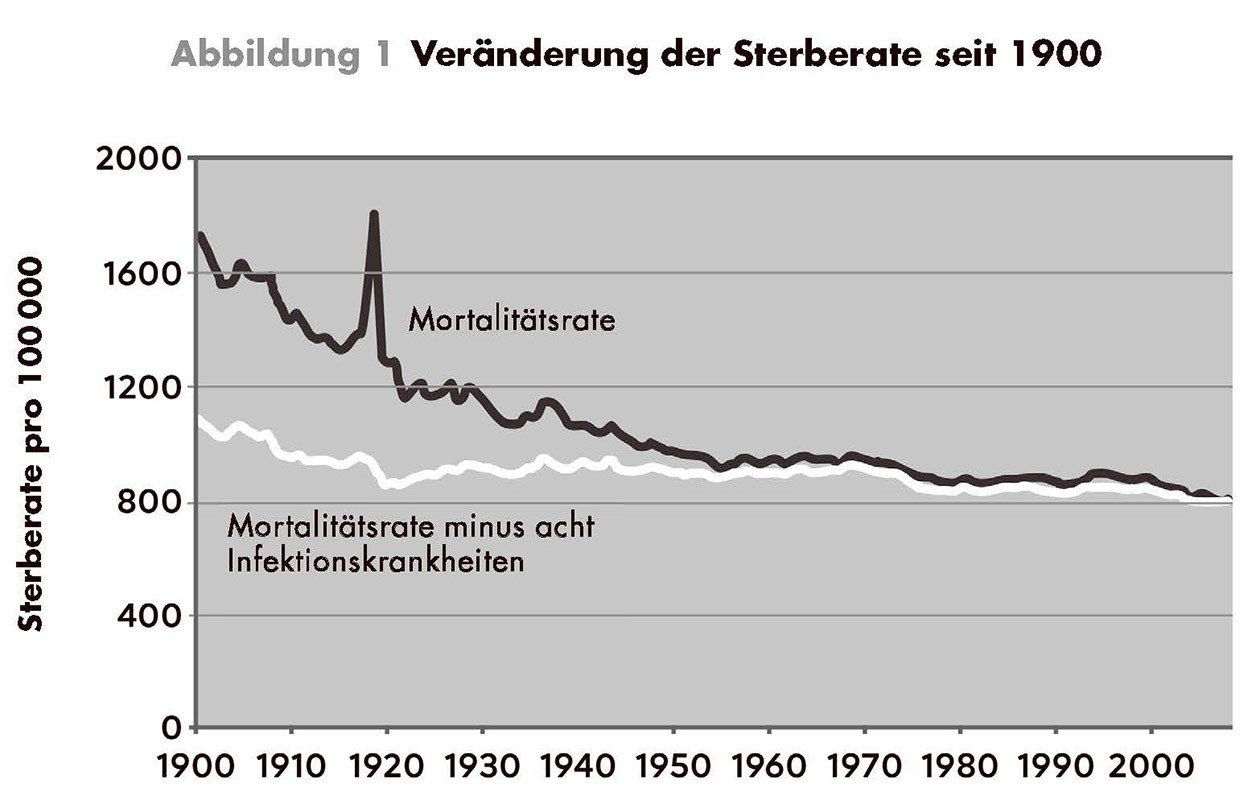
Aus diesem Diagramm geht hervor, wie wenig sich die Mortalitätsrate verändert hat, wenn man die acht relevantesten Infektionskrankheiten nicht berücksichtigt, die mit der Einführung von Antibiotika zu Beginn des 20. Jahrhunderts großenteils kontrollierbar wurden.
Quelle: Gordon (2016)
Noch verblüffender war vielleicht die rasante Entwicklung von nicht nur einem, sondern mehreren wirksamen Impfstoffen gegen COVID-19 in nicht einmal einem Jahr nach Ausbruch der Pandemie Anfang 2020. Das Virusgenom wurde nach den ersten Todesfällen in wenigen Wochen sequenziert, was die schnelle Formulierung von Impfstoffen ermöglichte, die gezielt auf das Oberflächenprotein des Virus einwirken. Auch die Fortschritte in der Behandlung von Covid-Patienten sind bemerkenswert gewesen; in weniger als zwei Jahren wurden mehrere virenhemmende Medikamente entwickelt. Dies ist Medizin 2.0 in Reinkultur.
Was langfristige Erkrankungen wie Krebs betrifft, hat sich Medizin 2.0 jedoch als weit weniger erfolgreich erwiesen. Während Bücher wie dieses immer betonen, dass sich die Lebenserwartung seit Ende des 19. Jahrhunderts fast verdoppelt hat, ist der Löwenanteil dieses Fortschritts möglicherweise vollständig auf Antibiotika und verbesserte sanitäre Anlagen zurückzuführen, wie Steven Johnson in seinem Buch Extra Life hervorhebt.[12] Der Ökonom Robert J. Gordon von der Northwestern University hat Mortalitätsdaten ab 1900 untersucht (siehe Abbildung 1) und Folgendes festgestellt: Wenn man Todesfälle durch die acht relevantesten Infektionskrankheiten außer Acht lässt, die mit der Einführung von Antibiotika in den 1930er-Jahren großenteils kontrollierbar wurden, sank die Gesamtsterberate über das 20. Jahrhundert hinweg nur geringfügig.[13] Das bedeutet, dass Medizin 2.0 kaum etwas gegen die apokalyptischen Reiter ausgerichtet hat.
Auf dem Weg zu Medizin 3.0
Während meiner nichtmedizinischen Tätigkeit erkannte ich, dass meine früheren Kollegen und ich dafür ausgebildet worden waren, die Probleme einer vergangenen Ära zu lösen: die akuten Erkrankungen und Verletzungen, deren Behandlung sich Medizin 2.0 gewidmet hatte. Diese Krankheiten spielten sich in einem sehr viel kürzeren Zeitrahmen ab; bei unseren Krebspatienten war die Zeit selbst der Feind. Und wir traten stets zu spät auf den Plan.
Vorher war mir das gar nicht so bewusst gewesen. Erst als mich während meiner kleinen Auszeit von der Medizin die Welt der Mathematik und Finanzen gefangen nahm und ich tagaus, tagein über die Natur des Risikos nachdachte, wurde es mir klar. Die Probleme der Banken waren gar nicht so verschieden von der Situation, mit der sich einige meiner Patienten konfrontiert sahen: Ihre scheinbar unbedeutenden Risikofaktoren hatten sich mit der Zeit zu einer nicht mehr aufzuhaltenden Katastrophe aufgetürmt. Auch chronische Krankheiten bahnen sich über Jahre und Jahrzehnte an – und haben sie sich erst einmal eingenistet, wird man sie kaum wieder los. Atherosklerose beispielsweise beginnt viele Jahrzehnte, bevor es bei der betreffenden Person zu einem koronaren »Ereignis« kommt, das zu ihrem Tod führen könnte. Doch erst dieses Ereignis, häufig ein Herzinfarkt, markiert zu oft den Punkt, an dem die Behandlung einsetzt.
Darum bin ich der Meinung, dass wir eine neue Sichtweise auf chronische Krankheiten, ihre Behandlung und die Bewahrung langfristiger Gesundheit entwickeln müssen. Diese neue Medizin – ich nenne sie Medizin 3.0 – verfolgt nicht das Ziel, die Leute zu verarzten und dann wieder nach Hause zu schicken, also etwa einen Tumor zu entfernen und dann das Beste zu hoffen, sondern vielmehr, von vornherein zu verhindern, dass sich der Tumor bildet und ausbreitet. Oder jenem ersten Herzinfarkt vorzubeugen. Oder jemanden von dem Weg abzubringen, der zu Alzheimer führt. Unsere Behandlungen wie auch unsere Präventions- und Diagnosemaßnahmen müssen sich so verändern, dass sie an die charakteristische Natur dieser Krankheiten mit ihrem langen, langsamen Verlauf angepasst sind.
Schon jetzt ist zu erkennen, dass sich die Medizin der heutigen Zeit rapide wandeln wird. Viele Fachleute sagen eine glorreiche neue Ära der »personalisierten« oder »Präzisionsmedizin« voraus, in der die Gesundheitsfürsorge auf unsere individuellen Bedürfnisse, bis hin zu unseren Genen, zugeschnitten ist. Das ist zweifellos ein hehres Ziel. Offenkundig gibt es keine zwei völlig identische Patientinnen, selbst wenn sie anscheinend an genau der gleichen Erkrankung der oberen Atemwege leiden. Eine Behandlung, die bei der einen anschlägt, kann sich bei der anderen als wirkungslos herausstellen, weil ihr Immunsystem möglicherweise anders reagiert oder ihre Infektion nicht bakteriell, sondern viral bedingt ist. Sogar heute noch ist der Unterschied äußerst schwer zu erkennen, was dazu führt, dass Millionen nutzlose Antibiotikarezepte ausgestellt werden.
Viele Experten glauben, dass diese neue Ära durch den technischen Fortschritt angetrieben wird, und vermutlich haben sie recht. Zugleich aber hat die Technologie (bisher) eher hemmend gewirkt. Lassen Sie mich das erklären. Einerseits sind wir dank verbesserter Technologien in der Lage, viel mehr Daten über Patienten als je zuvor zu sammeln, und die Patienten selbst können ihre eigenen Biomarker besser kontrollieren. Das ist gut. Noch besser ist, dass künstliche Intelligenz und maschinelles Lernen allmählich für die Verarbeitung dieser ungeheuren Datenmengen gerüstet sind und dann zu fundierteren Einschätzungen etwa für unser Risiko, eine Herz-Kreislauf-Erkrankung zu entwickeln, gelangen als die eher simplen Berechnungen aufgrund von Risikofaktoren, auf die wir uns bislang stützen. Außerdem wird auf die Möglichkeiten der Nanotechnologie verwiesen, welche Ärzte in die Lage versetzen könnten, Krankheiten mithilfe kleiner bioaktiver Moleküle, die in den Blutkreislauf injiziert werden, zu diagnostizieren und zu behandeln. Doch noch stehen uns die Nanobots nicht zur Verfügung, und ohne bedeutende öffentliche oder private Förderung könnte es noch eine Weile dauern, bis sie Wirklichkeit werden.
Das Problem ist, dass unsere Idee von einer personalisierten oder Präzisionsmedizin der Technologie, die für ihre vollständige Verwirklichung erforderlich ist, immer einige Schritte voraus bleibt. Das ist ein bisschen so wie bei dem Konzept des selbst fahrenden Autos, über das schon fast so lange geredet wird, wie Menschen bei Verkehrsunfällen getötet und verletzt werden. Zweifellos wäre es zu begrüßen, wenn menschliches Fehlverhalten möglichst gründlich aus der Gleichung gestrichen werden könnte, aber erst heute ist die Technologie so weit, den Abstand zu jener jahrzehntealten Vision zu verringern.
In den 1950er-Jahren hätte man für ein »selbst fahrendes« Auto bestenfalls einen Ziegelstein auf dem Gaspedal befestigen können. Dann hätte sich das Fahrzeug zwar allein fortbewegt, doch Abbremsen, Anhalten oder das Ausweichen vor einem Hindernis wäre unmöglich gewesen. Nicht gerade ideal. Aber heißt das, dass das ganze Konzept eines selbst fahrenden Autos unsinnig wäre? Nein, es heißt nur, dass wir damals noch nicht über das Handwerkszeug verfügten, das wir heute haben, um ein sowohl autonomes als auch sicheres Fahren zu ermöglichen: Computer, Sensoren, künstliche Intelligenz, maschinelles Lernen und so weiter. Jener einst so ferne Traum scheint nun in greifbare Nähe zu rücken.
In der Medizin sieht es ganz ähnlich aus. Vor zwei Jahrzehnten befestigten wir, bildlich gesprochen, noch einen Ziegelstein am Gaspedal. Heute nähern wir uns dem Punkt, an dem wir geeignete Technologien zur Anwendung bringen können, die uns helfen, Patienten als Individuen mit ganz spezifischen Eigenschaften zu behandeln. Beispielsweise haben sich Ärzte zur Beurteilung der Stoffwechselgesundheit ihrer Patienten traditionellerweise auf zwei Tests gestützt: einen, meist jährlich durchgeführten, Glucose-Toleranztest oder den bereits erwähnten HbA1c-Test, der den Durchschnittswert des Blutzuckers über die letzten 90 Tage schätzt. Solche Tests sind aber nur bedingt aussagekräftig, weil sie statisch und rückwärtsgewandt sind. Stattdessen tragen viele meiner Patienten ein Gerät bei sich, das den Blutzuckerspiegel in Echtzeit überwacht.
Mit Bezug darauf kann ich ihnen ganz konkret und differenziert etwas zu ihrer persönlichen Ernährung sagen, was auf diese Weise selbst vor zehn Jahren noch nicht möglich gewesen wäre. Diese Technologie namens kontinuierliche Glucosemessung (CGM) erlaubt mir zu verfolgen, wie ihr individueller Stoffwechsel auf ein bestimmtes Essverhalten reagiert, und gegebenenfalls eine rasche Ernährungsumstellung vorzuschlagen. Bald werden wir über sehr viel mehr derartige Sensoren verfügen, die uns ermöglichen, Therapien und Eingriffe sehr viel schneller und präziser durchzuführen. Dem selbst fahrenden Auto wird es besser gelingen, dem kurvigen Straßenverlauf zu folgen und nicht im Graben zu landen.
Meiner Ansicht nach geht es bei Medizin 3.0 jedoch nicht vornehmlich um Technologie. Sie erfordert vielmehr eine andere Denkweise, einen Wandel in unserer medizinischen Herangehensweise. Das lässt sich in vier zentrale Punkte unterteilen.
Erstens: Medizin 3.0 legt ein viel größeres Gewicht auf Prävention als auf Behandlung. Wann baute Noah seine Arche? Lange bevor es anfing zu regnen. Medizin 2.0 versucht herauszufinden, wie man nach dem Regen wieder trocken wird. Medizin 3.0 ist bewandert in Meteorologie und versucht vorherzusagen, ob wir unser Dach ausbessern oder ein Boot bauen sollten.
Zweitens: Medizin 3.0 betrachtet den Patienten als ein unverwechselbares Individuum. Medizin 2.0 behandelt alle mehr oder weniger gleich. Sie vertraut auf die Ergebnisse der klinischen Studien, die der evidenzbasierten Medizin zugrunde liegen. Bei diesen Versuchen gelangt man von einem heterogenen Input (den Versuchspersonen) zu homogenen Erkenntnissen (den für den Durchschnitt all dieser Personen gültigen Ergebnissen). Die evidenzbasierte Medizin fordert, dass wir diese Durchschnittswerte dann auf einzelne Personen anwenden. Doch leider entspricht kein Patient haargenau dem Durchschnitt. Medizin 3.0 nimmt die Ergebnisse der evidenzbasierten Medizin und geht noch einen Schritt weiter. Sie schaut sich die Daten gründlicher an, um zu bestimmen, inwiefern ein spezieller Patient der »durchschnittlichen« Versuchsperson ähnelt oder sich von ihr unterscheidet und ob sich die Ergebnisse auf ihn anwenden lassen oder nicht. Wir könnten also von einer »evidenzinformierten« Medizin sprechen.
Der dritte gedankliche Wandel betrifft unsere Einstellung zum Risiko. Unser Ausgangspunkt in Medizin 3.0 ist die ehrliche Einschätzung und Akzeptanz von Risiken – einschließlich der Risiken, die mit Nichtstun einhergehen.
Es gibt viele Beispiele für den fehlerhaften Umgang von Medizin 2.0 mit Risiko, doch besonders gravierend äußerte er sich im Zusammenhang mit der Hormonersatztherapie (HRT) für Frauen in der Post-Menopause, die schon lange übliche Praxis war, bevor 2002 die Ergebnisse einer Studie der Frauengesundheitsinitiative (WHI, von Women’s Health Initiative) veröffentlicht wurden. Bei dieser groß angelegten klinischen Studie, an der sich Tausende ältere Frauen beteiligten, wurden zahlreiche Gesundheitsdaten von Frauen, die sich einer HRT unterzogen, mit denen von Frauen verglichen, die das nicht taten. Die Studie stellte einen relativen Anstieg des Brustkrebsrisikos von 24 Prozent bei einer Teilmenge von Frauen fest, die sich einer HRT unterzogen.[14] Auf der ganzen Welt erschienen Schlagzeilen, die die HRT als gefährliche krebserregende Therapie verdammten. Mit einem Mal, aufgrund dieser einen Studie, wurde die Behandlung mit Hormonen praktisch tabu.
Das um 24 Prozent erhöhte Krebsrisiko, von dem die Rede war, klang tatsächlich beängstigend. Doch niemanden schien zu stören, dass die absolute Risikoerhöhung für Frauen, an Brustkrebs zu erkranken, winzig war. In der HRT-Gruppe erkrankten etwa fünf von tausend Frauen, dagegen in der Kontrollgruppe, die keine Hormone einnahm, vier von tausend. Die absolute Risikoerhöhung betrug nur 0,1 Prozent. HRT korrelierte möglicherweise mit jeweils einem weiteren Fall von Brustkrebs unter tausend Patientinnen. Und doch ging man davon aus, dass dieser verschwindend geringe Anstieg des absoluten Risikos alle Vorteile überwog, was bedeutete, dass Frauen mit Hitzewallungen und nächtlichem Schwitzen sowie geringerer Knochendichte und Muskelmasse zu rechnen hatten, neben weiteren unangenehmen Symptomen der Wechseljahre – ganz zu schweigen von einem möglicherweise erhöhten Risiko, an Alzheimer zu erkranken, wie wir in Kapitel 9 sehen werden.
Medizin 2.0 gab diese Therapie aufgrund einer einzigen klinischen Studie auf, statt die Einzelheiten zu ergründen und sich mit ihnen auseinanderzusetzen. Medizin 3.0 würde diese Studie berücksichtigen, aber zugleich ihre unweigerlichen Grenzen und immanenten Verzerrungen erkennen. Die zentrale Frage, die Medizin 3.0 stellen würde, lautet: Könnte diese Maßnahme der Hormonersatztherapie mit ihrer relativ geringen durchschnittlichen Risikoerhöhung innerhalb einer großen Gruppe von Frauen über fünfundsechzig nicht doch für eine ganz bestimmte Patientin mit ihrer individuellen Kombination von Symptomen und Risikofaktoren von Nutzen sein? Welche Parallelen oder Unterschiede sind bei ihr im Vergleich zur Studienpopulation zu beobachten? Hinzu kam, dass von den Frauen, die für die Studie ausgewählt wurden, keine wirklich über Beschwerden klagte und die meisten die Wechseljahre längst hinter sich hatten, was sie von Patientinnen, die über HRT nachdenken, deutlich unterschied. Wie gut lassen sich die Ergebnisse dieser Studie demnach auf Frauen übertragen, die sich kurz vor oder seit Kurzem in den Wechseljahren befinden (und vermutlich jünger sind)? Und gibt es vielleicht auch eine andere Erklärung für die leichte Risikoerhöhung, die bei dieser einen Untersuchung festgestellt wurde?[15]
Generell würde ich sagen, dass wir bei jeder einzelnen Patientin genauer hinschauen sollten, was die Abwägung von Risiken, Vor- und Nachteilen dieser Therapie angeht – und auch bei fast allem, was wir sonst tun könnten.
Der vierte und womöglich bedeutendste Wandel ist folgender: Während Medizin 2.0 überwiegend auf die Gesamtlebenszeit fokussiert ist und nahezu ausschließlich anstrebt, den Tod hinauszuzögern, richtet Medizin 3.0 ihr Augenmerk sehr viel stärker auf die gesunde Lebenszeit, die Lebensqualität.
Vom Konzept der gesunden Lebenszeit redete zur Zeit meines Medizinstudiums kaum jemand. Meine Professoren sagten so gut wie nichts dazu, was unsere Patienten zur Erhaltung ihrer körperlichen und geistigen Fähigkeiten im Alter tun könnten. Von sportlicher Betätigung redete praktisch keiner. Das Thema Schlaf wurde sowohl in den ersten Studienjahren als auch in der Assistenzarztzeit, als wir routinemäßig 24 Stunden am Stück arbeiteten, komplett ignoriert. Auch Ernährungsfragen wurden ganz am Rande oder überhaupt nicht behandelt.
Heute erkennt Medizin 2.0 die Relevanz der gesunden Lebenszeit zumindest an, doch die Standarddefinition – die Lebensphase, in der man frei von Krankheit oder Beeinträchtigung ist – ist meiner Meinung nach völlig unzureichend. Wir wünschen uns mehr vom Leben, als schlicht nicht krank oder beeinträchtigt zu sein. In der zweiten Hälfte unseres Lebens wollen wir uns in jeder Hinsicht gesund und vital fühlen.
Damit hängt zusammen, dass Langlebigkeit an sich und die gesunde Lebenszeit im Besonderen nicht wirklich in das Geschäftsmodell unseres gegenwärtigen Gesundheitssystems passen. Die meisten überwiegend präventiven Maßnahmen, die in meinen Augen zur Verlängerung der Gesamtlebenszeit und gesunden Lebenszeit nötig sind, werden von der Krankenversicherung nicht abgedeckt. Die Krankenkassen zahlen einem Arzt nicht viel dafür, dass er einem Patienten erklärt, er müsse seine Ernährung umstellen, oder dass er seinen Blutzuckerspiegel überwacht, um ihn bei der Vorbeugung von Typ-2-Diabetes zu unterstützen. Andererseits bezahlt die Kasse das (sehr teure) Insulin für denselben Patienten, nachdem er an Typ-2-Diabetes erkrankt ist. Entsprechend kann der Arzt von ihm verordnete Physiotherapie-Maßnahmen nicht abrechnen, wenn er beispielsweise für eine Patientin ein umfassendes Sportprogramm entwickelt, das ihre Muskulatur aufbaut und das Gleichgewicht schult, um Verletzungen zu vermeiden. Aber wenn sie stürzt und einen Oberschenkelhalsbruch davonträgt, übernimmt die Krankenversicherung die Kosten für OP und Reha. Das Geld wird nahezu vollständig für Behandlungen anstelle von Prävention ausgegeben – und wenn ich »Prävention« sage, meine ich damit Prävention von menschlichem Leid. Wenn wir weiter die gesunde Lebenszeit ignorieren, verurteilt dies die Menschen nicht nur zu einem kranken und gebrechlichen Leben im Alter, sondern treibt uns letzten Endes auch zweifellos in den Bankrott.
Wenn ich meinen Patienten diesen Ansatz erläutere, spreche ich häufig von Eisbergen – insbesondere von dem, der das Ende der ersten und letzten Fahrt der Titanic bedeutete. In jener Schicksalsnacht erhielt der mächtige Passagierdampfer um halb zehn von einem anderen Schiff die Warnmeldung, dass er auf ein Eisfeld zusteuere. Die Nachricht wurde ignoriert. Über eine Stunde später ging ein weiteres Telegramm mit der Warnung vor Eisbergen auf der Route des Schiffes ein. Der Funker der Titanic, der vollends damit beschäftigt war, trotz regem Funkverkehr mit Neufundland zu kommunizieren, antwortete (per Morsecode): »Raus aus der Leitung, Klappe halten.«[16]
Es gab noch mehr Probleme. Für eine nebelige Nacht mit schlechter Sicht hatte das Schiff zu viel Fahrt drauf. Die See war ungewöhnlich ruhig, was die Crew in falscher Sicherheit wiegte. An Bord waren mehrere Ferngläser, aber sie lagen in einem verschlossenen Schrank und niemand hatte den Schlüssel. Der Ausguck musste sich also allein auf seine Augen verlassen. Fünfundvierzig Minuten nach jenem letzten Funkspruch entdeckte der Ausguck den todbringenden Eisberg in weniger als 500 Metern Entfernung voraus. Jeder kennt das Ende der Geschichte.
Doch was wäre gewesen, wenn die Titanic über Radar und Sonar verfügt hätte (die erst im Zweiten Weltkrieg, also mehr als fünfzehn Jahre später, entwickelt wurden)? Oder, noch besser, über GPS und Satellitenbilder? Statt zu versuchen, sich heil durch das Labyrinth tödlicher Eisberge hindurchzumanövrieren und das Beste zu hoffen, hätte der Kapitän ein oder zwei Tage zuvor eine geringfügige Kurskorrektur vornehmen und das Unheil umschiffen können. Genau das tun Kapitäne heutzutage dank verbesserter Technik, mit der Schiffsunglücke titanischen Ausmaßes nun großenteils der Vergangenheit angehören und in rührseligen, nostalgischen Filmen mit einem überladenen Soundtrack ihr Dasein fristen müssen.
Das Problem ist, dass wir mit unseren medizinischen Werkzeugen nicht sehr weit über den Horizont hinausschauen können. Unser »Radar«, wenn man so will, ist nicht leistungsfähig genug. So erstrecken sich randomisierte klinische Studien über Statine als Primärprävention von Herz-Kreislauf-Erkrankungen vielleicht über fünf bis sieben Jahre, in denen die Probanden unter Beobachtung stehen. Der längste Zeitrahmen für Risikoprognosen beträgt zehn Jahre. Herz-Kreislauf-Erkrankungen können sich jedoch über Jahrzehnte hinweg anbahnen.
Medizin 3.0 betrachtet die Situation durch ein längeres Objektiv. Eine Vierzigjährige sollte sich mit ihrem Risikoprofil für Herz-Kreislauf-Erkrankungen auseinandersetzen, das nicht nur zehn, sondern dreißig oder vierzig Jahre in die Zukunft blickt. Darum brauchen wir Werkzeuge mit einer viel größeren Reichweite als klinische Studien von relativ kurzer Dauer. Wir brauchen Langstreckenradar, GPS, Satellitenbilder und alles, was es sonst noch gibt. Nicht bloß einen Schnappschuss.
Ich erkläre meinen Patienten, dass ich der Steuermann auf ihrem Schiff sein möchte. Mein Job, wie ich ihn verstehe, besteht darin, sie sicher durch das Eisfeld zu navigieren. Ich bin der Ausguck, der die Eisberge rund um die Uhr im Blick hat. Wie viele Eisberge gibt es da draußen? Welche sind uns am nächsten? Wenn wir unseren Kurs ändern, um ihnen aus dem Weg zu gehen, steuern wir dann neuen Gefahren entgegen? Lauern hinter dem Horizont, außer Sicht, noch größere, unheilvollere Eisberge?
Und das bringt uns zu dem vielleicht wichtigsten Unterschied zwischen Medizin 2.0 und Medizin 3.0. Bei Medizin 2.0 sind Sie als Passagier auf dem Schiff und reisen mehr oder weniger passiv mit. Medizin 3.0 verlangt Ihnen als Patient sehr viel mehr ab: Sie müssen gut informiert sein und sich einigermaßen mit medizinischen Begrifflichkeiten auskennen, Sie müssen wissen, was Ihre Ziele sind, und sich der Risiken bestens bewusst sein. Sie müssen bereit sein, lieb gewordene Gewohnheiten abzulegen, neue Herausforderungen anzunehmen und sich aus Ihrer Komfortzone herauszutrauen, falls es nötig ist. Ihre aktive Teilnahme ist gefordert. Sie stellen sich Problemen, auch wenn sie unbequem oder beängstigend sind, statt sie zu ignorieren, bis es zu spät ist. Für Sie steht eine Menge auf dem Spiel. Und Sie treffen wichtige Entscheidungen.
In diesem Szenario sind Sie nicht länger bloß ein Schiffspassagier. Sie sind der Kapitän.
Kapitel 3
Ziel, Strategie, Taktik
Ein Leitfaden zum Lesen dieses Buches
Strategie ohne Taktik ist der langsamste Weg zum Sieg.
Taktik ohne Strategie ist der Lärm vor der Niederlage.
Sun Tsu
Vor einigen Jahren flog ich nach San Francisco. Ich wollte zur Beerdigung der Mutter einer guten Studienfreundin, die ich hier Becky nenne. Weil Beckys Eltern in der Nähe von Palo Alto wohnten, wo ich mein medizinisches Grundstudium absolvierte, luden sie mich viele Male zum Essen ein. Oft aßen wir im Garten, den Beckys Mutter Sophie wunderschön angelegt hatte und sorgfältig pflegte.
Ich erinnere mich an Sophie als eine lebenssprühende, sportliche Frau, die alterslos schien. Seit meiner Hochzeit vor fünfzehn Jahren hatte ich sie allerdings nicht mehr gesehen. Von Becky erfuhr ich, was in der Zwischenzeit geschehen war. Mit Anfang siebzig hatte Sophie körperlich stark abgebaut, nachdem sie beim Gärtnern hingefallen war und sich dabei einen Muskelriss in der Schulter zugezogen hatte. Im Zuge dessen bekam sie bald so starke Rücken- und Nackenschmerzen, dass sie die Gartenarbeit und das Golfspielen aufgeben musste – ihre beiden Lieblingsbeschäftigungen im Ruhestand. Sie saß nur noch herum und wurde depressiv. In ihren letzten Lebensjahren wurde sie dann zunehmend dement, bis sie mit dreiundachtzig Jahren an einer Atemwegserkrankung starb.
Bei ihrer Trauerfeier bekräftigten alle, es sei ein »Segen«, dass Sophie nicht sehr lange an der Demenz hatte leiden müssen. Doch als ich auf der Kirchenbank saß, dachte ich darüber nach, dass sie in den letzten zehn Jahren ihres Lebens all den Aktivitäten, die ihr Freude bereitet hatten, nicht mehr hatte nachgehen können. Stattdessen war sie von starken Schmerzen geplagt gewesen. Davon sprach niemand. Wir waren zusammengekommen, um über Sophies biologischen Tod zu trauern, aber mich betrübte noch viel mehr, dass ihre letzten Lebensjahre so freudlos gewesen waren.
Meinen Patienten erzähle ich oft von Sophie – nicht weil ihre Geschichte so ungewöhnlich ist, sondern traurigerweise so typisch. Wir alle haben erlebt, dass es unseren Eltern, Großeltern, Ehepartnern oder Freunden ähnlich ergangen ist. Das Schlimme ist: Wir erwarten im Grunde schon, dass es alten Menschen so ergeht, und trotzdem unternehmen nur wenige von uns etwas, um nicht das gleiche Schicksal zu erleiden. Selbst Becky, die sich in den schwierigen letzten Jahren um ihre Mutter gekümmert hatte, kam es vermutlich nicht im Entferntesten in den Sinn, dass sie vielleicht genauso enden würde. Für die meisten Menschen ist die Zukunft ein abstrakter Nebel.
Ich erzähle Sophies Geschichte, um damit ein grundlegendes Konzept meiner Herangehensweise an Langlebigkeit zu verdeutlichen: Wir müssen über die späteren Jahrzehnte unseres Lebens – wenn wir siebzig, achtzig, neunzig oder noch älter sind – nachdenken und Pläne dafür schmieden. Für viele Menschen sind die zehn letzten Lebensjahre, wie für Sophie, nicht gerade eine glückliche Zeit. Typischerweise leiden sie dann an mindestens einem der vier apokalyptischen Reiter und den Begleiterscheinungen der jeweiligen Behandlungen. Ihre geistigen und körperlichen Fähigkeiten werden schwächer oder sind nicht mehr vorhanden. Generell sind sie nicht mehr in der Lage, Tätigkeiten auszuüben, die sie früher geliebt haben, sei es Gärtnern, Schach spielen, Fahrrad fahren oder was ihnen sonst Freude bereitet hat. Ich bezeichne diese Zeit als Marginal Decade, als »Randdekade« des Lebens, und für viele, wenn nicht die meisten Menschen ist sie eine Zeit der Reduzierung und Beschränkung.
Ich bitte alle meine Patienten, für sich selbst eine alternative Zukunft zu skizzieren. Was möchten Sie in Ihren späteren Jahren tun? Wie sieht der Plan für den Rest Ihres Lebens aus?
Jeder beantwortet diese Frage ein wenig anders – vielleicht möchte man reisen oder golfen, wandern gehen oder mit seinen Enkeln und Urenkeln spielen (das steht auf meiner Liste ganz oben). Sinn und Zweck dieser Aufgabe ist zweierlei. Erstens ist man gezwungen, sich mit der Endphase des eigenen Lebens auseinanderzusetzen, worüber die meisten Leute nicht gerne nachdenken. Ökonomen sprechen von »hyperbolischer Diskontierung«, der natürlichen Tendenz, eine sofortige Belohnung potenziellen künftigen Gewinnen vorzuziehen, insbesondere wenn diese Gewinne harte Arbeit erfordern. Zweitens führt die Aufgabe uns die große Bedeutung der gesunden Lebenszeit vor Augen. Wenn Becky im Alter ein gesundes, erfüllendes Leben führen und nicht das gleiche Schicksal wie ihre Mutter erleben möchte, ist sie angehalten, ihre körperlichen und geistigen Funktionen in jeder Dekade von nun an aufrechtzuerhalten und hoffentlich zu verbessern. Sonst wird die Schwerkraft des Alterns ihren Tribut fordern und Becky, wie ihre Mutter, in die Knie zwingen.
Als Mathefreak stelle ich Gesamtlebenszeit und gesunde Lebenszeit, wie in Abbildung 2, gern als mathematische Funktion dar – eines von vielen Diagrammen, die ich für meine Patienten zeichne. Die horizontale Achse (x-Achse) des Graphen steht für Ihre Gesamtlebenszeit – sie gibt an, wie lange Sie leben. Die vertikale Achse (y-Achse) steht gewissermaßen für die Gesamtheit Ihrer körperlichen und geistigen Funktionen – die beiden altersabhängigen Dimensionen der gesunden Lebenszeit. (Natürlich lässt sich die gesunde Lebenszeit nicht wirklich quantifizieren; ich hoffe, Sie verzeihen mir diese grobe Vereinfachung.)
Die durchgezogene schwarze Linie repräsentiert den natürlichen Verlauf Ihres Lebens ohne größere medizinische Interventionen: Zum Zeitpunkt null werden Sie geboren, und der Einfachheit halber sagen wir, dass Ihre körperliche und geistige Gesundheit zu diesem Zeitpunkt 100 Prozent beträgt. Etwa bis zu Ihrem fünften Lebensjahrzehnt bleibt Ihre Gesundheit relativ robust. Wahrscheinlich beginnt sie dann nach und nach, aber stetig abzunehmen, bis Sie irgendwann in den Sechzigern oder Anfang der Siebziger sterben. Das entspräche einer nicht untypischen Gesamtlebenszeit für Jäger und Sammler oder Mitglieder einer primitiven Agrargesellschaft, vorausgesetzt, sie entgehen einem frühen Tod durch Infektionskrankheiten oder andere Schicksalsschläge.
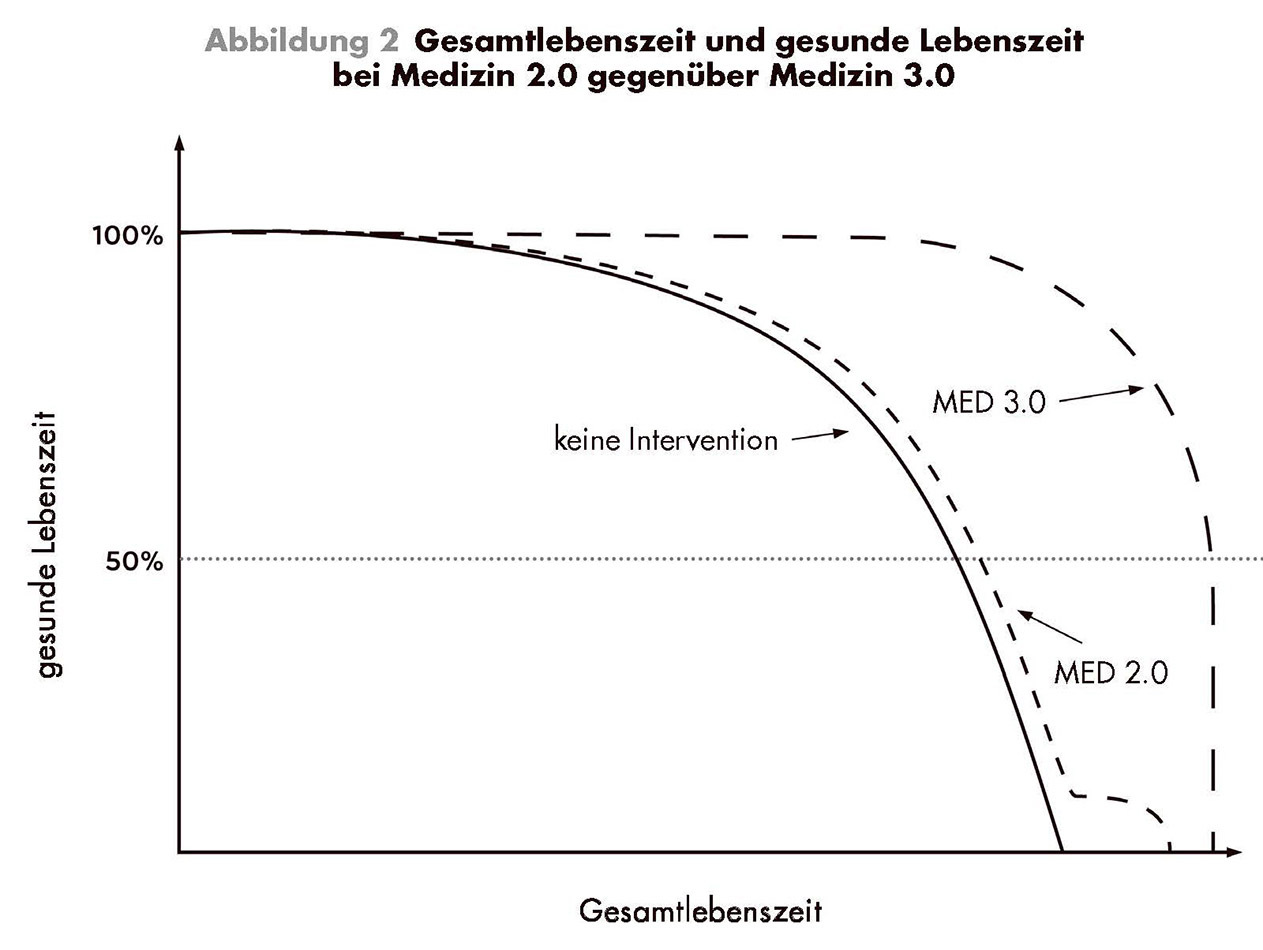
Nun schauen wir uns den typischen Verlauf des modernen Lebens an, der im Diagramm durch die kurz gestrichelte Linie mit der Bezeichnung »MED 2.0« repräsentiert ist. Dank relativem Komfort und größerer Sicherheit leben Sie nun ein wenig länger. Im mittleren Alter werden Sie jedoch allmählich einige Veränderungen registrieren. Sie büßen teilweise Ihre jugendliche Stärke und Kondition ein. Vielleicht bemerken Sie, dass Sie gelegentlich ein Passwort vergessen oder die Namen von Personen, die Sie kennenlernen, oder die Namen von Schauspielern aus Filmen, die Sie vor langer Zeit gesehen haben. Einige Freunde und Gleichaltrige erkranken an Krebs und Herz-Kreislauf-Krankheiten oder leiden an hohem Blutdruck und Diabetes oder Prädiabetes. Und Sie müssen auf Beerdigungen von Schulfreunden gehen.
Ab einem gewissen Punkt wird der Abstieg steiler. Schließlich, wenn Sie ungefähr siebzig bis fünfundsiebzig Jahre alt sind, haben sich Ihre geistigen und körperlichen Fähigkeiten etwa halbiert (dargestellt durch die gepunktete waagerechte Linie). Dies ist der von mir mehr oder weniger willkürlich festgelegte Punkt, ab dem Ihnen Dinge, die Sie tun wollen, nicht mehr leicht von der Hand gehen. Sie sind eingeschränkt, und Ihnen passieren häufiger Missgeschicke oder Unfälle mit gravierenderen Folgen. Sich mit vierzig, wenn Sie noch kräftig und widerstandsfähig sind, beim Skifahren den Oberschenkelknochen zu brechen, ist das eine; etwas ganz anderes ist es, wenn Sie ihn sich mit fünfundsiebzig beim Stolpern über die Bordsteinkante brechen und nur noch über 25 Prozent Ihrer früheren Belastbarkeit verfügen. Zugleich steigt auch das Risiko chronischer Krankheiten exponentiell an.
Hier greift nun Medizin 2.0 ein. Wir behandeln Ihre Krebs- oder Herz-Kreislauf-Erkrankung oder welches Leiden auch immer und verlängern Ihr Leben um ein paar Monate oder auch Jahre, wenn Sie Glück haben. Aus diesem Grund wird die Kurve der Gesamtlebenszeit und gesunden Lebenszeit dort flacher und verläuft eher waagerecht nach rechts, womit die Verschiebung des Todes dargestellt wird. Doch wenn wir uns ansehen, wo das passiert, erkennen wir, dass Ihre Gesundheitsspanne dort bereits einen sehr niedrigen Wert aufweist. Das bedeutet, dass Ihr Tod hinausgezögert wurde, ohne Ihre Lebensqualität signifikant zu verbessern – darin ist Medizin 2.0 Experte. So sieht die Randdekade aus, die die meisten von uns in unserem derzeitigen System erwartet.
Nun betrachten wir die lang gestrichelte Linie im Diagramm. Sie repräsentiert den idealen Verlauf Ihres Lebens. Den wünschen Sie sich. Statt bereits im mittleren Alter abzufallen, bleibt Ihre gesunde Lebenszeit auf gleicher Höhe oder verbessert sich sogar auf dem Weg in die Fünfziger und darüber hinaus. Mit fünfundfünfzig und gar fünfundsechzig Jahren werden Sie fitter und gesünder sein als mit fünfundvierzig und bleiben bis weit in die Siebziger und Achtziger, vielleicht sogar noch länger, körperlich und geistig fit. Sie werden wirken, als seien Sie zehn oder auch zwanzig Jahre jünger, als in Ihrem Personalausweis steht. Unter dieser Kurve ist viel mehr Freiraum, und dieser große Freiraum steht für Ihr längeres, besseres Leben – mehr Zeit für die Familie, für Ihre Leidenschaften, für Reisen oder weiterhin ein erfüllendes Arbeitsleben. Wenn der Abstieg schließlich einsetzt, ist er zwar steil, aber relativ kurz. Das bezeichne ich als Quadrierung der Langlebigkeitskurve.
In diesem Szenario leben wir länger, und wir leben länger besser. Wir übererfüllen die durchschnittliche Lebenserwartung und trotzen zudem den gesellschaftlichen Erwartungen, wie unser späteres Leben wohl aussehen wird. Statt einer trübseligen Randdekade genießen wir eher so etwas wie eine »Bonusdekade« – oder mehrere davon. Dies ist unser Ziel: den Tod hinauszögern und aus den zusätzlich geschenkten Jahren das Beste machen. So dürfen wir den Rest unseres Lebens genießen, statt ihn zu fürchten.
Die nächste naheliegende Frage lautet: Wie machen wir das? Wie verlängern wir gleichzeitig unsere Gesamtlebenszeit und die gesunde Lebenszeit? Wie bieten wir dem Tod in Gestalt der apokalyptischen Reiter die Stirn und verlangsamen zugleich den körperlichen, geistigen und seelischen Niedergang oder kehren ihn sogar um?
Wie sieht unser Plan aus?
Hier schlagen die meisten einen falschen Weg ein. Sie wollen eine Abkürzung nehmen, die direkt zur Taktik führt: Das dürfen Sie essen (oder nicht essen), so sollten Sie sich sportlich betätigen, dies sind die Nahrungsergänzungsmittel oder Medikamente, die Sie brauchen, und so weiter. Es gibt ganze Wagenladungen mit Büchern, die vorgeben, die Antworten zu kennen, aber das Buch, das Sie gerade lesen, gehört nicht dazu. Vielmehr glaube ich, dass wir genau an diesem Punkt innehalten und einen Schritt zurückgehen müssen, damit wir den wichtigsten Abschnitt im gesamten Prozess nicht überspringen: die Strategie.
Schauen wir noch einmal auf das Sun-Tsu-Zitat, das dieses Kapitel eingeläutet hat: »Taktik ohne Strategie ist der Lärm vor der Niederlage.« Das bezog sich auf Kriegsführung, aber in unseren Kontext passt es ebenso gut. Um unsere Ziele zu erreichen, brauchen wir zuallererst eine Strategie – einen übergeordneten Ansatz, ein gedankliches Gerüst oder ein mentales Modell, das sich auf wissenschaftliche Erkenntnisse stützt, auf unsere Ziele zugeschnitten ist und uns verschiedene Optionen bietet. Unsere spezifische Taktik ergibt sich aus unserer Strategie, und die Strategie ergibt sich aus unserem Ziel. Das Ziel kennen wir bereits, aber der Weg zum Sieg ist die Strategie.
Häufig macht man den großen Fehler, Strategie und Taktik zu vermengen, weil man denkt, dass sie ein und dasselbe sind. Das sind sie nicht. Den Unterschied erkläre ich gern mit einem der denkwürdigsten Boxkämpfe aller Zeiten: Muhammad Ali gegen George Foreman, der berühmte »Rumble in the Jungle« 1974 in Kinshasa, Zaire. Alis Ziel war natürlich, den Kampf gegen Foreman zu gewinnen und sich den Weltmeistertitel im Schwergewicht zurückzuholen. Alis Problem bestand darin, dass Foreman jünger, stärker und gemeiner war und als Favorit gehandelt wurde, der seine Gegner vernichtend schlug. Mit dem jovialen Typ, der heute Countertop-Grills verkauft, ist das kaum in Einklang zu bringen, aber damals hieß es, George Foreman sei der mieseste Hurensohn, der jemals Boxhandschuhe getragen habe. Er galt buchstäblich als unbesiegbar. Alle Experten waren sich einig, dass Ali, so schillernd und beliebt er auch war, keine Chance hatte – und darum brauchte er eine Strategie.
Ali wusste, dass er gegenüber Foreman einige leichte Vorteile hatte: Er war schneller, erfahrener und mental gefestigter. Außerdem wusste er, dass Foreman ein Hitzkopf war und schnell wütend wurde. Statt gegen jeden Punch von Foreman einen Konter zu setzen, beschloss Ali, den Jüngeren und Unerfahreneren dazu zu bringen, sich zu verausgaben, was ihn frustriert und müde und damit verletzbar machen würde. Wenn ihm das gelänge, wusste Ali, wäre der Kampf ausgeglichener. Also lautete seine Strategie: Mach Foreman wütend und lass ihn um sich schlagen, bis ihm die Luft ausgeht und du in die Offensive gehen kannst.
Aus dieser Strategie ergab sich die Taktik, die legendär geworden ist: Foreman erst mal mit einer Serie von rechten Geraden mit der Führhand anzugreifen, was derart respektlos war, dass es Foreman garantiert rasend machen würde. Niemand setzt solche Treffer gegen den Schwergewichtsweltmeister! Danach ließ Ali zu, dass ihn der erboste Foreman durch den Ring trieb und gegen die Seile drängte, was kräftezehrend war, während sich Ali darauf konzentrierte, den Schaden, der ihm zugefügt wurde, möglichst klein zu halten – das war das berühmte »Rope-a-Dope«.
In den ersten Runden glaubten alle, Foreman eingeschlossen, er werde Ali zermalmen. Doch weil Alis Strategie lautete, länger durchzuhalten als sein Gegner, hatte er sein Training darauf ausgerichtet, Prügel einzustecken. Etwa in der fünften Runde sieht man Foreman gleichsam an, wie ihm dämmert: Verdammt, mir geht die Puste aus! Ali hingegen hatte dank seiner besseren körperlichen Verfassung noch deutlich mehr Reserven. Und so gewann er den Kampf durch K. o. in der achten Runde.
Entscheidend ist: Die Taktik wendet man an, wenn man bereits im Ring steht. Die Strategie zu entwickeln ist die größere Herausforderung, weil sie verlangt, den Gegner sorgfältig zu studieren, seine Stärken und Schwächen zu erkennen und herauszufinden, wie man diese zum eigenen Vorteil einsetzt, und zwar lange bevor man in den Ring steigt. Diesen dreigeteilten Ansatz – vom Ziel zur Strategie zur Taktik – verfolgen wir auch auf dem Weg zur Langlebigkeit.
Unsere Strategie
Als Ali in den Kampf gegen Foreman ging, wusste er, dass die Zeit für ihn arbeiten würde. Je länger er seinen Gegner reizen konnte, um ihn müde zu machen, während er zugleich vermied, selber ausgeknockt zu werden, desto besser standen die Chancen, letzten Endes den Sieg davonzutragen. Wir haben dagegen das Pech, dass die Zeit definitiv nicht für uns arbeitet. In jedem Augenblick unseres Lebens drückt das Risiko von Krankheit und Tod uns nieder, so wie die Schwerkraft einen Weitspringer zu Boden zieht.
Natürlich erfordert nicht jedes Problem, mit dem wir konfrontiert werden, eine Strategie. Genauer gesagt, kaum eines. Wir brauchen keine Strategie, wenn wir das Ziel haben, keinen Sonnenbrand zu bekommen. Unsere taktischen Optionen sind offenkundig, uns mit Sonnenschutz einzureiben, lange Ärmel und Hosenbeine zu tragen und zudem einen großen Hut aufzusetzen – oder gar nicht erst in die Sonne zu gehen. Doch um länger besser zu leben, ist eine Strategie vonnöten, weil Langlebigkeit ein viel komplexeres Problem als ein Sonnenbrand ist.[17]
Länger zu leben bedeutet, den Tod durch alle vier apokalyptischen Reiter hinauszuzögern. Einen gravierenden Risikofaktor haben sie gemeinsam – das Alter. Mit zunehmendem Alter steigt das Risiko exponentiell an, dass sich in unserem Körper eine oder mehrere dieser Krankheiten einnisten. Gegen unser chronologisches Alter kommen wir leider nicht an – aber was genau verstehen wir unter »Altern«? Dabei geht es nicht bloß um das Verstreichen der Zeit, sondern um das, was nach und nach in unserem Körper, unter der Oberfläche, in unseren Organen und Zellen passiert. Der Zahn der Zeit nagt an jedem einzelnen Tag an uns.
»Der Alterungsprozess ist durch den fortschreitenden Verlust physiologischer Unversehrtheit gekennzeichnet, was die Funktionen beeinträchtigt und die Gefahr erhöht, an einer Krankheit oder Verletzung zu sterben«, schreiben die Autoren eines einflussreichen Artikels von 2013, der die »Kennzeichen des Alterns« zum Thema hat.[18] Sie fahren fort: »Dieser Verfall ist der bedeutendste Risikofaktor für gravierende Gesundheitsschädigungen des Menschen, wie Krebs, Diabetes, Herz-Kreislauf-Erkrankungen und neurodegenerative Erkrankungen.«
Der Alterungsprozess als solcher macht uns anfällig für diese Krankheiten, während er zugleich unsere gesunde Lebenszeit beeinträchtigt. Wer aufgrund eines Herzinfarkts tot zusammenbricht, ist nicht erst eine Stunde vorher krank geworden. Die Krankheit ist im Innern des Körpers im Laufe von Jahrzehnten still und unsichtbar vorangeschritten. Mit zunehmendem Alter werden die körpereigenen Abwehrmechanismen geschwächt, und die Krankheit gewinnt die Oberhand. Etwas Ähnliches war bei der COVID-19-Pandemie zu beobachten. Das Virus infizierte Menschen aller Altersgruppen, forderte aber unter der älteren Bevölkerung relativ gesehen weitaus mehr Todesopfer, weil es ihre Anfälligkeit für Krankheit und Tod schonungslos offenbarte und sich zunutze machte – etwa das geschwächte Immunsystem, die Probleme mit Herz und Kreislauf oder den Atemwegen. Bei unserer Strategie müssen wir also die Auswirkungen des Alterns berücksichtigen, so wie Ali sein eigenes fortgeschrittenes Alter in Betracht zog, als er darüber nachdachte, wie er Foreman besiegen könnte. Ohne die richtige Strategie hätte Ali den Kampf so gut wie sicher verloren.
Aus diesem Grund preschen wir nicht einfach zur Taktik vor, indem ich Ihnen sage, was Sie tun sollten. Falls Sie es nicht abwarten können, rate ich Ihnen, innezuhalten, tief durchzuatmen und es sich gemütlich zu machen. Ohne sich mit der Strategie und den zugrunde liegenden wissenschaftlichen Erkenntnissen vertraut zu machen, wird die Taktik nicht viel bewirken, und Sie werden in einer Endlosschleife zurzeit angesagte Diäten, trendige Work-outs und Nahrungsergänzungsmittel mit Wunderwirkung ausprobieren. Sie bleiben in der Medizin-2.0-Mentalität gefangen, weil Sie nach einer schnellen Lösung für Ihre Probleme suchen. Ein cleverer Taktiker werden Sie nur dann, wenn Sie sich auf Medizin 3.0 einlassen, die voraussetzt, dass aus Ihnen zunächst ein gewiefter Stratege wird.
In den nächsten Kapiteln tauchen wir tief in einige Mechanismen ein, die dem Alterungsprozess zugrunde liegen. Außerdem schauen wir uns die Funktionsweisen der einzelnen apokalyptischen Reiter an. Wie und wann beginnen sie? Welche inneren und äußeren Kräfte treiben ihre Entwicklung voran? Was bewirkt, dass sie sich dauerhaft einnisten? Und, was am wichtigsten ist, wie kann man sie hinauszögern oder bestenfalls ganz verhindern? Wie wir im nächsten Kapitel sehen werden, ist das der Grund für das außergewöhnlich hohe Alter von Hundertjährigen: Sie verzögern oder vermeiden das Einsetzen chronischer Krankheiten um Jahrzehnte länger als der Durchschnitt.
Auch mit der gesunden Lebenszeit werden wir uns eingehender beschäftigen – jenseits von Klischees und oberflächlicher Betrachtung. Die Standarddefinition als Lebensabschnitt, in dem man frei von Krankheit oder Beeinträchtigung ist, greift viel zu kurz. Wenn wir nicht krank und ans Haus gefesselt sind, sind wir »gesund«? Ich werde hier gern etwas deutlicher – so deutlich, dass ich meinen Patienten damit oft Unbehagen bereite.
Sehen wir es doch einmal so: Die Gesamtlebenszeit definiert sich über den Tod, der binär ist – zuerst lebt man und dann ist man tot. Endgültig. Aber vorher, manchmal auch schon lange vorher, erleiden die meisten Menschen eine Zeit des Niedergangs, die, so würde ich behaupten, gewissermaßen ein Sterben in Zeitlupe ist. Zweifellos war dies bei Sophie, Beckys Mutter, der Fall. Das kann schnell passieren, etwa nach einem schlimmen Unfall, aber normalerweise geht es so langsam vor sich, dass wir die Veränderung kaum wahrnehmen.
Ich definiere die gesunde Lebenszeit und ihre Verschlechterung mithilfe von drei Kategorien oder Vektoren. Der erste Vektor des Verfalls betrifft unsere geistigen Fähigkeiten. Die Verarbeitungsgeschwindigkeit nimmt ab. Wir können komplexe Probleme nicht mehr so schnell und leicht lösen wie früher. Unser Gedächtnis lässt nach. Auf unsere exekutiven Funktionen ist weniger Verlass. Unsere Persönlichkeit verändert sich, und wenn dieser Prozess lange genug fortschreitet, verlieren wir auch die Fähigkeit, uns als eigenständiges Selbst wahrzunehmen. Glücklicherweise entwickeln die meisten Menschen keine völlige Demenz, doch viele machen die Erfahrung, dass die kognitiven Kapazitäten im Alter abnehmen. Unser Ziel ist es, diese Entwicklung zu minimieren.
Der zweite Vektor des Verfalls betrifft die Abnahme und letztlich den Verlust der Körperfunktionen. Das kann vor oder nach dem geistigen Verfall eintreten, die Reihenfolge ist nicht festgelegt. Doch mit zunehmendem Alter werden wir gebrechlicher. Wir büßen Muskelmasse und Kraft sowie Knochendichte, Kondition und Stabilität ein, und der Gleichgewichtssinn wird beeinträchtigt, bis es kaum noch möglich ist, eine volle Einkaufstasche ins Haus zu tragen. Chronische Schmerzen halten uns davon ab, Dinge zu tun, die uns früher leichtgefallen sind. Gleichzeitig lässt uns möglicherweise das unaufhaltsame Fortschreiten einer Gefäßverkalkung kurzatmig werden, wenn wir zum Briefkasten am Ende der Einfahrt gehen, um die Zeitung zu holen (falls es überhaupt noch Zeitungen gibt, wenn wir erst alt sind). Oder wir sind noch recht aktiv und gesund, bis wir – wie Sophie – stürzen oder uns eine unerwartete Verletzung zuziehen, was uns in eine Abwärtsspirale zieht, aus der es kein Entrinnen mehr gibt.
Meine Patienten gehen nur selten davon aus, dass sie von diesem Verfall betroffen sein werden. Ich bitte sie, mir genau zu beschreiben, wie sie sich ihre Zukunft idealerweise vorstellen. Was wollen sie tun, wenn sie älter sind? Es ist verblüffend, wie rosig ihre Zukunftspläne meistens sind. Sie nehmen ganz selbstverständlich an, dass sie noch mit über siebzig und achtzig Snowboard fahren werden oder zum Kickboxen gehen.
Dann muss ich sie bremsen und ihnen erklären, dass sie dafür über ein gewisses Maß an Muskelkraft und Ausdauer verfügen müssen. Doch selbst schon früher, mit zweiundfünfzig zum Beispiel, reichen Kraft und maximale Sauerstoffaufnahme (VO2max) dafür kaum noch aus und werden so gut wie sicher weiter abnehmen. Demzufolge haben sie die Wahl, sich entweder mit dem Verfall abzufinden oder einen Plan zu entwickeln und sofort umzusetzen.
Ganz gleich, wie ehrgeizig Ihre Ziele für Ihre späteren Lebensjahre sind – ich schlage vor, dass Sie sich mit den »Aktivitäten des täglichen Lebens« vertraut machen, einer Checkliste, um die Gesundheit und Funktionsfähigkeit älterer Menschen einzuschätzen. Die Liste enthält elementare Aufgaben, wie das Zubereiten einer Mahlzeit, Gehen ohne Hilfe, Waschen und Körperpflege, Telefonieren, Einkaufen von Lebensmitteln, das Verwalten der persönlichen Finanzen und so weiter. Nun stellen Sie sich vor, Sie sind nicht mehr in der Lage, für Ihre Ernährung zu sorgen, sich zu waschen oder ein paar Hundert Meter weit zu gehen, um mit Freunden einen Kaffee zu trinken. Dies alles halten wir momentan für selbstverständlich, doch wenn wir unser Leben im Alter weiterhin aktiv gestalten wollen und uns zumindest diese minimalen Fähigkeiten bewahren möchten, müssen wir unsere Fitness auf ein festes Fundament stellen und es gewissenhaft instand halten.
Die dritte und letzte Kategorie des Verfalls hat meiner Ansicht nach mit seelischer Gesundheit zu tun. Im Gegensatz zu den anderen ist sie großenteils altersunabhängig. Sie kann äußerlich gesunde junge Menschen in den Zwanzigern betreffen oder in mittleren Jahren zum Problem werden, wie es bei mir der Fall war. Oder auch später im Leben. Laut Erhebungen erreicht die Lebenszufriedenheit ihren Tiefpunkt in den Vierzigern (genauer gesagt, mit siebenundvierzig Jahren), doch wie ich aus eigener schmerzlicher Erfahrung weiß, liegen die Ursachen für Unzufriedenheit und Kummer im mittleren Alter häufig weit zurück, in der Jugend oder Kindheit. Dass wir gefährdet sind, bemerken wir manchmal erst in einer Krisensituation – so ist es mir ergangen. Wie wir damit umgehen, hat einen entscheidenden Einfluss auf unsere körperliche Gesundheit, unsere Zufriedenheit und, ja, unser Überleben.
In meinen Augen ergibt das Konzept der Langlebigkeit nur dann wirklich Sinn, wenn wir allen diesen Vektoren des Verfalls gleichermaßen die Stirn bieten oder ihnen aus dem Wege gehen. Keine dieser einzelnen Komponenten der Langlebigkeit ist ohne die anderen viel wert. Hundert Jahre alt werden, ohne dass Geist und Körper intakt sind, möchte niemand. Ebenso wenig erstrebenswert ist es, ein wunderbares Leben zu führen, aber jung zu sterben. Und in guter körperlicher Verfassung zu altern, jedoch ohne Liebe, Freundschaft und eine sinnvolle Aufgabe, ist eine Hölle, die ich meinem schlimmsten Feind nicht wünsche.
Wichtig ist festzuhalten: Der Tod an sich ist unvermeidlich, aber für den geschilderten Verfall gilt das nicht unbedingt. Nicht jeder, der mit über achtzig oder neunzig stirbt, hat auf dem Weg dorthin die tiefen Täler des geistigen, körperlichen oder seelischen Abbaus durchschritten. Man kann einen anderen Weg wählen – und ich glaube, es liegt überwiegend an uns, ob wir in Abgründe geraten, auch wenn sie mit der Zeit immer schwerer zu umgehen sind. Wie wir in späteren Kapiteln sehen werden, lassen sich der geistige, der körperliche und auch der seelische Verfall mit der richtigen Taktik verlangsamen und mitunter sogar umkehren.
Der zweite entscheidende Punkt ist, dass Gesamtlebenszeit und gesunde Lebenszeit keine unabhängigen Variablen sind; sie sind eng miteinander verflochten. Wenn wir unsere Muskeln kräftigen und unsere kardiorespiratorische Fitness (aerobe Fitness) verbessern, senken wir unser allgemeines Sterberisiko sehr viel effektiver als mit irgendeinem Medikamentencocktail. Das Gleiche gilt für die geistige und seelische Gesundheit. Alles, was wir für die Verbesserung unserer gesunden Lebenszeit tun, verlängert so gut wie immer unsere Gesamtlebenszeit. Aus diesem Grund zielt unsere Taktik in erster Linie auf die Verbesserung der gesunden Lebenszeit ab.
Die Taktik
Der wichtigste Unterschied zwischen Medizin 2.0 und Medizin 3.0 betrifft die Frage, wie und wann wir unsere Taktik anwenden. Medizin 2.0 greift normalerweise erst ein, wenn eine akute Schädigung – eine Infektion oder ein Knochenbruch – vorliegt, die dann mit kurzfristigen Maßnahmen behandelt wird. Die Medizin-3.0-Taktik muss dagegen in unseren Alltag integriert werden – buchstäblich in Essen, Atmen und Schlafen.
Medizin 2.0 stützt sich, generell gesprochen, auf zwei Arten von Taktik: Eingriffe (zum Beispiel Operationen) und Medikamente. Unsere Medizin-3.0-Taktik umfasst fünf große Bereiche: sportliche Betätigung, Ernährung, Schlaf, seelische Gesundheit und exogene Moleküle, sprich Arzneimittel, Hormone oder Nahrungsergänzungsmittel. Über exogene Moleküle werde ich hier nicht allzu viel sagen, denn dann würde das Buch doppelt so lang. Nur so viel: Ich habe keine Angst vor Arzneimitteln, nur weil sie nicht »natürlich« sind. Viele Medikamente und Ergänzungsmittel, etwa Blutfettsenker, halte ich in unserer Langlebigkeitsausrüstung für unverzichtbar, und ich hoffe, dass wir in nicht allzu ferner Zukunft noch viel mehr solcher wirksamen Mittel zur Verfügung haben.
Doch wenden wir uns nun unserem ersten taktischen Bereich zu: der sportlichen Betätigung. Genau wie »gesunde Lebenszeit« ist »sportliche Betätigung« einer dieser ägerlichen, viel zu weit gefassten Pauschalbegriffe, die alles beinhalten können, vom Spaziergang im Park bis zur schweißtreibenden Überquerung eines Gebirgspasses mit dem Fahrrad, einer Tennispartie oder dem Training im Fitnessstudio mit schweren Gewichten. All das zählt als »sportliche Betätigung«, hat aber offenkundig ganz unterschiedliche Effekte (und auch Risiken). Also unterteilen wir diesen Begriff in seine wichtigsten Komponenten: Kraft, Stabilität, aerobe Effizienz und maximale aerobe Kapazität. Wenn Sie Ihre Gesamtlebenszeit und gesunde Lebenszeit maximieren möchten, müssen Sie auch Ihre Leistungsgrenzen in jedem dieser Bereiche erweitern. Um es noch einmal zu sagen: Mein Ziel ist nicht, Ihnen zu erklären, wie Sie schnell abnehmen oder sich ein prächtiges Sixpack antrainieren können. Wir wollen Körperkraft, Kondition und Stabilität bei ganz unterschiedlichen Bewegungsabläufen aufrechterhalten und dabei frei von Schmerzen und Beeinträchtigungen bleiben.
Auch in dieser Hinsicht hat sich meine Einstellung mit der Zeit verändert. Für mich hatte die Ernährung früher oberste Priorität, aber was Gesamtlebenszeit und gesunde Lebenszeit betrifft, betrachte ich sportliche Betätigung heute als wirksamstes »Medikament« in unserer Langlebigkeitsapotheke. Die Daten sprechen eine eindeutige Sprache: Sportliche Betätigung schenkt uns nicht nur ein längeres Leben, sondern bewahrt uns auch vor geistigem wie körperlichem Verfall – besser als jede andere Maßnahme. Außerdem fühlen wir uns meist besser, wenn wir uns sportlich betätigen, was bedeutet, dass es vermutlich auch auf die seelische Gesundheit einen – wenn auch schwerer messbaren – Effekt hat. Ich hoffe, dass Sie nach der Lektüre des Buches nicht nur das Wie, sondern auch das Warum verschiedener Arten sportlicher Betätigung durchschauen, sodass Sie sich ein Programm erarbeiten können, das Ihren persönlichen Zielen entspricht.
Unser zweiter Bereich ist die Ernährung. Ich werde Ihnen nicht sagen, dass Sie dieses, aber nicht jenes essen sollten, oder Ihnen eine ganz bestimmte Diät vorschreiben, an die sich jeder zu halten hat, und ganz bestimmt ergreife ich nicht Partei für eine Seite in dem sinnlosen, nie endenden Wettstreit zwischen kohlenhydratarm versus Paleo versus vegan und so weiter und so fort. Wir verzichten auf diese religiösen Diskussionen und stützen uns stattdessen auf biochemische Fakten. Laut unseren besten wissenschaftlichen Erkenntnissen spielt es durchaus eine Rolle, was wir essen. Ausschlaggebend ist jedoch, wie viel wir essen – wie viele Kalorien wir unserem Körper zuführen.
Wie Sie hier den goldenen Mittelweg finden, hängt von zahlreichen Faktoren ab. Ich möchte Ihnen dabei helfen, das für Sie beste Ernährungsmuster zu finden. Denken Sie aber bitte daran, dass keine der hier diskutierten Taktiken in Stein gemeißelt ist. Wir werden möglichst viele Quellen heranziehen, um herauszufinden, was funktioniert und was nicht. Eine gute Strategie erlaubt das Verfolgen neuer und das Verwerfen alter Taktiken, falls es unseren Zielen dient.
Der nächste Bereich ist der Schlaf, den ich und viele andere viel zu lange außer Acht gelassen haben. Zum Glück schenkt man ihm seit etwa einem Jahrzehnt die Aufmerksamkeit, die er verdient. Heute verstehen wir sehr viel besser, wie wichtig er ist und was bei gestörtem Schlaf über kurz oder lang schiefläuft (Spoiler: eine Menge). Es gibt kaum etwas Besseres als das Gefühl, wenn man nach einer wunderbar durchgeschlafenen Nacht erfrischt und voller Tatendrang aufwacht. Guter Schlaf ist entscheidend für unsere angeborenen körperlichen Regenerationsprozesse, insbesondere im Gehirn, wohingegen schlechter Schlaf eine Kaskade negativer Folgen hat, von Insulinresistenz bis zu vermindertem geistigen Leistungsvermögen und psychischen Gesundheitsproblemen. Ich gehörte auch zu denjenigen, die gerne die Nächte durchmachten und meinten, Schlaf sei nur was für Leute, die nichts Besseres zu tun hätten. Um es kurz zu machen: Ich wurde auf äußerst dramatische Weise eines Besseren belehrt. Heute bin ich davon überzeugt, dass das größte Problem des vollschlanken Peter gar nicht war, was er aß, sondern wie wenig er schlief.
Zum Schluss erforschen wir die Bedeutung der seelischen Gesundheit, die eine, wie ich glaube, in jeder Hinsicht ebenso wichtige Komponente der gesunden Lebenszeit ist wie die anderen vier. In diesem Bereich verfüge ich zwar kaum über Expertenwissen, aber eine Menge persönlicher Erfahrung. Ich kann also nicht, wie in den übrigen Kapiteln, auf viele schlagkräftige experimentelle Daten und Studien verweisen, aber dafür berichte ich von meiner eigenen sehr langen und schmerzlichen Reise zur Bewältigung von Dingen, die mir in der Vergangenheit zugestoßen waren, und zum Kitten von Beziehungen, die ich zerstört hatte. Zumindest könnte das als abschreckendes Beispiel dienen – und als Anstoß für Sie, den Zustand Ihres Seelenlebens einer Prüfung zu unterziehen, falls dies notwendig ist.
In Kapitel 17 gehe ich ausführlich auf meine Reise ein. Eine Bemerkung aus dieser Zeit ist mir, fast wie ein Mantra, lebhaft in Erinnerung geblieben. Zu Beginn unserer gemeinsamen Arbeit sagte eine Therapeutin, Esther Perel, zu mir: »Ist es nicht paradox, dass sich Ihr ganzes Berufsleben darum dreht, Menschen zu einem längeren Leben zu verhelfen, und Sie dabei keinerlei Energie darauf verwenden, sich weniger elend zu fühlen, seelisch weniger zu leiden?«
Und dann fuhr sie fort: »Warum wollen Sie länger leben, wenn Sie so unglücklich sind?«
Ihre Logik war so stichhaltig, dass sie mein Denken über Langlebigkeit von Grund auf veränderte.
Von evidenzbasiert zu evidenzinformiert
Zweifellos ist es wichtig, dass unsere Strategie auf wissenschaftlichen Erkenntnissen beruht. Doch leider stößt das leistungsstärkste Instrument von Medizin 2.0, die randomisierte kontrollierte Studie, an ihre Grenzen, wenn es um das Streben nach Langlebigkeit geht. Mit randomisierten kontrollierten Studien bestimmt man Ursache und Wirkung in relativ unkomplizierten, kurzfristigen Situationen. So ist es ziemlich einfach, eine Studie durchzuführen, die nachweist, dass Sonnencreme einem Sonnenbrand vorbeugt. Bei unserer Suche nach Langlebigkeit sind solche Studien jedoch nur begrenzt nützlich.
In dieser Hinsicht haben einige Leute vielleicht Probleme mit meinem Ansatz. Die Puristen der evidenzbasierten Medizin verlangen Daten aus randomisierten kontrollierten Studien (RCTs), bevor sie überhaupt irgendetwas unternehmen. Diese Studien sind der Goldstandard medizinischer Evidenz, doch offenbaren sie auch gravierende Beschränkungen von Medizin 2.0, angefangen mit ihrem engen Horizont. Gemeinhin eignen sich RCTs am besten für klinische Fragen, die eng umrissene Interventionen wie einen Impfstoff oder ein Medikament zur Cholesterinsenkung betreffen. Diese Behandlungsstudien erstrecken sich über relativ kurze Zeiträume von sechs Monaten bis zu höchstens fünf oder sechs Jahren und sollen zeigen, welchen Effekt die Behandlung im Hinblick auf ein bestimmtes Ergebnis hat. Senkt der Impfstoff die Rate von schweren Erkrankungen und Todesfällen? Senkt das Medikament den Cholesterinspiegel und beugt bei stark gefährdeten Personen dem akuten Herztod oder zumindest Herzinfarkten vor?
Diese Art von Studie ist die Grundlage der evidenzbasierten Medizin. Wenn unser Ziel jedoch Langlebigkeit ist, wird die Situation komplizierter. Eine klinische Studie, die auf ein Jahr oder auch für fünf Jahre angelegt ist, wird uns nichts verraten, was wir über Krankheitsprozesse wissen müssen, deren Entwicklung sich über Jahrzehnte hinzieht. Es wird nie eine klinische Studie geben, die uns Anhaltspunkte für eine Präventionsstrategie für Herz-Kreislauf-Erkrankungen bei einem Vierzigjährigen gibt. Eine solche Studie würde schlicht zu lange dauern. Darüber hinaus sind die Interventionen außerhalb der Pharmakologie sehr komplex, vor allem wenn sie sportliche Betätigung, Ernährung und Schlaf betreffen. Langlebigkeit auf diese Weise zu erforschen ist praktisch unmöglich – es sei denn, wir könnten hunderttausend Babys nach dem Zufallsprinzip auf vier oder fünf Gruppen aufteilen, in denen jeweils eine andere Intervention untersucht wird, und sie ihr Leben lang unter Beobachtung stellen. Dann erhielten wir (hoffentlich) ein grundsolides, evidenzbasiertes Rezept für die Maximierung von Gesamtlebenszeit und gesunder Lebenszeit. Natürlich sind die Hindernisse für eine solche Untersuchung unüberwindbar – nicht zuletzt, weil sie ein ganzes Jahrhundert in Anspruch nehmen würde.
Option B lautet: Wir analysieren die verschiedenen Arten von Daten, die uns zur Verfügung stehen, und entwickeln daraus eine Strategie. Damit lässt sich das Problem vielleicht nicht endgültig lösen, aber es kann uns zumindest die Richtung weisen. Unsere Option-B-Strategie beruht auf der Kombination von Erkenntnissen aus fünf verschiedenen Datenquellen, die jede für sich genommen vermutlich nicht aussagekräftig genug sind. Gemeinsam können sie uns jedoch eine solide Grundlage für unsere Taktik bieten. An die Stelle des vormals ausschließlich evidenzbasierten Gefüges muss nun aber eine Präzisionsmedizin treten, die evidenzinformiert und risikoadjustiert ist, also patientenbezogene Risiken berücksichtigt.
Unsere erste Datenquelle sind Studien über Hundertjährige – Menschen, die, oft bei guter Gesundheit, hundert Jahre oder älter geworden sind. Das sind extreme Sonderfälle, eine winzige Bevölkerungsschicht, die unsere übliche Lebenserwartung um zwei oder mehr Jahrzehnte übererfüllt hat. Im Großen und Ganzen konnten diese Menschen die Krankheiten, die die meisten von uns töten, hinauszögern oder vermeiden. Uns würde interessieren, wie sie das geschafft haben. Was haben Hundertjährige gemeinsam? Welche Gene teilen sie, die ihnen möglicherweise einen Vorteil gegenüber den früher Sterbenden verschaffen? Was erklärt ihr Überleben und ihre anscheinend langsamere Alterung? Und vor allem: Was kann der Rest der Bevölkerung tun, um ihnen nachzueifern?
Diese Evidenz wird dadurch erhärtet, dass Hundertjährige der »zu untersuchenden Spezies« angehören – sie sind Menschen. Leider werden Daten über Hundertjährige fast nie aus Experimenten, sondern aus Beobachtung gewonnen, weshalb wir nicht eindeutig auf Ursache und Wirkung schließen können. Die Lebensgeschichten und Gewohnheiten von Hundertjährigen sind, gelinde gesagt, nicht deckungsgleich, und dass es relativ wenige von ihnen gibt, bedeutet, dass es schwierig sein kann, überhaupt irgendwelche gültigen Schlüsse zu ziehen. (Im nächsten Kapitel werden wir ausführlicher auf Hundertjährige eingehen.)
Als Nächstes betrachten wir Daten zur Gesamtlebenszeit von »Tiermodellen«, beispielsweise von Labormäusen. Offenkundig ist es aus ethischer und logistischer Sicht viel einfacher, Taktiken zur Veränderung der Gesamtlebenszeit an Mäusen zu testen, die üblicherweise nur etwa zwei oder drei Jahre alt werden. Es gibt haufenweise Daten über die Auswirkungen verschiedener Interventionen, sowohl hinsichtlich Nahrung als auch durch exogene Moleküle, auf die Gesamtlebenszeit von Mäusen. Hier gilt natürlich die Einschränkung, dass Mäuse keine Menschen sind. Viele Medikamente haben sich bei Mäusen als wirksam erwiesen, um dann bei Studien an Menschen spektakulär zu versagen. Es gibt noch andere Arten von Tiermodellen, darunter ein winziger Fadenwurm der Spezies C. elegans, der häufig zu Forschungszwecken untersucht wird, sowie Taufliegen, Hunde, Primaten und sogar simple Hefezellen. Sie alle haben Vor- und Nachteile. Meine Faustregel lautet, dass ich eine Intervention für bedeutsam erachte, wenn sie nachweislich die Gesamtlebenszeit oder gesunde Lebenszeit bei mehreren Arten verlängert, welche einen evolutionsgeschichtlichen Zeitraum von einer Milliarde Jahren abdecken, also zum Beispiel von Würmern bis zu Affen.
Eine dritte und bedeutende Informationsquelle zur Stützung unserer Strategie bieten an Menschen durchgeführte Studien über die apokalyptischen Reiter – Herz-Kreislauf-Erkrankungen einschließlich Herzinfarkt und Schlaganfall, die das Herz-Kreislauf-System oder die Blutgefäße im Gehirn betreffen, Krebs, Alzheimer und verwandte neurodegenerative Krankheiten sowie Typ-2-Diabetes und verwandte Stoffwechselstörungen. Wie beginnen diese Krankheiten? Wie schreiten sie fort? Welche Risikofaktoren sind an ihrer Entstehung beteiligt oder verstärken sie? Welche zugrunde liegenden Faktoren haben sie gemeinsam? Was sind die besten Behandlungsmethoden für Menschen mit »fortgeschrittenen« Erkrankungen – und wie helfen sie uns beim Entwickeln einer Präventionsstrategie? Wir wollen jede dieser Krankheiten in- und auswendig kennenlernen, ihre Schwachstellen und möglichen Angriffspunkte erforschen, so wie Ali seinen Gegner Foreman vor dem Kampf genau unter die Lupe genommen hat.
Viertens setzen wir uns mit den molekularen und mechanistischen Ergebnissen aus der Untersuchung des Alterns bei Menschen wie auch Tiermodellen auseinander. Wir haben bereits eine Menge über die Zellveränderungen herausgefunden, die beim Alterungsprozess und bei bestimmten Krankheiten auftreten. Aufgrund dessen wurden auch schon Ideen entwickelt, wie man diese Veränderungen, etwa durch exogene Moleküle (zum Beispiel Medikamente) oder Änderungen im Verhalten (zum Beispiel sportliche Betätigung), beeinflussen kann.
Unsere letzte Erkenntnisquelle ist ein ausgesprochen cleveres Analyseverfahren namens Mendelsche Randomisierung (MR). Die MR ist das Bindeglied zwischen randomisierten kontrollierten Studien, die kausale Zusammenhänge feststellen können, und reiner Epidemiologie, die das häufig nicht kann. Später werden wir uns noch ausführlicher mit Epidemiologie beschäftigen; in bestimmten Fällen, etwa beim Nachweis einer Verbindung zwischen Rauchen und Lungenkrebs, hat sie sich als nützlich erwiesen, doch in komplexeren Szenarien war ihr Nutzen geringer. Die Mendelsche Randomisierung hilft beim Bestimmen von Kausalbeziehungen zwischen veränderbaren Risikofaktoren (zum Beispiel LDL-Cholesterin) und einem zu untersuchenden Ergebnis (zum Beispiel Krebs) in Situationen, in denen sich herkömmliche randomisierte Experimente nicht gut durchführen lassen. Das gelingt ihr, indem sie es der Natur überlässt, die Randomisierung vorzunehmen.[19] Indem sie die zufällige Variation relevanter Gene berücksichtigt und sie mit den beobachteten Ergebnissen abgleicht, vermeidet sie viele Verzerrungen und Störfaktoren, die den Nutzen der reinen Epidemiologie beschränken.
So haben einige epidemiologische Studien ein umgekehrtes Verhältnis zwischen LDL-Cholesterin und dem Krebsrisiko nahegelegt. Das heißt, dass Personen mit einem niedrigeren LDL-Cholesterin-spiegel ein höheres Risiko aufweisen, an Krebs zu erkranken. Doch ist diese Beziehung kausal? Das ist eine komplizierte, aber wichtige Frage. Wenn es so wäre, würde das bedeuten, dass eine Senkung des LDL-Cholesterinspiegels, etwa durch Statine, das Krebsrisiko erhöht, was offensichtlich nicht gut wäre. Da uns die Epidemiologie nichts über die Richtung der Kausalität verrät, müssen wir die MR heranziehen.
Im Rahmen der MR können wir mit Genvarianten arbeiten, die einen niedrigen, einen mittleren oder einen hohen LDL-Cholesterinspiegel bewirken. Da diese Gene zufällig verteilt sind, dienen sie als Stellvertreter eines randomisierten natürlichen Experiments. Indem wir die Beziehung zwischen dem jeweils resultierenden LDL-Cholesterinspiegel und der Krebshäufigkeit untersuchen, können wir die üblichen Störfaktoren der traditionellen Epidemiologie ausklammern. Und siehe da, ein niedriger LDL-Cholesterinspiegel verursacht keinen Krebs und erhöht nicht das Krebsrisiko.[20] Untersuchen wir mit dem gleichen Verfahren die Auswirkung des LDL-Spiegels auf Herz-Kreislauf-Erkrankungen (unsere abhängige Variable), so stellen wir fest, dass höhere LDL-Cholesterinwerte tatsächlich eine Ursache für die Entwicklung von Herz-Kreislauf-Erkrankungen sind (wie wir in Kapitel 7 sehen werden).[21]
Aufmerksamen Lesern wird nicht entgangen sein, dass in diesem Kapitel nirgendwo von absoluter Sicherheit die Rede ist. Damit musste ich erst klarkommen, als ich von der Mathematik zur Medizin überwechselte – in der Biologie lässt sich nur selten etwas im mathematischen Sinne eindeutig »beweisen«. Lebende Systeme sind chaotisch und verwirrend und komplex, und selbst beim Durchschauen recht einfacher Dinge lernen wir pausenlos hinzu. Wir können bestenfalls darauf hoffen, unsere Unsicherheit zu reduzieren. Ein gutes biologisches Experiment erhöht oder verringert lediglich unser Vertrauen in die Wahrscheinlichkeit, dass unsere Hypothese wahr oder falsch ist. (Auch wenn wir uns einiger Dinge ziemlich sicher sein können – beispielsweise spricht vieles für die Richtigkeit der Hypothese, dass die Ärztin, die Sie operiert, gut daran tut, sich vorher die Hände zu waschen und sterile Handschuhe anzuziehen.)
In Ermangelung mehrfach wiederholter jahrzehntelanger randomisierter klinischer Studien, die eindeutige Antworten auf unsere Fragen geben könnten, müssen wir uns auf Wahrscheinlichkeiten und das Abwägen von Risiken beschränken. Das ähnelt ein wenig der Entwicklung einer Anlagestrategie: Wir suchen nach der Taktik, die nach unserem aktuellen Wissensstand mit der größten Wahrscheinlichkeit einen überdurchschnittlichen Kapitalertrag erbringt, während wir zugleich unsere individuelle Risikobereitschaft berücksichtigen. Die Größe des so gewonnenen Vorteils wird an der Wall Street als »Alpha« angegeben. Wir leihen uns dieses Konzept hier für unsere Zwecke aus und wenden es auf die Gesundheit an. Ich behaupte, dass Sie mit einigen unorthodoxen, aber äußerst plausiblen Veränderungen Ihres Lebensstils die schwerwiegendsten Bedrohungen für Ihre Gesamtlebenszeit und gesunde Lebenszeit minimieren und Ihr persönliches Maß an Langlebigkeits-Alpha erzielen können.
Ich möchte Sie hier mit einer Menge an Werkzeugen ausstatten, die Sie auf Ihre eigene persönliche Situation anwenden können – ganz gleich, ob Sie auf Ihre Glucoseregulation achten müssen oder auf Ihr Gewicht, Ihre Kondition, Ihr Risiko, an Alzheimer zu erkranken, oder anderes. Ihre persönliche Taktik sollte niemals starr sein, sondern sich nach Bedarf entwickeln, während Sie durch das Leben mit all seinen Unwägbarkeiten gehen – und während wir immer mehr über die Wissenschaft des Alterns und die Eigenschaften von Krankheiten wie Krebs erfahren. Ihre Taktik kann (und muss) sich mit Ihren persönlichen Lebensumständen verändern, denn wie schon der große Philosoph Mike Tyson gesagt hat: »Jeder hat einen Plan, bis er eins aufs Maul kriegt.«
Ein Rat, den George Foreman gut hätte gebrauchen können.
Teil II
Kapitel 4
Hundertjährige
Je älter Sie werden, desto gesünder waren Sie
Whiskey ist eine gute Medizin. Er hält die Muskeln geschmeidig.
Richard Overton, 1906–2018
Auf seine alten Tage ließ es sich Richard Overton gut gehen: Er genoss sein Gläschen Bourbon und paffte eine Tampa-Sweet-Zigarre, die er am Gasherd seines Hauses in Austin, Texas, anzündete. Er legte Wert darauf, dass er niemals inhalierte – ein guter Rat. Der Mann, den alle als Mr. Overton kannten, wurde während der Amtszeit von Theodore Roosevelt geboren und starb Ende 2018 mit hundertzwölf Jahren.
Kaum zu toppen ist die Erklärung des britischen Erste-Weltkriegs-Veteranen Henry Allingham, der meinte, er sei dank »Zigaretten, Whiskey und zügelloser Frauen« hundertdreizehn Jahre alt geworden.[22] Schade, dass er die abenteuerlustige Französin Jeanne Calment nicht kannte, die einmal scherzte: »Ich habe nur eine einzige Falte, und auf der sitze ich.«[23] Sie fuhr Rad, bis sie hundert war, und rauchte bis hundertsiebzehn. Vielleicht hätte sie damit nicht aufhören sollen, denn sie starb fünf Jahre später mit hundertzweiundzwanzig Jahren. Sie gilt als der Mensch mit der längsten Lebensspanne.
Die mit hundertsechs Jahren vergleichsweise jugendliche Mildred Bowers zog ein kaltes Bierchen vor; jeden Tag pünktlich um vier Uhr nachmittags ließ sie es ploppen – irgendwo auf der Welt ist es dann ja wohl fünf, nicht wahr?[24] Theresa Rowley aus Grand Rapids, Michigan, machte ihre tägliche Diät-Cola dafür verantwortlich, dass sie es auf hundertvier Jahre brachte, während Ruth Benjamin aus Illinois überzeugt war, dass sie ihren hundertneunten Geburtstag nur wegen ihrer täglichen Portion Schinkenspeck feiern konnte. »Und ein paar Kartoffeln«, fügte sie hinzu. Verglichen mit Emma Morano aus dem Piemont, die bis zu ihrem Tod mit hundertsiebzehn Jahren jeden Tag drei Eier verzehrte, zwei davon roh, waren die drei allerdings noch Jungspunde.
Wenn wir Epidemiologen vom Saturn wären und keine anderen Informationen über Hundertjährige hätten als Artikel in Tageszeitungen wie USA Today und Frauenmagazinen à la Good Housekeeping, könnten wir zu dem Schluss kommen, das Geheimnis eines langen Lebens sei ein opulentes Frühstück in einem Diner, hinuntergespült mit einem Whiskey und gefolgt von einer guten Zigarre. Vielleicht stimmt das sogar. Eine andere Möglichkeit ist, dass uns diese berühmten Hundertjährigen in die Irre führen. Es lässt sich nicht mit Gewissheit sagen, weil wir die entsprechenden Experimente nicht durchführen können, sosehr es mir auch gefallen würde, die Fachzeitschrift JAMA aufzuschlagen und die Überschrift »Verlängern gefüllte Schoko-Donuts das Leben? Eine randomisierte klinische Studie« zu lesen.
Wir alle wünschen uns, es möge so etwas wie ein Geheimnis für ein längeres, gesünderes, glücklicheres Leben geben. Dieser Wunsch steht hinter dem großen Interesse zu erfahren, welche speziellen Gewohnheiten und Rituale diese extrem langlebigen Menschen pflegten. Menschen wie Madame Calment, die das Rendezvous mit Gevatter Tod hinausschieben konnten, obwohl sie ihr Leben lang geraucht haben oder andere schlimme Dinge taten, faszinieren uns. Lag es bei ihr am Radfahren? Oder hat es einen anderen Grund, etwa das Pfund Schokolade, das sie angeblich pro Woche zu verzehren pflegte?
Es lohnt sich, die etwas allgemeiner gefasste Frage zu stellen: Was haben gesunde Hundertjährige gemeinsam? Und, noch wichtiger, was können wir eventuell von ihnen lernen? Leben sie wegen oder trotz ihrer speziellen Verhaltensweisen wie Whiskeytrinken länger? Gibt es einen anderen gemeinsamen Faktor, der ihre Langlebigkeit erklärt, oder ist es einfach Glück?
Ernst zu nehmende Forschungen an großen Gruppen von Hundertjährigen ließen (weitere) Zweifel daran aufkommen, dass eine »gesunde« Lebensweise (ich kann mir die Anführungszeichen nicht verkneifen) nötig ist, um das Leben deutlich zu verlängern. Eine große Studie mit hundertjährigen aschkenasischen Juden, durchgeführt von Nir Barzilai am Albert Einstein College of Medicine in der Bronx, ergab, dass diese Menschen kein bisschen gesundheitsbewusster waren als alle anderen.[25] Vielleicht sogar im Gegenteil: Ein großer Teil dieser 500 Personen umfassenden Gruppe trank Alkohol und rauchte, manchmal schon über Jahrzehnte hinweg. Die männlichen Hundertjährigen der Einstein-Studie hatten im Alter von siebzig Jahren im Schnitt mit einer geringeren Wahrscheinlichkeit regelmäßig Sport getrieben als gleichaltrige Kontrollpersonen. Und viele waren übergewichtig. So viel zu einem gesunden Lebensstil.
Könnten die Hundertjährigen schlicht Glück gehabt haben? Allein ihr Alter macht sie zu extremen statistischen Ausreißern. Im Jahr 2021 lebten dem Census Bureau zufolge knapp unter 100 000 Hundertjährige in den Vereinigten Staaten.[26] Obwohl deren Zahl in gerade einmal zwanzig Jahren um 50 Prozent gestiegen ist, macht die Gruppe der über Hundertjährigen immer noch nicht mehr als 0,03 Prozent der Bevölkerung aus – oder einer von 3333 US-Amerikanern.
Nach zehn Jahrzehnten wird die Luft ziemlich schnell ziemlich dünn. Diejenigen, die es bis zu ihrem hundertzehnten Geburtstag schaffen, qualifizieren sich für den ruhmreichen Elitekader der »Supercentenarians«, die kleinste Altersgruppe, die weltweit zu jeder Zeit nur etwa dreihundert Mitglieder umfasst (wobei die Zahl schwanken kann). Um Ihnen einen Eindruck von der Exklusivität dieses Klubs zu geben: Auf jeden Supercentenarian kommen derzeit etwa neun Milliardäre.
Und doch hat bis jetzt noch niemand Jeanne Calments Rekord erreicht. Am nächsten herangekommen ist nachweislich die in Pennsylvania geborene Sarah Knauss; sie starb 1999 mit gerade hundertneunzehn Jahren. Seitdem wurde der älteste Mensch der Welt nur noch selten älter als hundertsiebzehn Jahre, und meistens handelte es sich dabei um eine Frau. Zwar gibt es immer wieder Personen, die behaupten, hundertvierzig Jahre oder älter zu sein, aber Jeanne Calment ist nach wie vor die Einzige, für die eine Lebensspanne von mehr als hundertzwanzig Jahren belegt ist. Das lässt einige Forschende vermuten, dass es sich dabei um die in den Genen verankerte Obergrenze für die menschliche Lebenserwartung handeln könnte.
Uns interessiert jedoch eine etwas andere Frage: Was versetzt manche Menschen in die Lage, die Achtzig-Jahr-Marke, die für die meisten von uns die Ziellinie darstellt, so locker zu überschreiten? Könnte ihre außergewöhnliche Langlebigkeit – und ihre außergewöhnliche Gesundheit bis ins hohe Alter – zuallererst eine Funktion ihrer Gene sein?
Studien mit skandinavischen Zwillingen ergaben, dass die Gene vermutlich nur für 20 bis 30 Prozent der Gesamtvariation in der menschlichen Lebensdauer verantwortlich sind.[27] Der Haken: Je älter man wird, desto größer die Rolle der Gene. Bei Hundertjährigen spielen sie eine sehr große Rolle. Wenn Sie die Schwester eines Hundertjährigen sind, verachtfacht sich die Wahrscheinlichkeit, dass Sie selbst dieses Alter erreichen.[28] Bei Brüdern von Hundertjährigen steigt die Wahrscheinlichkeit, selbst den hundertsten Geburtstag zu feiern, um das Siebzehnfache. Das legen die Daten der tausend Personen umfassenden New England Centenarian Study nahe, die seit 1995 extrem langlebige Individuen erfasst. (Da diese Personen in denselben Familien aufwuchsen und vermutlich ähnliche Gewohnheiten und Lebensweisen pflegten, könnte das Ergebnis in gewissem Umfang auch auf bestimmte Umweltfaktoren zurückzuführen sein.) Wenn Sie nicht mit hundertjährigen Geschwistern aufwarten können, ist die nächstbeste Möglichkeit, sich langlebige Eltern zu suchen.
Das ist einer der Gründe, weshalb ich bei Gesprächen mit meinen Patienten so großen Wert auf eine ausführliche Familiengeschichte lege: Ich muss wissen, wann und woran ihre nahen Verwandten gestorben sind. Was sind, genetisch gesehen, die möglichen »Eisberge«? Meine herzlichsten Glückwünsche, wenn Sie Hundertjährige in Ihrem Familienstammbaum haben. Solche Gene sind so etwas wie geerbtes Glück. In meiner eigenen Familie war man froh, wenn man das Rentenalter erreichte. Wenn Sie sind wie ich und die meisten anderen Leute, die dieses Buch lesen, dann werden Ihre Gene Sie vermutlich nicht allzu weit bringen. Warum also sollten wir uns überhaupt mit diesem Thema befassen?
Weil wir einer wesentlich wichtigeren Frage nachgehen wollen: Können wir – durch unser Verhalten – auf irgendeine Weise dieselben positiven Ergebnisse erzielen, die Hundertjährige über ihre Gene quasi umsonst erhalten? Oder etwas technischer formuliert: Können wir den Phänotyp von Hundertjährigen imitieren, die physischen Eigenschaften, die es ihnen ermöglichen, Krankheiten zu widerstehen und so lange zu leben, selbst wenn wir nicht ihren Genotyp besitzen?
Wenn diese Frage mit »Ja« beantwortet werden kann, wovon ich überzeugt bin, dann ist es ein lohnendes Unterfangen herauszufinden, wie das »Innenleben« dieser Gewinner der statistischen Langlebigkeitslotterie funktioniert, und darauf eine Strategie aufzubauen.
Als ich anfing, mich für Langlebigkeit zu interessieren, war meine größte Angst, wir könnten herausfinden, wie man den Tod hinausschiebt, ohne gleichzeitig die gesunde Lebensspanne der Menschen zu vergrößern – à la Tithonos (und à la Medizin 2.0). Mein Fehler war zu glauben, dass dies bereits jetzt das Schicksal der Hochbetagten ist und dass sie alle mehr oder weniger dazu verdammt sind, ihre Extrajahre in Pflegeheimen oder anderen Formen der Langzeitpflege zu verbringen.
Ein genauerer Blick auf die Daten einer Vielzahl großer Studien zu Hundertjährigen überall auf der Welt führt zu einem hoffnungsfroheren Bild. Es ist richtig, dass viele Hundertjährige gebrechlich und stärker gefährdet sind: Die Gesamtsterberate für Amerikaner im Alter von hundert und mehr Jahren liegt bei frappierenden 36 Prozent, das heißt, wenn Oma hunderteins ist, hat sie eine Chance von eins zu drei, in den nächsten zwölf Monaten zu sterben.[29] Der Tod klopft an ihre Tür. Wenn man noch tiefer gräbt, stellt man fest, dass viele der ältesten Alten aufgrund von Lungenentzündungen und anderen opportunistischen Infektionen aus dem Leben scheiden und nur wenige Hundertjährige, wie etwa Madame Calment, wirklich aufgrund ihres hohen Alters sterben. Doch die weitaus meisten fallen den Alterskrankheiten – den apokalyptischen Reitern des Alterns – zum Opfer, so wie wir anderen auch.
Der entscheidende Unterschied besteht darin, dass sie diese Krankheiten sehr viel später im Leben entwickeln als wir – wenn sie sie denn überhaupt bekommen. Wir sprechen hier nicht über zwei, drei oder fünf Jahre, wir sprechen von Jahrzehnten. Thomas Perls und seine Kollegen an der Boston University, die die New England Centenarian Study durchführen, fanden heraus, dass in der allgemeinen Bevölkerung im Schnitt eine von fünf Personen bis zum Alter von zweiundsiebzig Jahren eine Krebsdiagnose erhält.[30] In der Gruppe der Hundertjährigen wird diese Eins-zu-fünf-Schwelle erst mit hundert Jahren erreicht, das heißt fast drei Jahrzehnte später. Ganz ähnlich ist die Situation bei Herz-Kreislauf-Krankheiten: Bis zum Alter von fünfundsiebzig Jahren wurde diese Diagnose (mit klinischen Symptomen) bei einem Viertel der allgemeinen Bevölkerung gestellt, bei den Hundertjährigen wird diese Prävalenz erst mit zweiundneunzig erreicht. Dasselbe Muster gilt für Knochenschwund (Osteoporose), der Hundertjährige sechzehn Jahre später trifft als den Durchschnittsmenschen, sowie für Schlaganfall, Demenz und Bluthochdruck: Hundertjährige bekommen diese Krankheiten – wenn überhaupt – erst viel später.
Doch ihre Langlebigkeit ist nicht allein eine Folge aufgeschobener Krankheiten. Diese Menschen trotzen zudem oft dem Klischee vom hohen Lebensalter als einer Phase von Leiden und Verfall. Perls, Barzilai und andere Forscher beobachteten, dass Hundertjährige häufig in einem ziemlich guten gesundheitlichen Gesamtzustand sind – was nicht dem entspricht, was man erwarten würde. Natürlich heißt das nicht, dass jeder, der so lange lebt, Golf spielt oder Fallschirm springt, aber Perls’ 95-plus-Studienteilnehmer schnitten bei Standardtests für kognitive Funktionen und Fähigkeiten sehr gut ab, Tests, in denen es um Dinge des täglichen Lebens geht (wir haben in Kapitel 3 darüber gesprochen), wie die Zubereitung von Mahlzeiten oder das Schneiden der Zehennägel, etwas, das einfach aussieht, aber mit zunehmendem Alter immer schwerer fällt.
Seltsamerweise schneiden Männer sowohl bei den kognitiven als auch bei den funktionellen Tests besser ab, obwohl es unter den Hundertjährigen viermal mehr Frauen als Männer gibt. Auf den ersten Blick wirkt das paradox, da Frauen im Schnitt eindeutig länger leben als Männer. Perls glaubt, dass es hier eine Art Ausleseprozess gibt, denn Männer erleiden in ihren mittleren Jahren eher Herzinfarkte und Schlaganfälle als Frauen, bei denen sich die Empfänglichkeit dafür ein oder zwei Jahrzehnte nach hinten verlagert und die auch seltener an diesen Erkrankungen sterben.
Auf diese Weise werden anscheinend die anfälligeren Individuen aus der männlichen Bevölkerung ausgesiebt, sodass nur diejenigen Männer mit einer relativ robusten Gesundheit es auch bis zu ihrem hundertsten Geburtstag schaffen, während Frauen anscheinend mit altersbedingten Erkrankungen und Einschränkungen länger überleben können. Perls nennt es »ein zweischneidiges Schwert«, dass Frauen länger leben, aber oft bei schlechterer Gesundheit.[31] »Männer sind häufig besser in Form«, sagt er. (Die Autoren haben es nicht gemessen, aber ich vermute mal, dass es damit zu tun hat, dass Männer im Schnitt mehr Muskelmasse besitzen, und die weist eine starke Korrelation mit einer höheren Lebenserwartung und besseren Körperfunktionen auf, wie wir in den Sportkapiteln noch sehen werden.)
Selbst wenn sie in ihrem elften Lebensjahrzehnt nicht in so guter Form sind, haben diese Individuen – verglichen mit dem Rest der Bevölkerung – doch bereits viele Extrajahre in Gesundheit genossen. Ihre gesunde Lebenszeit war, ebenso wie ihre Gesamtlebenszeit, außerordentlich lang. Was noch überraschender ist: Perls’ Arbeitsgruppe stellte fest, dass sich die Supercentenarians und die »Semisupercentenarians« (Alter zwischen hundertfünf und hundertneun Jahren) tatsächlich einer noch besseren Gesundheit erfreuen als die gewöhnlichen Hundertjährigen. Sie sind die Super-Überlebenskünstler, und in diesem hohen Alter sind Gesamtlebenszeit und gesunde Lebenszeit ziemlich dasselbe. Perls und seine Kollegen formulierten es für eine Artikel-Überschrift so: »The Older You Get, the Healthier You Have Been« (»Je älter Sie werden, desto gesünder waren Sie«).[32]
Mathematisch ausgedrückt sorgen die Gene der Hundertjährigen bei ihren Trägern für eine Phasenverschiebung auf der Lebenszeitachse, das heißt, die Kurven für die Gesamtlebenszeit wie auch die gesunde Lebenszeit werden um ein, zwei (oder drei!) Jahrzehnte nach rechts verschoben. Diese Menschen leben nicht nur länger als ihre Altersgenossen, sie sind auch praktisch ihr Leben lang gesünder und biologisch jünger als diese. Mit sechzig hatten sie die Herzkranzgefäße von Fünfunddreißigjährigen. Mit fünfundachtzig sahen sie vermutlich aus, als seien sie in ihren Sechzigern, sie fühlten sich auch so, und ihre Körperfunktionen waren entsprechend. Sie machten den Eindruck, als seien sie eine Generation jünger, als das Geburtsdatum in ihrem Ausweis behauptete. Diesen Effekt wollen wir versuchen nachzuahmen.
Erinnern Sie sich? In Kapitel 3 haben wir im Zusammenhang mit der Grafik zu Gesamtlebenszeit und gesunder Lebenszeit die Begriffe »Randdekade« und »Bonusdekade« eingeführt. Da Medizin 2.0 die Gesamtlebenszeit oft in eine Lebensphase mit schlechter Gesundheit verlängert, vergrößert sie damit das »Morbiditätsfenster«, die Phase von Krankheiten und Beeinträchtigungen am Ende des Lebens. Menschen sind länger krank, bevor sie sterben. Sie verbringen ihre Randdekade überwiegend als Patienten. Wenn Hundertjährige sterben, dann sind sie in der Regel (wenn auch nicht immer) vorher sehr viel weniger lang krank oder stark beeinträchtigt gewesen als Personen, die zwei oder drei Jahrzehnte früher sterben. Der englische Fachbegriff dafür ist compression of morbidity, er bezeichnet das Verdichten und Verkürzen der Zeit des körperlichen Verfalls am Ende des Lebens und die Verlängerung der gesunden Lebenszeit.
Eines der Ziele von Medizin 3.0 ist es, den Menschen dabei zu helfen, ein Leben zu leben, das mehr dem von Hundertjährigen ähnelt, nur besser. Hundertjährige leben nicht nur länger, sondern auch bei besserer Gesundheit, was zur Folge hat, dass viele von ihnen in den Genuss von ein, zwei oder drei Bonusdekaden kommen. Mit neunzig sind sie oft gesünder als Durchschnittsmenschen in ihren Sechzigern. Wenn bei ihnen der körperliche Verfall einsetzt, ist er in der Regel kurz. Das ist es, was wir für uns wollen: länger leben mit einem gut funktionierenden Körper und ohne chronische Krankheiten und einer kürzeren Krankheitsphase am Ende unseres Lebens.
Was uns Durchschnittsmenschen von den Hundertjährigen unterscheidet, ist, dass wir versuchen müssen, Langlebigkeit und gute Gesundheit durch eigenes Zutun zu erreichen, während diese mehr oder weniger zufällig durch Glück und/oder Gene damit gesegnet zu sein scheinen. Das bringt uns zu den zwei nächsten Fragen: Wie verzögern oder vermeiden Hundertjährige chronische Krankheiten? Und wie können wir das ebenfalls erreichen?
An dieser Stelle kommen nun die Gene ins Spiel – die Langlebigkeitsgene, die die meisten von uns nicht besitzen, weil wir es versäumt haben, uns die richtigen Eltern auszusuchen. Aber wir können spezifische Gene identifizieren, die Hundertjährige zu ihrem Vorteil verhelfen, und vielleicht gelingt es uns, ihren Phänotyp, also das, was diese Gene bewirken, zu rekonstruieren.
Man könnte das für eine relativ einfache Aufgabe halten: Sequenziert das Genom von ein paar Tausend Hundertjährigen und schaut, welche Gene oder Genvarianten in dieser Gruppe häufiger vorkommen als in der allgemeinen Bevölkerung. Das wären dann die Kandidaten für unsere Suche nach Langlebigkeitsgenen. Doch als Forscher das taten und Tausende von Individuen mit genomweiten Assoziationsstudien untersuchten, kam so gut wie nichts heraus. Diese Personen schienen genetisch nur sehr wenig gemeinsam zu haben. Und ihre Langlebigkeit könnte doch nichts weiter als unverdientes Glück gewesen sein.
Warum sind Langlebigkeitsgene so schwer zu fassen? Und warum gibt es überhaupt nur so wenige Hundertjährige? Das hängt mit der natürlichen Selektion zusammen.
Moment mal, könnten Sie jetzt sagen. Haben wir nicht immer eingebläut bekommen, dass wir von Evolution und natürlicher Selektion im Laufe von Millionen von Jahren ständig weiter optimiert wurden, indem schlechte Gene aussortiert und gute Gene bevorzugt wurden – survival of the fittest und so. Also warum haben wir dann nicht alle die lebensverlängernden Gene der Hundertjährigen? Warum sind wir nicht »fit« genug, um hundert zu werden?
Die kurze Antwort lautet: Der Evolution ist es ziemlich egal, wie alt wir werden. Durch die natürliche Selektion wurden wir mit Genen ausgestattet, die uns ganz wunderbar dabei helfen, erwachsen zu werden, uns fortzupflanzen, unseren Nachwuchs und vielleicht auch den unserer Kinder (mit) großzuziehen. So gelangen die meisten von uns noch in relativ guter körperlicher Verfassung in ihr fünftes Lebensjahrzehnt. Danach geht es dann allerdings bergab. Der evolutionäre Grund dafür ist, dass die natürliche Selektion nach der reproduktiven Phase deutlich an Kraft verliert. Gene, die in der Mitte des Lebens oder noch später von Nachteil sind oder vielleicht sogar schaden, werden nicht herausselektioniert, weil sie bereits an die nächste Generation weitergegeben wurden. Nehmen wir ein augenfälliges Beispiel: das Gen (oder die Gene), das für den sogenannten androgenetischen Haarausfall (»Glatze«) bei Männern verantwortlich ist. Wenn wir jung sind, haben wir volles, glänzendes Haar, es trägt zu unserer Attraktivität für mögliche Partnerinnen bei. Aber die natürliche Selektion juckt es herzlich wenig, ob ein Mann (oder auch eine Frau) mit Mitte fünfzig noch im Besitz einer üppigen Haarpracht ist.
Zu meinem Glück ist Haarausfall nicht relevant für die Langlebigkeit. Aber dieses bekannte Phänomen erklärt auch, weshalb Gene, die eine Prädisposition für Alzheimer oder andere später im Leben auftretende Erkrankungen bedeuten, nicht aus unserem Genpool verschwunden sind. Kurz gesagt, für die natürliche Selektion spielt es keine Rolle, ob wir im Alter Alzheimer (oder Haarausfall) bekommen. Beides hat keinen Einfluss auf unsere reproduktive Fitness. Zu der Zeit, wenn sich Demenz bemerkbar macht, haben wir unsere Gene längst weitergegeben. Dasselbe gilt für Gene, die das Risiko für Herz-Kreislauf-Erkrankungen oder Krebs in der Lebensmitte erhöhen. Die meisten von uns tragen diese miesen Gene in sich – im Übrigen auch manche Hundertjährige. Möglicherweise haben uns einige dieser Gene früher im Leben sogar gewisse Vorteile verschafft; dieses biologische Phänomen heißt »antagonistische Pleiotropie«.
Eine plausible Theorie besagt, dass Hundertjährige so lange leben, weil sie bestimmte andere Gene besitzen, die sie vor genetischen »Schwachstellen« schützen, die typischerweise in unserem Erbgut vorkommen, zum Beispiel Gene, die Herz-Kreislauf-Erkrankungen und Krebs verhindern oder hinauszögern oder die ihre kognitiven Fähigkeit noch Jahrzehnte aufrechterhalten, während diese bei anderen verloren gehen. Doch selbst wenn es die natürliche Selektion schädlichen Genen erlaubt, sich im Alter zu entfalten, tut sie umgekehrt nichts, um hilfreiche, das Leben verlängernde Gene zu fördern, und zwar aus denselben Gründen. So kommt es, dass anscheinend keine zwei Hundertjährigen auf demselben genetischen Pfad ins Reich der Hochbetagten gelangen. Es gibt viele Wege zur Langlebigkeit, nicht nur einen oder zwei.
Nichtsdestoweniger hat sich in verschiedenen Studien eine Handvoll potenzieller Langlebigkeitsgene herauskristallisiert, und wie sich zeigt, könnten einige davon möglicherweise für unsere Strategie relevant sein. Eines der wirkmächtigsten Einzelgene, das bis jetzt entdeckt wurde, steht mit dem Cholesterinstoffwechsel und mit dem Glucosestoffwechsel in Beziehung – und mit dem Risiko, an Alzheimer zu erkranken.
Vielleicht haben Sie schon einmal davon gehört. Das Gen heißt ApoE und codiert ein Eiweiß (Apolipoprotein E, abgekürzt ApoE), das unter anderem am Transport und an der Verarbeitung von Cholesterin beteiligt ist. Von diesem Gen gibt es drei Varianten (Allele): ε2, ε3 und ε4. Am häufigsten kommt die Variante ε3 vor, doch wenn jemand ein oder zwei Kopien der Variante ε4 hat, scheint sich das Risiko, an Alzheimer zu erkranken, um den Faktor zwei bis zwölf zu erhöhen.[33] Aus diesem Grund teste ich alle meine Patienten auf ihren ApoE-Genotyp. In Kapitel 9 kommen wir darauf zurück.
Die ε2-Variante von ApoE andererseits scheint ihre Träger vor Demenz zu schützen – und sie steht offenbar in einem sehr engen Zusammenhang mit der Langlebigkeit. Eine Meta-Analyse aus dem Jahr 2019, die sieben verschiedene Langlebigkeitsstudien mit insgesamt fast 30 000 Teilnehmern zusammen auswertete, ergab, dass Personen, die mindestens eine Kopie der ε2-Variante des ApoE-Gens trugen (und keine ε4), eine 30 Prozent höhere Wahrscheinlichkeit hatten, ein sehr hohes Alter zu erreichen (definiert als siebenundneunzig Jahre für Männer und hundert Jahre für Frauen), als Menschen mit der Standardkombination ε3/ε3.[34] Inzwischen weiß man, ebenfalls aus dieser Analyse, dass Personen mit zwei Kopien von ε4 (eine von jedem Elternteil) eine 81 Prozent geringere Wahrscheinlichkeit haben, so lange zu leben. Das ist eine ziemliche Kehrtwende.
Auf die Funktion des Apolipoproteins E werden wir in Kapitel 9 noch ausführlich eingehen, doch für unsere Strategie ist es vermutlich in vielerlei Hinsicht von Bedeutung. Zuerst und ganz offensichtlich scheint es – in Abhängigkeit von der Variante – eine Rolle für das Verzögern (oder Nichtverzögern) des Beginns der Alzheimer-Krankheit zu spielen. Das ist wahrscheinlich kein Zufall, denn wie wir noch sehen werden, ist ApoE maßgeblich am Transport von Cholesterin durch unseren Körper und insbesondere im Gehirn beteiligt. Welche ApoE-Genvariante man trägt, hat auch großen Einfluss auf den Glucosestoffwechsel. Wegen seiner starken Korrelation mit der Langlebigkeit sollten wir unsere Bemühungen auf die kognitive Gesundheit konzentrieren und Themen rund um Cholesterin und Lipoproteine (die Moleküle, die Cholesterin transportieren und über die wir in Kapitel 7 sprechen) sowie den Glucosestoffwechsel besondere Aufmerksamkeit schenken (Kapitel 6).
Forscher haben zwei weitere Gene identifiziert, CETP und ApoC3, die sowohl mit Cholesterin zu tun haben als auch eine Korrelation mit extremer Langlebigkeit aufweisen (was vielleicht erklärt, weshalb Hundertjährige selten an Herz-Kreislauf-Erkrankungen sterben). Doch es ist unwahrscheinlich, dass ein einzelnes Gen (oder auch drei Dutzend Gene) alleine für die extreme Lebensdauer und die ausgezeichnete Gesundheit der Hundertjährigen verantwortlich ist. Breit angelegte genetische Studien legen nahe, dass möglicherweise Hunderte, wenn nicht gar Tausende von Genen involviert sein könnten, wobei jedes einzelne nur einen kleinen Beitrag leistet. So etwas wie das perfekte Genom für ein sehr langes Leben gibt es vermutlich nicht.
Für diejenigen unter uns, die in ihrem Familienstammbaum keine Hundertjährigen vorweisen können, ist das eigentlich eine gute Nachricht, denn es bedeutet, dass es selbst auf dieser genetischen Ebene keine allgemeingültige Lösung gibt; selbst für Hundertjährige könnte Langlebigkeit ein Spiel sein, bei dem jeder Zentimeter Boden zählt, den man gutmachen kann. Kleinere Interventionen, deren Effekte sich summieren, könnten uns dabei helfen, die längere Gesamtlebenszeit und gesunde Lebenszeit der Hundertjährigen nachzuahmen. Andersherum gesagt, wenn wir unsere Lebenserwartung übertreffen und länger besser leben wollen, müssen wir hart arbeiten, um uns das zu verdienen – mit kleinen Veränderungen, die sich aufsummieren.
In den zahlreichen, weltweit durchgeführten Studien zu Hundertjährigen ist noch ein anderer Kandidat für ein Langlebigkeitsgen aufgetaucht, der möglicherweise ebenfalls Hinweise für unsere Strategie liefern könnte. Es handelt sich um Varianten eines Gens namens FOXO3, die einen direkten Bezug zur Langlebigkeit zu haben scheinen.
Bradley Willcox von der University of Hawaii und Kollegen berichteten im Jahr 2008 über eine Langzeitstudie zu Gesundheit und Langlebigkeit an hawaiianischen Männern japanischer Abstammung: Ihre genetischen Analysen hatten ergeben, dass drei FOXO3-Varianten (sogenannte SNPs, Single Nucleotide Polymorphism, Varianten, die sich nur in einem Basenpaar unterscheiden) eine starke Assoziation mit gesundem Altern und Langlebigkeit aufwiesen.[35] Mehrere danach durchgeführte Studien fanden verschiedene andere langlebige Populationen, die offenbar ebenfalls über FOXO3-Mutationen verfügen, darunter Kalifornier, Neuengländer, Dänen, Deutsche, Italiener, Franzosen, Chinesen und amerikanische aschkenasische Juden, und so wird FOXO3 zu einem der wenigen potenziellen Langlebigkeitsgene, die in einer Vielzahl ethnischer Gruppen in vielen verschiedenen Regionen der Erde gefunden wurden.[36]
Das von FOXO3 codierte Protein gehört zu einer Familie sogenannter Transkriptionsfaktoren, die regeln, wie andere Gene exprimiert, also an- oder abgeschaltet werden. Für mich ist es so etwas wie die Instandhaltungsabteilung der Zelle. Es ist für vieles zuständig, unter anderem für verschiedene Reparaturarbeiten in Zellen, für die Steuerung des Stoffwechsels, für den Nachschub an Stammzellen und was sonst noch im »Haushalt« anliegt, etwa die Entsorgung von zellulärem Abfall. Allerdings erledigt es die einzelnen Tätigkeiten – Wischen, Schrubben, Wändeausbessern – nicht selbst, sondern delegiert die Arbeit an andere, spezialisiertere Gene, an Subunternehmer, wenn Sie so wollen. Sobald das FOXO3-Gen aktiviert ist, aktiviert es seinerseits Gene, die im Allgemeinen dafür sorgen, dass unsere Zellen gesund bleiben. Es scheint auch eine bedeutende Rolle dabei zu spielen, die Entstehung von Krebszellen aus gesunden Zellen zu verhindern.
An dieser Stelle taucht ein erster Hoffnungsschimmer auf, denn das FOXO3-Gen kann durch unser Verhalten aktiviert oder unterdrückt werden. Beispielsweise wird die Aktivität von FOXO3 etwas hochgefahren, wenn die Nährstoffe knapp sind oder wenn wir Sport treiben. Hier können wir ansetzen.
Die Genexpression selbst scheint – auch über FOXO3 hinaus – für die Langlebigkeit eine wichtige, wenn auch immer noch wenig verstandene Rolle zu spielen. Eine genetische Analyse von spanischen Hundertjährigen stellte fest, dass diese extrem jugendliche Genexpressionsmuster aufwiesen: Sie ähnelten mehr den Expressionsmustern von Kontrollpersonen in den Zwanzigern als denen von Kontrollpersonen in den Achtzigern.[37] Wie genau diese Hundertjährigen das bewerkstelligten, ist unklar, es könnte mit FOXO3 zusammenhängen – oder mit einem anderen, noch unbekannten Faktor, der die Genexpression reguliert.
Im Hinblick auf die Genetik hinter der Langlebigkeit haben wir immer noch mehr Fragen als Antworten, aber wenigstens ein paar hoffnungsvolle Hinweise. Während unser Genom als solches unveränderlich ist – zumindest in der nahen Zukunft –, kann die Genexpression durch Umwelt und Verhalten beeinflusst werden. Eine im Jahr 2007 durchgeführte Studie zeigte zum Beispiel, dass ältere Menschen, die ein regelmäßiges sportliches Trainingsprogramm aufgenommen hatten, nach sechs Monaten jugendlichere Genexpressionsmuster aufwiesen.[38] Das legt den Schluss nahe, dass beides, Genetik und Umwelt, für die Langlebigkeit eine Rolle spielen und dass es vielleicht möglich ist, Veränderungen herbeizuführen, die das »genetische Glück« der Hundertjährigen zumindest teilweise nachahmen.
Ich finde es hilfreich, Hundertjährige als Ergebnis eines natürlichen Experiments zu betrachten, aus dem wir etwas Wichtiges über ein längeres und besseres Leben lernen können. Nur dass in diesem Fall Darwin und Mendel (die Entdecker der natürlichen Selektion bzw. der Vererbungsregeln) die Wissenschaftler sind. Dieses Experiment beinhaltet eine Zufallsauswahl menschlicher Genome, die verschiedenen Umweltbedingungen und individuellen Verhaltensweisen ausgesetzt werden. Die Hundertjährigen besitzen die richtige Genkombination X, die sie brauchen, um in einer Umwelt Y (vielleicht mithilfe von Verhaltensweisen Z) zu überleben. Das Experiment ist nicht einfach, wahrscheinlich gibt es viele verschiedene Wege – genetische und andere – zur Langlebigkeit.
Es liegt auf der Hand, dass die meisten von uns mit Unarten wie jahrzehntelangem Rauchen und Trinken, denen einige Hundertjährige frönen, nicht durchkommen. Aber selbst wenn wir ihre »Taktiken« nicht imitieren (und in vielen Fällen wäre es besser, es nicht zu tun), könnte es dennoch hilfreich sein, für unsere eigene Strategie auf die Hundertjährigen zu schauen. Das, was sie so stark macht, ist ihre Fähigkeit, chronische Krankheiten zu vermeiden oder um ein, zwei oder sogar drei Jahrzehnte hinauszuzögern, und dabei einen relativ guten Gesundheitszustand zu behalten.
Diese Phasenverschiebung wollen wir erreichen. Aber mit Medizin 2.0 werden wir das nicht schaffen, da die sich fast ausschließlich darauf konzentriert, uns ein längeres Leben mit Krankheiten zu ermöglichen. Ihre Interventionen kommen fast immer zu spät, nämlich dann, wenn die Krankheiten bereits eingetreten sind. Wir müssen das andere Ende der Zeitachse in den Blick nehmen und versuchen, Krankheiten zu verhindern, bevor sie beginnen, oder sie nach hinten zu verschieben. Das muss im Mittelpunkt des Interesses stehen, nicht das Verlängern der Krankheitsdauer – und das nicht nur bei einer Erkrankung, sondern bei allen chronischen Krankheiten. Unser Ziel ist es, ohne Krankheiten länger zu leben.
Das führt uns zu einem anderen Fehler von Medizin 2.0, nämlich dass sie diese Erkrankungen im Allgemeinen voneinander getrennt betrachtet. Diabetes zum Beispiel behandeln wir, als gebe es keinen Zusammenhang mit Krebs und Alzheimer, obwohl er für beide Erkrankungen ein erhöhtes Risiko bedeutet. Dieser separatistische Ansatz spiegelt sich in der Struktur der National Institutes of Health wider, die getrennte Institute für Krebs, Herz-Kreislauf-Erkrankungen und so weiter haben. Wir behandeln sie als getrennte Einheiten, statt nach ihren Gemeinsamkeiten zu suchen.
»Wir versuchen, Herz-Kreislauf-Krankheiten, Krebs und Alzheimer immer schön nacheinander anzugehen, als ob diese Erkrankungen völlig unabhängig voneinander wären«, sagt S. Jay Olshansky, der an der University of Illinois Chicago die Demografie des Alterns erforscht, »und das, obwohl der Risikofaktor, der fast allem zugrunde liegt, was uns beim Älterwerden widerfährt – sowohl die Krankheiten, an denen wir leiden, wie auch die Gebrechlichkeit und die Einschränkungen, die mit ihnen einhergehen –, mit den biologischen Alterungsprozessen zu tun hat, die in uns ablaufen.«
Im nächsten Kapitel werden wir uns eine einzelne Intervention anschauen, ein Mittel, das die biologischen Alterungsprozesse vermutlich auf der Funktionsebene verlangsamt oder verschiebt. Es wird vielleicht auch für unsere Strategie relevant, aber im Augenblick heißt es, zwei Ansätze parallel zu verfolgen. Wir müssen an sehr frühe krankheitsspezifische Vorbeugung denken, mit der wir uns in den nächsten Kapiteln, die den apokalyptischen Reitern des Alterns gewidmet sind, im Detail befassen. Und wir müssen an sehr frühe generelle Vorbeugung denken, die – über häufige Treiber und Risikofaktoren – auf alle apokalyptischen Reiter gleichzeitig abzielt.
Wie wir sehen werden, überlagern sich diese Ansätze: Wenn man das Risiko für Herz-Kreislauf-Erkrankungen senkt, indem man bestimmte Lipoproteine (Cholesterin) angeht, kann damit auch das Alzheimer-Risiko verringert werden, nicht jedoch das Krebsrisiko. Die Schritte, die wir unternehmen, um die Stoffwechselgesundheit zu verbessern und Diabetes Typ 2 zu verhindern, verringern gleichzeitig ziemlich sicher auch das Risiko für Herz-Kreislauf-Krankheiten, Krebs und Alzheimer. Bestimmte Arten der sportlichen Betätigung senken das Risiko für alle chronischen Krankheiten, während andere dazu beitragen, die physische und die kognitive Resilienz (Widerstandskraft) aufrechtzuerhalten, die die Hundertjährigen zum größten Teil mit ihren Genen in die Wiege gelegt bekommen. Dieses Maß an Vorbeugung und Intervention mag, gemessen an den Standards der Medizin 2.0, übertrieben erscheinen, aber meiner Meinung nach ist es notwendig.
Schlussendlich denke ich, dass sich das Geheimnis der Hundertjährigen in einem Wort zusammenfassen lässt: Resilienz (Widerstandskraft). Sie sind in der Lage, Krebs und Herz-Kreislauf-Krankheiten zu widerstehen und sie zu vermeiden, selbst wenn sie jahrzehntelang geraucht haben. Sie sind in der Lage, sich eine ideale Stoffwechselgesundheit zu erhalten, oft trotz mieser Ernährungsgewohnheiten. Und sie widerstehen dem kognitiven und dem physischen Verfall, noch lange nachdem ihre Altersgenossen ihm erlegen sind. Diese Widerstandskraft wollen wir kultivieren, so wie sich Muhammad Ali vorbereitete, um George Foreman standhalten und ihn schließlich schlagen zu können. Er bereitete sich intensiv und clever vor, er trainierte lange auf diesen Kampf hin, und er wandte seine Taktik beim ersten Gongschlag an. Er hätte auf diese Weise nicht ewig weitermachen können, aber er schaffte genug Runden, um sein Ziel zu erreichen und den Kampf zu gewinnen.
Kapitel 5
Weniger essen, länger leben?
Die Wissenschaft von Hunger und Gesundheit
Wissenschaftler, die nach den Regeln anderer spielen,
können lange auf Entdeckungen warten.
Jack Horner
Im Herbst 2016 traf ich mich mit drei Freunden am George Bush Intercontinental Airport in Houston, um mit ihnen in einen Urlaub der etwas anderen Art aufzubrechen. Wir flogen elf Stunden über Nacht nach Santiago, Chile, wo wir Kaffee tranken und ein Frühstück zu uns nahmen, ehe wir in ein anderes Flugzeug stiegen, um noch einmal sechs Stunden nach Westen zu fliegen, 4000 Kilometer über das offene Meer zur Osterinsel, das abgeschiedenste von Menschen bewohnte Fleckchen der Erde. Wir waren alle in unseren Vierzigern, doch dieser Ausflug hatte nichts von einem typischen Wochenende unter Männern.
Die meisten Menschen kennen die Osterinsel wegen der an die tausend gigantischen Steinköpfe, den Moais, die entlang der Küste aufgereiht sind, aber es gibt dort noch sehr viel mehr. Ihren Namen erhielt die Insel von europäischen Entdeckern, die am Ostersonntag des Jahres 1722 dort landeten, aber bei den Einheimischen heißt sie Rapa Nui. Es ist ein extremer, isolierter, spektakulärer Ort. Die Insel hat die Form eines Dreiecks und eine Fläche von etwa 164 Quadratkilometern, entstanden ist sie durch die Aktivität von drei längst erloschenen Vulkanen, die vor Millionen von Jahren über 3000 Meter vom Meeresgrund aufstiegen. Ein Ende der Insel ist von hohen Kliffs umgeben, die steil in den unfassbar blauen Ozean abfallen. Die nächste menschliche Siedlung liegt 2000 Kilometer entfernt.
Wir waren nicht als Touristen hier. Wir befanden uns auf einer Pilgerfahrt zu den Ursprüngen eines der aufregendsten Moleküle, die die Medizin je gesehen hat, eines, von dem nur die wenigsten bislang gehört haben dürften. Wie dieses Molekül entdeckt wurde und wie es die Forschungen zur Langlebigkeit revolutionierte, gehört zu den unglaublichsten Geschichten der Biologie. Das Molekül, das unter dem Namen Rapamycin bekannt wurde, hat auch die Transplantationsmedizin tief greifend verändert und Millionen Patienten eine Chance auf ein zweites Leben gegeben. Doch das war nicht der Grund, warum wir 16 000 Kilometer weit an diesen entlegenen Ort gereist waren. Wir waren gekommen, weil sich gezeigt hatte, dass Rapamycin etwas kann, was bislang kein anderes Mittel konnte: das Leben eines Säugetiers verlängern.
Ein Mitglied unserer Gruppe, David Sabatini, damals Professor für Biologie am Whitehead Institute des Massachusetts Institute of Technology (MIT), war an der Entdeckung beteiligt. David half, den wichtigsten zellulären Wirkmechanismus von Rapamycin aufzuklären. Mit dabei war ein weiterer Biologe namens Navdeep Chandel (für seine Freunde kurz Nav), er ist mit David befreundet und erforscht an der Northwestern University Stoffwechsel und Mitochondrien, die kleinen Organellen, die in unseren Zellen für Energie (und noch viel mehr) sorgen. Tim Ferriss, ein guter Freund von mir, komplettierte unser Quartett. Tim ist Unternehmer und Autor, kein Wissenschaftler, aber er hat die Gabe, die richtigen Fragen zu stellen und eine frische Perspektive in die Dinge zu bringen. Außerdem wusste ich, dass er jeden Tag mit mir im Meer schwimmen würde, was mein Risiko, von einem Hai gefressen zu werden, um die Hälfte reduzieren würde.
Ein Zweck dieser Reise war es, einen Veranstaltungsort für eine wissenschaftliche Konferenz auszukundschaften, eine Konferenz, die sich ganz dieser aufregenden Substanz widmen sollte. Doch vor allem wollten wir zu dem Ort pilgern, von dem dieses außerordentliche Molekül stammte, und seine beinahe zufällige Entdeckung würdigen.
Nachdem wir unser Gepäck in einem 30-Betten-Touristenhotel abgestellt hatten, war unsere erste Station der Rano Kau, ein 320 Meter hoher erloschener Vulkan, der die Südwestecke der Insel dominiert. Unser Ziel war die Kratermitte, wo sich ein großer verlandeter See von etwa 1600 Meter Durchmesser befindet, der unter den Einheimischen einen mystischen Ruf genoss. Einer Legende zufolge gingen Menschen, wenn sie sich krank oder unwohl fühlten, in den Krater hinunter, manchmal verbrachten sie die Nacht dort, im Bauch des Vulkans, dem man besondere heilende Kräfte nachsagte.
Hier beginnt die Rapamycin-Geschichte. Gegen Ende des Jahres 1964 legte an der Osterinsel ein kanadisches Marineschiff an, das den langen Weg von Halifax hierher genommen hatte, an Bord befand sich ein Expeditionsteam aus Wissenschaftlern und Medizinern. Diese verbrachten mehrere Wochen dort, in denen sie forschten und den Einheimischen dringend benötigte medizinische Versorgung zukommen ließen; außerdem nahmen sie Proben von zahlreichen Arten der außergewöhnlichen Inselflora und -fauna sowie Bodenproben aus dem Krater mit nach Hause. Vielleicht hatten die Wissenschaftler wie wir von dessen sagenhaften heilenden Kräften gehört.
Ein paar Jahre später landete ein Döschen mit Osterinsel-Erde auf dem Labortisch eines Montrealer Biochemikers namens Suren Sehgal, der für eine kanadische Pharmafirma arbeitete, die damals Ayerst hieß. Sehgal stellte fest, dass diese Bodenprobe jede Menge eines unbekannten Stoffes enthielt, der sich als stark antimykotisch erwies (das heißt, er war hochwirksam gegen durch Pilze hervorgerufene Erkrankungen) und der offenbar von einem Bodenbakterium namens Streptomyces hygroscopicus produziert wurde. Sehgal wurde neugierig, isolierte das Bakterium und nahm es in Kultur, dann begann er, den mysteriösen Inhaltsstoff in seinem Labor zu testen. Er nannte ihn Rapamycin, nach Rapa Nui, dem Namen, den die Einheimischen für die Osterinsel verwendeten; die Endung -mycin wird üblicherweise für Antibiotika verwendet, die von Streptomyceten produziert werden. Dann jedoch schloss Ayerst von einem Tag auf den anderen sein Labor in Montreal, und Sehgal erhielt Weisung von oben, alle Substanzen, an denen er forschte, zu zerstören.
Sehgal missachtete diese Weisung und schmuggelte eine Dose Rapamycin aus dem Werk nach Hause. Sein Sohn Ajai, der ursprünglich das fünfte Mitglied unserer Pilgergruppe sein sollte, erinnert sich, wie er als Kind den Gefrierschrank öffnete, um sich ein Eis zu holen, und darin einen gut verpackten Behälter entdeckte, auf dem »NICHT ESSEN« stand. Die Dose überstand den Umzug der Familie nach Princeton, New Jersey, wohin Sehgal schließlich versetzt wurde, und als der Pharmariese Wyeth im Jahr 1987 Ayerst übernahm, wurde Sehgal von seinen neuen Chefs gefragt, ob er irgendwelche interessanten Projekte hätte, die er gerne weiterverfolgen würde. Er nahm die Dose Rapamycin aus dem Gefrierschrank und setzte seine Arbeit damit fort.
Sehgal glaubte, ein Mittel gegen Fußpilz gefunden zu haben, was schon eine große Sache gewesen wäre. Irgendwann, so erinnert sich Ajai, bereitete sein Vater mit dem Rapamycin eine Salbe für eine Nachbarin zu, die am ganzen Körper an einem üblen Hautausschlag litt, und der Ausschlag verschwand binnen kürzester Zeit. Aber es zeigte sich, dass Rapamycin weit mehr war als ein neues Fußpilzmittel: Es entfaltete enorme Wirkungen auf das Immunsystem, und im Jahr 1999 wurde es von der US-amerikanischen Arzneimittelbehörde (US Food and Drug Administration, abgekürzt FDA) als Medikament zugelassen, das verhinderte, dass der Körper von Transplantationspatienten die neuen Organe abstieß. Als Assistenzarzt in der Chirurgie verteilte ich es wie Pfefferminzdragees an Patienten mit Nieren- oder Lebertransplantation. Rapamycin, das auch unter dem Namen Sirolimus bekannt ist, wird außerdem zur Beschichtung von Gefäßstützen (Stents) verwendet, da es den erneuten Verschluss von damit versehenen Blutgefäßen verhindert. Die Erfolgsmeldungen setzten sich fort, selbst nach Sehgals Tod im Jahr 2003: Im Jahr 2007 erhielt ein Rapamycin-Analogon[39] namens Everolimus die Zulassung für die Behandlung einer bestimmten Art von Nierenkrebs.
Die chemische Verbindung wurde als so wichtig erachtet, dass Wyeth-Ayerst in den frühen 2000er-Jahren in der Nähe des Vulkankraters auf der Osterinsel eine Gedenktafel anbringen ließ, um den Ort zu ehren, an dem man Rapamycin gefunden hatte. Als wir die Tafel sehen wollten, mussten wir zu unserer Enttäuschung feststellen, dass sie gestohlen worden war.
Die vielen verschiedenen Anwendungen von Rapamycin haben mit einer Eigenschaft zu tun, die Sehgal zwar beobachtet, aber nie näher untersucht hatte: Es neigt dazu, die Prozesse zu verlangsamen, die das Zellwachstum und die Zellteilung steuern. David Sabatini gehörte zu der Handvoll Wissenschaftler, die den Staffelstab von Sehgal übernahmen und versuchten, dieses Phänomen aufzuklären. Die Funktionsweise von Rapamycin zu verstehen wurde zu Davids Lebensaufgabe. Er begann damit während seiner Promotion, als er sich durch einen Stapel Fachpublikationen arbeitete, die Sehgal persönlich für ihn fotokopiert hatte, und trug schließlich dazu bei, die Funktionsweise dieser einzigartigen Verbindung aufzuklären, an der noch mehrere andere Wissenschaftlerteams forschten.[40] Sie entdeckten, dass Rapamycin direkt auf einen wichtigen Proteinkomplex in der Zelle einwirkt, der den Namen mTOR (gesprochen »Em-Tor«) erhielt, für mechanistic target of rapamycin (übersetzt etwa: »Ansatzpunkt für den Rapamycin-Mechanismus«)[41].
Warum interessiert uns der mTOR-Komplex? Weil dieser Mechanismus auf zellulärer Ebene möglicherweise einer der wichtigsten Faktoren für Langlebigkeit ist. Mehr noch, er ist zudem »äußerst konservativ«, was heißt, dass er in praktisch allen Lebensformen vorkommt, von Hefen über Fliegen und Würmer bis hin zu uns Menschen.[42] In der Biologie bedeutet »konservativ«, dass etwas via natürliche Selektion weitergegeben wurde, und zwar quer durch eine Vielzahl von Spezies und Organismengruppen; es ist immer ein Zeichen dafür, dass die Evolution die betreffende Eigenschaft für sehr wichtig erachtet.
Es ist unglaublich: Dieses exotische Molekül, das auf einem entlegenen Fleckchen Erde mitten im Ozean gefunden wurde, verhält sich fast wie ein Schalter, der einen ganz bestimmten, in beinahe allen Lebewesen vorkommenden Zellmechanismus hemmt. Es passt perfekt, und das bringt mich auch heute noch jedes Mal zum Staunen, wenn ich daran denke.
Die Aufgabe von mTOR besteht im Wesentlichen darin, eine Balance herzustellen zwischen der Notwendigkeit, zu wachsen und sich fortzupflanzen, und der Verfügbarkeit der Nährstoffe.[43] Wenn viel Nahrung vorhanden ist, ist mTOR aktiv, und die Zelle (oder der Organismus) geht in den Wachstumsmodus, stellt neue Proteine her und teilt sich, letztlich mit dem Ziel, sich fortzupflanzen. Wenn Nährstoffe knapp sind, wird mTOR unterdrückt, und die Zellen gehen in eine Art »Recycling«-Modus über, bauen Zellbestandteile ab und machen einmal »Hausputz«. Zellteilung und Wachstum werden verlangsamt oder ganz eingestellt, und auch die Fortpflanzung wird vorübergehend ausgesetzt, damit der Organismus Energie sparen kann.
»Für die Zelle ist mTOR in gewisser Weise so etwas wie der Generalunternehmer«, erklärt Sabatini.[44] Er befindet sich an einer Stelle, an der lange und komplizierte Ketten von vor- und nachgeschalteten Stoffwechselwegen zusammenlaufen, die im Wesentlichen der Steuerung des Stoffwechsels dienen. Er registriert die Anwesenheit von Nährstoffen, insbesondere die von Aminosäuren, und hilft, Proteine zusammenzusetzen, die wichtigsten Bausteine der Zelle. Oder wie David es ausdrückte: »mTor hat bei allen wichtigen Abläufen in der Zelle die Finger im Spiel.«[45]
Am 9. Juli 2009 erschien eine kurze, aber wichtige Nachricht aus der Wissenschaft in der New York Times. »Antibiotic Delayed Aging in Experiments with Mice« (»Antibiotikum verzögert Alterung bei Labormäusen«) lautete die Überschrift. Bei dem »Antibiotikum« handelte es sich um Rapamycin, und der Studie zufolge lebten Mäuse, die die Substanz erhalten hatten, signifikant länger als der Durchschnitt der Kontrolltiere: Weibchen lebten 13 Prozent länger, Männchen 9 Prozent.
Die Nachricht war auf Seite A20 versteckt, aber das Versuchsergebnis war verblüffend. Obwohl die Mäuse die Substanz erst spät in ihrem Leben erhalten hatten, zu einem Zeitpunkt, an dem sie bereits 600 Tage alt waren (das würde bei Menschen einem Alter von etwa 60 Jahren entsprechen), hatte sie die verbleibende Lebenserwartung bei Männchen doch noch um 28 Prozent und bei Weibchen um 38 Prozent verlängert. Das war, als hätte man einer sechzigjährigen Frau eine Pille gegeben, die sie bis zum fünfundneunzigsten Lebensjahr leben lässt. Die Autoren der Studie, die im Fachmagazin Nature publiziert worden war, spekulierten, dass Rapamycin die Lebensdauer erhöhen könnte, »indem es den Tod durch Krebs zeitlich nach hinten verlagert, indem es Alterungsprozesse verlangsamt, oder beides«.[46] Die wahre Schlagzeile hier war jedoch, dass bislang kein anderes Molekül die Lebenszeit eines Säugetiers nachweislich verlängern konnte. Keines.
Die Ergebnisse waren auch deshalb so überzeugend, weil das Experiment von drei verschiedenen Arbeitsgruppen in drei verschiedenen Labors mit insgesamt 1901 genetisch verschiedenen Tieren durchgeführt worden war und die Ergebnisse durch die Bank konsistent waren. Obendrein konnten andere Labors diese Ergebnisse schnell und einfach reproduzieren,[47] was ausgesprochen selten vorkommt, sogar mit viel reißerischer verkündeten Ergebnissen.
Es mag Sie überraschen, aber die meisten Studien, die es in die Schlagzeilen schaffen, diejenigen, über die Sie in der Zeitung lesen oder in den Abendnachrichten hören, werden nie wiederholt. Typisches Beispiel: ein gut publiziertes Forschungsergebnis aus dem Jahr 2006, dass eine in den Schalen von Weintrauben (und in Rotwein) gefundene Substanz, das Resveratrol, das Leben übergewichtiger Mäuse verlängern kann.[48] In der Folge entstanden unzählige Nachrichten und Berichte und sogar ein längerer Beitrag für das Nachrichtenmagazin 60 Minutes über die positiven Wirkungen dieses erstaunlichen Moleküls (und, extrapoliert, des Rotweins). Die Absatzzahlen von Resveratrol-Nahrungsergänzungsmitteln schossen durch die Decke. Doch andere Labors konnten die ursprünglichen Ergebnisse nicht reproduzieren. Als man Resveratrol im Rahmen eines Programms des National Institute of Aging, in dem mögliche Antiaging-Maßnahmen überprüft wurden, ähnlich strengen Tests unterzog wie Rapamycin, verlängerte es die Lebensdauer einer vergleichbar diversen Mäusepopulation nicht.[49]
Das Gleiche gilt für andere gehypte Nahrungsergänzungsmittel wie zum Beispiel Nicotinamidribosid (NR), das die Lebenszeit von Mäusen ebenfalls nicht konsistent erhöhen konnte.[50] Und natürlich gibt es keine Daten, die belegen, dass eines dieser Nahrungsergänzungsmittel das Leben von Menschen verlängern oder deren Gesundheit verbessern könnte. Doch seit 2009 weist eine Studie nach der anderen nach, dass Rapamycin die Lebensdauer von Mäusen ziemlich zuverlässig erhöht.[51] Das Gleiche konnte für Hefen und Taufliegen gezeigt werden, manchmal zusammen mit genetischen Manipulationen, die die Aktivität von mTOR herabsetzten. Ein vernunftbegabter Mensch könnte daraus den Schluss ziehen, dass es vielleicht sein Gutes hat, mTOR – zumindest zeitweise – abzuschalten, und dass Rapamycin eventuell als Mittel zur Steigerung der Langlebigkeit taugt.
Für die Wissenschaftler, die sich mit dem Altern befassen, war der lebensverlängernde Effekt von Rapamycin wahnsinnig aufregend, aber eigentlich auch nicht wirklich überraschend. Er schien symbolisch für über Jahrzehnte, wenn nicht gar Jahrhunderte gesammelter Beobachtungen zu stehen, dass die Menge an verzehrter Nahrung irgendwie mit der Lebensdauer zusammenhängt. Die Idee lässt sich bis zu Hippokrates zurückverfolgen, aber moderne Experimente haben wieder und wieder gezeigt, dass eine Verringerung der Nahrungsaufnahme bei Labortieren das Leben verlängert.[52]
Der erste Mensch, der die Vorstellung vom »weniger essen« in rigoroser und dokumentierter Form in die Praxis umsetzte, war aber weder ein alter Grieche noch ein moderner Wissenschaftler, sondern ein italienischer Geschäftsmann des 15. und 16. Jahrhunderts namens Alvise Cornaro. Der wohlhabende Gutsbesitzer, den seine Freunde Luigi nannten und der durch die Entwässerung von Sümpfen und deren Umwandlung in fruchtbares Ackerland unglaublich reich geworden war, hatte eine schöne junge Frau und eine Villa mit eigenem Theater vor den Toren Venedigs. Er liebte es, rauschende Feste zu veranstalten. Doch als er auf die vierzig zuging, litt er an einem »Sack voller Gebrechen«: Magenschmerzen, Gewichtszunahme und ständigem Durst, dem klassischen Symptom von beginnendem Diabetes.
Der Grund dafür lag auf der Hand: zu viele Feste. Das Gegenmittel war ebenso klar: Keine opulenten Mahlzeiten und Gelage mehr, rieten ihm die Ärzte. Aber der vollschlanke Luigi sträubte sich. Er wollte seinen ausschweifenden Lebensstil nicht aufgeben. Als seine Symptome jedoch immer unerträglicher wurden, merkte er, dass er eine harte Kurskorrektur vornehmen musste, wenn er seine kleine Tochter aufwachsen sehen wollte. Er nahm seine ganze Willenskraft zusammen und setzte sich auf eine spartanische Diät, die aus zwölf Unzen (etwa 330 Gramm) Nahrung pro Tag bestand, in der Regel in Form eines Eintopfs mit Hühnerfleisch als Grundlage. Das war nahrhaft, aber nicht übermäßig sättigend. »Wenn ich vom Tisch aufstehe, habe ich stets das Gefühl, noch mehr essen und trinken zu können«, schrieb er später.
Nach einem Jahr mit diesem Ernährungsregime hatte sich Cornaros Gesundheitszustand dramatisch verbessert. Oder wie er es formulierte: »Ich fand mich all meiner Beschwerden ledig.« Er blieb bei seiner Ernährungsweise, und als er die Achtzig erreicht hatte, war er so begeistert darüber, dass er so lange und in so guter Gesundheit gelebt hatte, dass er sich genötigt fühlte, der Welt sein Geheimnis zu verraten. Er brachte ein autobiografisches Traktat mit dem Titel Discorsi della Vita Sobria (auf Deutsch erschienen mit dem Titel Vom maßvollen Leben)[53] zu Papier, wenn es sich von der Ansprache her auch nicht um die Gardinenpredigt eines absoluten Abstinenzlers handelte, denn er spülte seine Langlebigkeitsdiät mit zwei großen Gläsern Wein am Tag hinunter.
Cornaro starb im Jahr 1565, aber seine Empfehlungen überlebten ihn noch sehr lange. Sein Buch, übersetzt in mehrere Sprachen und gelobt von Berühmtheiten wie Benjamin Franklin und Thomas Edison, wurde in den nächsten paar Jahrhunderten mehrfach nachgedruckt, möglicherweise handelt es sich um den ersten Diät-Bestseller der Geschichte. Doch erst Mitte des 20. Jahrhunderts begannen Wissenschaftler damit, Cornaros Behauptung, durch weniger essen könne man das Leben (zumindest das von Labortieren) verlängern, strengen Tests zu unterziehen.
Wir sprechen hier nicht davon, Tieren einfach FdH (»Friss die Hälfte«) zu verordnen. Die Kalorienrestriktion (englisch caloric restriction, abgekürzt CR) ohne Mangelernährung ist eine exakte wissenschaftliche Methode, bei der eine Gruppe von Tieren (die Kontrolle) fressen kann, so viel sie möchte (ad libitum), während den Testgruppen ähnliches Futter mit allen notwendigen Nährstoffen, aber 25 bis 30 Prozent weniger Kalorien vorgesetzt wird. Die Tiere mit dem kalorienreduzierten Futter werden anschließend mit den Kontrollen verglichen.
Die Ergebnisse dieser Experimente waren bemerkenswert konsistent. So zeigen Studien aus den 1930er-Jahren, dass eine Restriktion der Kalorienaufnahme die Lebensdauer von Mäusen oder Ratten zwischen 15 und 45 Prozent erhöhen kann, je nachdem, in welchem Alter und in welchem Maß man die Tiere auf Diät setzte.[54] Nicht nur, dass diese Tiere auch deutlich gesünder zu sein schienen als sonst im jeweiligen Alter, sie entwickelten auch seltener spontan Tumore als normal ernährte Mäuse. Die Kalorienbeschränkung scheint auch die gesunde Lebenszeit zu verlängern, nicht nur die Gesamtlebenszeit. Man möchte annehmen, dass Hunger ungesund ist, aber die Wissenschaftler haben tatsächlich festgestellt, dass die Tiere umso länger lebten, je weniger sie zu fressen bekamen. Bis zu einem bestimmten Punkt scheint der Effekt dosisabhängig zu sein, fast wie ein Medikament.
Die lebensverlängernde Wirkung der Kalorienrestriktion scheint fast universell zu sein. Zahlreiche Labors konnten nachweisen, dass die Beschränkung der Kalorienaufnahme die Lebensdauer erhöht, nicht nur bei Ratten und Mäusen (meistens), sondern auch bei Hefen, Würmern, Fliegen, Fischen, Hamstern, Hunden und seltsamerweise sogar bei Spinnen. Bei fast jedem Modellorganismus, den man getestet hat, wurde die Lebensverlängerung beobachtet, mit Ausnahme der Hausfliege. Es scheint, als würden hungrige Tiere durch die Bank widerstandsfähiger und überlebensfähiger, zumindest unter den kontrollierten Bedingungen eines keimfrei gehaltenen Labors.
Das heißt nun aber nicht, dass ich meinen Patienten diese Art von radikaler Kalorienbeschränkung als Taktik empfehlen würde. Zum einen bleibt zweifelhaft, ob die Kalorienreduktion außerhalb des Labors sinnhaft wäre; sehr schlanke Tiere könnten leichter an Infektionen oder Unterkühlung sterben. Und während etwas »weniger essen« für Luigi Cornaro wie auch einige meiner Patienten sehr gut funktionierte, ist eine starke Kalorienrestriktion über längere Zeit für die meisten Menschen schwer bis unmöglich durchzuhalten. Darüber hinaus haben wir keine Belege dafür, dass eine extreme Kalorienrestriktion in einem so komplexen Lebewesen wie dem Menschen, der in einer wesentlich variableren Umwelt lebt als die Labortiere, die Langlebigkeitsfunktion maximieren könnte. Zwar würde sie das Risiko, an einer der typischen Alterskrankheiten zu sterben, wahrscheinlich zumindest bei manchen verringern, andererseits ist es nicht weniger wahrscheinlich, dass der Anstieg der Sterblichkeit aufgrund von Infektionen, Trauma und Gebrechlichkeit diese positiven Effekte wieder zunichtemacht.
Der wahre Wert der Forschung zur Kalorienrestriktion liegt in den Erkenntnissen, die sie für unser Verständnis des Alterungsprozesses an sich beigesteuert hat. Diese Studien halfen, zentrale Zellmechanismen zu entschlüsseln, die mit Nährstoffen und Langlebigkeit zu tun haben. Die Verringerung der Nährstoffmenge, die einer Zelle zur Verfügung steht, scheint eine Reihe von zelleigenen Mechanismen in Gang zu setzen, die die Stressresistenz der Zelle und die Effektivität der Stoffwechselvorgänge erhöhen – und die alle, irgendwie, mit mTOR zusammenhängen.
Ein Beispiel dafür ist ein Enzym namens AMP-aktivierte Proteinkinase, kurz AMPK. Man kann AMPK mit dem Warnlämpchen am Armaturenbrett eines Autos vergleichen, das einen niedrigen Füllstand im Benzintank anzeigt: Wenn es niedrige Nährstoffpegel (Benzin) registriert, wird es aktiv und löst eine Kaskade von Reaktionen aus.[55] Typischerweise geschieht das als Reaktion auf Nährstoffmangel, doch die AMPK wird auch aktiv, wenn wir Sport treiben, sie reagiert dann auf ein vorübergehendes Absinken der Nährstoffpegel. Und genau wie Sie – sobald die Warnlampe aufleuchtet – Ihre Fahrtroute ändern und die nächste Tankstelle ansteuern, statt zu Ihrer Großmutter durchzufahren, veranlasst AMPK die Zelle dazu, Energie zu sparen und nach anderen Energiequellen zu suchen.
Dazu regt sie zuerst die Produktion neuer Mitochondrien an, das sind die winzigen Organellen, die die Energie für die Zelle herstellen; dies geschieht durch einen Prozess, der als Mitochondrien-Biogenese bezeichnet wird. Im Laufe der Zeit – oder durch Nichtgebrauch – werden unsere Mitochondrien anfällig für oxidativen Stress und Genomschäden, was zu Fehlfunktion oder Totalversagen führt. Wird die Menge der verfügbaren Nährstoffe beschränkt, sei es durch verringerte Nahrungsaufnahme oder körperliche Betätigung, löst das die Produktion neuer, effizienterer Mitochondrien aus, die die alten und geschädigten ersetzen. Mit diesen frischen Mitochondrien kann die Zelle mit den zur Verfügung stehenden Nährstoffen mehr ATP herstellen, das Energiezahlungsmittel der Zelle. AMPK veranlasst den Körper außerdem, mehr »Brennstoff« für die neuen Mitochondrien bereitzustellen, indem er in der Leber Glucose produziert (darüber sprechen wir im nächsten Kapitel) und aus den Fettzellen dort gespeicherte Energie freisetzt.
Wichtiger ist allerdings, dass AMPK an der Hemmung der Aktivität des mTOR-Komplexes beteiligt ist, der das Zellwachstum steuert. Genauer gesagt, scheint ein rascher Abfall der Aminosäuremenge dafür zu sorgen, dass mTOR seine Tätigkeit einstellt und damit alle anabolen (aufbauenden) Prozesse, die mTOR kontrolliert. Statt neue Proteine herzustellen und Zellteilungen durchzuführen, geht die Zelle in einen Arbeitsmodus über, der energieeffizienter und weniger stressanfällig ist; dazu gehört die Aktivierung eines wichtigen zellulären Recyclingprozesses, der als Autophagie bezeichnet wird (das Wort bedeutet »[sich] selbst fressen« oder besser sogar »verschlingen«).
Autophagie steht für die katabole (abbauende) Seite des Stoffwechsels: Die Zelle hört auf, neue Proteine zu produzieren, und beginnt stattdessen, die alten Proteine und andere Zellstrukturen in ihre Aminosäurebausteine zu zerlegen, um daraus neue Proteine herzustellen. Es ist eine Art Zellrecycling, der Müll, der sich in der Zelle angesammelt hat, wird entfernt und einer neuen Verwendung zugeführt oder deponiert. Statt zu einem Baumarkt zu gehen und weitere Rohre, Schrauben oder Gipskarton zu kaufen, stöbert unser Zell-Bauunternehmer im Schutt des Hauses, das er gerade abgerissen hat, nach Material, das er eventuell wiederverwenden kann, entweder, um die Zelle zu reparieren oder neu aufzubauen, oder um es zu verbrennen, um Energie zu gewinnen.
Die Autophagie ist lebenswichtig.[56] Wenn sie nicht mehr funktioniert, stirbt der Organismus. Stellen Sie sich vor, was geschehen würde, wenn Sie Ihren Müll nicht mehr rausbringen, Ihr Haus wäre bald unbewohnbar. Der zelluläre Hausputz läuft allerdings nicht über Müllbeutel und Mülltonnen, vielmehr wird er von speziellen Organellen erledigt, den sogenannten Lysosomen, die packen die alten Proteine und andere Abfälle, Krankheitskeime eingeschlossen, ein und zerkleinern sie mithilfe von Enzymen, sodass sie wiederverwendet werden können. Darüber hinaus zerlegen die Lysosomen auch sogenannte Aggregate, das sind Klumpen schadhafter Proteine, die sich mit der Zeit ansammeln. Solche Proteinaggregate spielen bei Krankheiten wie Parkinson und Alzheimer eine Rolle, das heißt, es ist gut, sie loszuwerden; eine gestörte Autophagie-Funktion wurde mit Symptomen der Alzheimer-Krankheit und auch mit amyotropher Lateralsklerose (ALS), Parkinson und anderen neurodegenerativen Erkrankungen in Verbindung gebracht. Mäuse, denen ein bestimmtes Autophagie-Gen fehlt, sterben innerhalb von zwei bis drei Monaten an den Folgen der Nervenschädigungen.[57]
Dadurch, dass sie unsere Zellen von schadhaften Proteinen und anderem Zellabfall befreit, versetzt die Autophagie Zellen in die Lage, besser und effizienter zu funktionieren, und macht sie widerstandsfähiger gegen Stress. Wenn wir älter werden, lässt die Autophagie-Tätigkeit nach. Heute glaubt man, dass eine beeinträchtigte Autophagie-Funktion ein wichtiger Treiber für viele altersbedingte Erscheinungen und Beschwerden ist, etwa neurodegenerative Erkrankungen und Arthrose. Aus diesem Grund finde ich es so faszinierend, dass dieser enorm wichtige Zellmechanismus durch bestimmte Maßnahmen wie die vorübergehende Restriktion der Nährstoffmenge (durch Fasten oder körperliche Betätigung) – und die Substanz Rapamycin – beeinflusst werden kann. (Das Nobel-Komitee teilte diese Faszination und überreichte den Nobelpreis für Physiologie oder Medizin im Jahr 2016 dem japanischen Wissenschaftler Yoshinori Ohsumi für seine Arbeiten zur Aufklärung der genetischen Regulation der Autophagie.)
Und dennoch ist der Autophagie fördernde Effekt nur einer der Gründe, weshalb Rapamycin – nach Auffassung von Matt Kaeberlein, einem Forscher der University of Washington – eine Zukunft als Langlebigkeitsmedikament haben könnte. Kaeberlein beschäftigt sich schon seit Jahrzehnten wissenschaftlich mit Rapamycin und mTOR und glaubt, dass die Substanz noch weit mehr positive Wirkungen hat und dass Rapamycin und seine Abkömmlinge riesiges Potenzial für die Anwendung bei Menschen – zur Verlängerung der gesunden und der Gesamtlebenszeit – besitzen.
Obwohl Rapamycin bereits in vielen Anwendungsgebieten für Menschen zugelassen ist, gibt es gewaltige Hindernisse für klinische Studien, um seinen Effekt auf die menschliche Alterung zu testen – vor allem wegen möglicher Nebenwirkungen bei Gesunden, insbesondere das Risiko der Immunsuppression.
Ursprünglich wurde Rapamycin zugelassen, um Patienten nach Organtransplantationen dauerhaft damit zu behandeln; es ist Teil eines Cocktails aus drei oder vier Medikamenten, die den Teil des Immunsystems unterdrücken sollen, der ansonsten das neue Organ attackieren und zerstören würde. Diese immunsupprimierende Wirkung ist der Grund, weshalb man zögert, gesunden Menschen Rapamycin – und sei es nur zu Studienzwecken – zu verabreichen, um die Alterung zu verzögern, obwohl die umfangreichen an Tieren gewonnenen Daten nahelegen, dass es die gesunde und die Gesamtlebenszeit verlängern kann. Es sah so aus, als ließen sich die befürchteten immunsupprimierenden Wirkungen nicht umgehen. Und darum schien es unwahrscheinlich, dass die vielversprechenden Eigenschaften von Rapamycin jemals in Form eines lebensverlängernden Medikaments für Menschen Wirklichkeit würden.
Die Wende trat Ende Dezember 2014 mit der Veröffentlichung einer Studie ein, die zeigte, dass das Rapamycin-Analogon Everolimus bei einer Gruppe älterer Patienten tatsächlich die adaptive Immunantwort auf einen Impfstoff verstärkte.[58] Diese Studie wurde von Joan Mannick und Lloyd Klickstein durchgeführt, die damals bei dem Pharmakonzern Novartis arbeiteten; demnach zeigte die Patientengruppe, die einmal pro Woche eine mittlere Dosis Everolimus erhielt, offenbar die beste Immunantwort und die wenigsten Nebenwirkungen auf die Grippe-Impfung. Die Ergebnisse dieser Studie legten nahe, dass Rapamycin (und seine Abkömmlinge) womöglich eher als Immunmodulatoren denn als Immunsuppressoren wirkten, wie es zuvor fast immer dargestellt worden war. Das heißt, in bestimmten Dosierungen kann es die Immunität stärken, während es in einer anderen Dosierung die Immunreaktionen unterdrückt.
Bis zur Publikation dieser Studie hatte ich (wie viele andere) die Hoffnung schon fast aufgegeben, dass man Rapamycin je präventiv bei gesunden Menschen würde einsetzen können. Auch ich hatte angenommen, dass seine offensichtliche immunsupprimierende Wirkung ein zu schwer wiegendes Hindernis darstellt. Doch diese gut angelegte und gut kontrollierte Studie ließ den gegenteiligen Schluss zu. Die Immunsuppression trat offenbar bei täglich verabreichten niedrigen bis mittleren Rapamycin-Dosen ein. Die Teilnehmer dieser Studie hatten mittlere bis hohe Dosen Rapamycin erhalten, gefolgt von einer Einnahmepause, und diese versetzte Einnahme führte zum gegenteiligen Effekt, einer Verstärkung der Immunreaktion.
Es mag merkwürdig erscheinen, dass verschiedene Dosierungen desselben Medikaments so verschiedene Wirkungen haben, aber es ergibt Sinn, wenn man die Struktur von mTOR versteht, das eigentlich aus zwei separaten Komplexen besteht, mTOR-Komplex 1 (mTORC1) und mTOR-Komplex 2 (mTORC2). Die beiden Komplexe haben verschiedene Aufgaben, und es kommt, sehr vereinfacht ausgedrückt, zu den positiven Auswirkungen auf die Lebensdauer, wenn Komplex 1 gehemmt wird. Wenn man das Medikament täglich verabreicht, wie es für Transplantationspatienten üblich ist, scheinen beide Komplexe gehemmt zu werden, doch wenn man es nur kurz oder in bestimmten Abständen gibt, dann scheint es vor allem mTORC1 zu blockieren, sodass die positiven Effekte auf die Langlebigkeit eintreten, ohne unerwünschte Nebenwirkungen zu entfalten. (Ein Rapamycin-Analogon oder »Rapalog«, das selektiv an mTORC1 bindet, wäre daher ideal für den Einsatz zur Lebensverlängerung, doch bislang wurde noch kein erfolgreicher Kandidat entwickelt.)
Und weil dem so ist, bleiben die bekannten Nebenwirkungen ein Hindernis für alle klinischen Studien mit Rapamycin zur Geroprophylaxe oder Geroprävention (Verzögerung des Alterns) bei gesunden Menschen. Um dieses Problem zu umgehen, führt Kaeberlein eine große klinische Studie mit Rapamycin an Haushunden durch;[59] das ist eine ganz passable Annäherung an die Situation beim Menschen, da Haushunde große Säugetiere sind, die in derselben Umgebung leben wie Menschen und ähnliche Alterungsprozesse durchlaufen. In einer Vorstudie zu seinem »Dog Aging Project« stellte Kaeberlein fest, dass Rapamycin bei älteren Tieren anscheinend sogar die Herzfunktion verbessert.[60] »Was mich wirklich überrascht hat«, sagt er, »ist, dass Rapamycin auf unterschiedliche Art und Weise nicht nur den körperlichen Verfall hinauszuschieben, sondern den Allgemeinzustand zu verbessern scheint. In einigen Organen hat es offensichtlich verjüngende Funktion.«[61]
Kaeberlein hat auch beobachtet, dass unter Rapamycin systemische Entzündungen zurückgehen, möglicherweise, indem es die Aktivität sogenannter seneszenter Zellen unterbindet. Das sind »ältere« Zellen, die sich nicht mehr teilen, die aber noch nicht abgestorben sind; sie scheiden einen toxischen Cocktail aus entzündlichen Cytokinen aus, Molekülen, die die umgebenden Zellen schädigen können. Rapamycin scheint die Menge dieser entzündlichen Cytokine zu verringern. Es verbessert auch die »Krebsüberwachung«, also die Art und Weise, wie unser Körper, wahrscheinlich das Immunsystem, Krebszellen entdeckt und beseitigt. In einer weiteren Studie fand Kaeberleins Arbeitsgruppe kürzlich Verbesserungen im Zustand des Zahnfleischs älterer Hunde, die wohl auch auf Rapamycin zurückgehen.
Die Hauptphase des »Dog Aging Project«, an der 600 Haushunde teilnehmen, läuft gerade, Ergebnisse dieser großen klinischen Studie werden für 2026 erwartet. (Offenlegung eines möglichen Interessenkonflikts: Ich finanziere diese Forschungen mit.) Die Hunde erhalten das Rapamycin einmal pro Woche, ähnlich wie die Teilnehmer der oben erwähnten Studie aus dem Jahr 2014. Sollten die Ergebnisse positiv ausfallen, würde es mich nicht wundern, wenn Rapamycin in Zukunft öfter als Mittel zur Lebensverlängerung eingesetzt würde. Eine kleinere, aber stetig wachsende Zahl von Menschen, mich und einige meiner Patienten eingeschlossen, nehmen Rapamycin wegen seiner Antiaging-Eigenschaften bereits jetzt – außerhalb seiner zugelassenen Indikationen (off-label use). Ich kann nicht für alle sprechen, aber die Einnahme in größeren Abständen scheint unerwünschte Nebenwirkungen zu reduzieren, so jedenfalls meine Erfahrung.
Trotzdem bleiben die Hürden hoch, die für eine Zulassung für eine breitere Anwendung bei Menschen zu überwinden sind. Die weitaus meisten Menschen, die im Augenblick Rapamycin einnehmen, sind Transplantationspatienten, die bereits große gesundheitliche Probleme und oft mehrere Erkrankungen gleichzeitig haben. In einer solchen Gruppe werden die Nebenwirkungen oft als weniger bedeutsam angesehen, als dies bei gesunden Menschen der Fall wäre.
»Wenn es um die Behandlung gesunder Menschen geht, ist die Akzeptanz von Nebenwirkungen in der Öffentlichkeit und bei den Zulassungsbehörden sehr gering«, sagt Kaeberlein. »Wir haben die Absicht, den Alterungsprozess zu verlangsamen, bevor die Menschen krank werden, sie länger gesund zu halten. In vielerlei Hinsicht ist das das Gegenteil der traditionellen biomedizinischen Herangehensweise, bei der wir normalerweise warten, bis die Leute krank sind, und dann versuchen, ihre Krankheiten zu heilen.«
Das wahre Hindernis auf diesem Weg ist das regulatorische Rahmenwerk, das auf Medizin 2.0 fußt und das »das Altern verlangsamen« und »den Krankheitsausbruch hinauszögern« (noch) nicht als gleichberechtigte Endpunkte anerkennt. Es wäre eine Medizin-3.0-Anwendung dieses Mittels, wenn wir es nähmen, um gesunden Menschen dabei zu helfen, länger gesund zu bleiben, statt bestimmte Krankheiten zu heilen oder zu lindern. Darum würde es auch viel genauer unter die Lupe genommen und mit mehr Skepsis betrachtet werden. Aber wenn wir über die Prävention von Alterskrankheiten sprechen, an denen 80 Prozent von uns sterben, dann ist sicherlich eine ernsthafte Diskussion der Frage angebracht, ein wie hohes Risiko zum Erreichen dieses Ziels akzeptabel ist. Ich schreibe dieses Buch zum Teil auch deshalb, weil ich diese Diskussion voranbringen will.
Möglicherweise tut sich bereits etwas. Die amerikanische Arzneimittelzulassungsbehörde FDA hat grünes Licht für eine klinische Studie mit einem anderen Mittel gegeben, das sich positiv auf die Lebensdauer auswirken könnte, das Diabetes-Medikament Metformin. Die Studie heißt abgekürzt TAME (Targeting Aging with Metformin, deutsch etwa: mit Metformin gegen das Altern angehen) und kam ganz anders zustande. Metformin wird schon seit Jahren Millionen Menschen verabreicht. Im Laufe der Zeit bemerkten Wissenschaftler (und Studien schienen es zu belegen), dass Patienten, die regelmäßig Metformin nahmen, offenbar eine niedrigere Krebsrate hatten als die Durchschnittsbevölkerung. Und den Ergebnissen einer großen Datenanalyse aus dem Jahr 2014 zufolge lebten Diabetiker mit Metformin anscheinend sogar länger als Nichtdiabetiker, was schon sehr überraschend ist.[62] Doch keine dieser Beobachtungen beweist, dass Metformin geropräventiv wirkt – dafür braucht man eine klinische Studie.
Allerdings ist das Altern selbst nur schwer – wenn nicht unmöglich – genau zu messen. Deshalb beschloss der Leiter der TAME-Studie, Nir Barzilai, den wir schon im vorigen Kapitel kennengelernt haben, einen anderen Endpunkt zu wählen: Er untersucht, ob bei gesunden Menschen, die Metformin einnehmen, Alterskrankheiten später einsetzen als bei Personen, die das Mittel nicht einnehmen; der Krankheitsbeginn steht stellvertretend für das Altern. Ich hoffe sehr, dass wir eines Tages, vielleicht schon in naher Zukunft, auch mit Rapamycin, das meiner Meinung nach ein noch viel größeres Potenzial als Mittel zur Lebensverlängerung besitzt, eine solche Studie durchführen können.[63]
Doch jetzt wollen wir einen Moment innehalten und uns klarmachen, dass alles, worüber wir in diesem Kapitel gesprochen haben, von mTOR und Rapamycin bis zur Kalorienrestriktion, in eine einzige Richtung zeigt: Das, was wir essen und wie wir es verstoffwechseln, scheint für die Langlebigkeit eine enorm große Rolle zu spielen. Im nächsten Kapitel werden wir uns genauer ansehen, wie Stoffwechselerkrankungen chronische Krankheiten verursachen und fördern.
Kapitel 6
Die Überfluss-Krise
Wie passen unsere alten Gene mit der heutigen Ernährung zusammen?
Vermeidbares menschliches Leid wird oft nicht so sehr
von Dummheit als vielmehr von Nichtwissen verursacht, insbesondere von Nichtwissen über uns selbst.
Carl Sagan
Für den Umgang mit jungen Assistenzärzten in der Chirurgie existiert eine Art ungeschriebener Regel, die Hippokrates vielleicht so formuliert hätte: Achte zuallererst darauf, dass sie keinen Schaden anrichten. Diese Regel kam im Jahr 2001, während meiner ersten Monate in der Krebschirurgie am Johns Hopkins Hospital, voll zum Tragen. Einem Patienten sollte ein mit Krebs befallener Teil des Dickdarms entfernt werden, und zu meinen Aufgaben gehörte es, mit ihm am Tag davor ein Informationsgespräch zu führen und ihm einige Fragen zu stellen, damit wir für die Operation alles Notwendige von seiner medizinischen Vorgeschichte wussten.
Ich traf mich mit dem Patienten und beschrieb ihm den bevorstehenden Eingriff, erinnerte ihn daran, dass er nach 20 Uhr nichts mehr essen sollte, und stellte ihm eine Reihe von Routinefragen, unter anderem, ob er rauchte oder nicht und wie viel Alkohol er trank. Ich hatte geübt, diese letzte Frage auf eine freundliche, scheinbar beiläufige Art zu stellen, doch ich wusste, dass sie zu den wichtigsten Fragen auf meiner Liste gehörte. Wenn wir glaubten, dass ein Patient beträchtliche Mengen Alkohol konsumierte (typischerweise mehr als vier oder fünf Drinks oder 56 bis 60 Gramm Alkohol pro Tag), mussten wir das den Anästhesisten mitteilen, damit sie während der Aufwachphase bestimmte Medikamente, zum Beispiel Valium oder andere Benzodiazepine, verabreichten, um Entzugserscheinungen zu vermeiden. Andernfalls bestand die Gefahr, dass der Patient ins Delirium tremens fiel, was unter Umständen tödlich für ihn enden könnte.
Ich war erleichtert, als er mir mitteilte, dass er nur sehr wenig trank. Eine Sache weniger, um die man sich Gedanken machen musste. Am nächsten Tag schob ich den Patienten in den Operationssaal und hakte meine Checkliste für die Dinge, die junge Assistenzärzte zu tun hatten, ab. Die Anästhesisten brauchten ein paar Minuten, um ihn in Schlaf zu versetzen, danach konnte ich den Dauerkatheter in seine Blase legen, seine Haut mit Desinfektionsmittel bestreichen, die Abdecktücher befestigen und schließlich zur Seite treten, während der Chefarzt und der Oberarzt den ersten Schnitt setzten. Wenn ich Glück hatte, durfte ich beim Öffnen und Schließen des Abdomens assistieren. Andernfalls war ich dafür da, die Leber so wegzuhalten, dass die Operateure freie Sicht auf das Stück des Darms hatten, das sie entfernen wollten und das sich direkt unter der Leber befand.
Zunächst lief alles ganz normal. Die Chirurgen mussten sich durch etwas Bauchfett arbeiten, bis sie an die Bauchhöhle kamen, aber sonst nichts Ungewöhnliches. Bevor man die letzte von mehreren Membranen durchschneidet, die die Außenwelt von der Welt im Inneren der Bauchhöhle trennt, steigt die Spannung deutlich an. Das Erste, was man sieht, wenn der Schnitt größer wird, ist die Spitze der Leber, die für mich schon immer ein völlig unterschätztes Organ war. Die »coolen« Medizinstudis spezialisieren sich aufs Gehirn oder aufs Herz, aber das eigentliche Arbeitstier des menschlichen Körpers ist die Leber – und ihr Anblick ist einfach atemberaubend. Eine gesunde Leber hat normalerweise eine tief dunkelrotbraune Farbe und eine fantastisch seidig-glatte Textur. Man ist versucht, an Hannibal Lecter zu denken: Sie sieht wirklich aus, als könnte sie mit ein paar Fava-Bohnen und einem guten Chianti ein köstliches Mahl abgeben.
Die Leber dieses Patienten bot allerdings einen weniger appetitlichen Anblick, als sie aus dem Bauchnetz (Omentum) auftauchte. Statt gesund dunkelrot war sie undefinierbar orange marmoriert, mit hervortretenden gelben Fettknubbeln. Sie sah aus wie verdorbene Foie gras (Gänsestopfleber). Der Oberarzt blickte mich scharf an und bellte: »Sie sagten doch, der Mann sei kein Trinker!«
Offensichtlich litt dieser Mann unter schwerem Alkoholismus, seine Leber wies alle Anzeichen dafür auf. Und weil ich es nicht geschafft hatte, ihm diese Information zu entlocken, hatte ich vielleicht sein Leben in Gefahr gebracht.
Doch es stellte sich heraus, dass ich keinen Fehler gemacht hatte. Als der Patient nach der Operation aufwachte, bestätigte er, dass er so gut wie nie Alkohol trank. Meiner Erfahrung nach lügen Patienten, die vor einer Krebsoperation stehen, nur selten, wenn es um Alkohol oder andere Dinge geht, vor allem wenn sie wissen, dass sie später Valium oder – noch besser – ein paar Bier zum Klinikessen erhalten, wenn sie es zugeben. Aber dieser Patient hatte definitiv die Leber eines Alkoholikers, was uns allen sehr merkwürdig vorkam.
Während meiner Assistenzarztzeit machten wir diese Beobachtung allerdings noch öfter, und wir kratzten uns jedes Mal etwas verlegen am Kopf. Wir hatten keine Ahnung, dass wir Zeugen einer beginnenden stillen Epidemie – oder vielleicht deren Blüte – wurden.
Fünfzig Jahre zuvor hatte Samuel Zelman, ein Chirurg in Topeka, Kansas, eine ähnliche Situation erlebt. Er operierte einen Patienten, den er persönlich kannte, weil er im selben Krankenhaus als Hilfskraft arbeitete. Er wusste ganz sicher, dass der Mann nie Alkohol trank, und war umso überraschter, dass sich dessen Leber als ausgesprochene Fettleber herausstellte, ganz so wie Jahrzehnte später bei meinem Patienten.
Dieser Mann trank allerdings sehr viel – Cola. Zelman wusste, dass er schier unglaubliche Mengen der braunen Brause konsumierte, zwanzig oder mehr Flaschen pro Tag. Das waren noch die alten kleinen Cola-Flaschen, nicht die Riesenflaschen, die es heute gibt, aber Zelman rechnete aus, dass sein Patient auf diese Weise – zusätzlich zu seinen eh schon üppigen Mahlzeiten – noch weitere 1600 Kilokalorien pro Tag zu sich nahm. Unter seinen Kollegen, so notierte Zelman, war er »für seinen Appetit bekannt«.
Seine Neugierde war geweckt. Zelman rekrutierte 19 andere stark übergewichtige, nicht alkoholkranke Personen für eine klinische Studie.[64] Er untersuchte ihr Blut und ihren Urin und nahm Leberbiopsien an ihnen vor, das ist ein richtiger Eingriff, der mit einer richtig dicken Nadel ausgeführt wird. Bei all seinen Studienteilnehmern fanden sich Zeichen für eine gestörte Leberfunktion, die beunruhigend große Ähnlichkeit mit den bekannten Stadien von Leberschäden bei Alkoholikern hatten.
Dieses Krankheitsbild war zwar lange bekannt, aber kaum verstanden. Es wurde typischerweise dem Alkoholismus oder einer Hepatitis zugeschrieben. Als man anfing, es bei Teenagern zu beobachten, in den 1970er- und 1980er-Jahren, warnten besorgte Ärzte vor einer Epidemie von Jugendalkoholismus. Doch Alkohol war nicht der Schuldige. Im Jahr 1980 dachte sich ein Ärzteteam der Mayo Clinic für die bis dahin namenlose Krankheit die Bezeichnung »nichtalkoholische Fettleberhepatitis« (non-alcoholic steatohepatitis, NASH) aus.[65] Seit der Zeit hat sie sich zu einer globalen Plage entwickelt. Mehr als jeder Vierte auf diesem Planeten hat eine NASH oder ihren Vorläufer, die nichtalkoholische Fettleber (non-alcoholic fatty liver disease, NAFLD)[66]; die war es auch, die wir bei unserem Patienten im Operationssaal gesehen hatten.
Die nichtalkoholische Fettleber geht fast immer mit Adipositas (Fettleibigkeit) und Hyperlipidämie (stark erhöhte Blutfettwerte) einher, und doch wird sie, vor allem im Frühstadium, oft nicht bemerkt. Die meisten Patienten haben keine Ahnung, dass sie eine haben – und ihre Ärzte ebenso wenig, da weder NASH noch NAFLD äußerlich sichtbare Symptome hervorrufen. Die ersten Anzeichen tauchen in der Regel erst dann auf, wenn bei Blutuntersuchungen auf das Leberenzym Alanin-Aminotransferase (abgekürzt ALT) getestet wird. Erhöhte ALT-Werte deuten häufig darauf hin, dass mit der Leber etwas nicht in Ordnung ist, allerdings können sie auch von etwas anderem verursacht werden, zum Beispiel von einer noch nicht lange zurückliegenden Virusinfektion oder einem Medikament. Aber es gibt viele Menschen, deren Ärzte nicht ahnen, dass sie sich in einem frühen Stadium der Leberverfettung befinden, weil ihre ALT-Werte immer noch »normal« sind.
Nächste Frage: Was ist normal? Einem der führenden US-amerikanischen Unternehmen für Labordienstleistungen zufolge sind alle ALT-Werte unter 33 IU/l für Frauen und unter 45 IU/l für Männer akzeptabel. Aber »normal« ist nicht dasselbe wie »gesund«. Die Spanne der Referenzwerte für solche Tests beruht auf den aktuellen Perzentilen[67], aber wenn die Bevölkerung insgesamt immer weniger gesund ist, dann kann sich der Durchschnitt durchaus von den optimalen Werten unterscheiden. Ganz ähnlich war es mit dem Gewicht. Heute bringt ein durchschnittlicher amerikanischer Mann fast 100 Kilo auf die Waage. In den 1970er-Jahren wäre ein 100-Kilo-Mann als »stark übergewichtig« bezeichnet worden, heute ist er gerade einmal Durchschnitt.[68] Das heißt also, dass im 21. Jahrhundert »durchschnittlich« nicht notwendigerweise optimal heißt.
Mit Blick auf die ALT-Leberwerte hat das American College of Gastroenterology kürzlich seine Richtlinien überarbeitet und empfiehlt nun, die Leber klinisch untersuchen zu lassen, wenn die ALT-Werte von Männern über 33 und die von Frauen über 25 IU/l liegen – beides deutlich unter den aktuellen »Normal«-Werten.[69] Doch selbst diese Schwellenwerte könnten noch zu hoch sein: Eine Studie aus dem Jahr 2002, die Personen von der Teilnahme ausgeschlossen hatte, bei denen bereits eine Fettleber diagnostiziert war, empfiehlt, die Obergrenze bei 30 IU/l für Männer und bei 19 für Frauen anzusetzen.[70] Das heißt, selbst wenn Ihre Leberwerte innerhalb der Referenzspanne liegen, muss Ihre Leber nicht zwangsläufig gesund sein.
Nichtalkoholische Fettleber (NAFLD) und nichtalkoholische Fettleberhepatitis (NASH) sind im Grunde genommen zwei Stadien derselben Erkrankung. Die Fettleber ist das erste Stadium, das (kurz gesagt) eintritt, wenn mehr Fett in die Leber hineingelangt oder dort entsteht als aus ihr hinaustransportiert wird. Der nächste Schritt die metabolische Stufenleiter hinunter ist die Fettleberhepatitis, im Prinzip nichts anderes als die Fettleber plus Entzündung, ähnlich wie eine normale Hepatitis, nur ohne Viren als Verursacher. Die Entzündung führt zur Vernarbung der Leber, aber immer noch sind äußerlich keine Symptome erkennbar. Das klingt zwar Furcht einflößend, aber noch ist nicht alles verloren. Beide Krankheitsstadien sind noch reversibel. Wenn Sie es schaffen, das Fett aus der Leber zu entfernen (in der Regel durch Gewichtsverlust), verschwindet auch die Entzündung, und die Leberfunktionen normalisieren sich. Die Leber ist ein sehr resilientes Organ, eigentlich fast ein Wunder. Sie gehört zu den Organen mit der höchsten Regenerationsfähigkeit. Wenn ein gesunder Mensch einen Teil seiner Leber spendet, haben Spender und Empfänger etwa acht Wochen nach der Operation beide eine fast normal große und voll funktionsfähige Leber, wobei das Wachstum in den ersten beiden Wochen nach der OP am stärksten ist.
Mit anderen Worten, Ihre Leber kann sich von einem Beinahetotalschaden bis hin zu einer teilweisen Entfernung wieder erholen. Aber wenn man die nichtalkoholische Fettleberhepatitis (NASH) nicht in Schach hält oder rückgängig macht, dann schreiten die Schädigung und die Vernarbung fort bis zur Zirrhose. Das ist bei etwa 11 Prozent der Patienten mit NASH der Fall und sehr viel gefährlicher. Dann nämlich wird der zelluläre Aufbau des Organs angegriffen, und das ist sehr viel schwerer rückgängig zu machen. Ein Patient mit Zirrhose stirbt mit einiger Wahrscheinlichkeit an den verschiedenen Komplikationen seines Leberversagens, es sei denn, er erhält eine Lebertransplantation. Im Jahr 2001, als wir die Operation an dem Mann mit der Fettleber vornahmen, war die Fettleberentzündung in den Vereinigten Staaten mit etwas mehr als 1 Prozent der Grund für eine Lebertransplantation, bis 2025 wird die Fettleberentzündung mit Zirrhose den Prognosen zufolge die Hauptindikation für Lebertransplantationen sein.[71]
So schrecklich es klingt, aber die Zirrhose ist nicht der einzige Endpunkt, über den ich mir hier Gedanken mache. Die nichtalkoholische Fettleber (NAFLD) und die nichtalkoholische Fettleberhepatitis (NASH) bereiten mir deshalb Sorgen, weil sie die Spitze des Eisbergs einer globalen Epidemie von Stoffwechselerkrankungen darstellen, die von Insulinresistenz bis Diabetes Typ 2 reichen. Technisch gesprochen ist Diabetes Typ 2 eine genau definierte Krankheit, sehr klar beschrieben durch Glucose-Maßzahlen, aber ich betrachte sie schlicht als letzte Haltestelle einer Eisenbahnlinie, die bereits einige andere Stationen passiert hat, unter anderem Hyperinsulinämie, Prädiabetes und NAFLD/NASH. Wenn Sie sich irgendwo auf dieser Eisenbahnstrecke befinden, selbst wenn es die frühen Stadien der nichtalkoholischen Fettleber(-entzündung) sind, dann befinden Sie sich sehr wahrscheinlich auch auf dem Weg zu den anderen drei apokalyptischen Reitern des Alterns (Herz-Kreislauf-Erkrankung, Krebs und Alzheimer). Wie wir in den nächsten Kapiteln noch sehen werden, erhöht die Stoffwechselstörung Ihr Risiko beträchtlich, an einer dieser Krankheiten zu erkranken. Darum können Sie die apokalyptischen Reiter nicht bekämpfen, ohne zuerst die Stoffwechselstörung anzugehen.
Bitte beachten Sie, dass ich »Stoffwechselstörung« sage und nicht »Adipositas« oder »Fettleibigkeit«, der Lieblingsbuhmann im Gesundheitswesen. Das ist eine wichtige Unterscheidung. Angaben der Centers for Disease Control (eine Behörde des US-amerikanischen Gesundheitsministeriums, abgekürzt CDC) zufolge gelten über 40 Prozent der US-Bevölkerung als adipös (definiert als BMI[72] über 30), während ein weiteres Drittel übergewichtig ist (BMI 25–30).[73] Statistisch gesehen bedeutet starkes Übergewicht ein größeres Risiko für chronische Krankheiten, darum wird dem »Fettleibigkeitsproblem« so viel Aufmerksamkeit geschenkt, aber ich habe einen breiteren Ansatz: Starkes Übergewicht ist nur eines von mehreren Symptomen einer zugrunde liegenden Stoffwechselstörung, wie zum Beispiel Hyperinsulinämie, die ebenfalls zu Gewichtszunahme führt. Aber nicht jeder Adipöse hat einen kranken Stoffwechsel und nicht jeder mit einem kranken Stoffwechsel ist adipös. Zur Stoffwechselgesundheit gehört mehr als das Augenfällige.
Bereits in den 1960er-Jahren, lange bevor Fettleibigkeit zu einem weitverbreiteten Problem wurde, hatte ein Stanforder Endokrinologe namens Gerald Reaven beobachtet, dass extremes Übergewicht oft mit bestimmten anderen Anzeichen schlechter Gesundheit einherging. Seine Kollegen und er bemerkten, dass Herzinfarktpatienten oft hohe Nüchternblutzucker- und hohe Triglyceridwerte sowie erhöhten Blutdruck und viel viszerales Fett (Bauchfett) aufwiesen. Je mehr dieser Symptome auf der Checkliste abgehakt werden konnten, desto höher war das Herzinfarktrisiko der Patienten.
In den 1980er-Jahren gab Reaven dieser Kollektion miteinander zusammenhängender Erkrankungen den Namen »Syndrom X«, wobei »X«, wie er schließlich herausfand, die Insulinresistenz war. Heute bezeichnen wir dieses Problembündel als »metabolisches Syndrom«; es wird folgendermaßen definiert:
hoher Blutdruck (> 130/85 mm Hg)
hohe Triglyceridwerte (> 150 mg/dl)
niedriges HDL-Cholesterin (< 40 mg/dl bei Männern, < 50 mg/dl bei Frauen)
vermehrtes Viszeralfett (Bauchumfang > 102 cm bei Männern, > 88 cm bei Frauen)
erhöhter Nüchternblutzucker (> 110 mg/dl)
Wenn drei oder mehr dieser Kriterien auf Sie zutreffen, haben Sie das metabolische Syndrom – so wie 120 Millionen Amerikaner, wie man in einem Artikel der Fachzeitschrift JAMA im Jahr 2020 lesen konnte.[74] Etwa 90 Prozent der US-Bevölkerung haken zumindest einen dieser Punkte in der Checkliste ab.[75] Aber bitte beachten Sie: Adipositas ist nur eines der Kriterien; man kann das metabolische Syndrom auch haben, ohne stark übergewichtig zu sein. Das Problem geht eindeutig tiefer als einfach nur bis zur unerwünschten Gewichtszunahme. Das stützt meine Auffassung, dass Übergewicht an sich nicht die Ursache, sondern lediglich ein Symptom anderer Probleme darstellt.
Studien haben festgestellt, dass etwa ein Drittel derjenigen, die aufgrund ihres BMI als fettleibig gelten, gemessen an den Parametern für die Definition des metabolischen Syndroms (unter anderem Blutdruck, Triglyceride, Cholesterin und Nüchternblutzucker) tatsächlich stoffwechselgesund sind. Gleichzeitig zeigten einige Studien, dass zwischen 20 und 40 Prozent der Personen, die nicht zu den Adipösen gezählt werden, nach denselben Kriterien metabolisch krank sein könnten. Ein hoher Prozentsatz der stark Übergewichtigen ist auch metabolisch krank, aber wie Abbildung 3 zeigt, sitzen eine Menge Normalgewichtiger mit ihnen im selben Boot – und das sollte ein Weckruf für uns alle sein. Es geht nicht darum, wie viel Sie wiegen. Selbst wenn Sie dünn sein sollten, lohnt es sich für Sie, dieses Kapitel zu lesen.
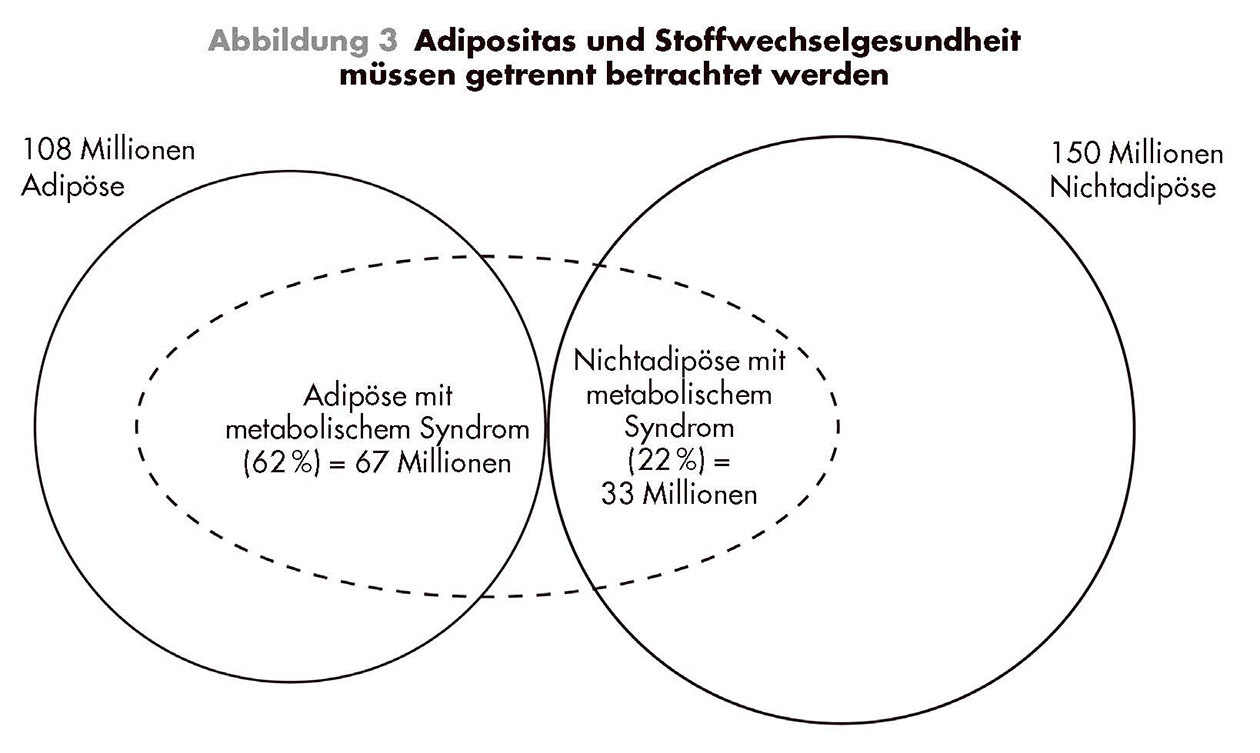
Relative Häufigkeit (Prävalenz) des metabolischen Syndroms in Bevölkerungsgruppen mit und ohne Adipositas.
Quelle: Interne Analyse, basierend auf Daten des National Institute of Diabetes and Digestive and Kidney Diseases (2021)
Die Abbildung (beruhend auf Daten der National Institutes of Health, NIH, und nicht auf dem zuvor erwähnten JAMA-Artikel) zeigt ziemlich deutlich, dass Fettleibigkeit und metabolisches Syndrom nicht dasselbe sind – ganz im Gegenteil. Etwa 42 Prozent der US-Bevölkerung gelten als adipös (BMI > 30). Von vorsichtig geschätzten 100 Millionen Amerikanern, auf die die Kriterien des metabolischen Syndroms zutreffen (deren Stoffwechsel also nicht gesund ist), ist fast genau ein Drittel nicht adipös. Viele Menschen aus dieser Gruppe sind übergewichtig (BMI 25–29,9), doch beinahe zehn Millionen Amerikaner mit Normalgewicht (BMI 19–24,9) haben ebenfalls keinen gesunden Stoffwechsel.
Einige Studienergebnisse legen nahe, dass die letztgenannte Gruppe vielleicht sogar besonders gefährdet ist. Eine große Metaanalyse von Studien mit einer Nachbeobachtungszeit von bis zu 11,5 Jahren zeigte, dass Personen aus dieser Kategorie ein bis zu dreimal höheres Risiko hatten als stoffwechselgesunde Normalgewichtige, und zwar sowohl für die Gesamtmortalität (Sterblichkeit aller Ursachen zusammengenommen) wie auch für kardiovaskuläre Ereignisse (zum Beispiel Herzinfarkte oder Schlaganfälle).[76] Andererseits wiesen stoffwechselgesunde adipöse Teilnehmer in diesen Studien kein statistisch signifikant erhöhtes Risiko auf. Fazit ist, dass nicht die Fettleibigkeit zu einer schlechteren Gesundheit führt, sondern das metabolische Syndrom. Und damit beschäftigen wir uns hier.
Unter Stoffwechsel versteht man all die Prozesse, durch die Nährstoffe, die wir aufnehmen, so in ihre Bestandteile zerlegt werden, dass unser Körper sie verwerten kann. Bei stoffwechselgesunden Menschen werden die Nährstoffe verarbeitet und an die richtigen Bestimmungsorte transportiert. Doch bei Menschen mit krankem Stoffwechsel landen viele der aufgenommenen Kalorien nicht dort, wo sie gebraucht werden – im besten Fall, im schlimmsten richten sie sogar Schaden an.
Wenn Sie beispielsweise einen Donut essen, muss Ihr Körper entscheiden, was er mit den darin enthaltenen Kalorien macht. Auch auf die Gefahr hin, die Sache etwas zu sehr zu vereinfachen, kommen für die Kohlenhydrate in Ihrem Donut zwei Weiterverarbeitungswege infrage. Erstens, sie können in Glykogen verwandelt werden, die Speicherform von Glucose, die für den baldigen Verbrauch vorgesehen ist. Etwa 75 Prozent des Glykogens landen in der Skelettmuskulatur, während die restlichen 25 Prozent in die Leber wandern, diese Mengenverhältnisse sind jedoch veränderlich. Ein erwachsener Mann kann typischerweise insgesamt etwa 1600 Kalorien in Form von Glykogen an diesen beiden Stellen speichern, genug Energie, um damit zwei Stunden intensives Ausdauertraining zu absolvieren. Darum sollte man seine Brennstoffspeicher vor einem Marathonlauf oder einer langen Fahrradtour irgendwie auffüllen, andernfalls droht die Gefahr, dass einem die Energie ausgeht und »der Mann mit dem Hammer« oder der »Hungerast« kommt, was alles andere als eine angenehme Erfahrung ist.
Eine der vielen wichtigen Aufgaben der Leber ist es, gespeichertes Glykogen in Glucose zurückzuverwandeln und dann so dosiert in den Blutkreislauf zu bringen, dass der Blutzuckerspiegel möglichst immer gleich hoch ist, dieser Zustand wird als Glucose-Homöostase bezeichnet. Die Blutzuckerregulation ist eine unglaublich filigrane Aufgabe: Im Blutkreislauf eines durchschnittlichen erwachsenen Mannes zirkulieren zu jeder Zeit etwa fünf Gramm (ein Teelöffel voll) Glucose. Diese Menge reicht gerade für ein paar Minuten, dann ist die Glucose bereits von der Muskulatur und vor allem vom Gehirn aufgenommen worden, sodass die Leber ständig nachliefern und dabei darauf achten muss, dass der Spiegel mehr oder weniger konstant bleibt. Bitte machen Sie sich klar, dass fünf Gramm Glucose, verteilt über den gesamten Blutkreislauf, normal sind, während sieben Gramm, eineinhalb Teelöffel, bedeuten, dass Sie Diabetes haben. Wie ich schon sagte, die Leber ist ein faszinierendes Organ.
Weit mehr, ja fast unendlich viel Energie können wir allerdings in Form von Fett speichern, das ist der zweite mögliche Zielort für die Kalorien in unserem Donut. Selbst ein relativ schlanker Erwachsener trägt unter Umständen zehn Kilogramm Fett in seinem Körper herum, was beeindruckenden 90 000 Kalorien gespeicherter Energie entspricht.
Die Entscheidung, wohin die Energie aus dem Donut geliefert wird, treffen die Hormone, hauptsächlich das Insulin, das von der Bauchspeicheldrüse ausgeschüttet wird, wenn der Körper die Anwesenheit von Glucose registriert, das letzte Abbauprodukt fast aller Kohlenhydrate (wie auch derjenigen im Donut). Insulin hilft dabei, die Glucose dorthin zu bringen, wo sie gebraucht wird, wobei die Glucose-Homöostase erhalten bleiben muss. Sollten Sie zufällig bei einer Etappe der Tour de France mitfahren oder einer anderen intensiven körperlichen Betätigung nachgehen, wenn Sie den Donut essen, dann werden die in ihm enthaltenen Kalorien im Handumdrehen in den Muskeln verbrannt. Bei einem Menschen mit überwiegend sitzender Tätigkeit erschöpfen sich die Glykogenspeicher in der Muskulatur nicht so schnell, darum landet die überschüssige Energie aus dem Donut zum größten Teil in den Fettzellen (genauer: Sie wird in Form von Triglyceriden in den Fettzellen eingelagert).
Der Dreh dabei ist, dass Fett – in diesem Fall das Unterhautfettgewebe (subkutanes Fett) – tatsächlich der sicherste Ort zum Speichern überschüssiger Energie ist. Fett an sich ist nichts Schlechtes. Dort lagern wir die Kalorien ein, die wir gerade nicht brauchen. So hat sich das in der Evolution entwickelt. Heutzutage mag Fett kulturell oder ästhetisch unerwünscht sein, doch das Unterhautfett spielt weiter eine wichtige Rolle für die Aufrechterhaltung der Stoffwechselgesundheit. Gerald Shulman, seines Zeichens Endokrinologe an der Yale University und einer der führenden Diabetesforscher, veröffentlichte einmal ein elegantes Experiment, um die Notwendigkeit von Fett zu demonstrieren: Er pflanzte insulinresistenten Mäusen operativ etwas Fettgewebe ein, dadurch wurden sie zwar fetter, aber er stellte fest, dass ihre Stoffwechselstörung danach fast sofort behoben war.[77] Die neuen Fettzellen der Mäuse saugten die überschüssige Glucose auf und deponierten sie sicher.
Stellen Sie sich Fettgewebe als eine Art Pufferzone für den Stoffwechsel vor, die überschüssige Energie aufnimmt und speichert, bis sie gebraucht wird. Wenn wir mehr Donuts essen, werden deren Kalorien in unserem Unterhautfettgewebe gespeichert; sobald wir eine lange Wanderung unternehmen oder eine längere Strecke schwimmen, wird ein Teil dieses Fetts für die Verwendung in der Muskulatur wieder freigesetzt. Es entsteht ein kontinuierlicher Fettstrom, und solange wir unsere Fettspeicherkapazität nicht überschreiten, ist alles in Ordnung.
Wenn wir aber weiterhin mehr Energie aufnehmen, als wir brauchen, dann füllen sich die subkutanen Fettzellen allmählich, insbesondere wenn von der gespeicherten Energie wenig verbraucht wird. Ist irgendwann die Obergrenze der Speicherkapazität im Unterhautfettgewebe erreicht und werden trotzdem weiter Kalorien aufgenommen, dann muss die ganze Energie trotzdem irgendwo eingelagert werden. Die verzehrten Donuts (oder was auch immer) können zwar immer noch in Fett umgewandelt werden, aber nun muss der Körper andere Orte für die Speicherung finden.
Man könnte das, was dann geschieht, mit einer vollen Badewanne vergleichen. Wenn Sie den Wasserhahn aufgedreht lassen, obwohl die Wanne voll und der Abfluss verschlossen ist (Sie also überwiegend sitzend tätig sind), dann beginnt das Wasser über den Rand der Badewanne zu laufen und fließt an Stellen, wo Sie es weder brauchen noch haben wollen, zum Beispiel auf den Boden des Badezimmers, in Heizungsschlitze oder die Treppe hinunter. Das Gleiche gilt für das überschüssige Fett. Wenn immer weiter Kalorien hereinströmen, ist die Speicherkapazität des Unterhautfettgewebes irgendwann erschöpft, und das Fett, das nicht mehr eingelagert werden kann, »läuft über« in andere Körperbereiche: ins Blut (in Form von Triglyceriden) oder in die Leber (wo es die Entstehung der nichtalkoholischen Fettleber vorantreibt), ins Muskelgewebe (wo es direkt zur Insulinresistenz der Muskulatur beiträgt, wie wir gleich sehen werden) und sogar rund um Herz und Bauchspeicheldrüse (Pankreas) (Abbildung 4). Natürlich ist keine dieser Körperstellen für die Ansammlung von Fett geeignet; die nichtalkoholische Fettleber ist nur eine von vielen unerwünschten Folgen dieser Fettschwemme.[78]
Das Fett »läuft« auch in Ihren Bauchraum und sammelt sich zwischen Ihren Organen. Während das subkutane Fett als relativ harmlos erachtet wird, hat es das viszerale Fett in sich. Dessen Fettzellen geben in unmittelbarer Nähe Ihrer wichtigsten inneren Organe Cytokine wie TNF-alpha und IL-6 ab, die eine Schlüsselfunktion bei Entzündungsprozessen haben und diese vorantreiben. Daher rührt vermutlich der Zusammenhang zwischen vermehrtem Bauchfett und dem erhöhten Risiko für Krebs und Herz-Kreislauf-Krankheiten.
Die Fettspeicherkapazitäten sind individuell sehr unterschiedlich. Wenn wir bei unserer Badewannenanalogie bleiben: Manche Menschen verfügen über eine subkutane Fettspeicherkapazität, die der Füllmenge einer Standardbadewanne entspricht, bei anderen hat sie eher Whirlpoolformat, und wieder andere müssen mit einem Kinderbadewännchen auskommen. Und natürlich spielt es auch eine Rolle, wie viel »Wasser« über den Wasserhahn in die Wanne hineinfließt (die Kalorien aus der Nahrung) und wie viel Wasser durch den Abfluss aus der Wanne herausfließt (Energieverbrauch durch sportliche Betätigung oder Ähnliches).
Die individuelle Fettspeicherkapazität scheint von genetischen Faktoren beeinflusst zu werden. Es ist eine Verallgemeinerung, aber Menschen asiatischer Abstammung haben im Durchschnitt offenbar häufig niedrigere Fettspeicherkapazitäten als solche europäischer Herkunft.[79] Aber es gibt noch andere Faktoren, die zumindest teilweise erklären, weshalb manche Menschen stark übergewichtig und trotzdem metabolisch gesund sind, während andere dünn aussehen und dennoch drei oder mehr Anzeichen für das metabolische Syndrom aufweisen. Diese Menschen sind – den Forschungsergebnissen von Mitch Lazar von der University of Pennsylvania zufolge – am stärksten gefährdet, weil eine dünne Person schlicht über weniger Möglichkeiten verfügt, Fett sicher zu speichern.[80] Wenn alle sonstigen Umstände gleich sind, verfügt eine etwas fülligere Person wohl über eine größere Fettspeicherkapazität und damit einen größeren metabolischen Spielraum als jemand, der gertenschlank daherkommt.
Die Bauchfettmenge muss nicht besonders groß sein, um Probleme zu verursachen. Nehmen wir an, Sie seien männlich, vierzig Jahre alt und 100 Kilo schwer. Wenn Sie 20 Prozent Körperfett haben, entsprechen Sie in etwa dem Durchschnittsamerikaner (50. Perzentile) Ihres Alters und Geschlechts und tragen im gesamten Körper verteilt 20 Kilogramm Fett mit sich herum. Selbst wenn nur 2,25 Kilogramm davon Bauchfett wären, hätten Sie laut Statistik ein extrem hohes Risiko für Herz-Kreislauf-Krankheiten und Diabetes Typ 2, Sie befänden sich unter den 5 Prozent Ihrer Geschlechts- und Altergenossen mit dem höchsten Risiko. Aus diesem Grund rate ich meinen Patienten dringend, einmal im Jahr einen DEXA-Scan machen zu lassen; mit dieser Methode, der genannten Dual-Röntgen-Absorptiometrie, kann man die Körperzusammensetzung bestimmen, wobei ich weit mehr am viszeralen Fett interessiert bin als am Gesamtkörperfett.
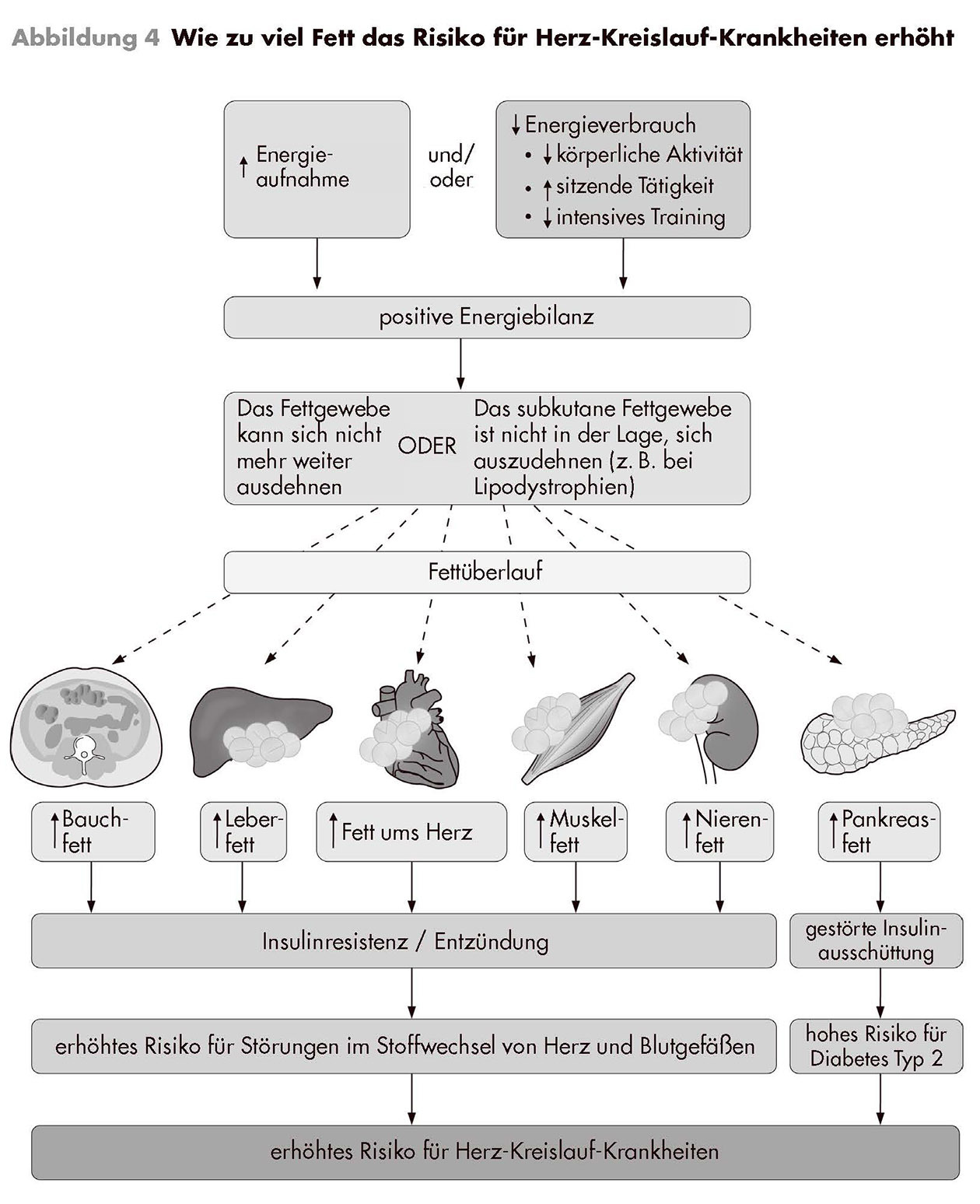
Quelle: Tchernof und Després (2013)
Unter Umständen kann es ziemlich lange dauern, bis Sie an diesem Punkt angekommen sind, aber dann haben Sie ein Problem – selbst wenn Sie und Ihr Arzt sich dessen nicht bewusst sind. Fett sammelt sich an vielen Stellen, wo es nicht hingehört, wie in Ihrer Leber, zwischen Ihren inneren Organen oder sogar um Ihr Herz herum – und das völlig unabhängig von Ihrem Gewicht. Eine der ersten Stellen, wo das überlaufende Fett Probleme verursacht, ist die Muskulatur; dort mogelt es sich zwischen die Muskelfasern, Sie kennen das von einem schön marmorierten Steak. Wenn sich der Prozess fortsetzt, tauchen sogar mikroskopisch kleine Fetttröpfchen in Ihren Muskelzellen auf.
Wahrscheinlich ist das der Beginn der Insulinresistenz, zu diesem Schluss kommt Gerald Shulman nach 30 Jahren intensiver Forschung.[81] Diese Fetttröpfchen könnten die ersten Endstationen für die überschüssige Energie, den Fettüberlauf sein, und wenn es zu viele werden, beginnen sie das komplexe Netzwerk der insulinabhängigen Transportmechanismen zu stören, die normalerweise Glucose in die Muskelzelle bringen, damit sie dort »verbrannt« werden kann. Wenn diese Mechanismen nicht mehr funktionieren, werden die Zellen »taub« für die Insulinsignale. Später greift die sogenannte Insulinresistenz auf andere Gewebe wie die Leber über, doch Shulman glaubt, dass sie in der Muskulatur entsteht. Ein wichtiger Faktor in diesem Geschehen ist offenbar mangelnde Bewegung. Wenn jemand nicht körperlich aktiv ist und keine Energie via Muskeltätigkeit verbraucht, dann entwickelt sich die vom Fettüberlauf vorangetriebene Insulinresistenz sehr viel schneller. (Aus diesem Grund verlangte Shulman von seinen Studienteilnehmern, in der Regel junge Collegestudenten, ganz auf körperliche Aktivität zu verzichten, um sie in Richtung Insulinresistenz zu treiben.)
Insulinresistenz ist ein Begriff, den wir häufig hören, doch was bedeutet er genau? Technisch gesprochen heißt das, dass Zellen, als Erstes die Muskelzellen, die Signale, die vom Insulin ausgehen, nicht mehr aufnehmen. Aber man kann sich die Zelle auch vorstellen wie einen Ballon, der mit Luft aufgeblasen wird. Irgendwann sind wir an dem Punkt, an dem es schwierig wird, noch mehr Luft in den Ballon zu bekommen. Man muss immer kräftiger pusten. Hier kommt nun Insulin ins Spiel, es hilft dabei, den Aufblasvorgang zu verstärken. Die Bauchspeicheldrüse (Pankreas) beginnt, mehr und mehr Insulin zu produzieren, um auf diese Weise überschüssige Glucose aus dem Blut zu entfernen und in die Zellen zu packen. Das funktioniert eine Zeit lang, der Blutzuckerspiegel bleibt im Normalbereich, aber irgendwann ist eine Grenze erreicht, und der »Ballon« (die Zelle) kann keine »Luft« (Glucose) mehr aufnehmen.
Ab da wird das Problem in den üblichen Blutuntersuchungen sichtbar, da die Nüchternglucose zu steigen beginnt. Das bedeutet, dass Ihr Insulin- und Ihr Blutzuckerspiegel hoch ist und Ihre Zellen die Schotten für weitere Glucoseaufnahme dicht gemacht haben. Wenn sich nichts ändert, ermüdet das Pankreas und verliert die Fähigkeit, eine Insulinantwort auszulösen. Verschlimmert wird die Situation, Sie können es sich denken, wenn sich inzwischen auch in die Bauchspeicheldrüse Fett eingelagert hat. Sie sehen hier, wie eine Abwärtsspirale entsteht: Der Fettüberlauf führt zur Entstehung der Insulinresistenz, daraus ergibt sich die Einlagerung von immer mehr Fett, bis unser Körper Kalorien schließlich nur noch als Fett speichern kann. An der Produktion und der Verteilung von Fett sind noch viele andere Hormone beteiligt, unter anderem Testosteron, Östrogen, Cortisol und die hormonsensitive Lipase[82]. Cortisol ist besonders wirkungsvoll, mit einem zweischneidigen Effekt: Es kann subkutanes Fett abziehen (was generell nichts Schlechtes ist) und es durch das schädlichere viszerale Fett ersetzen. Aus diesem Grund hängen Stresslevel und Schlaf, die beide Einfluss auf die Cortisolfreisetzung haben, ebenfalls mit dem Stoffwechsel zusammen. Doch Insulin scheint das wirkmächtigste Hormon zu sein, was die Förderung der Fettansammlung angeht, da es wie eine Art Tor zu einer Einbahnstraße agiert, es lässt Fett nur in die Zelle hinein und verhindert die Freisetzung von Energie aus den Fettzellen (über einen als Lipolyse bezeichneten Prozess).[83] Bei Insulin geht es nur um Fettspeicherung, nicht um Fettverwendung.
Bleibt der Insulinspiegel dauerhaft hoch, tauchen weitere Probleme auf. Fettzuwachs und letztendlich Fettleibigkeit stellen nur eines der Symptome eines Krankheitsbildes namens Hyperinsulinämie dar. Meiner Meinung nach sind es nicht einmal die ernstesten Symptome: Wir werden in den kommenden Kapiteln noch sehen, dass Insulin auch ein mächtiger Signalgeber für das Zellwachstum ist und Atherosklerose ebenso fördern kann wie Krebs. Und wenn sich die Insulinresistenz zu entwickeln beginnt, ist der Zug schon sehr weit gekommen auf seinem Weg zu Diabetes Typ 2, der eine Menge unangenehmer Konsequenzen mit sich bringt.
Das nur langsam wachsende Bewusstsein für die nichtalkoholische Fettleber(-hepatitis) ist wie ein Déjà-vu der aufkommenden globalen Diabetes-Typ-2-Epidemie vor hundert Jahren. Wie Krebs, Alzheimer, Herz-Kreislauf-Erkrankungen gilt auch Diabetes Typ 2 als »Zivilisationskrankheit«, das heißt, sie ist erst in der modernen Zeit merklich in Erscheinung getreten. Bei Naturvölkern und in vergangenen Zeiten war sie weitgehend unbekannt. Ihre Symptome jedoch kennt man seit Tausenden von Jahren, etwa im alten Ägypten und im alten Indien, aber erst der griechische Arzt Aretaios von Kappadokien gab ihr den Namen »Diabetes« und beschrieb sie als das »Zerfließen von Fleisch und Gliedern in Urin«.[84]
Damals war Diabetes extrem selten und wurde nur selten beobachtet. Als Diabetes Typ 2 zu Beginn des frühen 18. Jahrhunderts auftauchte, war es zunächst eine Krankheit der obersten Schichten, weil Päpste, erfolgreiche Künstler, reiche Kaufleute, Adlige sich das modische neue Luxusgut Zucker leisten konnten. Der Komponist Johann Sebastian Bach litt möglicherweise darunter, ähnlich wie andere berühmte Persönlichkeiten.[85] Es gab Überlappungen mit Gicht, einer besser bekannten Klage der dekadenten Upperclass. Das war kein Zufall, wie wir noch sehen werden.
Im frühen 20. Jahrhundert schließlich wurde Diabetes zu einer Krankheit der Massen. Im Jahr 1940 schätzte der berühmte Diabetologe Elliott Joslin, dass etwa eine von drei- bis vierhundert Personen Diabetes hatte,[86] was eine enorme Steigerung gegenüber nur wenige Jahrzehnte früher erhobenen Zahlen darstellte, aber immer noch relativ selten war. Bis zum Jahr 1970, also etwa die Zeit meiner Geburt, war die Prävalenz auf eine von fünfzig Personen gestiegen.[87] Heute leiden in den Vereinigten Staaten mehr als 11 Prozent der Bevölkerung, eine von neun Personen, an klinischem Diabetes Typ 2, das geht aus einem Bericht der Centers for Disease Control (CDC) hervor, in dem mehr als 29 Prozent der Erwachsenen über fünfundsechzig Jahre erfasst wurden.[88] Weitere 38 Prozent der Amerikaner – mehr als eine von drei Personen – weisen mindestens eines der Zeichen für Prädiabetes (Diabetesvorstufen) auf. Das heißt, dass sich fast die Hälfte der US-amerikanischen Bevölkerung auf dem Weg zu Diabetes Typ 2 befindet oder bereits dort angekommen ist.
Eine kleine Anmerkung: Unter den häufigsten Todesursachen in den Vereinigten Staaten rangiert Diabetes Typ 2 nur auf Platz sieben oder acht, hinter Nierenerkrankungen, Unfällen und Alzheimer. Im Jahr 2020 wurden Diabetes Typ 2 nur etwas mehr als 100 000 Todesfälle zugeschrieben, ein Bruchteil dessen, was für Herz-Kreislauf-Erkrankungen oder Krebs ermittelt wurde.[89] Was die Zahlen angeht, möchte man Diabetes wohl kaum einen apokalyptischen Reiter des Alterns nennen. Doch ich denke, dass Diabetes Typ 2 weit mehr Todesopfer fordert und wir den Einfluss dieser Erkrankung unterschätzen. Patienten mit Diabetes haben ein wesentlich höheres Risiko für Herz-Kreislauf-Erkrankungen, Krebs, Alzheimer und andere Demenzerkrankungen. Man könnte sagen, Diabetes und die damit zusammenhängende Stoffwechselstörung ist das, was all diese Krankheitsbilder gemein haben. Darum lege ich so großen Wert auf die Stoffwechselgesundheit, und darum beschäftige ich mich schon lange mit der Epidemie dieser Stoffwechselerkrankung, die sich nicht nur in den Vereinigten Staaten, sondern überall auf der Welt abspielt.
Warum findet die Epidemie gerade jetzt statt?
Die einfachste Erklärung ist vermutlich, dass unser Stoffwechsel, der sich im Laufe von Jahrmillionen Evolution entwickelt hat, nicht über die geeignete Ausstattung verfügt, um mit unserer heutigen Ernährung, die es erst seit etwas mehr als hundert Jahren gibt, zurechtzukommen. Die Evolution ist nicht länger auf unserer Seite, weil sich unsere Umwelt viel schneller verändert hat, als unser Genom es konnte. Die Evolution hat es uns ermöglicht, Fett anzusetzen, wenn Nahrungsmittel im Überfluss vorhanden sind: Je mehr Energie wir speichern konnten, in unserer fernen Vergangenheit, desto größer waren die Chancen, zu überleben und sich fortzupflanzen. Wir mussten in der Lage sein, längere Zeit ohne Essen auszukommen, und die natürliche Selektion sorgte dafür, dass diejenigen mit Genen, die halfen, Energie in Form von Fett zu speichern und einzulagern, einen Überlebensvorteil hatten. Auf diese Weise vermochten unsere frühen Vorfahren Zeiten von Nahrungsknappheit, Kälteperioden und körperliche Stresssituationen wie Krankheit und Schwangerschaft zu überstehen. In unserer heutigen Umwelt jedoch, in der viele Menschen in den hoch entwickelten Ländern fast unbegrenzten Zugang zu Kalorien haben, erweisen sich diese Gene als weniger vorteilhaft.
Ein weiteres Problem ist, dass Kalorien nicht alle in derselben Art und Weise im Körper umgesetzt werden. Eine fast allgegenwärtige Kalorienquelle in unserer heutigen Ernährung ist Fructose, und sie hat sich – im Übermaß konsumiert – als mächtiger Treiber der metabolischen Dysfunktion herausgestellt. Dabei ist Fructose gewiss kein neuer Nährstoff. Es handelt sich um die Zuckerart, die in fast allen Früchten vorkommt und als solche in der Ernährung vieler Tierarten – von Flughunden und Kolibris bis hin zu Bären, Affen und Menschen – unverzichtbar ist. Doch wie sich herausgestellt hat, besitzen wir Menschen die einzigartige Fähigkeit, Kalorien aus Fructose in Fett umzuwandeln.[90]
Viele Leute dämonisieren Fructose geradezu, vor allem wenn sie als HFCS (High Fructose Corn Syrup, auf Deutsch »Maissirup mit hohem Fructoseanteil«) vorliegt, ohne wirklich zu verstehen, warum sie so schädlich sein soll. Die Geschichte dahinter ist kompliziert, aber faszinierend. Der springende Punkt: Fructose wird anders verstoffwechselt als andere Zucker. Wenn unser Körper Fructose zusammen mit anderen Arten von Nahrungsmitteln verarbeitet, entstehen große Mengen Harnsäure, die man vor allem als Ursache von Gicht kennt, die aber wohl auch mit erhöhtem Blutdruck in Zusammenhang zu steht.
Vor mehr als zwanzig Jahren bemerkte Rick Johnson, ein Nephrologe an der University of Colorado, dass der Konsum von Fructose offenbar nicht nur den Blutdruck in die Höhe treibt, sondern auch die Fettbildung steigert. »Wir stellten fest, dass Fructose Effekte hervorrief, die sich nicht mit ihrem Kaloriengehalt erklären ließen«, sagte Johnson.[91] Der Schuldige schien die Harnsäure zu sein. Andere Säugetiere, und sogar einige andere Primaten, besitzen ein Enzym namens Uricase, das hilft, die Harnsäure abzubauen. Doch uns Menschen fehlt dieses wichtige und offenkundig nützliche Enzym, und so kommt es bei uns zur Anreicherung von Harnsäure, mit all ihren negativen Folgen.
Johnson und sein Team begannen – in Zusammenarbeit mit dem britischen Anthropologen Peter Andrews, einem pensionierten Wissenschaftler des Natural History Museum in London und Experten für die Evolution der Primaten –, unsere Evolutionsgeschichte zu erforschen.[92] Andere hatten bereits herausgefunden, dass das Enzym Uricase aufgrund einer Zufallsmutation bereits in ferner Vergangenheit verloren gegangen war, unklar blieb jedoch, weshalb sich diese Mutation halten konnte. Johnson und Andrews durchkämmten Stammbäume und Fossilfunde und formulierten dann eine verblüffende Theorie: Möglicherweise war diese Mutation entscheidend für die Evolution des Menschen.
Nach der Geschichte, der sie auf die Spur kamen, wanderten vor Millionen von Jahren Primatenvorfahren von uns aus Nordafrika ins heutige Europa. Zu jener Zeit war Europa üppig grün, mit subtropischer Vegetation, doch die Wälder veränderten sich, als das Klima langsam abkühlte. Laubabwerfende Bäume und offene Graslandschaften ersetzten den tropischen Wald, und die Bäume, von deren Früchten sich die Affen ernährten – vor allem die Feigen, die quasi ihr Grundnahrungsmittel waren –, begannen zu verschwinden. Schlimmer noch, die Affen hatten nun eine neue und ungemütliche kalte Jahreszeit zu gewärtigen, die wir heute »Winter« nennen. Wenn sie überleben wollten, mussten die Affen einen Teil der Kalorien, die sie zu sich nahmen, als Fett einlagern. Doch das war leichter gesagt als getan, denn ihre bisherige Evolution hatte sich in Afrika abgespielt, wo Nahrung immer verfügbar war. Aus diesem Grund hatte die Fettspeicherung in ihrem Stoffwechsel keinen Vorrang.
Irgendwann ereignete sich im Genom unserer Primatenvorfahren eine Zufallsmutation, die ihre Fähigkeit, Fructose in Fett zu verwandeln, sozusagen anknipste: Das Gen für das Enzym Uricase wurde »stumm geschaltet« oder ging verloren. Wenn die Affen jetzt Fructose konsumierten, produzierte ihr Körper jede Menge Harnsäure, sodass sie sehr viel mehr Fructosekalorien als Fett deponieren konnten. Diese neu erworbene Fähigkeit zur Fettspeicherung ermöglichte es ihnen, in einem kälteren Klima zu überleben. Sie konnten sich im Sommer mit Früchten den Bauch vollschlagen und Speck für den Winter ansetzen.
Diese Affen oder ihre evolutionären Nachfahren wanderten irgendwann wieder zurück nach Afrika; aus ihnen entwickelten sich im Laufe der Zeit die Hominiden und schließlich die Art Homo sapiens – wobei sich das stillgelegte Uricase-Gen immer weiter vererbte. Diese Mutation trug auch dazu bei, dass sich die Menschen über die ganze Erde ausbreiten konnten, weil sie in der Lage waren, Energie zu speichern und Kältephasen sowie Jahreszeiten ohne Nahrungsüberfluss zu überleben.
In der modernen Welt ist dieser Fettspeichermechanismus nicht mehr von Nutzen. Wir müssen uns keine Gedanken mehr machen, ob wir genügend Früchte sammeln und Fett für den Winter ansetzen können. Dank der Wunder der Lebensmitteltechnologie schwimmen wir heute geradezu in Fructose, vor allem in Form von Softdrinks, aber auch versteckt in so unschuldig wirkenden Fertigprodukten wie Salatdressings oder Joghurtzubereitungen.[93]
Ganz gleich, in welcher Form sie auftritt, Fructose stellt kein Problem dar, wenn sie so konsumiert wird wie von unseren Vorfahren, bevor Zucker jederzeit leicht verfügbar war: in Form von echten Früchten. Es ist sehr schwer, beispielsweise vom Verzehr von zu vielen Äpfeln dick zu werden, denn die Fructose aus den Äpfeln kommt relativ langsam und gemischt mit Wasser und Ballaststoffen in unserem System an; unser Darm und unser Stoffwechsel können dann ganz normal mit ihr umgehen. Etwas anderes ist es jedoch, wenn wir ein paar Liter Apfelsaft trinken, darauf kommen wir gleich zu sprechen.
Fructose ist nicht der einzige Nahrungsbestandteil, aus dem Harnsäure entsteht; Lebensmittel mit einem hohen Puringehalt, wie zum Beispiel Fleisch, Käse, Sardellen oder Bier, lassen den Harnsäurespiegel ebenfalls steigen. Aus diesem Grund war Gicht – eine Krankheit, die von zu viel Harnsäure im Blut verursacht wird – unter adligen Gourmands früherer Zeiten (und auch unter heutigen Vielfraßen) so weit verbreitet. Ich bestimme bei meinen Patienten den Harnsäurespiegel nicht nur, weil hohe Werte für mehr Fetteinlagerung sorgen, sondern auch, weil es einen Zusammenhang mit Bluthochdruck gibt. Hohe Harnsäurewerte sind ein frühes Warnzeichen, dass wir uns die Stoffwechselgesundheit oder die Ernährung eines Patienten anschauen sollten, oder auch beides.
Ein anderes Thema ist, dass Glucose und Fructose auf zellulärer Ebene sehr unterschiedlich verstoffwechselt werden. Wenn eine Hirnzelle, eine Muskelzelle, eine Darmzelle oder welcher Zelltyp auch immer Glucose abbaut, dann hat sie umgehend ATP (Adenosintriphosphat), die Energiewährung der Zelle, zur Verfügung. Diese Energie gibt es allerdings nicht umsonst: Die Zelle muss etwas ATP aufwenden, um mehr ATP zu gewinnen, so wie auch Sie manchmal Geld ausgeben müssen, um Geld zu bekommen. Im Glucose-Stoffwechsel wird diese Form des Energieaufwands von einem bestimmten Enzym geregelt, das die Zelle davon abhält, zu viel ATP für den Stoffwechsel »auszugeben«.
Wenn wir allerdings in großen Mengen Fructose verarbeiten, kommt ein anderes Enzym zum Einsatz, und das tritt bei den ATP-Ausgaben nicht auf die Sparbremse.[94] Stattdessen sinkt das Energieniveau (der ATP-Level) in der Zelle schnell und dramatisch ab. Das rasche Abfallen des Energieniveaus lässt die Zelle glauben, dass wir noch hungrig sind. Die Mechanismen sind etwas kompliziert, aber Fazit ist, dass Fructose – obwohl sie energiereich ist – unseren Stoffwechsel austrickst und ihm vorgaukelt, dass wir Energie verbrauchen – und darum mehr Nahrung aufnehmen und mehr Energie in Fettform speichern müssen.[95]
Auf einer anderen Ebene, der der Organe, bedeutet der Konsum großer Mengen Fructose in flüssiger Form eine Überforderung des Darms; das, was nicht verarbeitet werden kann, wird zur Leber umgeleitet, wo viele der Kalorien als Fett enden. Ich hatte schon Patienten, die sich auf diese Weise mit allzu vielen »gesunden« Frucht-Smoothies eine nichtalkoholische Fettleber angetrunken haben: Sie haben zu schnell zu viel Fructose zu sich genommen. Mit der beinahe unbegrenzten Verfügbarkeit von flüssiger Fructose, zusammen mit unserer sowieso schon kalorienreichen modernen Ernährung, ist das Stoffwechselversagen vorprogrammiert, wenn wir nicht aufpassen (und vor allem, wenn wir nicht körperlich aktiv sind).
Manchmal denke ich an den Patienten zurück, der mich mit der Fettleber bekannt gemacht hat. Er und »Patient null« von Samuel Zelman, der Mann, der mehrere Liter Cola am Tag trank, sie hatten dasselbe Problem: Sie nahmen wesentlich mehr Kalorien zu sich, als sie brauchten. Letzten Endes, das glaube ich immer noch, spielen die überschüssigen Kalorien doch die größte Rolle.
Natürlich war mein Patient nicht wegen seiner Fettleber im Krankenhaus, sondern wegen seines Darmkrebses. Seine Operation war ein voller Erfolg: Wir entfernten den von Krebs befallenen Teil des Darmes, und er erholte sich schnell. Sein Darmkrebs war bereits fortgeschritten, hatte aber noch keine Metastasen gebildet oder gestreut. Ich kann mich erinnern, dass der operierende Chirurg ziemlich zuversichtlich war, was die OP angeht, da wir den Krebs noch rechtzeitig entfernt hatten. Dieser Mann war vielleicht vierzig oder fünfundvierzig Jahre alt gewesen und hatte noch ein langes Leben vor sich.
Was wohl aus ihm geworden ist? Offensichtlich hatte er sich in einem frühen Stadium einer metabolischen Dysfunktion befunden. Ich frage mich immer noch, ob die beiden Erkrankungen, die Fettleber und der Krebs, vielleicht auf irgendeine Weise miteinander zusammenhingen. Wie wir in Kapitel 8 noch sehen werden, sind starkes Übergewicht und gestörter Stoffwechsel zwei große Risikofaktoren für Krebs. Könnten die Stoffwechselprobleme des Mannes in irgendeiner Weise seinen Krebs gefördert haben? Was wäre geschehen, wenn die zugrunde liegenden Probleme, die ganz eindeutig zu seiner Fettleber geführt hatten, zehn oder mehr Jahre früher entdeckt worden wären? Hätten wir uns überhaupt je getroffen?
Ich halte es für relativ unwahrscheinlich, dass sich Medizin 2.0 überhaupt mit ihm und seiner Situation beschäftigt hätte. Das übliche Vorgehen, es wurde in Kapitel 1 kurz angesprochen, ist, zu warten, bis der Langzeit-Blutzuckerwert (HbA1c) die magische Schwelle von 6,5 Prozent überstiegen hat, erst danach wird die Diagnose Diabetes Typ 2 gestellt. Doch zu diesem Zeitpunkt kann sich die betreffende Person bereits in einem Stadium mit erhöhtem Risiko befinden, wie wir in diesem Kapitel gesehen haben. Wenn wir die grassierende Epidemie von Stoffwechselerkrankungen bekämpfen wollen, für die die Fettleber lediglich ein Vorbote ist, müssen wir wesentlich früher ansetzen.
Ein Grund, weshalb ich das Konzept des metabolischen Syndroms für wertvoll halte, ist, dass es dazu beiträgt, diese Erkrankungen als Teil eines Kontinuums zu betrachten und nicht als einzelne Krankheiten, die man hat oder nicht. Die fünf relativ einfachen Kriterien sind nützlich, um das Risiko auf Bevölkerungsebene vorherzusagen. Nach meinem Dafürhalten warten wir aber immer noch zu lange ab, bis wir etwas zum Problem erklären, wenn wir uns auf diese Kriterien stützen. Warum sollte man warten, bis drei von fünf Kriterien erfüllt sind? Jedes für sich genommen stellt normalerweise bereits ein schlechtes Zeichen dar. Medizin 3.0 hätte den Ansatz, schon früher nach den Warnsignalen zu suchen. Wir wollen eingreifen, bevor Patienten ein metabolisches Syndrom entwickeln.
Das heißt, auf die frühesten Anzeichen von Problemen zu achten. Bei meinen eigenen Patienten untersuche ich regelmäßig verschiedene Biomarker für den Stoffwechsel, mein besonderes Augenmerk gilt dabei erhöhten Harnsäurewerten, erhöhten Homocysteinwerten, chronischen Entzündungszeichen und selbst leicht erhöhten ALT-Leberenzymen. Lipoproteine, auf die wir im nächsten Kapitel ausführlich zu sprechen kommen, sind ebenfalls wichtig, vor allem die Triglyceride. Ich achte besonders auf das Mengenverhältnis von Triglyceriden zu HDL-Cholesterin (es sollte kleiner sein als 2:1, besser noch kleiner als 1:1) und auf die Menge an VLDL, ein Lipoprotein, das Triglyceride transportiert – hier können überall schon viele Jahre, bevor ein Patient die Lehrbuchdefinition für das metabolische Syndrom erfüllt, Veränderungen auftreten. Diese Biomarker helfen uns, ein besseres Bild von der allgemeinen Stoffwechselgesundheit eines Menschen zu erhalten, als lediglich den Langzeit-Blutzucker zu betrachten, der für sich genommen nicht besonders spezifisch ist.
Aber das Erste, wonach ich suche, sind erhöhte Insulinwerte, sie sind für mich der Kanarienvogel in der Kohlenmine des gestörten Stoffwechsels. Wie wir gesehen haben, ist die erste Reaktion des Körpers auf eine beginnende Insulinresistenz die Steigerung der Insulinproduktion. Erinnern Sie sich an unseren Vergleich mit dem Ballon: Wenn es schwieriger wird, Luft (Glucose) in den Ballon (die Zelle) zu bekommen, dann müssen wir fester und immer fester pusten (also mehr Insulin produzieren). Zunächst scheint das zu funktionieren, der Körper ist weiterhin in der Lage, die Glucose-Homöostase, also einen konstanten Blutzuckerspiegel, aufrechtzuerhalten. Doch das Insulin, vor allem das postprandiale Insulin (siehe unten), hat schon zu steigen begonnen.
Ein Test, den ich gerne mit meinen Patienten mache, ist der orale Glucosetoleranztest (oGTT). Dafür nehmen sie 300 Milliliter einer widerlich süßen, fast nicht trinkbaren Flüssigkeit namens Glucola zu sich, die 75 Gramm reine Glucose enthält und damit etwa doppelt so viel Zucker wie eine normale Marken-Cola.[96] Anschließend messen wir in den nächsten zwei Stunden bei den Patienten alle 30 Minuten Blutzucker und Insulin. Typischerweise steigt ihr Blutzucker an, gefolgt von einem Anstieg des Insulins, danach sinkt der Blutzuckerspiegel gleichmäßig ab, weil das Insulin seine Arbeit tut und die Glucose aus dem Blut entfernt.
Auf den ersten Blick sieht alles gut aus: Insulin hat seine Arbeit getan und die Glucose unter Kontrolle gebracht. Doch bei Personen in den frühen Stadien von Insulinresistenz steigt der Insulinspiegel in den ersten 30 Minuten dramatisch an und bleibt dann für die nächste Stunde erhöht, manchmal steigt er sogar noch weiter. Diese sogenannte postprandiale Insulinspitze ist eines der größten frühen Warnzeichen, dass eben nicht alles in Ordnung ist.
Gerald Reaven, der 2018 im Alter von neunundachtzig Jahren starb, hätte dem sicher zugestimmt. Jahrzehntelang kämpfte er für die Anerkennung von Insulinresistenz als primäre Ursache für Diabetes Typ 2, inzwischen ist die Idee allgemein akzeptiert. Und dennoch ist der Diabetes nur eine von mehreren Gefahren: Studien beobachteten im Zusammenhang mit Insulinresistenz einen gewaltigen Anstieg der Risiken für Krebs (bis zwölfmal höher), Alzheimer (fünfmal höher) und Tod durch Herz-Kreislauf-Krankheiten (fast sechsmal höher),[97] was nur noch einmal unterstreicht, weshalb die Behandlung oder besser noch das Verhindern von Stoffwechselstörungen ein Eckpfeiler meines Langlebigkeitskonzepts ist.
Es scheint zumindest plausibel, dass mein Fettleber-Patient irgendwann erhöhte Insulinwerte entwickelte, lange vor seiner Krebsoperation. Aber es ist ebenso unwahrscheinlich, dass Medizin 2.0 auch nur darüber nachgedacht hätte, ihn zu behandeln, was für mich schwer nachvollziehbar ist. Wenn irgendein anderes Hormon derart aus dem Gleichgewicht geraten wäre, zum Beispiel ein Schilddrüsenhormon oder gar Cortisol, hätten die Ärzte schnell eingegriffen, um den Normalzustand wiederherzustellen. Letzteres könnte ein Symptom für das Cushing-Syndrom sein, während Ersteres ein Zeichen für Morbus Basedow oder eine andere Form einer Schilddrüsenüberfunktion wäre. Diese endokrinen, das heißt das Hormonsystem betreffenden Erkrankungen müssen sofort, nachdem die Diagnose gestellt ist, behandelt werden. Nichts zu unternehmen wäre ein Behandlungsfehler. Nur bei der Hyperinsulinämie warten wir aus irgendeinem Grund ab und tun nichts. Erst wenn die Diagnose Diabetes Typ 2 steht, wird endlich gehandelt. Das wäre, als würde man bei der Basedow-Krankheit warten, bis die Augen aus den Höhlen hervortreten (wie man es typischerweise bei Personen mit unbehandelter Schilddrüsenüberfunktion beobachten kann), ehe man mit der Behandlung beginnt.
Es ist mehr als rückständig, dass wir die Hyperinsulinämie nicht wie eine eigenständige endokrine Erkrankung behandeln. Ich behaupte, dass wir dadurch für die menschliche Gesundheit und die Langlebigkeit mehr erreichen würden als mit jeder anderen Therapiemaßnahme. In den nächsten drei Kapiteln werden wir uns die drei anderen großen Alterskrankheiten näher ansehen – die Herz-Kreislauf-Erkrankungen, Krebs und die neurodegenerativen Krankheiten –, die alle auf irgendeine Weise von einem gestörten Stoffwechsel gefördert werden. Und es wird Ihnen hoffentlich klar werden, so wie es mir klar wurde, dass der logische erste Schritt bei unserem Versuch, den Tod hinauszuschieben, darin besteht, unseren Stoffwechsel in Ordnung zu bringen.
Die gute Nachricht ist, dass wir darauf großen Einfluss haben. Veränderungen in den Bereichen Ernährung, körperliche Aktivität und Schlaf (siehe Teil III) können das Blatt zu unseren Gunsten wenden. Die schlechte Nachricht ist, dass wir uns dafür bemühen müssen, den heute normalen Umweltbedingungen ein Schnippchen zu schlagen, die sich mit zu viel Essen, zu wenig Bewegung und zu wenig Schlaf gegen unsere alten (und einstmals hilfreichen) Fettspeicher-Gene verschworen haben.
Kapitel 7
Die Pumpe
Herz-Kreislauf-Krankheiten, die Todesursache Nr. 1, angehen und sie verhindern
Handeln birgt ein gewisses Risiko, das wird immer so sein. Ein wesentlich höheres Risiko liegt jedoch darin, nicht zu handeln.
Harry S. Truman
Ein Nachteil meiner Profession ist, dass sich zu viel Wissen zu einer Art Fluch entwickeln kann. Als ich mich, nach einem Ausflug in die Wirtschaft, wieder ganz der Medizin zuwandte, dämmerte mir, dass ich bereits weiß, wie ich wohl sterben werde: Ich bin prädestiniert für den Herztod.
Ich frage mich, weshalb es so lange gedauert hat, bis ich den Wink des Schicksals verstanden hatte. Als ich fünf Jahre alt war, starb Francis, der ältere Bruder meines Vaters, sein Lieblingsbruder von den acht Geschwistern, im Alter von sechsundvierzig Jahren am plötzlichen Herztod. Als mein Bruder Paul zwei Jahre später auf die Welt kam, gab ihm mein immer noch trauernder Vater den zweiten Vornamen Francis. Und so wie bestimmte Vornamen in Familien zur Tradition werden, scheint meine zudem eine Neigung zum frühen Herztod zu haben. Ein weiterer Onkel erlitt mit zweiundvierzig einen tödlichen Herzinfarkt, während ein dritter bis neunundsechzig durchhielt, ehe sein Herz ihn umbrachte, in dem Alter nicht ganz so ungewöhnlich, aber immer noch viel zu jung.
Mein Vater hatte Glück, er hat es (bis jetzt) auf stattliche fünfundachtzig Jahre gebracht. Doch auch in einem seiner Herzkranzgefäße sitzt ein Stent, der ihn an ein kleineres »Ereignis« in seinen Mittsechzigern erinnert. Eines Tages verspürte er an seinem Arbeitsplatz in einem Steinbruch einen Schmerz in der Brust und landete in der Notaufnahme, wo man feststellte, dass er vor Kurzem einen Infarkt gehabt haben musste. Der Stent, eine kleine Hülse aus Metalldraht, wurde etwa ein Jahr später gesetzt. Ich bin nicht wirklich überzeugt, dass der Stent irgendetwas brachte – als er ihn bekam, hatte mein Vater keinerlei Beschwerden –, aber vielleicht machte er ihm so viel Angst, dass er daraufhin besser auf seine Medikamenteneinnahme und seine Ernährung achtete.
Obwohl mein eigenes Cholesterinprofil hervorragend ist und ich mich vernünftig ernähre, normalen Blutdruck habe und nur selten Alkohol trinke, habe ich ein erhöhtes Risiko. Ich komme mir vor wie in der Anekdote von Charlie Munger über den Typen, der wissen will, wo er sterben wird, damit er diesen Ort auf jeden Fall meiden kann. Leider findet der Herztod seine Opfer allzu oft von sich aus.
Während meines Medizinstudiums stellte der Pathologie-Professor, den wir im ersten Jahr hatten, gerne eine Fangfrage: In welcher Form (mit welchen Symptomen) präsentieren sich kardiovaskuläre Erkrankungen am häufigsten? Es war nicht der Schmerz in der Brust oder im linken Arm, es war auch nicht die Kurzatmigkeit, die Antworten, die am häufigsten gegeben wurden, es war der plötzliche Herztod. Man weiß, dass der Patient eine kardiovaskuläre Erkrankung hatte, weil er gerade daran gestorben ist. Aus diesem Grund, so behauptete mein Prof, sind Pathologen die einzigen Ärzte, die kardiovaskuläre Erkrankungen wirklich verstehen. Sein Punkt: Sobald ein Pathologe Ihre Arterien sieht, sind Sie tot.
Die Sterblichkeitsraten nach solchen erstmaligen, überraschenden Herzinfarkten sind signifikant gesunken – dank Verbesserungen bei den lebensrettenden Sofortmaßnahmen und rechtzeitigen Interventionen wie Herzkatheter und Medikamente, die Blutgerinnsel auflösen, wodurch ein Herzinfarkt fast im Keim erstickt werden kann; dennoch endet etwa ein Drittel der Ereignisse tödlich, wie Ron Krauss, leitender Wissenschaftler und Direktor der Atheroskleroseforschung am Children’s Hospital Oakland Research Institute, erklärt.
Global stellen die atherosklerosebedingten Herz-Kreislauf-Erkrankungen (ASCVD), zu denen unter anderem die koronare Herzkrankheit und der ischämische Schlaganfall (»Hirninfarkt«) gehören, die Haupttodesursache dar. Heron (2021); WHO (2019) Angaben der Centers of Disease Control (CDC) zufolge sterben in den Vereinigten Staaten jeden Tag schätzungsweise 2300 Personen an einer dieser Krankheiten,[98] nicht einmal Krebs tötet mehr Menschen. Dabei sind nicht nur Männer gefährdet: Das Risiko, an einer atherosklerosebedingten Krankheit zu sterben, ist für Amerikanerinnen zehnmal höher als der Tod infolge von Brustkrebs (kein Druckfehler: eine von drei gegenüber eine von dreißig).[99] Doch die rosa Schleifen für Brustkrebs sind weit häufiger zu sehen als die von der American Heart Association ausgegebenen roten Schleifen, die ein Bewusstsein für Herz-Kreislauf-Erkrankungen bei Frauen schaffen sollen.
Der Tod meiner Onkel bleibt für mich ein Rätsel. Sie lebten in Ägypten, und ich habe keine Ahnung, wie ihr Blutbild aussah, oder, wichtiger noch, in welchem Zustand ihre Herzkranzgefäße sich befanden. Ich bin mir ziemlich sicher, dass sie rauchten, aber vielleicht hätten sie, wie mein Vater, ihre Herzinfarkte überlebt, wenn sie Zugang zu besserer medizinischer Versorgung gehabt hätten. Vielleicht konnten sie ihrem Schicksal aber nicht entgehen, weil es in ihren Genen lag. Ich weiß nur, dass zweiundvierzig für einen Tod durch Herzinfarkt wirklich sehr jung ist.
Dass meine Onkel jung starben, wusste ich immer, aber was das für mich bedeutet, ging mir erst mit Mitte dreißig auf, als ich selbst zum ersten Mal Vater wurde. Plötzlich stürzte das Bewusstsein meiner eigenen Sterblichkeit auf mich ein wie eine Riesenwelle, die während einer meiner langen Schwimmtouren aus dem Nichts auftaucht. Dieses Buch wäre ohne meine Familiengeschichte vermutlich nicht geschrieben worden.
Wie die meisten Sechsunddreißigjährigen hatte der etwas vollschlanke Peter bislang keinen Gedanken an Herz-Kreislauf-Erkrankungen verschwendet. Warum auch? Mein Herz war stark genug, mich durch den 34 Kilometer breiten Catalina Channel schwimmen zu lassen, dabei arbeitete es mehr als 14 Stunden gleichmäßig durch und schnurrte in meiner Brust so ruhig wie ein Dieselmotor. Ich war in großartiger Form, dachte ich. Trotzdem war ich besorgt, eben wegen meiner Familiengeschichte. Darum bestand ich darauf, dass mein Arzt ein CT von meinem Herzen machte, und das hat mein Leben komplett verändert.
Die Computertomografie wurde so durchgeführt, dass sie eventuelle Verkalkungen in meinen Herzkranzgefäßen entdecken konnte, die Zeichen einer fortgeschrittenen Atherosklerose. Die Auswertung ergab, dass ich einen Calcium-Score von 6 hatte. Das klingt niedrig, und in absoluten Zahlen ist es das auch; jemand mit einer schweren koronaren Herzerkrankung könnte auf einen Score von über 1000 kommen. Aber bei einem Sechsunddreißigjährigen sollte er null sein. Mit einem Score von 6 hatte ich mehr Calcium in meinen Herzkranzgefäßen als 75 bis 90 Prozent der Menschen meines Alters. Als ich mich eingehender mit der Pathologie dieser Erkrankung beschäftigte, musste ich betroffen feststellen, dass ich schon etwas spät dran war. Anhand des Calcium-Scores lässt sich das zukünftige Risiko prognostizieren, aber er ist gleichzeitig ein Maß für frühere wie für aktuelle Schäden. Und ich fiel schon völlig aus dem Raster. Ich war erst Mitte dreißig, doch ich hatte die Arterien eines Fünfundfünfzigjährigen.
Diese Enthüllung wühlte mich auf, aber nach allem, was ich heute weiß, war das eigentlich nicht überraschend. Zu der Zeit hatte ich Übergewicht und stand kurz vor der Insulinresistenz, zwei große Risikofaktoren, die beide dazu beitragen, eine Umgebung zu schaffen, die die Entwicklung von atherosklerotischen Läsionen begünstigt und beschleunigt. Aber weil mein Calcium-Score »nur« 6 war und der wichtigste Cholesterinwert, der des (»schlechten«) LDL-Cholesterins, im »Normalbereich« lag, erhielt ich den ärztlichen Rat – Achtung! – abzuwarten. Kommt Ihnen das bekannt vor?
Nichts tun ist nicht meine Art, wie Sie vielleicht schon gemerkt haben. Ich hatte das Gefühl, auf einem falschen Weg zu sein, und musste herausfinden, wie ich das ändern konnte. Meine Wissbegierde war der Startschuss für eine Jahre dauernde Suche nach einem tieferen Verständnis der Atherosklerose. Und was ich – mit der großzügigen Hilfe meiner Mentoren Tom Dayspring, Allan Sniderman und Ron Krauss (um nur einige zu nennen), allesamt Experten von Weltruf auf dem Gebiet der Pathologie des Herzens und/oder der Lipidforschung – entdeckte, war absolut verblüffend.
Obwohl es sich bei Herz-Kreislauf-Erkrankungen um die häufigsten altersbedingten Krankheiten handelt, lassen sie sich leichter verhindern als Krebs oder Alzheimer. Wir wissen viel darüber, wie und warum sie beginnen und wie sie fortschreiten. Man kann sie nicht in der gleichen Weise heilen oder umkehren, wie es (manchmal) mit Diabetes Typ 2 möglich ist, aber wenn man es clever anstellt und früh damit anfängt, lassen sie sich relativ leicht nach hinten verschieben.
Außerdem haben wir hier eines der relativ seltenen Beispiele, wo Medizin 2.0 schon auf Prävention setzt, zumindest in einigen Bereichen. Wir verfügen über ein recht großes Sortiment an blutdruck- und cholesterinsenkenden Medikamenten, die das Risiko für viele Patienten deutlich senken, wir können Blutuntersuchungen machen und bildgebende Verfahren einsetzen (wie für meinen Calcium-Score), die uns zumindest eine Momentaufnahme, mag sie auch noch so unscharf sein, unserer kardiovaskulären Gesundheit liefern. Es ist ein Anfang.
Aber obwohl wir die atherosklerosebedingte Krankheiten recht gut verstehen und obwohl wir über viele Mittel verfügen, um sie zu verhindern, sterben in den Vereinigten Staaten Jahr für Jahr immer noch mehr Menschen daran als an Krebs, und viele von ihnen häufig aus völlig heiterem Himmel. Wir verlieren den Krieg. Ich behaupte nicht, alle Antworten zu kennen, aber ich denke, das liegt zumindest zum Teil daran, dass es immer noch ein paar blinde Flecken in unserem Verständnis dessen gibt, was das Erkrankungsrisiko wirklich erhöht, wie es sich entwickelt und vor allem, wann wir handeln müssen, um seine Dynamik zu bremsen.
Das Hauptproblem ist, meiner Meinung nach, die klassische Medizin 2.0: Die Richtlinien für den Umgang mit kardiovaskulären Risiken beruhen auf einem viel zu kurzen Zeithorizont, verglichen mit der Dauer der Erkrankungen. Wir müssen viel früher mit der Behandlung, mit der Prävention beginnen. Wenn wir das richtig hinbekämen, hätten wir einen enormen Nutzen zu erwarten: Die große Zahl männlicher Hundertjähriger auf Sardinien, zum Beispiel, wird in der Regel mit ihrer Fähigkeit erklärt, Herz-Kreislauf-Krankheiten zu vermeiden oder aufzuschieben. Im Alter zwischen achtzig und hundert sterben nirgendwo in Italien weniger Männer daran als auf Sardinien.[100]
Davon sind wir weit entfernt. Die kardiovaskulären Erkrankungen sind unser größter Killer, der schlimmste der apokalyptischen Reiter des Alterns. Ich hoffe, ich kann Sie auf den folgenden Seiten überzeugen, dass das nicht sein muss – dass es mit der richtigen Strategie und Aufmerksamkeit für die richtigen Risikofaktoren zur richtigen Zeit möglich sein müsste, einen Großteil von Morbidität und Mortalität zu beseitigen, die immer noch mit atheroklerosebedingten Herz-Kreislauf-Erkrankungen einhergehen.
Kurz gesagt: Das sollte die zehnthäufigste Todesursache sein, nicht die häufigste.
Wissenschaftler erforschen die medizinischen Geheimnisse des Herzens fast schon so lange, wie Dichter seine metaphorischen Tiefen zu ergründen suchen. Es ist ein wunderbares Organ, ein Muskel, der unermüdlich in jedem Augenblick unseres Lebens Blut durch unseren Körper pumpt. Wenn wir Sport treiben, hat das Herz eine hohe Schlagzahl, während des Schlafes fährt es die Frequenz herunter, und zwischen den Schlägen kann es sie sogar noch nachjustieren, eine äußerst wichtige Fähigkeit, die sogenannte Herzfrequenzvariabilität. Wenn das Herz stehen bleibt, ist es vorbei mit uns.
Ein ähnliches Wunderwerk ist unser Blutgefäßsystem, Abertausende miteinander verbundene Venen, Arterien und Kapillargefäße, die ausgebreitet und aneinandergelegt mehr als zweimal um die ganze Erde reichen würden (etwa 96 000 Kilometer, wenn Sie nachrechnen wollen).[101] Jedes einzelne Blutgefäß muss Materialwissenschaftler und Ingenieure zum Staunen bringen: Es kann sich ein paar Dutzend Mal pro Minute zusammenziehen und wieder ausdehnen, es lässt lebenswichtige Substanzen durch seine Gefäßwände treten und vermag sich an enorme Schwankungen des Blutdrucks anzupassen, und das mit minimalen Ermüdungserscheinungen. Wenn ein Blutgefäß beschädigt ist, wachsen an seiner Stelle neue nach und gewährleisten damit den ununterbrochenen Blutfluss durch den Körper.
So unglaublich es klingt, unser Blutkreislauf ist dennoch alles andere als vollkommen, tatsächlich ist er fast wie dafür geschaffen, im Verlauf eines normalen Lebens Atherosklerose und dadurch bedingte Erkrankungen zu entwickeln. Das liegt großenteils an einer weiteren wichtigen Funktion unseres Gefäßsystems. Das bringt nämlich nicht nur Sauerstoff und Nährstoffe in die Gewebe hinein und Abfallstoffe aus ihnen heraus, nein, unser Blut transportiert auch Cholesterin zwischen den Zellen hin und her.
Es ist praktisch zum Unwort geworden: Cholesterin. Ihr Arzt spricht es wahrscheinlich mit einem Stirnrunzeln aus, denn jeder weiß, dass Cholesterin ein böses Zeug ist. Zumindest ein Teil davon, Sie wissen schon, das »schlechte« oder »LDL«- Cholesterin, das unweigerlich dem »guten« oder »HDL«- Cholesterin gegenübergestellt wird. Ich muss mich regelmäßig zusammenreißen, wenn ich diese Begriffe höre, weil sie so bedeutungslos sind. Und das »Gesamtcholesterin«, der erste Wert, den einem Menschen auftischen, wenn man über Herz-Kreislauf-Krankheiten spricht, hat für Ihr kardiovaskuläres Risiko nur unwesentlich mehr Bedeutung als Ihre Augenfarbe. Also lassen Sie uns die Sache noch einmal aufrollen und einen Blick darauf werfen, was Cholesterin wirklich ist, was es tut und welchen Beitrag es zu Herz-Kreislauf-Erkrankungen leistet.
Cholesterin ist lebensnotwendig. Es wird für die Herstellung von einigen der wichtigsten Körperbestandteilen gebraucht, zum Beispiel Bausteine für Zellmembranen, Hormone wie Testosteron, Progesteron, Östrogen und Cortisol, aber auch Gallensäuren, die für die Verdauung der Nahrung gebraucht werden. Alle Zellen können ihr eigenes Cholesterin produzieren, doch gut 20 Prozent unseres (großen) Körpervorrats liegt in der Leber, die als eine Art Cholesterindepot fungiert, von wo aus der Stoff zu den Zellen geschickt wird, die ihn brauchen, und in das er über den Blutkreislauf zurückgebracht wird.
Cholesterin gehört zur Familie der Lipide (Fette), darum ist es nicht wasserlöslich. Das heißt, es kann sich nicht wie Glucose oder Natrium in unserem Blutplasma lösen und sich frei durch das Blutgefäßsystem bewegen. Dafür muss es in winzige runde Teilchen verpackt werden, die sogenannten Lipoproteine (das letzte L in HDL und LDL), die wie kleine Fracht-U-Boote arbeiten. Wie ihr Name vermuten lässt, bestehen Lipoproteine zum Teil aus Lipiden (innen) und zum Teil aus Proteinen (außen). Das Protein ist im Wesentlichen das Transportmittel, das die Reise durch unser Blutplasma ermöglicht, mit einer wasserunlöslichen Fracht aus Lipiden, inklusive Cholesterin, Triglyceriden und Phospholipiden, außerdem Vitaminen und anderen Proteinen, die zu Geweben in weiter entfernten Körperbereichen gebracht werden müssen.
HDL und LDL heißen mit »vollem Namen« high-density bzw. low-density lipoproteins (Lipoproteine hoher bzw. niedriger Dichte); die Namen beziehen sich auf die Menge an Fett, die sie im Vergleich zu Proteinen jeweils transportieren. LDLs transportieren mehr Lipide, HDLs mehr Proteine im Vergleich zu Fett, deswegen haben Letztere eine höhere Dichte. Zudem tauschen diese Partikel (und andere Lipoproteine) häufig ihre Fracht untereinander aus – ein Grund, weshalb ich mich über die Etiketten »gutes« und »schlechtes« Cholesterin so aufrege. Wenn ein HDL sein »gutes« Cholesterin an ein LDL-Teilchen übergibt, wird das Cholesterin dann plötzlich »schlecht«?
Die Antwort lautet: Nein, denn es ist nicht das Cholesterin an sich, das die Probleme verursacht, sondern die Natur der Partikel, in denen es transportiert wird. Deren »Hülle« besteht aus ein oder mehreren großen Proteinmolekülen, den sogenannten Apolipoproteinen, die ihm Struktur und Stabilität verleihen und, was noch wichtiger ist, die dafür sorgen, dass es wasserlöslich wird. HDL-Partikel werden in einen Molekültyp verpackt, den man als Apolipoprotein A (ApoA) bezeichnet, die Hülle für LDL dagegen gehört zur Gruppe der Apolipoproteine vom Typ B (ApoB). Diese Unterscheidung mutet trivial an, aber sie hat ganz direkt mit der Ursache des Atheroskleroseproblems zu tun: Jedes einzelne Lipoprotein, das zur Atherosklerose beiträgt – nicht nur LDL, sondern noch ein paar andere[102] –, trägt die ApoB-Kennung.
Ein weiteres großes Missverständnis im Zusammenhang mit Herz-Kreislauf-Erkrankungen ist, dass sie irgendwie durch das Cholesterin in unserer Nahrung verursacht werden sollen. Nach dieser veralteten und stark vereinfachenden Auffassung führt der Verzehr von Lebensmitteln, die viel Cholesterin enthalten, dazu, dass sich das sogenannte schlechte Cholesterin in unserem Blut anreichert und an den Wänden der Arterien ablagert, so als würden Sie das Fett, in dem Sie morgens Ihren Frühstücksspeck braten, danach jedes Mal aus der Pfanne in den Ausguss gießen. Früher oder später wird der Abfluss verstopft sein.
Insbesondere Eier wurden 1968 in einer öffentlichen Erklärung der American Heart Association als Schuldige ausgemacht, sie sollten wegen ihres hohen Cholesteringehalts ursächlich an der Entstehung von Herz-Kreislauf-Erkrankungen beteiligt sein.[103] Jahrzehntelang schmorten sie daraufhin im Ernährungs(-beratungs)-fegefeuer, selbst nachdem unzählige Forschungsarbeiten gezeigt hatten, dass Cholesterin (und insbesondere der Verzehr von Eiern) nicht das Geringste mit Herz-Kreislauf-Erkrankungen zu tun hat. Erhöhter Konsum von gesättigten Fetten kann den Spiegel Atherosklerose verursachender Lipoproteine im Blut steigen lassen, aber den größten Teil des Cholesterins, das wir mit unserer Nahrung aufnehmen, scheiden wir postwendend mit dem Stuhl wieder aus.[104] Das meiste Cholesterin in unserem Blutkreislauf wird tatsächlich von unseren eigenen Zellen hergestellt.[105] Trotzdem warnten die offiziellen Ernährungsrichtlinien uns jahrzehntelang vor dem Verzehr cholesterinreicher Nahrungsmittel, und unter den Ernährungsinfos auf der Verpackung steht immer noch, wie viel Cholesterin in einer Portion des betreffenden Lebensmittels enthalten ist.
Selbst Ancel Keys, der berühmte Ernährungswissenschaftler, der zu den Gründervätern der Idee gehörte, dass gesättigte Fette zu Herzinfarkt führen, wusste, dass das Unsinn ist. Er erkannte den Ursprung des Problems: Die Grundlagenforschung zu Cholesterin und Atherosklerose wurde in der Regel mit Kaninchen (als Versuchstieren) durchgeführt, die aber verfügen über die einzigartige Fähigkeit, Cholesterin aus der Nahrung ins Blut aufzunehmen und daraus atherosklerotische Plaques zu bilden. Der Fehler war zu glauben, dass Menschen ebenfalls so leicht Cholesterin aus der Nahrung aufnehmen können. »Es gibt keine wie auch immer geartete Beziehung zwischen Cholesterin in der Nahrung und Cholesterin im Blut«, so Ancel Keys 1997 in einem Interview.[106] »Keine. Und das wissen wir schon die ganze Zeit. Cholesterin in der Nahrung spielt nicht die geringste Rolle, es sei denn, Sie sind ein Huhn oder ein Kaninchen.«
Aber es dauerte noch einmal fast zwanzig Jahre, bis das Beratergremium, das für die Ernährungsrichtlinien der US- Regierung zuständig ist, endlich (2015) einräumte: »Cholesterin ist kein Nährstoff, bei dem man einen zu hohen Konsum befürchten muss.«[107] Gut, dass wir das geklärt haben.
Der letzte Mythos, mit dem wir aufräumen müssen, ist die Vorstellung, dass kardiovaskuläre Erkrankungen in erster Linie »alte« Menschen treffen und wir uns demzufolge bei zwanzig-, dreißig-, vierzigjährigen Patienten über Prävention nicht groß Gedanken machen müssen. Ganz falsch. Nie werde ich den Ein-Fragen-Schnelltest vergessen, dem mich Allan Sniderman 2014 beim Abendessen auf dem Dulles Airport unterzog: »Wie hoch ist bei Herzinfarkten der Anteil von Menschen unter fünfundsechzig?« Ich tippte einer von vier und dachte, das sei hoch geschätzt, aber ich lag viel zu niedrig. Ganze 50 Prozent aller schwereren kardiovaskulären Ereignisse bei Männern (und ein Drittel bei Frauen), wie Herzinfarkt, Schlaganfall oder Eingriffe, bei denen ein Stent oder ein Transplantat zum Einsatz kommt, treten vor dem fünfundsechzigsten Lebensjahr ein.[108] Bei Männern findet ein Viertel aller Ereignisse vor dem vierundfünfzigsten Lebensjahr statt.
Doch selbst wenn die Ereignisse an sich überraschend eintreten, lauerte das Problem schon seit Jahren im Untergrund. Atherosklerose ist eine Krankheit, die sich langsam, schleichend entwickelt, deshalb bin ich in diesem Punkt so unnachgiebig. Das Risiko für solche »Ereignisse« steigt in der zweiten Lebenshälfte steil an, aber einige Wissenschaftler glauben, dass die zugrunde liegenden Prozesse bereits in der späten Adoleszenz, manchmal sogar schon im Teenageralter in Gang gesetzt werden. Das Risiko wächst im Laufe unseres Lebens, und Zeit ist der kritische Faktor. Darum ist es so wichtig, dass wir verstehen, wie es sich entwickelt und vergrößert, damit wir eine Strategie entwickeln können, um es zu verlangsamen oder anzuhalten.
Als ich noch ein Büro hatte, in der Zeit vor Corona, stand dort ein sehr aufgeräumter Schreibtisch, aber ein bestimmtes Buch lag immer darauf: der Atlas of Atherosclerosis Progression and Regression von Herbert C. Stary.[109] Es wird sicher nie zum Bestseller werden, aber auf dem Gebiet der kardiovaskulären Pathologie ist es legendär. Es hat sich auch als äußerst effektives Mittel erwiesen, um meinen Patienten den Ernst der Lage zu erklären; das liegt an seinen vielen grausigen Fotos von arteriellen Läsionen, wie sie entstehen, sich entwickeln und aufreißen, Fotos, die alle die Arterien von Toten zeigen, die in ihren Dreißigern oder Vierzigern waren, als sie starben. Die Geschichte, die hier anschaulich in allen Details ausgebreitet wird, ist gleichermaßen faszinierend und Furcht einflößend. Wenn ich damit durch bin, zeigen viele meiner Patienten einen derart gequälten Gesichtsausdruck, als hätten sie gerade ein großformatiges Fotobuch durchgeblättert, in dem ihr eigener Tod dokumentiert wird.
Die Analogie ist nicht perfekt, aber ich stelle mir Atherosklerose gerne als Schauplatz eines Verbrechens vor – als einen Einbruch, jedenfalls so ungefähr. Nehmen wir eine Straße, sie steht für das Blutgefäß, und die Straße wird von Häusern gesäumt, das ist die Arterienwand. Der Zaun vor jedem Haus kann mit dem Endothel verglichen werden, einer zwar dünnen, aber sehr wichtigen Gewebeschicht, die all unsere Arterien und Venen auskleidet, ebenso aber auch Organe wie die Nieren. Das Endothel besteht nur aus einer einzigen Zelllage und dient als semipermeable (halbdurchlässige) Barriere zwischen dem Gefäßlumen (dem Straßenraum, wo das Blut fließt) und der eigentlichen Gefäßwand; es kontrolliert die Passage von Materialien, Nährstoffen und weißen Blutkörperchen in die Blutbahn und aus ihr heraus. Es hilft außerdem, das Gleichgewicht von Flüssigkeit und Elektrolyten aufrechtzuerhalten; Probleme mit dem Endothel können zu Ödemen (Wassereinlagerungen) und Schwellungen führen. Eine weitere wichtige Aufgabe des Endothels ist es, das Gefäß zu weiten oder zu verengen, um den Blutfluss zu erhöhen oder zu vermindern; dieser Prozess wird von Stickstoffmonoxid (NO) moduliert. Und schließlich reguliert das Endothel noch Gerinnungsvorgänge, die bedeutsam werden können, wenn Sie sich etwa aus Versehen in den Finger schneiden. Es handelt sich also um eine ziemlich wichtige kleine Struktur.
Auf der Straße ist viel los, ständig strömen Blutzellen, Lipoproteine und andere Plasmabestandteile vorbei, die im Blutkreislauf zirkulieren, und alles schrammt am Endothel entlang. Es lässt sich kaum verhindern, dass cholesterinhaltige Lipoprotein-Partikel gelegentlich die Barriere durchbrechen und in einen Bereich gelangen, den man als Subendothel bezeichnet, in unserem Bild wäre es der Eingangsbereich eines Hauses. Normalerweise ist das in Ordnung, so als ob Gäste für einen Kurzbesuch vorbeikommen. Sie kommen rein und sie gehen wieder. HDL-Partikel tun das im Allgemeinen: Mit dem ApoA-Marker versehene Teilchen können die Endothelbarriere problemlos in beide Richtungen passieren. LDL-Partikel und andere Teilchen mit dem ApoB-Protein dagegen neigen schnell einmal dazu, auf der Innenseite hängen zu bleiben.
Und dieser Unterschied macht die HDL-Partikel zu den »guten« und die LDL-Partikel zu den »schlechten« Lipoproteinen, nicht das Cholesterin, das sie beide transportieren. Das Problem beginnt, wenn LDL-Partikel in der Arterienwand stecken bleiben und oxidieren, das heißt, das Cholesterin und andere Moleküle in ihrem Inneren, wie zum Beispiel Phospholipide, kommen in Kontakt mit einem hochreaktiven Sauerstoffmolekül (ROS, reactive oxygen species, auch Sauerstoffradikal genannt), der Ursache von oxidativem Stress. Die Oxidation der Lipide in den LDL bringt die Reaktionskaskade in Gang, die zu Atherosklerose führt.
Nun, da es im Subendothel hockt und oxidiert ist, wodurch es einen leicht toxischen Charakter bekommt, verhält sich LDL/ApoB nicht länger wie ein höflicher Gast, sondern weigert sich zu gehen und lädt noch ein paar Kumpel, andere LDL, zur Party ein. Von denen bleiben auch einige hängen und oxidieren. Es ist kein Zufall, dass die beiden größten Risikofaktoren für Herz-Kreislauf-Erkrankungen, Rauchen und Bluthochdruck, das Endothel schädigen. Beim Rauchen geschieht das auf chemischem Weg, beim Blutdruck mechanisch, doch am Ende steht die Endothelschädigung, die ihrerseits dazu führt, dass mehr LDL zurückgehalten wird. Je mehr oxidiertes LDL sich ansammelt, desto größer werden die Schäden am Endothel.
Ich spreche zwar von LDL, aber der Schlüsselfaktor ist eigentlich der Kontakt mit allen Partikeln, die den ApoB-Marker tragen. Je mehr dieser Teilchen – nicht nur LDL, sondern auch VLDL und noch einige andere – in Ihrem Blutgefäßsystem kreisen, desto höher ist das Risiko, dass ein paar davon das Endothel passieren und stecken bleiben. Zurück zu unserem Bild von der Straße: Stellen Sie sich vor, wir hätten, sagen wir, eine Tonne Cholesterin, verteilt auf vier große Pick-ups, die Straße hinunterzutransportieren. Die Wahrscheinlichkeit für einen Unfall wäre relativ gering. Doch was wäre, wenn wir die gleiche Menge Cholesterin, verteilt auf 500 dieser kleinen E-Scooter, die überall durch unsere Städte flitzen (auch in Austin, wo ich wohne), transportieren wollten? Wir würden vermutlich ein Riesendurcheinander[110] erleben. Um das wahre Ausmaß Ihres Risikos einschätzen zu können, müssen wir wissen, wie viele dieser ApoB-Teilchen in Ihrem Blutkreislauf zirkulieren. Deren Zahl ist von sehr viel größerer Bedeutung als die Gesamtmenge an Cholesterin, die sie mit sich führen.
Wenn man ein gesundes Herzkranzgefäß nimmt und es über längere Zeit hohen Konzentrationen von ApoB-Partikeln aussetzt, dann wird eine gewisse Menge LDL (und VLDL) im Subendothel hängen bleiben und oxidieren, was dazu führt, dass sich die Teilchen zu Aggregaten zusammenlagern. Als Reaktion auf diesen Einbruch wählt das Endothel das biochemische Äquivalent zur Notrufnummer 112 und ruft damit spezialisierte Immunzellen, sogenannte Monozyten, auf den Plan, um die Eindringlinge zu stellen. Monozyten sind große weiße Blutkörperchen, die sich im Subendothel in Makrophagen verwandeln, noch größere und gefräßigere Immunzellen, die manchmal mit der Computerspielfigur Pac-Man verglichen werden. Makrophagen (der Name bedeutet »großer Esser«) verschlucken die aggregierten oder oxidierten LDL und versuchen, sie aus der Arterienwand zu entfernen. Wenn sie allerdings zu viel Cholesterin aufnehmen, blähen sie sich zu Schaumzellen auf, die so heißen, weil sie unter dem Mikroskop ein bisschen wie Badeschaum aussehen. Wenn sich genügend Schaumzellen angesammelt haben, bilden sie einen fatty streak – im wahrsten Sinne des Wortes einen Fettstreifen, der mit bloßem Auge zu sehen ist, wenn man bei einer Autopsie ein Herzkranzgefäß längs aufschneidet.
Der fatty streak ist der Vorläufer der atherosklerotischen Plaque, und wenn Sie beim Lesen dieses Buches fünfzehn Jahre oder älter sind, dann können Sie damit rechnen, dass sich in Ihren Arterienwänden bereits ein paar befinden. Jawohl, ich sagte fünfzehn und nicht fünfzig, die Plaquebildung ist ein lebenslanger Prozess, der schon sehr früh einsetzt. Aus Autopsien von jungen Menschen, die bei Unfällen, Tötungsdelikten oder aufgrund anderer nichtkardiovaskulärer Ursachen gestorben waren, weiß man, dass tatsächlich bereits ein Drittel der Sechzehn- bis Zwanzigjährigen zum Zeitpunkt ihres Todes atherosklerotische Läsionen oder Plaques in den Herzkranzgefäßen aufwiesen.[111] Wir sprechen von Teenagern.
Das heißt nicht, dass sie kurz vor einem Herzinfarkt stehen. Die Atherosklerose entwickelt sich sehr langsam. Das könnte auch am Eingreifen von HDL liegen. Wenn ein HDL-Teilchen an unserem Tatort voller Schaumzellen und Fettstreifen auftaucht, kann es das Cholesterin aus den Makrophagen heraussaugen, ein Prozess, der als Delipidierung bezeichnet wird. Es schlüpft dann wieder durch das Endothel zurück in die Blutbahn und liefert das überschüssige Cholesterin in der Leber und in anderen Geweben (Fettzellen und Hormondrüsen eingeschlossen) ab, damit es wiederverwendet werden kann.
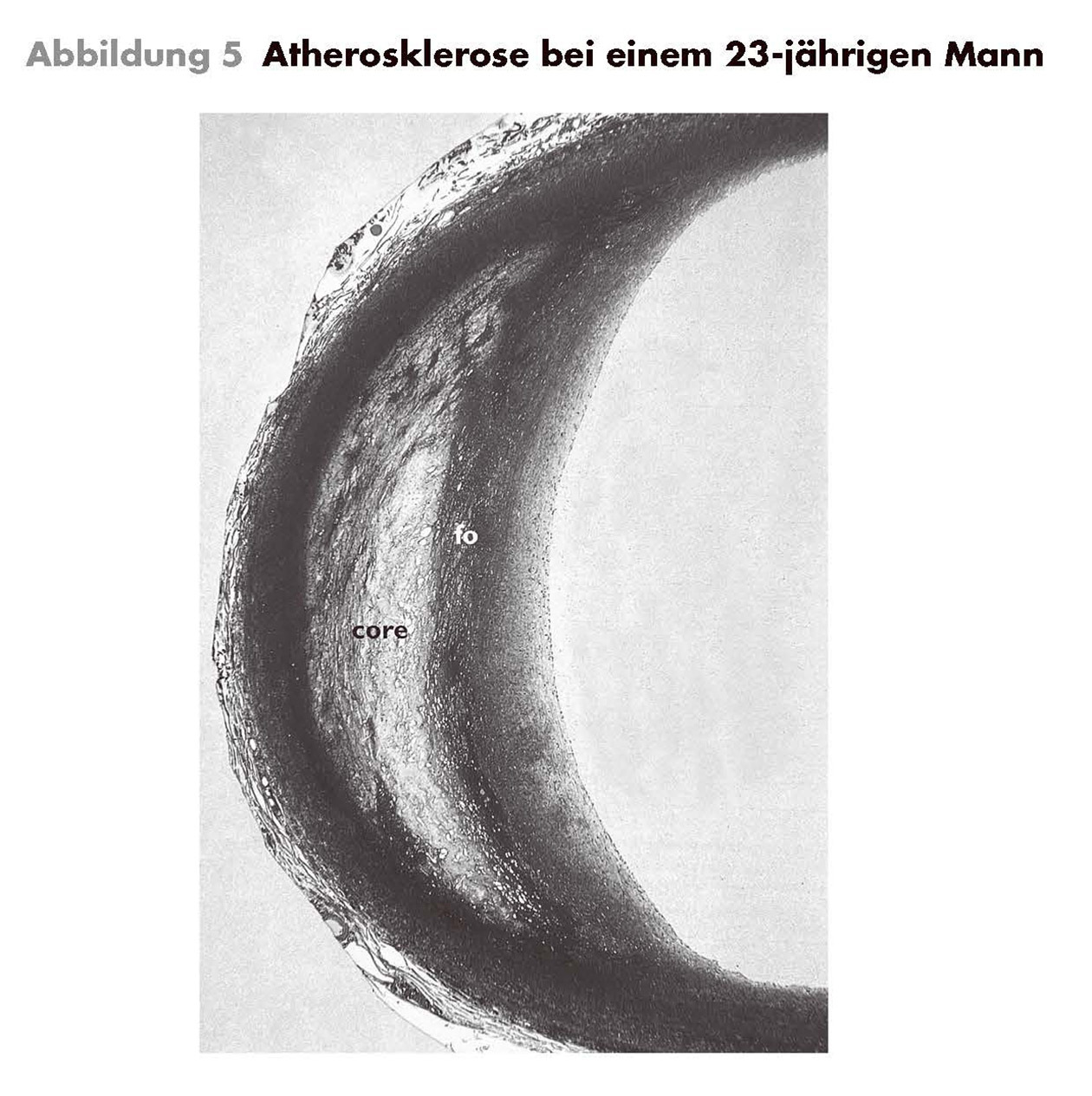
Querschnitt durch einen Ast der linken Koronararterie, den Ramus interventricularis anterior (RIVA), eines der wichtigsten Gefäße für die Blutversorgung des Herzens, bei einem 23-jährigen Mann, der einem Tötungsdelikt zum Opfer fiel. In der Arterienwand ist bereits eine ausgedehnte atherosklerotische Schädigung zu sehen: Ein deutlicher Kern (»core«) aus Lipiden, Makrophagen und Schaumzellen (»fo«) im Endothel beginnt, sich in Richtung Lumen auszudehnen, den Hohlraum, durch den das Blut fließt. Der Mann hätte vielleicht noch nicht so bald nicht mit einem Herzinfarkt rechnen müssen, aber die Krankheit ist nichtsdestoweniger bereits weit fortgeschritten.
Quelle: Stary (2003)
Unter anderem wegen dieser Rolle beim »Cholesterinabfluss« wird HDL als »gut« bezeichnet, aber es kann noch mehr. Neuere Forschungen legen nahe, dass HDL viele weitere Funktionen hat, die als Atheroskleroseschutz wirksam sind, zum Beispiel hilft es, die Integrität des Endothels aufrechtzuerhalten, es drängt Entzündungen zurück, und es neutralisiert oder stoppt die Oxidation von LDL, wie eine Art arterielles Antioxidationsmittel.
Die Rolle von HDL ist weit weniger gut verstanden als die von LDL. Der Cholesteringehalt Ihrer LDL-Partikel, Ihr »schlechter« Cholesterinwert (angegeben als LDL-C)[112], ist (als Maßzahl) tatsächlich eine recht gute Näherung an seine biologische Wirkung; viele Studien haben eine starke Korrelation zwischen LDL-C und »Ereignis«-Risiko nachgewiesen. Aber der Wert für das noch viel wichtigere »gute« Cholesterin, das HDL-C in Ihrem Blutbild, verrät mir nicht wirklich viel, wenn überhaupt etwas über Ihr Risikoprofil als Ganzes. Das Risiko scheint zu sinken, wenn das HDL-C etwa bis zur 80. Perzentile ansteigt. Versuche, die HDL-Cholesterin-Konzentration mit Gewalt, also mit speziellen Medikamenten, nach oben zu treiben, haben das kardiovaskuläre Risiko allerdings kein bisschen senken können. Der Schlüssel scheint eine verbesserte Funktionsweise der Teilchen zu sein – doch bis jetzt wissen wir noch nicht, wie wir das erreichen (oder messen) können.
Ob HDL die Erklärung dafür ist, dass Hundertjährige erst zwanzig Jahre später Herz-Kreislauf-Erkrankungen entwickeln, wenn überhaupt, können wir nicht sagen. Sie erinnern sich? Drei der berühmtesten »Langlebigkeitsgene«, die bislang entdeckt wurden, haben mit dem Transport und der Verarbeitung von Cholesterin zu tun (ApoE und zwei andere, CETP und ApoC3). Aber es sind nicht nur die Hundertjährigen. Ich habe Patienten, deren Lipoproteinprofil sich liest wie ein Todesurteil, mit unglaublich hohen LDL-C- und ApoB-Werten, aber wenn ich mir ihre anderen Untersuchungsergebnisse ansehe, Calcium-Score, CT-Angiogramm oder was auch immer, finde ich keine Krankheitszeichen. Im Augenblick haben wir noch keine zufriedenstellende Antwort für dieses Phänomen. Ich bin der festen Überzeugung, dass wir anfangen müssen, HDL besser zu verstehen, und hoffentlich auch herausfinden, wie man seine Funktion steigern kann, wenn wir irgendwelche Fortschritte bei der medikamentösen Behandlung von Herz-Kreislauf-Krankheiten machen wollen.
Doch ich schweife ab. Kehren wir zu unserem Tatort zurück, wo die ständig wachsende Zahl von Schaumzellen zu einer fettigen Masse zu verschmelzen beginnt, wie der sich verflüssigende Inhalt eines Haufens prall gefüllter Müllsäcke, die jemand vors Haus geworfen hat. Daraus entsteht der Kern unserer atherosklerotischen Plaque. Und hier schlägt nun das, was als Einbruch begann, in eine echte Hausbesetzung um. In einem Versuch, den Schaden zu begrenzen, wandern glatte Muskelzellen aus der Arterienwand hin zu der vermüllten Stelle und sondern eine Art Matrix ab, die sie rundum abschließen soll, wie Narbengewebe. Diese Matrix sitzt dann wie eine Bindegewebskappe auf Ihrer funkelnagelneuen Plaque.
Und noch mehr schlechte Nachrichten: Nichts von dem, was sich bis hierher zugetragen hat, lässt sich ohne Weiteres mit den verschiedenen Tests nachweisen, die wir typischerweise verwenden, um das kardiovaskuläre Risiko von Patienten abzuschätzen. Wir können eventuell Entzündungszeichen entdecken, zum Beispiel erhöhte Werte für das C-reaktive Protein, ein beliebter (aber schlechter) Indikator für Entzündungsprozesse in den Arterien. Aber die liegen meist noch unter unserem medizinischen Radar. Wenn man sich die Herzkranzgefäße in diesem frühen Stadium mit einem CT-Scan ansieht, sieht man sie vermutlich nicht, wenn man nur nach dem Calcium Ausschau hält. (Mit einer fortgeschritteneren CT-Technik, dem sogenannten CT-Angiogramm, stehen die Chancen besser, die Schädigungen in diesem Stadium zu entdecken. Ich ziehe sie deshalb den Nullachtfünfzehn-Versionen des Calcium-Scans vor[113], auch weil man damit die »weichen«, noch nicht verkalkten Plaques erkennen kann.)
Je länger dieser Reparaturversuch oder Umbauprozess dauert, desto größer wird die Plaque. Zuerst erfolgt die Ausdehnung in Richtung Außenwand der Arterie, doch später kann sie sich auch zum Lumen hin wölben und damit den Durchgangsverkehr in der Straße blockieren, um bei unserem Bild zu bleiben. Die Verengung des Lumens wird auch als Stenose bezeichnet; sie ist auf einem Angiogramm zu erkennen.
An einem bestimmten Punkt dieses Prozesses setzt die Verkalkung der Plaque ein. Dann endlich kann man sie auch auf einem normalen Calcium-Scan sehen. Die Verkalkung ist nichts anderes als ein weiterer Versuch des Körpers, den Schaden zu reparieren, indem er die Plaque stabilisiert, um die so wichtigen Arterien zu schützen. Aber das ist, als würden Sie den Reaktor von Tschernobyl in Beton eingießen: Sie sind froh, dass er dort ist, aber Sie wissen auch, dass allein das enorme Ausmaß der Schäden in dem Gebiet einen solchen Eingriff überhaupt rechtfertigen kann. Ein positiver Calcium-Score bedeutet, dass es mit an Sicherheit grenzender Wahrscheinlichkeit noch mehr Plaques in der Nähe gibt, die stabilisiert (verkalkt) sein können oder auch nicht.
Wenn eine Plaque instabil wird, erodiert oder gar reißt, dann haben Sie wirklich ein Problem. Eine geschädigte Plaque kann zur Bildung eines Gerinnsels führen, das das Lumen des Blutgefäßes möglicherweise verengt oder völlig blockiert. Oder, was noch schlimmer ist, das sich vielleicht ablöst und einen Herzinfarkt oder einen Schlaganfall verursacht. Darum mache ich mir mehr Sorgen wegen nicht verkalkter Plaques als wegen verkalkter.
Dennoch verhalten sich die meisten atherosklerotischen Plaques ziemlich undramatisch. Sie wachsen heimlich, still und leise vor sich hin und verschließen nach und nach das Blutgefäß, bis dieser Verschluss eines Tages zum Problem wird, sei es wegen der Plaque selbst oder wegen eines von der Plaque freigesetzten Gerinnsels. Ein Mensch mit einer überwiegend sitzenden Lebensweise merkt vielleicht gar nicht, dass er verengte Herzkranzgefäße hat, bis er rausgeht, um Schnee zu schippen. Die plötzlich erhöhte Anforderung an das Kreislaufsystem kann eine Ischämie (das Blut kann nicht genug Sauerstoff liefern) oder einen Infarkt auslösen (Gewebe stirbt ab, weil es nicht mehr vom Blut versorgt wird) – medizinische Laien sprechen dann vom Herzinfarkt oder vom Schlaganfall.
Der scheint zwar überraschend einzutreten, aber die Gefahr lauerte schon lange im Verborgenen.
Als ich mit Mitte dreißig mein persönliches Risiko für Herz-Kreislauf-Erkrankungen erkannte, hatte ich keinen blassen Schimmer, wie die dafür verantwortlichen komplexen Prozesse ablaufen. Rückblickend ist klar, dass ich einige der größeren und kleineren Risikofaktoren bereits abgehakt hatte. Ich rauchte nicht, und Rauchen zählt zu den größten umweltbedingten Treibern des Risikos, und ich hatte einen normalen Blutdruck, aber ich hatte andere Probleme. Wie mein Calcium-Scan enthüllte, befand sich im oberen Abschnitt meines Ramus interventricularis anterior, einem Ast der linken Koronararterie und einem der wichtigsten Gefäße für die Blutversorgung des Herzens, bereits eine kleine verkalkte Plaque. Möglicherweise spielten sich damals noch andere unschöne Dinge dort ab, doch weil ich kein CT-Angiogramm machen ließ, konnte ich nicht wissen, welche weiteren Schäden in meinen Herzkranzgefäßen vorhanden waren. Alles, was noch nicht verkalkt war, wurde von dem Calcium-Scan nicht erfasst.
Der etwas vollschlanke Peter befand sich also schon auf dem Weg zu einer Herz-Kreislauf-Erkrankung. Als ich vierzig wurde, näherte sich mein Bauchumfang der 100-Zentimeter-Marke, ein eindeutiges Zeichen für meinen gestörten Stoffwechsel. Unter meinem Gürtel sammelte ich vermutlich viszerales Fett an. Außerdem war ich insulinresistent, ein enormer Risikofaktor für kardiovaskuläre Erkrankungen. Mein Blutdruck war noch in Ordnung, aber ich vermute, er hätte sich ziemlich schnell verschlechtert, je älter ich wurde, denn Bluthochdruck grassiert in meiner Familie. Wahrscheinlich hatte ich auch bereits hohe Harnsäurewerte, die – wie wir im vorigen Kapitel gesehen haben – oft zusammen mit hohem Blutdruck und anderen Zeichen einer Stoffwechselstörung auftreten. Alle diese Aspekte zusammen tragen zu einer weiteren notwendigen (aber nicht hinreichenden) Bedingung für die Entwicklung der Atherosklerose bei – der Entzündung. Vor allem die Barrierefunktion des Endothels ist in großer Gefahr, durch die Entzündung Schaden zu nehmen.
Aber kein Arzt hätte mich wegen irgendeines dieser Vorzeichen behandelt. Mein Blutbild ließ kein ernst zu nehmendes Risiko erkennen. Mein LDL-C lag bei 110–120 Milligramm pro Deziliter, etwas höher als normal, aber kein Grund zur Beunruhigung, vor allem nicht bei Jüngeren. Meine Triglycerid-Werte waren erhöht, etwas über der Marke von 150 Milligramm pro Deziliter, aber auch sie ließen die Alarmglocken nicht läuten. Heute weiß ich, dass diese Zahlen mit ziemlicher Sicherheit eine hohe Konzentration von ApoB-Partikeln anzeigen, aber niemand machte sich die Mühe, den ApoB-Wert zu bestimmen.
Damals, vor fast 15 Jahren, war es nicht üblich, den ApoB-Wert zu messen, also die Menge der ApoB-haltigen Partikel. Seither wurden mehr und mehr Belege dafür gefunden, dass ApoB kardiovaskuläre Erkrankungen sehr viel besser vorhersagen kann als die übliche einfache LDL-Cholesterin-Messung. Im Jahr 2021 wurde in der Zeitschrift JAMA Cardiology eine Analyse veröffentlicht, die zeigte, dass jede Erhöhung von ApoB um eine Standardabweichung das Risiko für einen Herzinfarkt bei Patienten ohne vorherige kardiovaskuläre Ereignisse oder diagnostizierte Herz-Kreislauf-Erkrankung (das heißt ohne Primärprävention) um 38 Prozent erhöht.[114] Das ist eine sehr starke Korrelation. Aber selbst heute empfehlen die Richtlinien der American Heart Association noch den LDL-C-Test und nicht den für ApoB. Ich lasse alle meine Patienten regelmäßig auf ApoB testen und rate Ihnen, Ihren Arzt darum zu bitten, wenn Sie ihn das nächste Mal aufsuchen. (Und lassen Sie sich nicht mit dem Kostenargument abwimmeln, der Test kostet zwischen zwanzig und dreißig US-Dollar.)
(Anm. d. Übs.: Die Deutsche Gesellschaft für Kardiologie empfiehlt den ApoB-Test »für die Risikobewertung, besonders bei Personen mit hohen Triglycerid-Werten, Diabetes mellitus, Adipositas oder metabolischem Syndrom. Es kann, sofern verfügbar, alternativ zur LDL-C-Analyse als primäre Messung für Screening, Diagnose und Behandlung genutzt werden.« Quelle: Deutsche Gesellschaft für Kardiologie – Herz- und Kreislaufforschung e. V. (2020): ESC/EAS Pocket Guidelines. Diagnostik und Therapie der Dyslipidämien, Version 2019, Börm Bruckmeier Verlag GmbH, Grünwals)
Ich war immer noch in den Dreißigern, erfüllte aber schon drei der wichtigen Vorbedingungen für eine Herz-Kreislauf-Erkrankung: deutlich erhöhte Lipoproteine oder ApoB, oxidiertes oder modifiziertes LDL (das die Plaques verursachte, die in meinem Calcium-Scan zu erkennen waren) und ausgesprochen hohe Entzündungswerte. Nichts davon reicht als einziger Grund aus, um mit Sicherheit die Entstehung einer Herz-Kreislauf-Erkrankung vorherzusagen, aber alle drei sind notwendig, um eine zu entwickeln. Zum Glück sind wir in der Lage, viele dieser Krankheitszeichen zu modulieren oder fast vollständig rückgängig zu machen – inklusive ApoB übrigens –, wenn wir die Lebensweise und die Medikation entsprechend anpassen. Im letzten Teil werden wir ausführlich darüber sprechen, aber ich lege sehr großen Wert darauf, den ApoB-Wert zu senken, die Konzentration des Partikels, das all diese Probleme hervorruft. (Kurz gesagt: Bringen Sie ihn so früh wie möglich so weit wie möglich runter.)
Doch bevor wir uns diesem Thema widmen, möchte ich über ein weiteres tödliches, aber relativ wenig bekanntes Lipoprotein sprechen, das vermutlich dafür verantwortlich ist, dass ganze Friedhöfe mit Opfern des plötzlichen Herztods gefüllt sind, mit Menschen, deren klassische Cholesterinwerte und Risikofaktorprofile völlig in Ordnung waren. Mich betrifft das glücklicherweise nicht, aber einen sehr guten Freund von mir, und dass es rechtzeitig entdeckt wurde, hat ihm vermutlich das Leben gerettet.
Anahad O’Connor lernte ich 2012 während einer Frankreichreise kennen, die wir der French-American Foundation und einem Preis verdankten, der uns beiden zuerkannt worden war. Wir verstanden uns auf Anhieb, was vielleicht auch daran lag, dass wir auf diesem Trip die Einzigen waren, die auf das pain au chocolat verzichteten und stattdessen ins Fitnessstudio gingen. Außerdem schrieb er für die New York Times über Gesundheit und Wissenschaft, wir hatten also genügend Gesprächsstoff.
Da ich ein Cholesterin-Nerd bin, setzte ich Anahad zu, nach unserer Rückkehr in die Vereinigten Staaten alle Lipoproteine testen zu lassen. Er sah mich belustigt an – warum sollte er das tun? Er war erst Anfang dreißig, Vegetarier und extrem fit, mit einem Körperfettanteil von vielleicht 6 oder 7 Prozent. Seine Lipide sollten tadellos sein. Aber man weiß ja nie, sein Vater war an einem Aneurysma gestorben, das könnte auf Kreislaufprobleme hindeuten.
Wie erwartet, sahen die Werte für die Standardlipide großartig aus. Nur ein Wert tanzte aus der Reihe, darum schlug ich vor, dass er einen Calcium-Scan machen lassen sollte, so wie ich, damit wir ein besseres Bild von seinen Arterien bekämen. Und dann fing die Sache an, interessant zu werden. Sie erinnern sich? Mein Calcium-Score hatte bei 6 gelegen und mir signalisiert, dass mein Risiko höher war als das von 75 bis 90 Prozent meiner Altersgruppe. Anahads Calcium-Score betrug 125, für jemanden, der so jung und ansonsten gesund war, jenseits von Gut und Böse. »Kann das wirklich sein?«, fragte er.
Es kann. Wie sich herausstellte, war der Schuldige ein wenig bekannter, aber ziemlich tödlicher Partikeltyp, der als Lipoprotein (a), abgekürzt Lp(a), bezeichnet wird. Dieser Teufelsbraten von einem Lipoprotein entsteht, wenn sich eines der gewöhnlichen LDL-Partikel mit einem anderen, selteneren Protein namens Apolipoprotein(a), kurz Apo(a) (nicht zu verwechseln mit ApolipoproteinA oder ApoA, das HDL-Partikel kennzeichnet), zusammenlagert. Das Apo(a) wickelt sich locker um das LDL, mit vielen verschlungenen Abschnitten, die man wegen ihrer Ähnlichkeit mit einem dänischen Gebäck gleichen Namens als »Kringle« bezeichnet. Und diese Kringle machen das Lp(a) so gefährlich, denn während die LDL-Partikel in der Blutbahn kreisen, nehmen sie kleine Stücke oxidierter Fettmoleküle auf und schleppen sie mit.
Wie mir mein Lipid-Guru Tom Dayspring erklärte, ist das nicht unbedingt schlecht. Es gibt Hinweise, dass die Lp(a)-Teilchen vielleicht eine Art Putztruppe oder Kehrmaschine sind, die unerwünschten und möglicherweise schädlichen Lipidabfall einsammeln und bei der Leber abliefern. Aber weil Lp(a) zur Familie der ApoB-Partikel gehört, kann es ebenfalls durch das Endothel dringen und sich in der Arterienwand festsetzen; aufgrund seiner Struktur ist es sogar noch wahrscheinlicher, dass Lp(a) mit seiner Fracht aus unbrauchbar gewordenen Lipiden dort eher stecken bleibt als ein normales LDL-Partikel. Noch schlimmer, wenn es erst einmal drin ist, verhält es sich fast wie ein Gerinnungsfaktor und verstärkt die Bildung von Plaques in den Arterien.
Häufig macht Lp(a) mit einem plötzlichen, scheinbar viel zu frühen Herzinfarkt auf sich aufmerksam. Das passierte zum Beispiel Bob Harper, dem Gastgeber der amerikanischen Ausgabe von Biggest Loser, der im Jahr 2017 mit zweiundfünfzig Jahren in einem New Yorker Fitnessstudio einen Herzstillstand erlitt. Er überlebte, weil er von einem der Umstehenden eine Herzdruckmassage erhielt, bis der Rettungsdienst eintraf. Zwei Tage später wachte er im Krankenhaus auf und fragte sich, was ihn da ereilt hatte. Wie sich herausstellte, war ein hoher Lp(a)-Spiegel der Grund. Die Gefahr war ihm nicht im Geringsten bewusst gewesen.
Das Szenario ist keineswegs untypisch: Wenn ein Patient zu mir kommt und sagt, sein Vater, sein Großvater oder seine Tante oder alle drei seien relativ jung an irgendeinem Herz-Kreislauf-Problem gestorben, schaue ich als Erstes, ob der Lp(a)-Wert erhöht ist. Das ist nämlich der häufigste erbliche Risikofaktor für Herz-Kreislauf-Erkrankungen, und er ist auch deshalb so gefährlich, weil er bei Medizin 2.0 noch immer unter dem Radar fliegt, obwohl sich das gerade zu ändern beginnt.
Die meisten Menschen haben nur eine relativ geringe Konzentration dieses speziellen Lipoproteins im Blut, doch bei manchen Individuen ist sie hundertmal höher als bei anderen. Dieser Unterschied ist im Wesentlichen genetisch bedingt, und bei etwa 20 bis 30 Prozent der US-Bevölkerung liegt der Spiegel so hoch, dass sie ein erhöhtes Risiko besitzen;[115] zudem haben Menschen afrikanischer Abstammung im Durchschnitt oft höhere Spiegel als Menschen, deren Wurzeln in Europa oder dem Mittelmeerraum liegen. Aus diesem Grund sollten Sie unbedingt nach einem Lp(a)-Test fragen, wenn in Ihrer Familie schon häufiger frühe Herzinfarkte vorkamen. Wir machen diesen Test bei jedem Patienten, wenn wir ihm zum ersten Mal Blut abnehmen. Weil erhöhte Lp(a)-Spiegel zum größten Teil genetisch bedingt sind, muss man den Test auch nur ein einziges Mal machen (und die Richtlinien der kardiologischen Fachgesellschaften empfehlen einen einmaligen Test seit Neuestem ebenfalls).
Anahad hatte Glück, dass er auf diese Weise von seinem Risiko erfuhr. An seinem Calcium-Score war abzulesen, dass seine Arterien durch Lp(a) bereits erhebliche atherosklerotische Schädigungen erlitten hatten. Abgesehen von den Schäden, die es den Herzkranzgefäßen zufügt, kann Lp(a) auch die Aortenklappe zerstören, eine der wichtigsten Strukturen im Herzen; das geschieht durch die Bildung winziger knöcherner Teilchen in den Taschen der Herzklappe, was zu einer Verengung oder einem Verschluss der Aortenklappe führt.
Für Anahad und andere Menschen mit erhöhten Lp(a)-Spiegeln gibt es keine einfache Lösung. Auf Verhaltensänderungen wie sportliche Betätigung oder Ernährungsumstellung scheint Lp(a), anders als LDL, nicht zu reagieren. Eine Medikamentengruppe, die sogenannten PCSK9-Hemmer, die darauf abzielen, die ApoB-Konzentrationen insgesamt zu senken, vermag die Lp(a)-Spiegel offenbar um circa 30 Prozent zu drücken, doch bislang haben wir noch keine Daten, die zeigen, ob dadurch auch die Ereignisse (Infarkte), die diesem Teilchen zugeschrieben werden, zurückgehen.[116] Daher besteht die einzige echte Behandlungsmöglichkeit für Lp(a) derzeit darin, die ApoB-Partikel insgesamt mit drastischen Maßnahmen anzugehen. Selbst wenn wir Lp(a) – außer über die PCSK9-Hemmer – nicht direkt senken können, können wir die übrige ApoB-Konzentration ausreichend weit herunterfahren, dass das Gesamtrisiko der Patienten vermindert wird.[117] Anahad ist noch relativ jung, darum hat er mehr Zeit, sich mit seinen anderen Risikofaktoren zu beschäftigen.
Zum Glück haben wir das Problem gefunden, bevor es ihn fand.
Wie lässt sich das kardiovaskuläre Risiko senken?
In gewisser Weise sind der vollschlanke Peter und Anahad O’Connor wie zwei Seiten einer Medaille. Obwohl unsere Geschichten auf den ersten Blick nicht viel gemeinsam haben, unterstreichen sie die schleichende, fast schon heimtückische Natur von Herz-Kreislauf-Erkrankungen: Mein Risiko hätte offensichtlich sein müssen, angesichts meiner Familiengeschichte, während die Erkrankung bei Anahad unsichtbar blieb, bis er zufälligerweise einen Calcium-Scan bekam, den man bei gesund erscheinenden Menschen in den Dreißigern normalerweise nicht macht. Es war das schiere Glück, dass wir von unseren Risiken erfuhren, denn kaum ein Arzt hätte bei Leuten unseres Alters nach Herz-Kreislauf-Erkrankungen gesucht.
Aus unseren beiden Geschichten lassen sich drei blinde Flecken von Medizin 2.0 ablesen, was den Umgang mit Herz-Kreislauf-Erkrankungen angeht: erstens, eine zu stark vereinfachte Sicht auf die Lipide, die nicht erfasst, wie wichtig die Gesamtmenge an Lipoprotein (ApoB) ist und wie dringend nötig es ist, sie zu senken, um das Risiko wirklich zu mindern; zweitens, ein genereller Mangel an Wissen über andere »böse« Mitspieler wie Lp(a); und drittens, die Nichtberücksichtigung des langen zeitlichen Verlaufs atherosklerosebedingter Erkrankungen und welche Folgen es hätte, wenn wir uns um echte Prävention bemühen würden.
Wenn ich das erste Blutbild eines Patienten vor mir habe, wandern meine Augen sofort zu zwei Werten, dem von ApoB und dem von Lp(a). Die anderen Zahlen sehe ich mir ebenfalls an, doch diese beiden verraten mir am meisten über das Herz-Kreislauf-Risiko des Patienten. Der ApoB-Wert gibt nicht nur die Konzentration der LDL-Partikel an (die, wie Sie sich sicher erinnern, einen höheren Vorhersagewert besitzen als die Konzentration des Cholesterins LDL-C, das sich in ihrem Inneren befindet), sondern erfasst gleichzeitig die Konzentration der VLDL-Partikel, die als Mitglieder der ApoB-Familie ebenfalls zu Atherosklerose beitragen können. Außerdem kann selbst jemand mit einem niedrigen ApoB-Wert immer noch einen gefährlich hohen Lp(a)-Spiegel haben.[118]
Sobald Sie die zentrale Bedeutung von ApoB eingesehen haben, lautet die nächste Frage: Um wie viel muss ich diesen Wert (oder LDL-C, seinen Näherungswert) senken, um eine nennenswerte Risikominderung zu erreichen? Die verschiedenen Behandlungsrichtlinien geben unterschiedliche Zielwerte an, typischerweise 100 Milligramm pro Deziliter für Patienten mit normalem Risiko und 70 Milligramm pro Deziliter für Patienten mit hohem Risiko. Nach meinem Dafürhalten ist das immer noch viel zu hoch. Vereinfacht gesagt, denke ich, dass man ApoB und LDL-C gar nicht zu stark absenken kann, wenn keine Nebenwirkungen aufgrund der Behandlung auftreten. Wir wollen sie so niedrig wie möglich haben.
Peter Libby, einer der führenden Experten auf dem Gebiet der kardiovaskulären Erkrankungen, und Kollegen schrieben 2019 in der Fachzeitschrift Nature Reviews: »Atherosklerose gäbe es wahrscheinlich nicht [Hervorhebung von mir], wenn die LDL-C-Konzentration das physiologisch Notwendige (das in einer Größenordnung von 10 bis 20 Milligramm pro Deziliter liegt) nicht überschritte.«[119] Weiter schreiben die Autoren: »Wenn die gesamte Bevölkerung LDL-Konzentrationen ähnlich denen von Neugeborenen (oder von Erwachsenen der meisten anderen Tierarten) beibehielte, könnte Atherosklerose eine seltene Erkrankung sein.«
Übersetzung: Wenn wir alle die ApoB-Level behielten, die wir als Baby hatten, gäbe es auf der ganzen Erde nur so wenige Herz-Kreislauf-Erkrankungen, dass kein Mensch sie kennen würde. So wie die 3-Hydroxi-Isobuttersäure-Krankheit. Wie bitte, die kennen Sie nicht? Könnte daran liegen, dass bisher überhaupt nur 13 Fälle beschrieben wurden.[120] Das ist eine seltene Krankheit. Ich scherze ein bisschen, aber ich meine, atherosklerosebedingte Erkrankungen sollten nicht einmal unter den zehn häufigsten Todesursachen sein, wenn wir sie nur aggressiver behandeln würden. Stattdessen haben wir weltweit jedes Jahr über 18 Millionen Tote durch atherosklerosebedingte Krankheiten.[121]
Vermutlich sind viele Ärzte (und wohl auch viele Leser dieses Buches) geschockt angesichts eines derart niedrigen Zielwerts für LDL-C: 10 bis 20 Milligramm pro Deziliter. Viele Behandlungsrichtlinien erachten das Absenken des LDL-C-Wertes unter 70 Milligramm pro Deziliter für zu »aggressiv«, selbst in der Sekundärprävention bei Hochrisikopatienten, also Menschen, die bereits einen Herzinfarkt erlitten haben. Auch die Frage, ob solche extrem niedrigen LDL-C- und ApoB-Level sicher sind, ist berechtigt, schließlich ist Cholesterin im menschlichen Körper allgegenwärtig und unentbehrlich. Aber bedenken Sie Folgendes: Kleine Kinder, die vermutlich den größten Teil des Cholesterins brauchen, um die enorme Nachfrage ihres schnell wachsenden Nervensystems zu befriedigen, haben ähnlich niedrige Cholesterinmengen im Blut, ohne dass ihre Entwicklung dadurch gestört wird. Warum? Weil das Cholesterin in all Ihren Lipoproteinen zusammengenommen – nicht nur LDL, sondern auch HDL und VLDL – gerade einmal 10 bis 15 Prozent des gesamten Cholesterinpools Ihres Körpers ausmacht. Die Sorge ist also unbegründet, wie auch die Ergebnisse von Studien zeigen, in denen man keine unerwünschten Effekte bei extrem niedrigen LDL-Konzentrationen fand.[122]
Das ist mein Ausgangspunkt bei jedem neuen Patienten, sei er nun wie Anahad (mit einem einzigen großen Risikofaktor) oder sei er wie ich (mit vielen kleineren Risikofaktoren). Unser erster Tagesordnungspunkt heißt: die Menge an ApoB-Partikeln reduzieren, vor allem die LDL, aber auch die VLDL, die ebenfalls gefährlich werden können. Und zwar drastisch reduzieren, nicht nur ein bisschen oder nach und nach. Sie sollen so weit runter wie möglich und lieber früher als später. Außerdem müssen wir auf andere Risikomarker achten, insbesondere die, die mit der Stoffwechselgesundheit zusammenhängen, wie Insulin, Bauchfett und Homocystein[123], das in hoher Konzentration mit einem stark erhöhten Risiko für Herzinfarkt, Schlaganfall und Demenz einhergeht.
Sie werden bemerken, dass ich dem HDL-C wenig Beachtung schenke, denn obwohl niedrige HDL-C-Werte mit einem höheren Risiko einhergehen, scheint es hier keinen ursächlichen Zusammenhang zu geben. Darum ist es in klinischen Studien bisher nicht gelungen, mit Medikamenten, die HDL-C erhöhen sollten, die Risiken zu mindern und die Zahl der »Ereignisse« zu verringern. Hinweise für die Gründe liefern zwei elegante Studien, die sich der Mendelschen Randomisierung bedienten (siehe Kapitel 3) und die die HDL-C-Frage von zwei Seiten untersuchten: Erstens: Ist niedriges HDL-C die Ursache für den Anstieg des Herzinfarktrisikos? Ergebnis: Nein.[124] Zweitens: Ist die Erhöhung des HDL-C-Spiegels die Ursache für die Verminderung des Herzinfarktrisikos? Ergebnis: Nein.[125]
Warum? Wahrscheinlich weil, gleich welchen positiven Beitrag HDL-Partikel im Kampf um die Arterienwände leisten, es (wieder einmal) von ihrer Funktion abzuhängen scheint – die offenbar in keinem Zusammenhang mit ihrer Cholesterinfracht steht. Doch die Funktionsfähigkeit von HDL können wir nicht testen, und solange wir nicht besser verstehen, wie HDL eigentlich funktioniert, bietet es keinen Ansatz für die Therapie.
Lipoproteine sind nicht die einzigen bedeutsamen Risikofaktoren für Herz-Kreislauf-Erkrankungen, wie bereits erwähnt, schädigen Rauchen und Bluthochdruck das Endothel direkt. Daher heißen die ersten nicht verhandelbaren Schritte zum Vermindern des kardiovaskulären Risikos: aufhören zu rauchen und den Blutdruck einstellen.
Über Ernährung werden wir später noch ausführlich sprechen, aber mein persönlicher erster Schritt zur Risikominderung war eine Ernährungsumstellung, mit der ich meine Triglyceridwerte (die, wenn sie hoch sind, zu ApoB beitragen, wie das bei mir der Fall war) senken und, noch wichtiger, meinen Insulinspiegel in den Griff bekommen wollte. Ich musste meinen Stoffwechsel in Ordnung bringen. Ich sollte vielleicht anmerken, dass ich mich seinerzeit für eine ketogene Diät entschieden habe, eine Ernährungsweise, die vielleicht nicht für jeden funktioniert und die ich heute auch nicht mehr praktiziere. Aus meiner klinischen Erfahrung kann ich sagen, dass es bei etwa einem Drittel bis der Hälfte der Menschen, die große Mengen gesättigter Fette verzehren (was mit einer ketogenen Diät manchmal Hand in Hand geht), zu einem dramatischen Anstieg der ApoB-Partikel kommt, was wir natürlich nicht wollen.[126] Einfach ungesättigte Fette, die unter anderem in nativem Olivenöl Extra, in Macadamianüssen und in Avocados enthalten sind, haben nicht diesen Effekt, weswegen ich versuche, meine Patienten dazu zu bringen, mehr von diesen Nahrungsmitteln zu konsumieren; ihr Anteil kann bis 30 Prozent des gesamten Fettverzehrs betragen. Es geht nicht unbedingt darum, die Fettmenge insgesamt zu begrenzen, sondern die Ernährung in Richtung Fette zu verändern, die für ein besseres Blutfettprofil sorgen.
Bei den meisten, wenn nicht gar allen meiner Patienten ist das ApoB-Level, das wir anstreben – das von Kindern –, mit Diät allein nicht zu erreichen, das heißt, wir müssen parallel zur Ernährungsumstellung auch Medikamente einsetzen. In diesem Bereich haben wir glücklicherweise mehr Präventionsoptionen als für Krebs oder neurodegenerative Erkrankungen. Statine sind die bei Weitem am häufigsten verschriebene Medikamentengruppe zur Regulierung der Lipide, aber es gibt noch mehrere andere Optionen, die für einen bestimmten Patienten vielleicht besser passen, oder es kann notwendig werden, zwei Medikamentenklassen zu kombinieren; es ist gar nicht ungewöhnlich, dass ein Patient zwei Lipidsenker erhält, die über verschiedene Mechanismen wirken. Diese Mittel werden häufig als »Cholesterinsenker« bezeichnet, doch ich denke, wir sollten sie besser unter dem Gesichtspunkt der ApoB-Reduzierung betrachten, denn sie verstärken die Fähigkeit des Körpers, die ApoB-Teilchen aus dem Blutkreislauf zu holen. Und das ist ja unser Ziel. Meist geschieht das über die Erhöhung der Aktivität der LDL-Rezeptoren in der Leber, die das Cholesterin aus der Blutbahn aufnehmen.
Diesen Effekt erzielen unterschiedliche Arzneistoffe auf unterschiedlichen Wegen. In der ersten Verteidigungs- (oder Angriffs-)Linie stehen üblicherweise die Statine, sie hemmen die Cholesterinsynthese und veranlassen die Leber zu einer verstärkten Expression von LDL-Rezeptoren, wodurch mehr LDL aus der Blutbahn entfernt wird. Statine haben möglicherweise noch weitere positive Effekte, unter anderem wirken sie offensichtlich entzündungshemmend, und wenn ich auch nicht der Auffassung bin, man solle sie dem Trinkwasser zusetzen, wie schon vorgeschlagen wurde, so denke ich doch, dass es sehr hilfreiche Mittel sind, die bei vielen Patienten die ApoB- oder LDL-Konzentration senken. Nicht jeder verträgt Statine problemlos. Etwa 5 Prozent der Patienten erleiden nicht akzeptable Nebenwirkungen, vor allem Muskelschmerzen, die mit der Medikamenteneinnahme zusammenhängen.[127] Bei einem kleineren, aber nicht zu vernachlässigenden Teil der Patienten kippt die Glucose-Homöostase, vielleicht eine Erklärung dafür, warum unter dem Einfluss von Statinen ein leichter Anstieg des Diabetesrisikos beobachtet wird.[128] Bei anderen Patienten kommt es zu einer unsymptomatischen Erhöhung der Leberenzyme, noch häufiger sogar, wenn die Patienten gleichzeitig Ezetimib einnehmen, einen Cholesterinsenker aus einer anderen Wirkstoffgruppe.[129] All diese Nebenwirkungen verschwinden schnell und vollständig, sobald das betreffende Medikament abgesetzt wird. Bei denen, die sie vertragen (und das sind die meisten), wende ich Statine früh und häufig an. (Für mehr Information zu bestimmten Statinen und anderen ApoB-senkenden Medikamenten siehe den Überblick am Ende dieses Kapitels.)
Das bringt uns zum letzten und vielleicht größten blinden Fleck von Medizin 2.0: der Zeit.
Der Prozess, den ich in diesem Kapitel beschrieben habe, entwickelt sich sehr langsam – nicht in zwei oder drei oder auch fünf Jahren, sondern im Lauf von Jahrzehnten. Aus der Tatsache, dass es jüngere Leute mit Läsionen und Plaques gibt, ohne dass es öfter zu kardiovaskulären Ereignissen kommt, können wir schließen, dass die Erkrankung über einen beträchtlichen Zeitraum keine größeren Schäden anrichtet. Der Tod durch eine Herz-Kreislauf-Erkrankung ist nicht unvermeidlich: Hundertjährige schieben ihn um Jahrzehnte nach hinten, viele vermeiden ihn ganz, weil ihre Arterien so sauber bleiben wie die von Menschen, die eine ganze Generation jünger sind. Auf irgendeine Weise gelingt es ihnen, den ganzen Prozess zu verlangsamen.
Fast alle Erwachsenen weisen irgendwelche Gefäßschäden auf, unabhängig davon, wie jung und gesund sie aussehen oder wie makellos ihre Arterien sich auf dem Calcium-Scan darstellen. Es gibt immer Schäden, vor allem an Stellen, an denen Scherkräfte Stress verursachen oder an denen der Blutdruck lokal erhöht ist, beispielsweise in Gefäßbiegungen oder -aufgabelungen. In irgendeiner Form begleitet uns die Atherosklerose unser ganzes Leben lang. Aber die meisten Ärzte halten es für »Übertherapie«, einen Patienten zu behandeln, wenn dessen errechnetes Zehn-Jahres-Risiko für ein schweres kardiovaskuläres Ereignis (zum Beispiel einen Herzinfarkt oder Schlaganfall) unter 5 Prozent liegt; sie argumentieren, dass der Nutzen nicht größer sei als die Risiken oder dass die Kosten für die Behandlung zu hoch seien. Meiner Meinung nach belegt das nur die weitverbreitete Unkenntnis des unaufhaltsamen, langfristigen Verlaufs von Herz-Kreislauf-Erkrankungen. Der Zeithorizont von zehn Jahren ist viel zu kurz bemessen. Wenn wir wollen, dass weniger Menschen an kardiovaskulären Krankheiten sterben, dann müssen wir anfangen, über Prävention bei Vierzig- und vielleicht sogar bei Dreißigjährigen nachzudenken.
Vielleicht kann man jemandem zu einem bestimmten Zeitpunkt tatsächlich ein »niedriges Risiko« attestieren – aber mit welchem zeitlichen Horizont? Der Standard sind zehn Jahre. Doch was, wenn der Zeithorizont der »Rest meines Lebens« ist?
Dann gibt es niemanden mit niedrigem Risiko.
Als ich meinen ersten Calcium-Scan machen ließ, im Jahr 2009 mit sechsunddreißig Jahren, war mein Zehn-Jahres-Risiko so niedrig, dass man es nicht berechnen konnte. Die am häufigsten angewendeten mathematischen Modelle zur Risikoabschätzung haben eine Altersuntergrenze von vierzig oder fünfundvierzig Jahren. Meine Daten ließen sich nicht einmal einspeisen. Darum verwundert es nicht, dass meine Befunde bei niemandem die Alarmglocken läuten ließen. Trotz meines Calcium-Scores von 6 lag mein Zehn-Jahres-Risiko für Herzinfarkt weit unter 5 Prozent.
Im Jahr 2016, sieben Jahre nach dem ersten Calcium-Scan, ließ ich ein CT-Angiogramm (den besseren Scan mit höherer Auflösung) machen. Es zeigte denselben kleinen Calciumfleck, aber keine Hinweise auf weitere weiche Plaques an anderen Stellen. Im Jahr 2022 ließ ich erneut ein CT-Angiogramm anfertigen, mit demselben Ergebnis. Es fanden sich wieder keinerlei Hinweise irgendeiner Art auf weiche Plaques, nur der kleine Calciumfleck von 2009 war immer noch da.[130] Zumindest in der Auflösung der schärfsten CT-Scanner, die derzeit erhältlich sind, lässt sich kein Grund für die Annahme finden, meine Atherosklerose sei in den vergangenen dreizehn Jahren weiter fortgeschritten.
Ich weiß nicht, ob das bedeutet, dass ich kein Risiko habe – offen gestanden bezweifle ich es –, aber anders als früher habe ich keine Angst mehr, an einer kardiovaskulären Krankheit zu sterben. Wie es aussieht, hat sich mein langes, umfassendes Präventionsprogramm ausgezahlt. Jetzt, mit fünfzig, fühle ich mich wesentlich besser als mit sechsunddreißig, und welche Maßzahl man auch nimmt, mein Risiko ist deutlich niedriger, als es meinem Alter entspricht. Einer der Hauptgründe dafür ist, dass ich früh damit angefangen habe, viel früher, als Medizin 2.0 je irgendeine Intervention vorgeschlagen hätte.
Und trotzdem beharren die meisten Ärzte und Kardiologieexperten immer noch darauf, dass man mit dreißig zu jung für eine Primärprävention von Herz-Kreislauf-Krankheiten ist. Diese Auffassung stellt ein Artikel infrage, der 2018 in der Fachzeitschrift JAMA Cardiology erschienen ist und in dem unter dem Gesichtspunkt Risiko und Prävention der Zehn-Jahres-Horizont mit dem Dreißig-Jahres-Horizont verglichen wurde.[131] Einer der Autoren war Allan Sniderman. Die Analyse, die er und seine Kollegen durchgeführt haben, ergab Folgendes: Wenn man statt der üblichen zehn Jahre einen zeitlichen Rahmen von dreißig Jahren betrachten und frühzeitig aggressive Vorsorgemaßnahmen ergreifen würde – etwa bei bestimmten Patienten früher mit der Statinbehandlung beginnen –, dann könnten Hunderttausende kardiovaskulärer Ereignisse zusätzlich verhindert und in der Konsequenz viele Menschenleben gerettet werden.
Für den Kontext: Die meisten Studien zu Statinen in der Primärprävention (das heißt der Verhinderung des ersten Herz-Kreislauf-Ereignisses) dauern etwa fünf Jahre und finden typischerweise eine number needed to treat (abgekürzt NNT, das ist die Zahl der Patienten, die mit einem bestimmten Medikament behandelt werden muss, um ein Leben zu retten) zwischen 33 und 130, je nachdem, wie die Ausgangsrisikolage bei den Patienten war. (Interessanterweise dauerten die längsten Statin-Studien gerade einmal sieben Jahre.) Betrachtet man jedoch das Potenzial der Risikominderung über einen Zeitrahmen von 30 Jahren, wie es die Sniderman-Studie tat, dann sinkt die Zahl der NNT bis auf sieben ab. Das heißt, auf je sieben Personen, denen wir in diesem frühen Stadium Statine verabreichen, kommt unter Umständen ein gerettetes Leben. Das ist einfache Mathematik: Das Risiko steigt proportional zur ApoB-Exposition mit der Zeit an. Je früher der Kontakt mit ApoB und damit das Risiko verringert wird, desto größer sind die positiven Effekte im Laufe der Zeit – und desto größer wird die Verminderung des Gesamtrisikos.
Das bringt den fundamentalen Unterschied zwischen Medizin 2.0 und Medizin 3.0 im Bereich der kardiovaskulären Krankheiten auf den Punkt. Für Erstere hat sich Prävention vor allem mit den relativ kurzfristigen Risiken zu beschäftigen, während Medizin 3.0 einen wesentlich tiefer gehenden Ansatz wählt und versucht, die primären Ursachen des Krankheitsprozesses zu identifizieren und zu beseitigen: die ApoB-Partikel. Das führt zu ganz neuen Behandlungskonzepten. Beispielsweise hat ein Fünfundvierzigjähriger mit erhöhten ApoB-Werten ein niedrigeres Zehn-Jahres-Risiko als ein Fünfundsiebzigjähriger mit niedrigen ApoB. Medizin 2.0 würde sagen, der Fünfundsiebzigjährige muss behandelt werden (wegen seines Alters), der Fünfundvierzigjährige aber nicht. Medizin 3.0 sagt: Vergiss das Zehn-Jahres-Risiko und behandle in beiden Fällen die Ursache – bei dem Fünfundvierzigjährigen muss das ApoB so weit wie möglich abgesenkt werden.
Wenn man erst einmal verstanden hat, dass die ApoB-Partikel – LDL, VLDL und Lp(a) – mit den atherosklerosebedingten kardiovaskulären Erkrankungen in einer kausalen (ursächlichen) Beziehung stehen, stellt sich die Situation komplett verändert dar. Der einzige Weg, diese Erkrankungen aufzuhalten, ist die Beseitigung der Ursache, und jetzt ist der beste Zeitpunkt, damit anzufangen.
Sie sind immer noch nicht ganz überzeugt? Dann denken Sie mal über folgendes Beispiel nach. Wir wissen, dass es einen ursächlichen Zusammenhang zwischen Rauchen und Lungenkrebs gibt. Sollen wir jemanden erst auffordern, mit dem Rauchen aufzuhören, wenn sein Zehn-Jahres-Risiko für Lungenkrebs eine bestimmte Schwelle überschreitet? Oder andersherum, halten wir es für richtig, dass Leute rauchen, bis sie fünfundsechzig sind, und dann damit aufhören? Oder sollten wir nicht alles in unserer Macht Stehende tun, um jungen Leuten, die vielleicht gerade erst mit dem Rauchen angefangen haben, zu helfen, es wieder aufzugeben?
Wenn man es so betrachtet, ist die Antwort eindeutig. Je früher Sie der Schlange den Kopf abschneiden, desto niedriger ist das Risiko, von ihr gebissen zu werden.
Kurzer Überblick über lipidsenkende Medikamente
Auf dem Markt gibt es sieben Statine, doch ich beginne in der Regel mit Rosuvastatin und weiche davon nur ab, wenn es aufgrund der Medikamenteneinnahme zu unerwünschten Nebenwirkungen kommt (zum Beispiel zu Symptomen oder Veränderungen bei Biomarkern). Ich verfolge mit aller Macht das Ziel, für das Peter Libby plädiert hat: Ich will die ApoB-Konzentration auf 20 oder 30 Milligramm pro Deziliter herunterboxen, wie man sie bei Kindern findet.
Für Patienten, die Statine nicht vertragen, nehme ich einen neueren Wirkstoff namens Bempedoinsäure, der in einen anderen Stoffwechselweg eingreift, aber am Ende dasselbe bewirkt: Er hemmt die Cholesterinsynthese und zwingt die Leber dadurch, die Zahl der LDL-Rezeptoren zu erhöhen und damit die LDL aus dem Blut zu holen. Während Statine jedoch die Cholesterinsynthese im gesamten Körper hemmen, und vor allem in den Muskeln, wirkt Bempedoinsäure nur in der Leber. Die unerwünschten Nebenwirkungen der Statine, insbesondere die Muskelschmerzen, unterbleiben dadurch.
Ein anderes Medikament mit dem Wirkstoff Ezetimib verhindert die Aufnahme von Cholesterin aus dem Verdauungstrakt.[132] Auf diese Weise verringert sich die Cholesterinmenge in der Leber, was wieder zu einer vermehrten Bildung von LDL-Rezeptoren und einem verstärkten Entfernen von ApoB-Partikeln aus der Blutbahn führt, genau das, was wir haben wollen. Ezetimib wird gerne in Kombination mit Statinen angewandt, die ja die Cholesterinsynthese hemmen. Allerdings verstärkt der Körper dann als Reaktion darauf oft die Cholesterinaufnahme aus dem Darm, also genau den Prozess, den Ezetimib sehr effektiv blockiert.
Die Zahl der LDL-Rezeptoren kann mit einer Wirkstoffklasse hochgeregelt werden, die wir vorhin kurz erwähnt haben, die sogenannten PCSK9-Hemmer. Die machen ein Protein namens PCSK9 unbrauchbar, das LDL-Rezeptoren abbaut; damit erhöht sich die Halbwertszeit der Rezeptoren, und die Leber kann mehr ApoB aus dem Blut fischen. Werden die PCSK9-Inhibitoren in Monotherapie, also alleine eingesetzt, haben sie die gleiche Wirkung auf ApoB und LDL-C wie hoch dosierte Statine, meistens jedoch werden sie zusätzlich zur Statintherapie gegeben. Die Kombination von Statinen und PCSK9-Inhibitoren ist das schärfste pharmakologische Schwert, das wir gegen ApoB haben. Ein weiteres Plus: Statine senken die Lp(a)-Konzentration nicht, doch PCSK9-Inhibitoren tun das bei den meisten Patienten, und zwar in der Regel um circa 30 Prozent.
Die Triglyceride tragen ebenfalls zur ApoB-Partikel-Last bei, weil sie vor allem in VLDL transportiert werden. Mit diätetischen Maßnahmen versuchen wir, die Triglyceride zu vermindern, doch wenn Veränderungen in der Ernährung nicht genügen oder in Fällen, in denen das wegen genetischer Faktoren nichts bringt, sind Fibrate die Wirkstoffe der Wahl.
Der Wirkstoff Eicosapentaensäure-Ethylester (auch Icosapent-Ethyl) wird aus Fischöl gewonnen. Ein Medikament, das vier Gramm dieses Wirkstoffs in pharmazeutisch reiner Form enthält, wurde 2019 von der US-amerikanischen Arzneimittelbehörde FDA zur Behandlung von Patienten mit erhöhten Triglycerid-Werten zugelassen.
Kapitel 8
Zellen außer Kontrolle
Neue Wege im Kampf gegen den Killer namens Krebs
Manchmal muss man eine Schlacht mehr als
einmal schlagen, um sie zu gewinnen.
Margaret Thatcher
Steve Rosenberg war noch ein junger Assistenzarzt, als er dem Patienten begegnete, der den weiteren Verlauf seiner Karriere bestimmen sollte – und vielleicht auch die Behandlung von Krebserkrankungen im Allgemeinen. Im Zuge seiner Ausbildung arbeitete er 1968 an einem Krankenhaus für Veteranen in Massachusetts, als ein Mann in den Sechzigern wegen einer relativ simplen Gallenblasenoperation eingeliefert wurde. Über den Bauch des Mannes, der James DeAngelo hieß, verlief eine lange Narbe. Wie er sagte, stammte diese von einer weit zurückliegenden Operation, bei der ihm ein Magentumor entfernt worden sei. Außerdem habe er Metastasen in der Leber gehabt, die man aber nicht angerührt habe.
Rosenberg war sicher, dass sein Patient da etwas durcheinanderbrachte. Es wäre ein Wunder gewesen, wenn er auch nur sechs Monate mit metastasierendem Magenkrebs überlebt hätte. Doch laut DeAngelos Krankenunterlagen war genau das passiert. Vor zwölf Jahren war er in dasselbe Krankenhaus gekommen und hatte über Unwohlsein und Antriebslosigkeit geklagt. Zu jener Zeit, so war es im Arztbericht zu lesen, trank er drei bis vier Flaschen Whiskey pro Woche und rauchte täglich ein bis zwei Päckchen Zigaretten. Die Chirurgen hatten in seinem Magen einen faustgroßen Tumor und in der Leber kleinere Metastasen entdeckt. Den Magentumor hatten sie mit der Hälfte des Magens entfernt, aber die Tumoren in der Leber so belassen, weil es ihnen zu riskant erschien, sie alle gemeinsam herauszuoperieren. Dann hatten sie den Mann wieder zugenäht und zum Sterben nach Hause geschickt, was er aber offensichtlich nicht getan hatte.
Als Rosenberg die Gallenblasen-OP vornahm, beschloss er, sich in DeAngelos Bauchraum ein wenig umzusehen. Er tastete hinter die Leber und erwartete, unter den weichen blauroten Lappen verbliebene Tumoren zu fühlen – unverwechselbar, hart und rund, gespenstisch fremdartig –, aber da waren keinerlei Anzeichen von irgendwelchen Auswüchsen. »Ohne Zweifel hatte dieser Mann eine gefährliche, unheilbare Krebserkrankung gehabt, die ihn innerhalb kürzester Zeit hätte umbringen müssen«, schrieb Rosenberg 1992 in seinem Buch The Transformed Cell (dt. Die veränderte Zelle). »Niemand, weder wir noch irgendjemand anders, hatte seine Krankheit behandelt. Und jetzt war er geheilt.«[133]
Wie konnte das sein? In der gesamten medizinischen Literatur fand Rosenberg nur vier Fälle, in denen es zu einer vollständigen und spontanen Rückbildung von metastasierendem Magenkrebs gekommen war. Er stand vor einem Rätsel. Schließlich kam er jedoch zu folgendem Schluss: DeAngelos Immunsystem hatte den Krebs abgewehrt und die verbliebenen Tumoren in der Leber getötet, so wie Sie oder ich eine Erkältung abwehren. Sein eigener Körper hatte den Krebs besiegt. Irgendwie.
In der herkömmlichen Krebsforschung konnte man sich so etwas damals kaum vorstellen. Aber Rosenberg glaubte auf etwas Bedeutsames gestoßen zu sein. In The Transformed Cell beschreibt er seine Suche nach einer Möglichkeit, sich das Immunsystem für den Kampf gegen den Krebs zunutze zu machen. Doch trotz vereinzelter kleiner Erfolge ließ sich das geheimnisvolle Phänomen, das DeAngelos Tumoren den Garaus gemacht hatte, nicht ergründen. In den ersten zehn Jahren überlebte keiner von Rosenbergs Patienten. Kein einziger. Aber er gab nicht auf.
Während er als Krebsforscher keine entscheidenden Ergebnisse vorweisen konnte, hatte er als Krebschirurg mehr Erfolg: 1985 operierte er Präsident Ronald Reagan, der an Dickdarmkrebs erkrankt war, und alles ging gut. Rosenbergs Ziel war jedoch, Krebsoperationen ganz und gar überflüssig zu machen. Punkt. Mitte der 1980er-Jahre gab es endlich einen Hoffnungsschimmer – gerade hell genug, um ihn weiter voranzutreiben.
Sobald ich The Transformed Cell als Medizinstudent gelesen hatte, wusste ich, dass ich Krebschirurg werden und mit Steve Rosenberg zusammenarbeiten wollte. Schon vor meiner Bewerbung zum Medizinstudium hatte ich mich für Krebs interessiert. Nachdem ich den Bachelor of Science gemacht hatte, besuchte ich für ein Jahr Kurse, die für die Aufnahme an einer medizinischen Hochschule gefordert wurden. In dieser Zeit hospitierte ich auf der Kinderkrebsstation des Kingston General Hospital in Ontario, wo ich Zeit mit Kindern verbrachte, die sich einer Krebsbehandlung unterzogen. Zum Glück ist Leukämie im Kindesalter ein Gebiet, auf dem Medizin 2.0 große Fortschritte gemacht hat. Trotzdem überlebten nicht alle Kinder, und ihre Tapferkeit, die Qualen, die sie und ihre Eltern durchlitten, und die liebevolle Fürsorge der für sie zuständigen medizinischen Teams berührten mich tiefer, als es irgendein technisches oder mathematisches Problem vermocht hätten. Das alles bestätigte mich in meinem Entschluss, von der Ingenieurswissenschaft zur Medizin zu wechseln.
In meinem dritten Jahr an der medizinischen Hochschule erhielt ich die Gelegenheit, vier Monate in Rosenbergs Labor mitzuarbeiten – im Epizentrum der amerikanischen Krebsforschung. Als ich dort ankam, war es schon fast drei Jahrzehnte her, dass Richard Nixon 1971 den nationalen War on Cancer ausgerufen hatte. Zuerst hatte man gehofft, Krebskranke in fünf Jahren »heilen« zu können, rechtzeitig zur Zweihundertjahrfeier der USA. Doch auch 1976 trotzte die Krankheit nach wie vor hartnäckig allen Versuchen, sie auszumerzen, und 2001, als ich den ersten Teil meines Medizinstudiums abschloss, war sie immer noch unbesiegt. Und so ist es im Grunde auch heute noch.
Obwohl über das National Cancer Institute schon weit über 100 Milliarden Dollar in die Forschung geflossen sind, dazu viele weitere Milliarden aus der Privatindustrie und öffentlichen Wohltätigkeitsorganisationen, trotz aller Solidaritätsbekundungen und buchstäblich Millionen veröffentlichter Artikel in der PubMed-Datenbank ist Krebs die zweithäufigste Todesursache in den Vereinigten Staaten und auch in Deutschland, direkt hinter Herz-Kreislauf-Erkrankungen. Zusammen sind diese beiden für fast die Hälfte aller Todesfälle in den USA verantwortlich, wobei wir die Entstehung und Entwicklung von Herz-Kreislauf-Erkrankungen allerdings schon recht gut erforscht haben und über einige wirksame Mittel zur Prävention und Behandlung verfügen. Demzufolge ist die Sterberate durch kardio- und zerebrovaskuläre Krankheiten seit Mitte des 20. Jahrhunderts um zwei Drittel gesunken. Einer Krebserkrankung fallen dagegen immer noch fast genauso viele Amerikaner zum Opfer wie vor fünfzig Jahren.
Es gab allerdings Fortschritte im Kampf gegen einige Krebsarten, insbesondere Leukämie (vor allem bei Kindern, wie bereits erwähnt). Bei Erwachsenen mit Leukämie verdoppelte sich die 10-Jahres-Überlebensrate zwischen 1975 und 2000 annähernd und stieg von 23 auf 44 Prozent.[134] Beim Hodgkin- und Non-Hodgkin-Lymphom, insbesondere bei Ersterem, sind die Überlebensraten ebenfalls gestiegen. Doch das sind nur relativ kleine Siege in einem »Krieg«, der bisher nicht allzu erfolgreich verläuft.
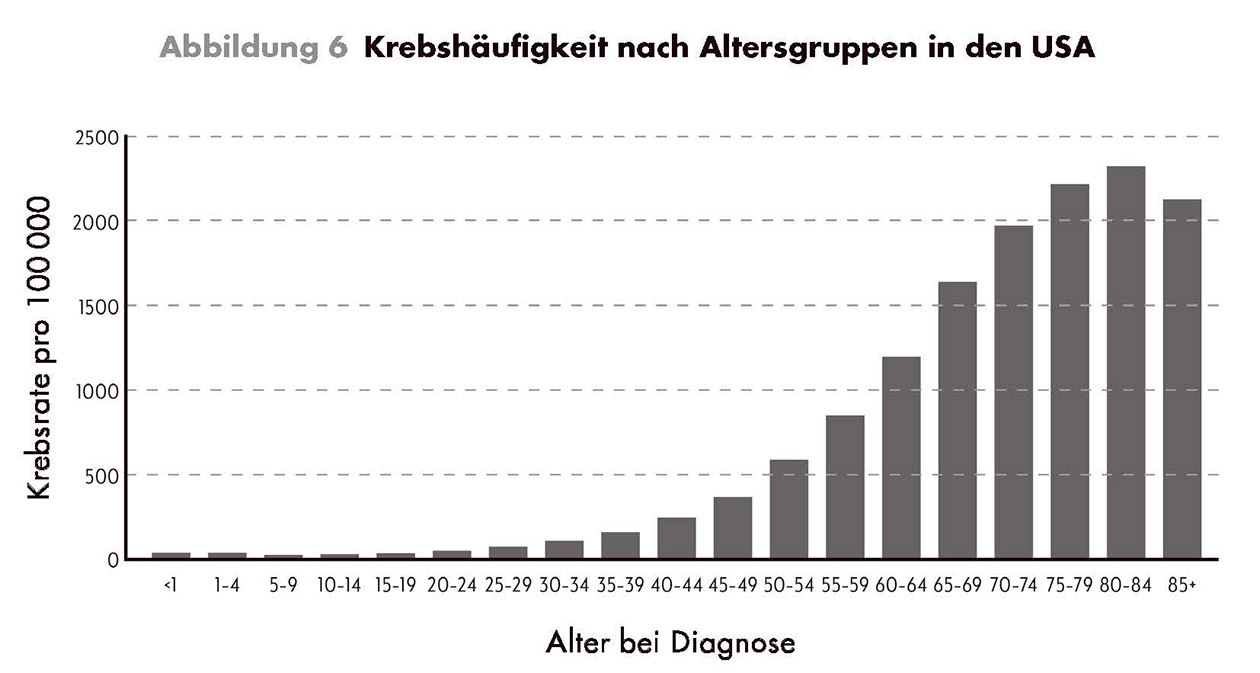
Quelle: National Cancer Institute (2021).
Wie die Herz-Kreislauf-Erkrankungen ist auch Krebs eine Alterskrankheit. Die Prävalenz steigt demnach mit jedem Lebensjahrzehnt exponentiell an, wie aus Abbildung 6 ersichtlich ist. Tödlich kann er jedoch in nahezu jedem Alter sein, besonders in mittleren Jahren. Das mittlere Alter bei einer Krebsdiagnose beträgt sechsundsechzig Jahre, aber im Jahr 2017 gab es unter Personen zwischen fünfundvierzig und vierundsechzig Jahren mehr Krebstote als Todesfälle durch Herz-Kreislauf-Erkrankungen, Lebererkrankungen und Schlaganfälle zusammen.[135] Falls sich dieses Jahr die letzten Trends bestätigen, wird laut dem National Cancer Institute die gleiche Altersgruppe 2023 ebenfalls fast 40 Prozent der geschätzt 1,7 Millionen neuen Krebsfälle in den Vereinigten Staaten ausmachen.[136] Doch wenn der Krebs diagnostiziert wird, hat er sich vermutlich schon seit Jahren, möglicherweise auch schon Jahrzehnten, entwickelt. Dabei denke ich voll Trauer an drei meiner Schulfreundinnen und -freunde, die in den letzten zehn Jahren mit nicht einmal fünfundvierzig Jahren an Krebs gestorben sind. Nur von einer konnte ich mich verabschieden, bevor sie starb. Auch von den Lesern dieses Buches hat wahrscheinlich jeder schon Ähnliches erlebt.
Das Problem ist, dass es keine hochwirksame Behandlung gegen Krebs gibt, wenn er sich erst einmal eingenistet hat. Unsere Mittel sind begrenzt. Viele (wenn auch nicht alle) solide Tumoren lassen sich operativ entfernen, was bereits im antiken Ägypten praktiziert wurde. Die Kombination von Operation und Bestrahlung hat sich als recht wirksame Waffe gegen die meisten lokalen Krebsarten mit soliden Tumoren erwiesen. Doch obwohl wir mit diesem Ansatz schon ziemlich erfolgreich sind, scheinen unsere Möglichkeiten zur Krebsbekämpfung in der Hinsicht bereits so gut wie ausgeschöpft zu sein. Mehr ist wohl nicht herauszuholen. Zudem ist Operieren nur begrenzt sinnvoll, wenn der Krebs bereits metastasiert ist, also gestreut hat. Das Wachstum von metastasierendem Krebs lässt sich mit Chemotherapie verlangsamen, aber er kommt praktisch immer zurück und ist dann häufig noch resistenter als vorher. Unser Richtwert für den Erfolg einer Krebsbehandlung liegt typischerweise bei einer Überlebensdauer von höchstens fünf Jahren. Von einer Heilung wagen wir nicht zu sprechen.
Das zweite Problem ist, dass wir praktisch nicht in der Lage sind, Krebs im Frühstadium zu erkennen. Viel zu oft entdecken wir Tumoren erst, wenn sie andere Symptome hervorrufen, doch dann sind sie oft schon zu groß, um entfernt zu werden – oder, noch schlimmer, der Krebs ist bereits in andere Bereiche des Körpers vorgedrungen. Während meiner Ausbildung habe ich das viele Male erlebt: Nachdem wir bei Patienten einen Tumor (oder mehrere) entfernt hatten, starben sie trotzdem ein Jahr später, weil sich der Krebs an einer anderen Stelle, zum Beispiel in der Leber oder Lunge, festgesetzt hatte.
Auf diesen Erfahrungen beruht unsere dreigeteilte Strategie im Kampf gegen Krebs. Unser erstes, naheliegendes Ziel ist, eine Krebserkrankung, so wie es bei so vielen Hundertjährigen der Fall ist, von vornherein zu vermeiden – also, mit anderen Worten: Prävention. Krebsprävention ist jedoch kompliziert, weil wir noch nicht ebenso gründlich wie bei Atherosklerose verstehen, was den Ausbruch und das Fortschreiten der Krankheit bewirkt. Überdies scheint bei dieser Erkrankung der Zufall oder, anders gesagt, schlicht pures Pech eine große Rolle zu spielen. Dennoch helfen uns einige Indizien, die wir in den beiden folgenden Abschnitten erörtern.
Die nächste Komponente der Strategie sind neuere und ausgeklügeltere Behandlungen, die auf die vielfältigen Schwachstellen von Krebs abzielen, wie der unstillbare metabolische Hunger schnell wachsender Krebszellen und ihre Anfälligkeit für neue immunbasierte Therapien – die Früchte jahrzehntelanger Arbeit von Forschern wie Steve Rosenberg. Insbesondere die Immuntherapie halte ich für außerordentlich vielversprechend.
Drittens, und das ist vielleicht am wichtigsten, müssen wir versuchen, den Krebs so früh wie möglich zu entdecken, sodass wir unsere Therapien effektiver gestalten können. Ich empfehle meinen Patienten ein frühzeitiges, aggressives und breit gefächertes Screening, wie etwa eine Darmspiegelung (oder andere Screeningverfahren für Darmkrebs) schon im Alter von vierzig Jahren und nicht erst, wie standardmäßig empfohlen, mit fünfundvierzig oder fünfzig, da alles dafür spricht, dass man die meisten Krebsarten am besten im Frühstadium bekämpfen kann. Vorsichtig optimistisch bin ich auch, was die Kombination dieser altbewährten Vorsorgemaßnahmen mit aufkommenden Verfahren betrifft. Dazu gehört die sogenannte Liquid Biopsy, die Flüssigbiopsie, mit der sich Krebszellen-DNA anhand eines simplen Bluttests aufspüren lässt.
Nachdem der Krieg gegen den Krebs nun schon über fünf Jahrzehnte anhält, ist offenkundig keine einzelne »Heilbehandlung« in Sicht, die die Krankheit in die Schranken weist. Am erfolgversprechendsten ist vielmehr die fortschreitende Entwicklung von Möglichkeiten, Krebs an allen drei erwähnten Fronten zu bekämpfen: Prävention, zielgerichtetere und wirksamere Behandlungen sowie eine umfassende und präzise Vorsorge, um ihn früh zu entdecken.
Was ist Krebs?
Dass Krebs so tödlich – und furchterregend – ist, liegt vor allem daran, dass wir nach wie vor nur wenig darüber wissen, wie er entsteht und warum er sich ausbreitet.
Krebszellen unterscheiden sich in zwei wichtigen Aspekten von normalen Zellen. Entgegen landläufiger Meinung wachsen Krebszellen nicht etwa schneller – vielmehr hören sie schlicht nicht auf zu wachsen, wenn sie es sollten. Aus irgendeinem Grund ignorieren sie irgendwann die Signale des Körpers, die ihnen befehlen, wann sie zu wachsen haben und wann sie das Wachstum einstellen müssen. Dieser Prozess setzt vermutlich ein, wenn in normalen Zellen bestimmte Genmutationen auftreten. So stoppt das Gen PTEN normalerweise das Wachstum oder die Teilung von Zellen (und damit ihre Entwicklung zu Krebszellen).[137] Bei Krebskranken, zum Beispiel bei etwa 31 Prozent der Männer mit Prostatakrebs und 70 Prozent der Männer mit fortgeschrittenem Prostatakrebs, ist das Gen häufig mutiert oder »verloren gegangen«. Solche »Tumorsuppressoren« sind für unser Verständnis der Erkrankung von zentraler Bedeutung.
Die zweite Eigenschaft, die Krebszellen definiert, ist ihre Fähigkeit, von einem Teil des Körpers in einen weit entfernten zu wandern, in dem sie nichts zu suchen haben. Das bezeichnet man als Metastasierung. Sie ermöglicht beispielsweise einer in der Brust befindlichen Krebszelle, in die Lunge zu streuen. Aufgrund dieser Ausbreitung wird Krebs von einem lokalen, beherrschbaren Problem zu einer tödlichen systemischen Krankheit.
Von diesen beiden gemeinsamen Merkmalen abgesehen weisen die verschiedenen Krebsarten jedoch kaum Ähnlichkeiten auf. Der Entwicklung einer generellen »Heilbehandlung« steht vor allem entgegen, dass Krebs keine singuläre, einfache, klar umrissene Erkrankung ist, sondern ein unfassbar komplexes Leiden.
Vor etwa zwei Jahrzehnten startete das National Cancer Institute eine große und ehrgeizige Studie namens The Cancer Genome Atlas. Ihr Ziel war die Sequenzierung von Tumorzellen, um die genetischen Veränderungen, die verschiedene Krebsarten wie Brust-, Nieren- und Leberkrebs verursachen, präzise zu bestimmen. Dieses Wissen sollte Forscher beim Entwickeln von Therapien unterstützen, die auf genau diese Mutationen abzielten. Einer der Wissenschaftler, die das Projekt angeregt hatten, sagte: »Dies sind die Startblöcke, die wir zur Entwicklung einer Heilbehandlung brauchen.«[138]
Die ersten Ergebnisse des Cancer Genome Atlas, die ab 2008 in einer Serie von Artikeln veröffentlicht wurden, sorgten jedoch eher für Verwirrung als Klarheit. Statt für jede Krebsart ein klares Muster von Genveränderungen zu offenbaren, stieß die Studie auf eine enorme Komplexität. Jeder Tumor wies im Durchschnitt über hundert verschiedene Mutationen auf, und diese Mutationen schienen beinahe zufällig zu sein. Eine Handvoll Gene erwies sich als Treiber, darunter TP53 (auch bekannt als p53, das sich in der Hälfte aller Krebsarten findet), KRAS (häufig bei Bauchspeicheldrüsenkrebs), PIC3 A (häufig bei Brustkrebs) und BRAF (häufig bei Melanomen). Nur ganz wenige dieser bekannten Mutationen, wenn überhaupt, traten bei allen Tumoren auf. Tatsächlich schien es überhaupt keine einzelnen Gene zu geben, die Krebs »verursachten«; vielmehr sah es so aus, als gebe es Kombinationen zufälliger somatischer Mutationen, also Mutationen, die in einer Körperzelle entstehen, welche Krebs hervorriefen. Demnach unterscheidet sich das Genom einer Brustkrebszelle nicht nur von dem einer Darmkrebszelle (was die Forscher erwartet hatten). Auch zwei Brustkrebstumoren ähneln einander nicht sehr. Wenn zwei Frauen Brustkrebs im gleichen Stadium haben, unterscheiden sich ihre Tumorgenome wahrscheinlich sehr stark voneinander. Darum wäre es schwierig, wenn nicht unmöglich, aufgrund des genetischen Profils der Tumoren für beide Frauen eine Behandlung zu entwickeln, die für beide gleichermaßen passend wäre. Statt den Wald genau zu kartografieren, führte uns der Cancer Genome Atlas immer tiefer in ein Baumlabyrinth hinein.
So hatte es zumindest damals den Anschein. Letzten Endes hat sich die Genomsequenzierung als äußerst mächtige Waffe gegen den Krebs erwiesen – wenn auch ganz anders, als man es zwei Jahrzehnte zuvor gedacht hatte.
Selbst wenn wir Krebs lokal erfolgreich behandeln, können wir nie sicher sein, dass er tatsächlich verschwunden ist. Wir können nicht feststellen, ob bereits Krebszellen gestreut haben und in anderen Organen lauern, um sich dort einzunisten. Dieser metastasierende Krebs verursacht die meisten krebsbedingten Todesfälle. Wenn wir die Sterberate durch Krebs beträchtlich senken wollen, müssen wir metastasierenden Krebsarten besser vorbeugen sowie uns bei ihrer Entdeckung und Behandlung verbessern.
Mit einigen Ausnahmen, wie dem Gliablastom oder anderen aggressiven Hirntumoren sowie bestimmten Arten von Lungen- und Leberkrebs, werden solide Tumoren typischerweise erst lebensbedrohlich, wenn sie sich auf andere Organe ausbreiten. Brustkrebs tötet nur dann, wenn er metastasiert. Prostatakrebs tötet nur dann, wenn er metastasiert. Ein Leben ohne diese Organe ist möglich. Wenn Sie also die traurige Nachricht erhalten, dass jemand an Brust- oder Prostatakrebs oder gar an Bauchspeicheldrüsen- oder Dickdarmkrebs gestorben ist, so war dies der Fall, weil der Krebs auch andere, lebenswichtigere Organe wie das Gehirn, die Lunge, die Leber und die Knochen befallen hat. Sobald dies geschehen ist, sinken die Überlebenschancen rapide.
Was aber bringt Krebszellen dazu zu streuen? Das wissen wir noch nicht richtig, und wir werden es auch nicht so bald herausfinden, weil nur rund 5 bis 8 Prozent der amerikanischen Krebsforschungsförderung für die Erforschung der Metastasierung vorgesehen sind.[139] Auch bei der Entdeckung von Metastasen sind unsere Möglichkeiten noch sehr begrenzt, obwohl ich glaube, dass wir bei der Krebsfrüherkennung kurz vor entscheidenden Durchbrüchen stehen, worauf wir später noch eingehen. Den größten Teil unserer Energie verwenden wir bisher auf die Behandlung von metastasierten Krebserkrankungen, was extrem schwierig und problematisch ist. Sobald der Krebs gestreut hat, werden die Karten neu gemischt – dann müssen wir von der lokalen zu einer systemischen Behandlung übergehen.
Momentan bedeutet das meist Chemotherapie. Entgegen landläufiger Meinung ist es gar nicht so schwierig, Krebszellen zu töten. In meiner Garage und unter meiner Küchenspüle habe ich ein Dutzend potenzielle chemotherapeutische Wirkstoffe stehen. Ihre Etiketten kennzeichnen sie als Glas- oder Rohrreiniger, aber mit Krebszellen würden sie ebenfalls kurzen Prozess machen. Das Problem besteht natürlich darin, dass diese Gifte auch jede benachbarte normale Zelle abtöten würden und mit einiger Wahrscheinlichkeit schließlich auch den Patienten. Es geht also darum, den Krebs zu töten und zugleich die normalen Zellen zu verschonen. Selektives Töten ist der Schlüssel zum Erfolg.
Die traditionelle Chemotherapie ist in einer Grauzone zwischen Gift und Medizin angesiedelt. Das im Ersten Weltkrieg als Waffe eingesetzte Senfgas war ein direkter Vorläufer von einem der ersten chemotherapeutischen Wirkstoffe, die teilweise immer noch verwendet werden. Diese Medikamente greifen den Replikationszyklus von Zellen an, und weil sich Krebszellen schnell teilen, schaden ihnen die Chemo-Wirkstoffe mehr als normalen Zellen. Allerdings gibt es auch viele wichtige nicht-krebsartige Zellen, die sich häufig teilen, wie die der Mund- und Darmschleimhaut, der Haarfollikel sowie Finger- und Fußnägel, weshalb typische chemotherapeutische Wirkstoffe Nebenwirkungen wie Haarausfall und Magen-Darm-Beschwerden auslösen. Zudem, wie der Krebsforscher Robert Gatenby hervorhebt, entwickeln diejenigen Krebszellen, die die Chemotherapie überleben, schließlich Mutationen, die sie widerstandsfähiger machen – so wie Kakerlaken, die eine Resistenz gegen Insektizide entwickeln.
Die Nebenwirkungen der Chemotherapie mögen zunächst wie ein faires Tauschgeschäft gegen die »Aussicht auf ein paar weitere nützliche Jahre« erscheinen, wie der 2011 verstorbene Autor Christopher Hitchens in den Memoiren über seine Krebserkrankung Mortality (dt. Endlich) schrieb.[140] Doch als sich die Behandlung seines metastatischen Speiseröhrenkrebses in die Länge zog, änderte er seine Meinung. »Ich lag Tag um Tag da und versuchte vergeblich, den Augenblick aufzuschieben, in dem ich schlucken musste. Jedes Mal, wenn ich es tat, floss eine diabolische Flut des Schmerzes meine Kehle empor und fand ihren Höhepunkt in etwas, das sich anfühlte wie der Tritt eines Mulis in die Lendenwirbelsäule. … Und dann blitzte unvermittelt der Gedanke auf: Hätte man mir dies alles im Voraus gesagt – wäre dann meine Entscheidung zugunsten der Behandlung ausgefallen?«[141]
Hitchens erfuhr den gravierendsten Makel der modernen Chemotherapie am eigenen Leib: Sie ist systemisch, aber nicht spezifisch genug, um nur Krebszellen und keine gesunden Zellen anzugreifen. Darum litt er an grässlichen Nebenwirkungen. Letzten Endes werden erfolgreiche Behandlungen systemisch und auf einen bestimmten Krebstyp zugeschnitten sein müssen. Sie werden eine Schwachstelle ausnutzen können, die Krebszellen eigen ist, während normale Zellen unbehelligt bleiben (und natürlich auch der Patient). Doch wie könnte eine solche Schwachstelle aussehen?
Nur weil Krebs mächtig ist, muss er nicht auch unbesiegbar sein. 2011 identifizierten die beiden führenden Krebsforscher Douglas Hanahan und Robert Weinberg zwei zentrale Merkmale von Krebs, die den Weg zu neuen Therapien sowie möglichen Methoden zur Verringerung des Krebsrisikos weisen konnten.[142] Erstens haben viele Krebszellen einen veränderten Stoffwechsel und nehmen große Mengen an Glucose auf. Zweitens besitzen Krebszellen die gruselige Fähigkeit, dem Immunsystem zu entkommen, das normalerweise Jagd auf beschädigte und gefährliche Zellen macht, um sie zu zerstören. Dieses Problem versuchen Steve Rosenberg und andere schon seit Jahrzehnten zu lösen.
Stoffwechsel und Immunüberwachung finde ich hochinteressant, weil sie beide systemisch sind – eine notwendige Bedingung für jede neue Behandlung von metastasierendem Krebs. Therapien, die sich darauf konzentrieren, würden sich Eigenschaften von Krebs zunutze machen, die möglicherweise tumorspezifischer sind als die unkontrollierte Replikation von Zellen. Doch weder der metabolische noch der immunbasierte Ansatz der Krebsbekämpfung sind neu – dank der beharrlichen, jahrzehntelangen Arbeit von Forschern verfügen wir bereits über ein Fundament für Fortschritte in beiden Bereichen.
Der Stoffwechsel von Krebszellen
Wie mittlerweile wohl klar geworden ist, betrachten wir Krebs gemeinhin vor allem als eine genetisch bedingte Erkrankung, die von Mutationen mit unbekannter Ursache ausgelöst wird. Zweifellos unterscheiden sich Krebszellen genetisch von normalen menschlichen Zellen. Doch seit etwa hundert Jahren untersucht eine Handvoll Forscher eine weitere spezifische Eigenschaft von Krebszellen, und die betrifft ihren Stoffwechsel.
In den 1920er-Jahren entdeckte der deutsche Physiologe Otto Warburg, dass Krebszellen einen merkwürdigen Heißhunger auf Glucose haben.[143] Sie verschlingen bis zu vierzigmal mehr davon als gesunde Zellen. Diese Krebszellen »atmeten« jedoch nicht so wie normale Zellen, indem sie Sauerstoff aufnahmen und über die Mitochondrien große Mengen von ATP, die Energiewährung der Zellen, produzierten. Stattdessen schienen sie einen anderen Weg zu nutzen, den Zellen gewöhnlich wählen, wenn sie Energie unter anaeroben Bedingungen erzeugen, also ohne über genügend Sauerstoff zu verfügen – was beispielsweise der Fall ist, wenn wir sehr schnell rennen. Merkwürdig daran war, dass die Krebszellen dieses ineffiziente Verfahren bevorzugten, obwohl ihnen reichlich Sauerstoff zur Verfügung stand.
Das kam Warburg ausgesprochen seltsam vor. Bei der normalen aeroben Atmung kann eine Zelle ein Glucosemolekül in bis zu 36 Einheiten ATP umwandeln. Unter anaeroben Bedingungen erbringt die gleiche Glucosemenge unter dem Strich jedoch nur 2 Einheiten ATP. Dieses Phänomen erhielt die Bezeichnung Warburg-Effekt.[144] Noch heute lokalisiert man potenzielle Tumoren unter anderem dadurch, dass man dem Patienten radioaktiv markierte Glucose injiziert und dann via PET-Scan verfolgt, wohin der größte Teil der Glucose wandert. Areale mit abnorm hoher Glucosekonzentration zeigen an, dass dort ein Tumor sitzen könnte.
1931 erhielt Warburg den Nobelpreis für Physiologie oder Medizin, weil er in der Elektronentransportkette, einem zentralen Mechanismus für die Energieproduktion in der Zelle, ein entscheidendes Enzym entdeckt hatte. Als er 1970 starb, war die von ihm aufgespürte merkwürdige Laune des Krebsstoffwechsels fast schon in Vergessenheit geraten.[145] Die Entdeckung der DNA-Struktur durch James Watson, Francis Crick, Maurice Wilkins und Rosalind Franklin im Jahr 1953 hatte – nicht nur in der Krebsforschung, sondern in der gesamten Biologie – einen revolutionären Paradigmenwechsel ausgelöst.
In einem Meinungskommentar, der 2009 in der New York Times erschien, schrieb Watson: »Als ich Ende der 1940er-Jahre an meiner Promotion arbeitete, waren die Platzhirsche der Biologie die Biochemiker, die herauszufinden versuchten, wie die am Intermediärstoffwechsel beteiligten Moleküle hergestellt und abgebaut werden. Nachdem meine Kollegen und ich die Doppelhelix der DNA entdeckt hatten, hatten plötzlich die Molekularbiologen in der Biologie das Sagen, die vor allem herausfinden wollten, wie die in der DNA-Sequenz codierte Information zur Bildung der Nukleinsäuren und Proteine einer Zelle genutzt wird.«[146]
Doch fast vierzig Jahre nachdem dem Krebs der Krieg erklärt worden war, gelangte Watson zu der Überzeugung, dass die Genetik keineswegs der Schlüssel zu einer erfolgreichen Krebsbekämpfung sei. »Vielleicht müssen wir das Hauptaugenmerk unserer Forschung statt auf die Decodierung der genetischen Anweisungen für den Krebs auf die Ergründung der chemischen Reaktionen in den Krebszellen richten«, schrieb er. Es sei an der Zeit, nach Therapien zu suchen, die gleichermaßen auf den Stoffwechsel von Krebs und seine Genetik abzielten.
Einige wenige Wissenschaftler hatten die metabolischen Aspekte von Krebs schon die ganze Zeit im Blick gehabt. Lew Cantley, heute im Dana-Farber Cancer Institute von Harvard tätig, untersucht den Krebsstoffwechsel seit den 1980er-Jahren, als man dies für eine aus der Zeit gefallene Idee hielt. Eine der rätselhaften Fragen, über die er sich den Kopf zerbrochen hat, lautete, warum Krebszellen auf diese höchst ineffiziente Weise Energie erzeugen müssen. Wie Cantley, Matthew Vander Heiden und Craig Thompson in einem Artikel von 2009 darlegten, könnte gerade die Ineffizienz des Warburg-Effekts der entscheidende Punkt sein.[147] Der Energieertrag sei zwar gering, aber zugleich würden zahlreiche Nebenprodukte erzeugt – zum Beispiel Laktat, das auch bei intensivem Sport gebildet wird. Tatsächlich entstehen bei der Umwandlung von Glucose in Laktat so viele zusätzliche Moleküle, dass die Autoren behaupteten, die relativ kleine Energiemenge sei das eigentliche »Nebenprodukt«.
Dieser scheinbare Irrsinn hat Methode: Wenn sich eine Zelle teilt, spaltet sie sich nicht einfach in zwei kleinere Zellen auf. Der Vorgang erfordert nicht nur die Teilung des Zellkerns und all der Zellbestandteile, die wir im Biologieunterricht lernen mussten, sondern auch die gesamten Materialien, die zum Aufbau einer kompletten neuen Zelle benötigt werden. Diese erscheinen nicht plötzlich aus dem Nichts. Die normale aerobe Zellatmung produziert ausschließlich Energie in Gestalt von ATP plus Wasser und Kohlendioxid, die als Baumaterial nicht von großem Nutzen sind (außerdem werden die beiden Letzteren ausgeatmet). Der Warburg-Effekt, den man auch als anaerobe Glykolyse bezeichnet, wandelt die gleiche Menge an Glucose in ein bisschen Energie und eine Menge von chemischen Bausteinen um – die dann zu einem raschen Bau von Zellen genutzt werden. Mithilfe des Warburg-Effekts treiben Krebszellen also ihre eigene Vermehrung an. Gleichzeitig bedeutet er aber auch eine mögliche Schwachstelle im Schutzpanzer der Krebszelle.[148]
In der Mainstream-Krebsforschung bleiben diese Theorien umstritten, doch der Zusammenhang zwischen Krebs und Stoffwechselstörung lässt sich kaum noch leugnen. In den 1990er-Jahren und Anfang der 2000er, als die Zahl der Raucher und der auf Rauchen zurückgeführten Krebserkrankungen abnahm, trat stattdessen eine neue Bedrohung auf. Fettleibigkeit und Typ-2-Diabetes weiteten sich zu einer nationalen und dann globalen Epidemie aus. Zudem schienen sie viele Krebsarten zu begünstigen, wie etwa Speiseröhren-, Leber- und Bauchspeicheldrüsenkrebs. Laut der American Cancer Society erhöht Übergewicht maßgeblich das Risiko, an Krebs zu erkranken oder vorzeitig zu sterben. Nur Rauchen ist noch gefährlicher.
Man nimmt an, dass weltweit 12 bis 13 Prozent aller Krebsfälle auf Fettleibigkeit zurückzuführen sind.[149] Fettleibigkeit steht mit 13 verschiedenen Krebsarten in Zusammenhang, darunter Bauchspeicheldrüsen-, Speiseröhren-, Nieren-, Eierstock- und Brustkrebs sowie mehrere Myelome (siehe Abbildung 7). Auch durch Typ-2-Diabetes wird das Risiko für bestimmte Krebsarten erhöht, in manchen Fällen (etwa bei Bauchspeicheldrüsen- und Gebärmutterschleimhautkrebs) sogar verdoppelt.[150] Extreme Fettleibigkeit (BMI ≥ 40) erhöht das Risiko, an Krebs zu sterben, bei Männern um 52 und bei Frauen um 62 Prozent.
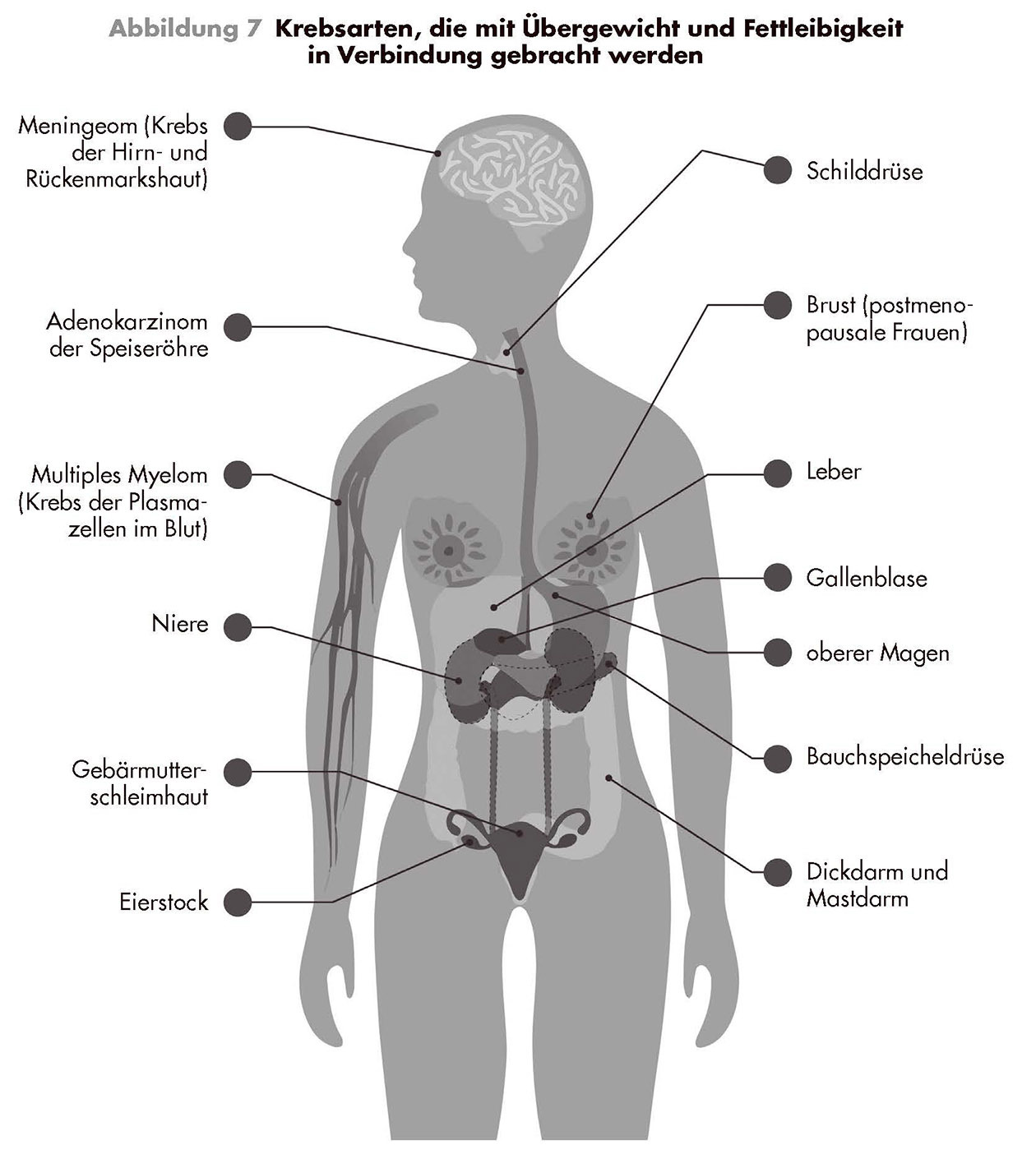
Quelle: NCI (2022a).
Ich vermute, dass der Zusammenhang zwischen Fettleibigkeit, Diabetes und Krebs in erster Linie durch Entzündungsprozesse und Wachstumsfaktoren wie Insulin hervorgerufen wird. Starkes Übergewicht, insbesondere viel viszerales Fett (und anderes Fett außerhalb von subkutanen Speichern), begünstigt Entzündungsvorgänge, da absterbende Fettzellen verschiedene entzündungsfördernde Cytokine in den Blutkreislauf abgeben (siehe Abbildung 4 in Kapitel 6). Die Umgebung einer solchen chronischen Entzündung kann dazu beitragen, dass sich normale Zellen zu Krebszellen entwickeln. Zudem wird eine Insulinresistenz befördert, woraufhin der Insulinspiegel allmählich steigt. Und wie wir sehen werden, spielt Insulin im Krebsstoffwechsel eine gefährliche Rolle.
Diese Erkenntnis verdanke ich weiteren Arbeiten von Lew Cantley. Er und seine Mitarbeiter haben eine Familie von Enzymen namens PI3-Kinasen, oder PI3K, entdeckt, die eine zentrale Rolle beim Vorantreiben des Warburg-Effekts spielt, indem sie die Glucoseaufnahme in die Zelle beschleunigt.[151] PI3K öffnet gewissermaßen ein Tor in der Zellwand und ermöglicht Glucose hineinzuströmen, die daraufhin das Zellwachstum anregt. Krebszellen weisen spezifische Mutationen auf, die PI3K aktivieren und zugleich das tumorsuppressive Protein PTEN ausschalten, über das wir oben bereits gesprochen haben. Wird PI3K durch Insulin und IGF-1, einen insulinähnlichen Wachstumsfaktor, aktiviert, kann die Zelle rasch sehr viel Glucose aufnehmen, um ihr Wachstum voranzutreiben. Auf diese Weise fungiert Insulin als eine Art Wegbereiter für Krebs.
Dies wiederum lässt vermuten, dass metabolische Therapien, einschließlich Ernährungsumstellungen, die den Insulinspiegel senken, möglicherweise dazu beitragen, das Wachstum einiger Krebsarten zu verlangsamen und das Krebsrisiko zu senken. Zudem gibt es bereits Belege dafür, dass Eingriffe in den Stoffwechsel Einfluss auf die Krebsrate haben können. Wie wir gesehen haben, sterben Labortiere, die kalorienreduziert ernährt werden, sehr viel langsamer an Krebs als Kontrolltiere, die so viel fressen dürfen, wie sie wollen. Weniger zu fressen scheint ihnen einen gewissen Schutz zu bieten. Für Menschen könnte das Gleiche gelten: Eine Studie über Kalorienrestriktion beim Menschen kam zu dem Ergebnis, dass die Einschränkung der Kalorienaufnahme den PI3K-Signalweg unmittelbar herunterreguliert – allerdings in Muskeln (die nicht anfällig für Krebs sind).[152] Das könnte eher an dem niedrigeren Insulinspiegel als an einem niedrigeren Glucosespiegel liegen.
Es ist zwar kompliziert, wenn nicht gar unmöglich, die Genmutationen zu verhindern, die die Entstehung von Krebs fördern, doch relativ einfach, die metabolischen Faktoren zu beeinflussen, die ihn nähren. Ich will nicht behaupten, es sei möglich, Krebs »auszuhungern«, oder irgendeine spezielle Diät würde ihn wie durch Zauberhand vertreiben. Krebszellen scheinen immer in der Lage zu sein, sich den Energievorrat zu beschaffen, den sie benötigen. Was ich sagen möchte, ist: Wir sorgen einfach dafür, dass wir uns von dem Bereich zwischen Insulinresistenz und Typ-2-Diabetes fernhalten, in dem unser Krebsrisiko eindeutig ansteigt. In meinen Augen ist dies ein leicht erreichbares Ziel der Krebsprävention, genau wie das Ziel, mit dem Rauchen aufzuhören. Unseren Stoffwechsel gesund zu erhalten ist ein entscheidender Bestandteil unserer Antikrebsstrategie. Im nächsten Abschnitt schauen wir uns an, inwiefern Eingriffe in den Stoffwechsel auch andere Arten der Krebstherapie unterstützen konnten.
Neue Behandlungsarten
Die Entdeckung des PI3K-Signalwegs durch Lew Cantley führte zur Entwicklung einer ganzen Klasse von Medikamenten, die den Krebsstoffwechsel ins Visier nehmen. Drei dieser Medikamente, die sogenannten PI3K-Inhibitoren, wurden von der FDA zur Behandlung bestimmter rezidivierender Blutkrebsarten und Lymphome zugelassen, und Ende 2019 erfolgte die Zulassung eines vierten gegen Brustkrebs. Sie schienen jedoch nicht so gut zu wirken, wie aufgrund der bedeutenden Rolle von PI3K für das Wachstum von Krebszellen prognostiziert worden war. Außerdem hatten sie die unangenehme Nebenwirkung, den Blutzuckerspiegel anzuheben, was wiederum einen sprunghaften Anstieg des Insulinspiegels und von IGF-1 bewirkte, weil die Zelle versuchte, die PI3K-Hemmung zu umgehen – was wir laut unserer Theorie unbedingt vermeiden möchten.
2014 kam es zu einem gemeinsamen Abendessen mit Cantley, der damals Direktor des Meyer Cancer Center am Weill Cornell Medical College in Manhattan war, und Siddhartha Mukherjee, praktizierender Onkologe, Forscher und Autor von The Emperor of All Maladies (dt. Der König aller Krankheiten), einer »Krebsbiografie«, wofür er den Pulitzer-Preis bekam.[153] Als großer Bewunderer von Sids Arbeiten setzte ich mich voller Aufregung zu diesen beiden Giganten der Onkologie.
Beim Essen erzählte ich ihnen von einem Fall, bei dem man die Behandlung mit einem PI3K-Inhibitor durch eine Art metabolischer Therapie ergänzt hatte. Das ging mir häufig im Kopf herum, weil die Patientin die Frau eines sehr guten Freundes war. Bei Sandra (nicht ihr richtiger Name) war sechs Jahre zuvor Brustkrebs diagnostiziert worden. Er hatte bereits in die Lymphknoten und die Knochen gestreut. Wegen der schlechten Prognose wurde sie in eine klinische Studie aufgenommen, bei der ein PI3K-Inhibitor in Kombination mit herkömmlichen Therapien getestet werden sollte.
Sandra war eine ausgesprochen motivierte Patientin. Vom Tag ihrer Diagnose an war sie bereit, alles Erdenkliche zu tun, um das Blatt zu ihren Gunsten zu wenden. Sie stürzte sich auf jeden Artikel über die Auswirkungen der Ernährung auf Krebs und war zu dem Schluss gekommen, dass eine Diät zur Senkung des Insulin- und IGF-1-Spiegels ihre Behandlung unterstützen würde. Also stellte sie sich einen Ernährungsplan zusammen, der überwiegend aus Blattgemüse, Olivenöl, Avocados, Nüssen und geringen Mengen an Proteinen, meist aus Fisch, Eiern und Geflügel, bestand. Genauso wichtig war jedoch, was in dem Plan nicht enthalten war: Zuckerzusatz und raffinierte Kohlenhydrate. Während der ganzen Zeit unterzog sie sich regelmäßigen Bluttests, um sicherzugehen, dass die Insulin- und IGF-1-Spiegel niedrig blieben.
In den darauffolgenden Jahren starben alle anderen Frauen, die an Sandras Versuchsstandort an der Studie teilnahmen. Keine einzige überlebte. Die Patientinnen waren mit modernster Chemotherapie und dem PI3K-Inhibitor behandelt worden, doch der metastasierende Brustkrebs hatte gesiegt. Die Studie wurde eingestellt, weil klar war, dass die Medikamente nicht wirkten. Mit Ausnahme von Sandra. Warum war sie noch am Leben, während Hunderte andere Frauen mit der gleichen Krankheit im gleichen Krankheitsstadium gestorben waren? Hatte sie einfach nur Glück gehabt? Oder konnte es sein, dass ihre äußerst strenge Diät, die wahrscheinlich zur Senkung ihres Insulin- und IGF-1-Spiegels führte, ihr Schicksal gewendet hatte?
Mir schwante, dass es so war. Ich glaube, wir müssen ein Auge auf diese statistischen Ausreißer haben, die »wie durch ein Wunder« überleben. Auch wenn es sich nur um anekdotische Fälle handelt, verschaffen sie uns vielleicht hilfreiche Erkenntnisse über diese tödliche, mysteriöse Krankheit. Um es mit den Worten von Steve Rosenberg zu sagen: »Diese Patienten helfen uns, die richtigen Fragen zu stellen.«
In seinem 592 Seiten starken Opus magnum über Krebs, das 2010 erschien, hatte Mukherjee jedoch kaum ein Wort über den Stoffwechsel und metabolische Therapien verloren. Wie er mir später verriet, hielt er es damals für verfrüht. Als ich ihm nun bei unserem Essen von der Geschichte erzählte, wirkte er interessiert, aber skeptisch. Cantley schnappte sich eine Serviette und kritzelte eine Grafik darauf. Das Problem bei den PI3K-Inhibitoren sei, so erläuterte er, dass sie durch die Hemmung des mit Insulin in Verbindung stehenden PI3K-Signalwegs letztlich die Insulin- und Glucosekonzentration im Blut erhöhen. Weil der Glucose der Weg in die Zelle versperrt werde, verbleibe mehr davon im Blutkreislauf. Daraufhin meine der Körper, er müsse mehr Insulin produzieren, um all die Glucose loszuwerden, was durch die Aktivierung von PI3K womöglich die Wirkung des Medikaments teilweise umkehre. Was aber wäre, wenn wir die PI3K-Inhibitoren mit einer Insulin minimierenden oder ketogenen Diät kombinieren würden?
Aus dieser groben Skizze auf einer Serviette entstand eine Studie, deren Ergebnisse 2018 mit Mukherjee und Cantley als Seniorautoren in Nature veröffentlicht wurde.[154] Laut der Studie bewirkte die Kombination einer ketogenen Diät mit PI3K-Inhibitoren, dass Mäuse, denen man menschliche Krebstumoren implantiert hatte, besser auf eine Behandlung ansprachen. Die Ergebnisse sind von Bedeutung, weil sie nicht nur zeigen, dass der Stoffwechsel einer Krebszelle ein sinnvolles Therapieziel ist, sondern auch, dass die Stoffwechsellage eines Patienten die Wirksamkeit eines Medikaments beeinflussen kann. Im vorliegenden Fall schien die sonst eher enttäuschende Behandlung im Zusammenwirken mit der ketogenen Ernährung der Tiere sehr viel besser anzuschlagen als zuvor. Es ist wie beim Boxen – auch dort ist eine Kombination häufig viel wirkungsvoller als ein einzelner Punch. Verfehlt der erste Schlag seine Wirkung, ist der zweite bereits auf dem Weg und zielt genau auf den Punkt, wohin sich der Gegner vermutlich bewegen wird. (Mukherjee und Cantley haben anschließend ein gemeinsames Start-up-Unternehmen gegründet, um die Idee einer kombinierten medikamentös-diätetischen Behandlung weiter zu erforschen.)
Auch bei anderen Ernährungsinterventionen hat sich herausgestellt, dass sie die Wirksamkeit der Chemotherapie verbessern und zugleich die Kollateralschäden am gesunden Gewebe begrenzen. Valter Longo von der University of Southern California und andere haben entdeckt, dass Fasten oder eine fastenähnliche Diät die Widerstandsfähigkeit normaler Zellen gegen eine Chemotherapie erhöhen und die Krebszellen gleichzeitig anfälliger für die Behandlung machen. Es erscheint vielleicht kontraproduktiv, Krebspatienten eine Fastenkur zu empfehlen, aber laut Forschern hatte sie keine gravierenden negativen Auswirkungen auf Patienten, die eine Chemotherapie erhielten, und in einigen Fällen kann sie ihre Lebensqualität verbessert haben. Eine randomisierte Studie an 131 Krebspatienten, die sich einer Chemotherapie unterzogen, erbrachte, dass diejenigen Patienten, die eine »Quasi-Fastenkur« durchführten (im Grunde eine sehr kalorienarme Diät, die für die Zufuhr essenzieller Nährstoffe sorgte und zugleich das Hungergefühl dämpfte), mit größerer Wahrscheinlichkeit auf die Chemotherapie ansprachen und sich körperlich und emotional besser fühlten.[155]
Das widerspricht völlig der herkömmlichen Praxis, bei der man Chemotherapiepatienten ermuntert, so viel wie möglich zu essen, und zwar typischerweise hochkalorische und sogar stark zuckerhaltige Nahrung. Die American Cancer Society empfiehlt »Kuchen mit Eiscremehäubchen«.[156] Die Ergebnisse der besagten Studien legen jedoch nahe, dass es keine gute Idee ist, den Insulinspiegel bei Krebskranken in die Höhe zu treiben. Weitere Untersuchungen müssen erfolgen, aber die Arbeitshypothese lautet: Weil Krebszellen einen solch gierigen Stoffwechsel haben, reagieren sie anfälliger auf eine Nährstoffreduzierung als normale Zellen – oder, noch wahrscheinlicher, auf eine Reduzierung von Insulin, das den für den Warburg-Effekt entscheidenden PI3K-Signalweg aktiviert.
Diese sowie die oben erörterte Studie von Mukherjee und Cantley weisen darüber hinaus auf eine weitere wichtige Erkenntnis hin, die wir aus diesem Kapitel ziehen können: Um Krebs erfolgreich zu behandeln, braucht es meist mehr als nur eine Therapiemethode. Wie mir Keith Flaherty, praktizierender Onkologe und Direktor der Klinischen Forschung am Massachusetts General Hospital, erklärte, besteht die beste Strategie zur Krebsbekämpfung vermutlich darin, gleichzeitig oder nacheinander an mehreren Schwachstellen der Krankheit anzusetzen. Indem wir verschiedene Therapien zusammenführen, wie bei der Kombination eines PI3K-Inhibitors mit einer ketogenen Diät, können wir den Krebs an mehreren Fronten angreifen, was gleichzeitig die Wahrscheinlichkeit minimiert, dass er (über Mutationen) eine Resistenz gegen eine bestimmte Behandlung entwickelt. In der konventionellen Chemotherapie setzt sich das allmählich durch – aber damit es durchschlagende Wirkung entfaltet, brauchen wir zunächst noch mehr wirksame Behandlungsmethoden, die noch besser in der Lage sind, Krebszellen gezielt zu zerstören, ohne dabei gesunden Zellen und dem Patienten Schaden zuzufügen.
Im folgenden Abschnitt schauen wir uns an, inwiefern die einstmals obskure Idee der Immuntherapie zu mehreren potenziell bahnbrechenden Krebstherapien geführt hat, die diesem Anspruch gerecht werden könnten.
Die Verheißung der Immuntherapie
Genau wie der Stoffwechsel blieb auch die Immuntherapie in The Emperor of All Maladies unerwähnt. Als das Buch im Jahr 2010 veröffentlicht wurde, hatte sie kaum jemand auf dem Radar. Doch als Ken Burns nur fünf Jahre später seinen Dokumentarfilm über das Buch herausbrachte, nahmen sie wie auch Steve Rosenberg darin großen Raum ein, was verdeutlicht, wie sehr sich unser Denken über Krebs und insbesondere Immuntherapie gerade im letzten Jahrzehnt gewandelt hat.
Das Immunsystem ist darauf programmiert, zwischen »Nichtselbst« und »Selbst« zu unterscheiden – das heißt, eindringende Pathogene und Fremdkörper unter unseren eigenen gesunden Zellen zu identifizieren und sie zu töten oder zu neutralisieren. Als Immuntherapie bezeichnet man jede Therapie, die versucht, das Immunsystem eines Patienten zu stärken oder zu aktivieren, um eine Infektion oder ein anderes Leiden zu bekämpfen (Beispiel: Impfungen). Will man auf diese Weise gegen Krebs vorgehen, steht man vor dem Problem, dass Krebszellen zwar abnormal und gefährlich, streng genommen aber unsere eigenen Zellen sind, also zum »Selbst« gehören. Sie haben sich raffinierterweise so entwickelt, dass sie vom Immunsystem und speziell von unseren T-Zellen, dem Killerkommando des Immunsystems, das mit Eindringlingen normalerweise kurzen Prozess macht, nicht als Feind erkannt werden. Damit eine Krebs-Immuntherapie Erfolg hat, müssen wir also in allererster Linie dem Immunsystem beibringen, unsere eigenen Zellen, die sich in Krebszellen verwandelt haben, zu erkennen und zu eliminieren. Es muss das »böse Selbst« (Krebs) vom »guten Selbst« (alle anderen Selbst-Zellen) unterscheiden können.
Rosenberg war nicht der Erste, der versucht hat, das Immunsystem gegen Krebs zu wappnen. Schon im 19. Jahrhundert hatte William Coley, ein in Harvard ausgebildeter Chirurg, vermerkt, dass ein Patient mit einem lebensbedrohlichen Tumor verblüffenderweise offenbar infolge einer schweren Infektion nach einer Operation genesen war. Daraufhin begann Coley Experimente mit bakteriellen Impfungen, von denen er hoffte, dass sie bei anderen Patienten eine ähnliche Immunantwort hervorrufen würden. Seine medizinischen Kollegen entsetzte jedoch die Vorstellung, Patienten Keime zu injizieren, und als es anderen Forschern nicht gelang, Coleys Ergebnisse zu reproduzieren, wurden seine Ideen verworfen und als Quacksalberei abgetan. Trotzdem kam es gelegentlich zu Spontanremissionen: Die Symptome einer Krebserkrankung gingen zurück, ohne dass es dafür eine plausible Erklärung gab – so wie in dem Fall, den Rosenberg als junger Assistenzarzt beobachtet hatte. So erhielt man faszinierende Einblicke in die Heilkräfte des menschlichen Körpers.
Das Problem war nicht leicht zu lösen. Rosenberg versuchte es mit einem Ansatz nach dem anderen, aber ohne Erfolg. Ein »Krebsimpfstoff« ließ sich nicht herstellen. Viele Jahre experimentierte er mit Interleukin-2 (IL-2), einem Cytokin, das bei der Immunantwort eine wichtige Rolle spielt (im Wesentlichen verstärkt es die Aktivität der Lymphozyten, weißen Blutzellen, die Entzündungen bekämpfen). In Versuchen an Tiermodellen mit metastasierendem Krebs hatte es gewirkt, doch beim Menschen waren die Ergebnisse gemischt – die Patienten mussten Tage, wenn nicht Wochen auf der Intensivstation verbringen, und viele starben an den massiven Nebenwirkungen. 1984 gelang es schließlich, bei Linda Taylor, einer Melanompatientin im Spätstadium, allein mit hoch dosiertem IL-2 eine Remission, das Abklingen der Krankheitserscheinungen, zu bewirken.
Dies war ein entscheidender Wendepunkt, denn er zeigte, dass das Immunsystem Krebs abwehren konnte. Doch noch immer überwogen die Rückschläge die Erfolge, denn hoch dosiertes IL-2 schien nur bei Melanomen und Nierenzellkrebs zu wirken, und das auch nur bei 10 bis 20 Prozent der Patienten, die an diesen beiden Krebsarten erkrankt waren.[157] Man hatte versucht, dem Problem mit dem Gießkannenprinzip zu Leibe zu rücken, während Präzision gefragt war. Also wandte Rosenberg seine Aufmerksamkeit direkt den T-Zellen zu. Wie konnte man sie dazu bringen, Krebszellen zu erkennen und zu bekämpfen?
Es vergingen viele weitere Jahre mit verschiedenen Versuchen, aber dann übernahmen Rosenberg und sein Team ein in Israel entwickeltes Verfahren, bei dem T-Zellen aus dem Blut eines Patienten gewonnen und per Gentechnik mit Antigenrezeptoren ausgestattet wurden, die auf die Tumoren des Patienten zugeschnitten waren. Nun waren die T-Zellen darauf programmiert, den Krebs zu bekämpfen. Diese »chimären Antigenrezeptor-T-Zellen« (CAR-T) wurden im Labor vervielfältigt und dem Patienten dann wieder mittels Infusion zurückgegeben.
2010 konnten Rosenberg und sein Team ihren ersten Erfolg mit einer CAR-T-Behandlung vermelden – bei einem Patienten mit einem fortgeschrittenen follikulären Lymphom, der bereits mehrere konventionelle Behandlungsrunden hinter sich gebracht hatte, einschließlich Chemotherapie sowie einer anderen Art von Immuntherapie, aber alles ohne Erfolg.[158] Auch andere Gruppen wendeten das Verfahren an, und 2017 wurden endlich die beiden ersten CAR-T-basierten Behandlungen von der FDA zugelassen (womit sie die ersten jemals von der FDA anerkannten Zell- und Gentherapien waren) – eine für Lymphom bei Erwachsenen und eine weitere für akute lymphoblastische Leukämie, den häufigsten Krebs bei Kindern. Es hatte fast fünfzig Jahre gedauert, doch letzten Endes hatte Steve Rosenbergs »obskure« Idee einen Durchbruch erzielt.
So elegant CAR-T-Behandlungen auch sind – als erfolgreich haben sie sich lediglich bei einer einzigen Krebsart, dem B-Zell-Lymphom, erwiesen. Alle B-Zellen, ob es normale oder Krebszellen sind, exprimieren ein Protein, das als CD19 bezeichnet wird und die Zielscheibe für den tödlichen Angriff der CAR-T-Zelle bildet. Da wir auch ohne B-Zellen leben können, schaltet CAR-T sämtliche CD19-tragenden Zellen aus. Leider haben wir bislang noch keine entsprechenden Marker für andere Krebsarten identifiziert.
Wenn wir die Gesamtsterberate durch Krebs senken wollen, brauchen wir einen Behandlungstyp, der auf breiter Linie Erfolg verspricht. Glücklicherweise entwickelte sich der Ansatz der Immuntherapie weiter. Mittlerweile, etwas mehr als zehn Jahre später, wurde eine Handvoll Krebsmedikamente zugelassen, die auf Immuntherapie basieren. Neben CAR-T gibt es nun eine Klasse von Medikamenten, die als Checkpoint-Inhibitoren bezeichnet werden und die entgegengesetzte Herangehensweise verfolgen. Statt T-Zellen dazu zu aktivieren, Krebszellen zu töten, helfen die Checkpoint-Inhibitoren, den Krebs für das Immunsystem sichtbar zu machen.
Um eine sehr lange und faszinierende Geschichte kurz zu fassen:[159] James Allison, ein Forscher aus Texas, der sich schon fast so lange wie Steve Rosenberg mit der Immuntherapie beschäftigt, fand heraus, wie sich Krebszellen vor dem Immunsystem verstecken. Sie nutzen sogenannte Checkpoints, die normalerweise unsere T-Zellen regulieren und sie daran hindern, Amok zu laufen und gesunde Zellen anzugreifen, was zu einer Autoimmunerkrankung führen würde. Im Prinzip fragen die Checkpoints die T-Zellen ein letztes Mal: »Seid ihr wirklich sicher, dass ihr diese Zelle töten wollt?«
Allison entdeckte Folgendes. Wenn man bestimmte Checkpoints – insbesondere einen namens CTLA-4 – blockierte, waren die Krebszellen enttarnt und schutzlos und konnten von den T-Zellen zerstört werden. Er testete das Verfahren an Mäusen, die aufgrund genetischer Veränderung Krebs entwickelten. Als er bei einem seiner ersten Experimente morgens ins Labor kam, stellte er fest, dass alle Mäuse, die die Checkpoint-Inhibitor-Therapie erhalten hatten, noch lebten, während alle anderen tot waren. Es ist erfreulich, wenn Versuchsergebnisse so eindeutig sind, dass man nicht einmal eine statistische Analyse durchführen muss.
Im Jahr 2018 teilte sich Allison den Nobelpreis mit dem japanischen Wissenschaftler Tasuku Honjo, der an einem etwas anderen Checkpoint, PD-1, geforscht hatte. Die Arbeit dieser beiden Wissenschaftler hat zur Zulassung von zwei Medikamenten geführt – eines mit dem Antikörper Ipilimumab, das CTLA-4 hemmt, und eines mit dem Antikörper Pembrolizumab, das PD-1 ins Visier nimmt.
Alle Nobelpreise sind beeindruckend, aber dieser gefällt mir besonders gut. Die Checkpoint-Inhibitoren haben nicht nur einem dritten Nobelpreisträger, dem früheren US-Präsidenten Jimmy Carter, das Leben gerettet, der 2015 wegen eines metastasierenden Melanoms mit Pembrolizumab behandelt wurde, sondern auch einem sehr guten Freund von mir, einem früheren Kollegen, den ich hier Michael nenne. Er war erst Anfang vierzig, als bei ihm ein sehr großer Dickdarmtumor entdeckt wurde, der eine sofortige Operation erforderte. Ich kann mich noch an das Cover der Zeitschrift erinnern, die ich voller Angst durchblätterte, als ich während der OP im Wartezimmer saß. Michael ist der netteste Mensch, den ich kenne, und zur Zeit unserer Zusammenarbeit schaffte er es mit seiner Brillanz und seinem Witz auch an den schlimmsten Tagen immer wieder, mich aufzumuntern. Der Gedanke, ihn womöglich zu verlieren, war unerträglich.
Seine Familie und Freunde waren überglücklich, als die Operation erfolgreich verlief und die pathologische Untersuchung trotz der Größe des Primärtumors kein Anzeichen von Krebs in den nahe gelegenen Lymphknoten erbrachte. Einige Monate später aber wandelte sich unsere Freude erneut in Entsetzen, als wir erfuhren, dass der Krebs bei Michael auf eine genetische Störung, das sogenannte Lynch-Syndrom, zurückzuführen war. Wer am Lynch-Syndrom leidet, weiß das normalerweise, weil die Krankheit dominant vererbt wird. Doch da Michael adoptiert worden war, hatte er keine Ahnung, in welcher Gefahr er schwebte. Die für das Lynch-Syndrom spezifischen Mutationen bewirken so gut wie sicher, dass ihre Träger, so wie Michael, schon in jungen Jahren Dickdarmkrebs entwickeln, aber auch das Risiko, an anderen Krebsarten zu erkranken, ist sehr hoch. Und tatsächlich – fünf Jahre nachdem Michael erfolgreich jener ersten tödlichen Kugel ausgewichen war, rief er an, um zu berichten, dass er nun an einem Adenokarzinom der Bauchspeicheldrüse litt. Das war noch schlimmer als beim ersten Mal, denn wie wir beide wussten, ist dieser Krebs fast immer tödlich.
Michael ging zum besten Pankreas-Chirurgen der Umgebung, der seine schlimmsten Befürchtungen bestätigte: Eine Operation war nicht möglich, weil der Krebs schon zu weit fortgeschritten war. Michael blieben höchstens noch neun bis zwölf Monate zu leben. Noch herzzerreißender war, dass er und seine Frau im selben Jahr zum ersten Mal Eltern geworden waren – sie hatten Zwillingsmädchen bekommen. Vor Kurzem hatte im New England Journal of Medicine gestanden, dass einige Patienten mit einer Mismatch-Reparatur-Defizienz (die häufig beim Lynch-Syndrom auftritt und dadurch gekennzeichnet ist, dass Fehlpaarungen in DNA-Doppelsträngen nicht von körpereigenen Proteinen beseitigt werden) erfolgreich mit Pembrolizumab, dem PD-1-Antikörper, behandelt worden waren.[160] Es war eine vage Hoffnung, aber durchaus nicht abwegig, dass das Medikament Michael helfen könnte. Michaels Ärzte waren bereit, ihn daraufhin zu testen, und es bestätigte sich, dass Michael tatsächlich ein geeigneter Kandidat für die Behandlung war. Er wurde sofort in eine klinische Studie aufgenommen. Die Behandlung schlägt nicht bei allen Patienten an, aber bei Michael zeigte sie Wirkung – sein Immunsystem bekämpfte den Tumor und vernichtete zu guter Letzt alle Anzeichen für Bauchspeicheldrüsenkrebs in seinem Körper.
Somit ist er nun zum zweiten Mal krebsfrei und mehr als dankbar, dass er eine Krankheit überlebt hat, die ihn hätte töten können, als seine Zwillingsmädchen noch im Säuglingsalter waren. Nun darf er sie aufwachsen sehen. Allerdings schoss sein Immunsystem beim Angriff auf den Krebs etwas über das Ziel hinaus und zerstörte auch seine Bauchspeicheldrüse. Demzufolge leidet er nun an Typ-1-Diabetes, da er kein Insulin mehr produzieren kann. Die Bauchspeicheldrüse hat er verloren, aber dafür sein Leben gerettet – das scheint unter dem Strich ein fairer Tausch zu sein.
Michael hatte Glück. Bislang helfen die verschiedenen zugelassenen Immuntherapiebehandlungen jedoch nur recht wenigen Patienten. Etwa ein Drittel der Krebsarten lässt sich mit Immuntherapie bekämpfen, und von den betreffenden Patienten überlebt nur ein Viertel. Laut einer Analyse der Onkologen Nathan Gay und Vinay Prasad konnte die Immuntherapie nur 8 Prozent der potenziellen Todesfälle aufgrund von Krebs verhindern.[161] Wenn’s passt, funktioniert sie gut, aber nur bei wenigen Patienten und mit großen Kosten. Trotzdem wären noch vor zwanzig Jahren – als mich meine Ausbildung zum Krebschirurgen so sehr frustrierte – Patienten wie Ex-Präsident Carter oder mein Freund Michael und unzählige weitere allesamt gestorben.
Ich und andere, die viel mehr wissen als ich, glauben jedoch daran, dass wir bislang nur einen Bruchteil der potenziellen Leistungsfähigkeit der Immuntherapie entdeckt haben.
Zurzeit wird erforscht, wie sich die Immuntherapie mit anderen Behandlungsarten kombinieren ließe. In einem kürzlich erschienenen Artikel wird von einer klinischen Studie berichtet, bei der eine platinbasierte Chemotherapie in Kombination mit einem Checkpoint-Inhibitor angewandt wurde, was die Überlebenschancen von Lungenkrebspatienten allgemein verbesserte.[162] Der Checkpoint-Inhibitor allein blieb ohne Wirkung, aber irgendetwas an der Chemotherapie veranlasste den Krebs, stärker auf die Immuntherapie zu reagieren oder für sie »sichtbarer« zu werden, wenn man so will. Dies ist eine Weiterführung der bereits erwähnten Idee, Therapien miteinander zu koppeln.
Um den Wirkungsbereich der Immuntherapie zu erweitern, müssen wir unsere Immunzellen dazu bringen, ein größeres Spektrum an Krebszellen aufzuspüren und zu eliminieren und nicht nur einige wenige Typen. Genanalysen haben erbracht, dass etwa 80 Prozent der epithelialen Krebsarten (das heißt von soliden Tumoren) Mutationen aufweisen, die das Immunsystem erkennen kann – was sie für eine immunbasierte Behandlung potenziell anfällig macht.[163]
Ein sehr vielversprechendes Verfahren ist die adoptive Zelltherapie (oder adoptiver Zelltransfer, ACT). ACT ist eine Form der Immuntherapie, bei der zusätzliche T-Zellen, wie Verstärkungstruppen für eine Armee, in einen Patienten transferiert werden, um die Kampfkraft gegen seinen Tumor zu erhöhen. Diese T-Zellen besitzen Antigene, die auf den spezifischen Tumortyp des Patienten abgestimmt sind. Das ähnelt der bereits erörterten CAR-T-Zelltherapie, hat aber einen viel größeren Anwendungsbereich. Ein wachsender Tumor überfordert schnell die Kapazität des Immunsystems, ihn zu entdecken und zu töten. Es gibt schlicht zu wenige T-Zellen für den Job, vor allem wenn der Tumor bereits klinisch feststellbar ist. Aus diesem Grund ist eine spontane Rückbildung wie bei James DeAngelo so selten. Der ACT liegt im Wesentlichen die Idee zugrunde, den Krebs mit einer großen Anzahl zielgerichteter T-Zellen zu besiegen, so wie die Verstärkung einer Armee mit einem speziell ausgebildeten Killerkommando.
Es gibt zwei Spielarten der ACT. Man kann entweder aus dem Tumor eines Patienten eine Probe entnehmen und diejenigen T-Zellen isolieren, die den Tumor als Bedrohung erkennen. Diese bezeichnet man als tumorinfiltrierende Lymphozyten (TILs). Möglicherweise gibt es aber nur einige Millionen davon, was für eine wirkungsvolle Immunantwort gegen den Tumor nicht ausreicht. Entnimmt man die TILs, vertausendfacht sie und leitet sie per Infusion zurück in den Patienten, ist eine deutlich bessere Immunantwort zu erwarten. Alternativ kann man T-Zellen aus dem Blut des Patienten gewinnen und sie genetisch so modifizieren, dass sie seinen spezifischen Tumor erkennen. Beide Ansätze haben Vor- und Nachteile,[164] doch ein wichtiger Punkt ist, dass die ACT eine auf jeden einzelnen Patienten zugeschnittene Krebsbehandlung ermöglicht.
Dies alles ist offenkundig ein kostspieliges Unterfangen und mit aufwendiger Laborarbeit verbunden, aber auch sehr Erfolg versprechend. Der Machbarkeitsbeweis wurde erbracht, doch es bleibt noch eine Menge zu tun – nicht nur, um die Wirksamkeit des Ansatzes weiter zu verbessern, sondern auch, um diese Behandlung leichter und in einem größeren Rahmen verfügbar zu machen. Zudem mögen die Kosten zunächst untragbar erscheinen, doch dem ist entgegenzusetzen, dass die konventionelle Chemotherapie ebenfalls sehr teuer ist und die Remission fast nie anhält.
An der immunbasierten Krebstherapie ist verblüffend, dass sie nicht nur wirkt, sondern nachhaltig wirkt. Bei Patienten mit metastasierenden Tumoren ist der Krebs nach einer Chemotherapie häufig verschwunden. Doch leider ist dieser Erfolg so gut wie nie von Dauer. Immer kehrt der Krebs in irgendeiner Form zurück. Wenn Patienten jedoch auf eine Immuntherapie ansprechen und eine vollständige Remission eintritt, bleibt das häufig auch so. 80 bis 90 Prozent dieser Patienten sind auch fünfzehn Jahre später noch krebsfrei.[165] Das ist außergewöhnlich – viel besser als die kurze Fünfjahresfrist, nach der wir üblicherweise einen Erfolg der konventionellen Krebsbehandlung feiern. Man scheut sich, das Wort geheilt zu verwenden, aber bei Patienten, die auf eine Immuntherapie ansprechen, kann man durchaus davon ausgehen, dass der Krebs verschwunden ist.
Die wichtige Botschaft lautet also, dass es Hoffnung gibt. Zum ersten Mal in meinem Leben macht der War on Cancer Fortschritte, wenn wir davon überhaupt noch sprechen können. Nun gibt es Behandlungen, die das Leben Tausender Menschen retten können und tatsächlich retten, für die es vor gerade einmal zehn Jahren keine Rettung gegeben hätte. Vor zwanzig Jahren hatte man mit einem metastasierenden Melanom noch eine durchschnittliche Lebenserwartung von etwa einem halben Jahr. Nun beträgt sie zwei Jahre, und rund 20 Prozent der Betroffenen sind dann vollständig geheilt. Das ist ein messbarer Fortschritt, der praktisch allein der Immuntherapie zu verdanken ist. Eine verbesserte Früherkennung von Krebs, auf die wir im letzten Abschnitt dieses Kapitels eingehen, wird die Wirksamkeit unserer Immuntherapiebehandlungen vermutlich noch steigern.
Die Immuntherapie hat einen steinigen Weg hinter sich, und auf diesem Weg gab es viele Hindernisse, die ihr Ende hätten bedeuten können. Letztlich hat sie sich durchgesetzt, weil ihre chimärischen Erfolge doch keine Chimären waren. Der größte Dank aber gilt der Entschlossenheit und Hartnäckigkeit visionärer Wissenschaftler wie James Allison, Tasuku Honjo, Steve Rosenberg und anderer, die auch dann weitergemacht haben, wenn ihre Arbeit fruchtlos und vielleicht gar verrückt erschien.
Früherkennung
Das letzte und vielleicht wichtigste Instrument in unserem Antikrebs-Arsenal ist frühes, aggressives Screening. Das ist zwar nach wie vor ein kontroverses Thema, doch alles spricht dafür, dass es unter dem Strich so gut wie immer von Nutzen ist, wenn man Krebs früh erkennt.
Leider stehen wir heute noch vor dem gleichen Problem wie zu meiner Zeit als Assistenzarzt: Krebs wird zu häufig erst dann erkannt, wenn er größer geworden ist und Metastasen gebildet hat. Gegen diese fortgeschrittenen Krebserkrankungen gibt es kaum eine wirksame Behandlung. Abgesehen von den wenigen Krebsarten, die auf Immuntherapien ansprechen, können wir in den meisten Fällen nur hoffen, den Tod ein wenig hinauszuzögern. Die Zehn-Jahres-Überlebensrate bei Patienten mit einer metastasierten Krebserkrankung ist praktisch noch dieselbe wie vor fünfzig Jahren, nämlich gleich null. Wir müssen mehr tun, als nur auf neuartige Therapien zu hoffen.
Wenn Krebs schon früh, in Stadium I, erkannt wird, steigen die Überlebensraten sprunghaft an. Das hat teilweise mit simpler Mathematik zu tun: In diesen früheren Stadien gibt es noch weniger Krebszellen, und sie weisen weniger Mutationen auf, weshalb sie besser auf die Behandlung mit den bereits vorhandenen Medikamenten, einschließlich einiger Immuntherapien, ansprechen. Ich würde sogar behaupten, dass die Früherkennung unsere beste Waffe ist, um die Krebssterblichkeit radikal zu senken.
Diese Behauptung ist nicht nur intuitiv plausibel, sondern bestätigt sich bereits bei einem flüchtigen Blick auf Daten, die die Erfolgsraten bei der Behandlung spezifischer Krebsarten mit Metastasen mit einer adjuvanten (das heißt postoperativen) Behandlung vergleichen. Betrachten wir zunächst die Daten zu Dickdarmkrebs. Patienten mit metastasiertem Dickdarmkrebs, bei denen der Krebs also schon gestreut und benachbarte Lymphknoten sowie weitere Bereiche des Körpers, etwa die Leber, befallen hat, werden normalerweise mit einer Kombination aus drei Medikamenten, dem sogenannten FOLFOX-Regime, behandelt. Diese Behandlung verspricht eine mittlere Überlebenszeit von etwa 31,5 Monaten,[166] was bedeutet, dass ungefähr die Hälfte der Patienten länger lebt und die andere Hälfte nicht. So oder so wird aber praktisch keiner der Patienten in zehn Jahren noch am Leben sein. Wenn Patienten mit Dickdarmkrebs in Stadium III erfolgreich operiert wurden, der Krebs also vollständig entfernt worden ist und nicht sichtbar in entfernte Organe gestreut hat, erhalten sie eine Nachbehandlung mit genau demselben FOLFOX-Regime. Doch dann überleben ganze 78,5 Prozent dieser Patienten weitere sechs Jahre – die mittlere Überlebenszeit ist mehr als doppelt so lang wie bei den Patienten mit Metastasen –, und 67 Prozent von ihnen sind auch zehn Jahre nach der Operation noch am Leben.[167] Das ist ein beeindruckender Unterschied.
Wie lässt sich das erklären? Der Unterschied hat mit der Gesamtmenge der Krebszellen pro Patient zu tun. Bei fortgeschrittenem, metastasiertem Krebs gilt es, zig Milliarden, wenn nicht gar Hunderte Milliarden Krebszellen zu bekämpfen. Bei weniger fortgeschrittenem Krebs konnten zwar zweifellos immer noch Millionen oder auch Milliarden Krebszellen dem Skalpell entrinnen, aber ihre weitaus geringere Menge bedeutet, dass es auch weniger Mutationen und demzufolge geringeren Widerstand gegen die Behandlung gibt.
Bei Brustkrebspatientinnen sieht es ähnlich aus. Frauen mit HER2-positivem metastasiertem Brustkrebs[168] können mit einer mittleren Überlebenszeit von knapp fünf Jahren rechnen, wobei standardmäßig eine Behandlung mit drei chemotherapeutischen Medikamenten erfolgt. Handelt es sich jedoch um einen kleineren (< 3 cm), lokal begrenzten HER2-positiven Tumor, der operativ entfernt wird, und schließt sich eine adjuvante Behandlung mit nur zwei dieser drei Medikamente an, haben die Patientinnen eine 93-prozentige Chance, mindestens weitere sieben Jahre ohne die Krankheit zu überleben.[169] Es ist wie bei der Immuntherapie: Je geringer die Zahl der Krebszellen ist, desto besser wirken gemeinhin die Medikamente und desto größer sind die Überlebenschancen.
Leider sind wir – noch – nicht sehr gut darin, Krebs in diesen frühen Stadien zu entdecken. Von Dutzenden verschiedenen Krebsarten gibt es nur fünf, für die es anerkanntermaßen verlässliche Screeningverfahren gibt: Lungenkrebs (bei Rauchern), Brustkrebs, Prostatakrebs, Darmkrebs (Krebs des Dick- und Mastdarms) und Gebärmutterhalskrebs. Dennoch wird in Mainstream-Richtlinien von einigen Arten der Früherkennung abgeraten, so etwa von der Mammografie bei Frauen und dem PSA-Bluttest bei Männern, der die Menge an Prostata-spezifischem Antigen bestimmt. Das hat zum einen mit den Kosten zu tun und zum anderen mit der Gefahr falsch positiver Befunde, die zu unnötigen oder sogar gefährlichen Behandlungen führen können (und damit weitere Kosten verursachen). Das sind ernst zu nehmende Probleme. Doch lassen wir die Kostenfrage einmal beiseite und wenden uns dem Problem falsch positiver Befunde zu.
Weil bestimmte Tests signifikant viele falsch positive Befunde erbringen, sollten wir laut Medizin 2.0 bei den meisten Personen auf diese Tests verzichten. Punkt. Doch aus Sicht von Medizin 3.0 sieht die Sache anders aus: Diese Tests sind potenziell nützlich und fast das Einzige, was wir haben. Was also können wir tun, um sie nützlicher und präziser zu machen?
Alle diagnostischen Tests erfordern ein Abwägen zwischen Sensitivität, also der Fähigkeit des Tests, eine bestehende Krankheit zu erkennen (seine Richtig-positiv-Rate ausgedrückt in Prozent), und Spezifität, also der Fähigkeit zu bestimmen, dass jemand nicht an dieser Krankheit leidet (seine Richtig-negativ-Rate). Gemeinsam geben diese Werte die Gesamtgenauigkeit des Tests an. Zusätzlich müssen wir aber auch die Prävalenz der Krankheit in unserer Zielpopulation bedenken. Wie groß ist die Wahrscheinlichkeit, dass die Person, die wir testen, diese Krankheit tatsächlich hat? Die Sensitivität von Mammografie liegt bei rund 85 Prozent, ihre Spezifität bei leicht über 90 Prozent. Wenn wir aber eine Population mit einem relativ niedrigen Brustkrebsrisiko untersuchen, in der, sagen wir, 1 Prozent der betreffenden Frauen Brustkrebs hat, dann wird auch ein Test mit annehmbarer Sensitivität ziemlich viele falsch positive Befunde ergeben. Tatsächlich liegt der »positive prädiktive Wert« der Mammografie in dieser Niedrigrisikogruppe bei nur etwa 10 Prozent. Das bedeutet: Wenn Ihr Test positiv ausfällt, besteht lediglich eine Wahrscheinlichkeit von 1 zu 10, dass Sie tatsächlich an Brustkrebs erkrankt sind. In anderen Populationen mit höherer Gesamtprävalenz (und größerem Gesamtrisiko) schneidet der Test viel besser ab.
Das Beispiel der Mammografie verdeutlicht, dass wir bei der Auswahl der Personen, die wir testen, sehr strategisch vorgehen und uns ihr Risikoprofil genau anschauen müssen. Zudem müssen wir verstehen, was unser Test uns mitteilen kann und was nicht. Für sich genommen ist kein einziger diagnostischer Test hundertprozentig zuverlässig. Es wäre also dumm, sich auf nur einen Test zu verlassen – und zwar nicht nur bei Brustkrebs, sondern auch in vielen anderen Bereichen. Wir müssen verschiedene Testoptionen miteinander kombinieren – bei Brustkrebs zusätzlich zur Mammografie beispielsweise auch Ultraschall und MRT mit einbeziehen. Auf diese Weise erreichen wir eine bessere Trennschärfe, und es werden weniger überflüssige Eingriffe vorgenommen.
Kurz gesagt sind nicht die Tests an sich das Problem, sondern die Art und Weise, wie wir sie nutzen. Prostatakrebs-Screening ist ein noch besseres Beispiel. Früher hieß es schlicht: »Ihr PSA-Wert ist X oder höher. Darum müssen wir eine Prostatabiopsie vornehmen, was schmerzhaft ist und viele unangenehme Nebenwirkungen haben kann.« Heute beachten wir auch andere Parameter, wie die PSA-Geschwindigkeit (wie schnell sich das PSA im Lauf der Zeit verändert), PSA-Dichte (PSA pro Gewebevolumen, abhängig von der Größe der Prostata) und freies PSA (Vergleich der Menge von PSA, die an Trägerproteine im Blut gebunden ist, mit ungebundenem PSA). Zieht man auch diese Faktoren in Betracht, ist PSA ein viel besserer Indikator für das Prostatakrebsrisiko.
Darüber hinaus gibt es weitere Tests, zum Beispiel einen Bluttest, mit dem man spezifische Proteine aufspürt, die die Aggressivität und potenzielle Gefährlichkeit der Prostatakrebserkrankung eines Patienten besser einschätzen helfen. Die entscheidende Frage lautet: Wird der Patient, so wie viele Männer, mit Prostatakrebs sterben oder an Prostatakrebs? Wenn wir das herausfinden wollen, sollten wir darauf achten, dabei nicht sein Leben zu zerstören und ihm keinen Schaden zuzufügen. Kombiniert man die soeben beschriebenen Bluttests mit multiparametrischer MRT, so ist die Gefahr, eine unnötige Biopsie oder Operation durchzuführen, sehr gering.
Eine ähnliche, aber weniger heftige Kontroverse hat sich um die Früherkennung von Darmkrebs entwickelt, die seit Langem eine Art Initiationsritus für Menschen im mittleren Alter ist.[170] Bei der Koloskopie sucht man nicht nur nach ausgewachsenen Tumoren, sondern auch nach Polypen, wobei es sich um Ausstülpungen der Darmschleimhaut handelt. Die meisten Polypen bleiben klein und harmlos und entwickeln sich nie zu Krebs, aber einige können bösartig werden und in die Darmwand hineinwachsen. Nicht alle Polypen werden zu Krebs, doch Dickdarmkrebs entwickelt sich immer aus Polypen. Darum ist eine Koloskopie so wichtig. Der Arzt kann nicht nur sich potenziell zu Krebs entwickelnde Ausstülpungen entdecken, bevor sie gefährlich werden, sondern auch umgehend eingreifen und mit dem Koloskop Polypen zur weiteren Untersuchung entfernen. So lassen sich Screening und chirurgische Eingriffe in ein und demselben Verfahren durchführen – ein faszinierendes Instrument.
Nach den herkömmlichen Richtlinien werden Screenings zur Früherkennung von Darmkrebs in den USA für Personen mit durchschnittlichem Krebsrisiko im Alter zwischen fünfzig und fünfundsiebzig Jahren empfohlen, in Deutschland gibt es ebenfalls ab fünfzig eine Empfehlung zur Früherkennung. Diese Vorsorgeuntersuchungen werden vom Affordable Care Act vollumfänglich abgedeckt. Wenn keine Polypen entdeckt werden und ein durchschnittliches Krebsrisiko besteht, muss das Verfahren nach allgemeingültigen Richtlinien nur alle zehn Jahre wiederholt werden. Sehr viele Daten sprechen jedoch dafür, dass ein erstes Screening schon vor dem fünfzigsten Geburtstag erfolgen sollte, selbst wenn die Patienten kein überdurchschnittliches Risiko aufweisen (das heißt, wenn in der Familie noch kein Fall von Dickdarmkrebs oder einer entzündlichen Darmerkrankung aufgetreten ist). Etwa 70 Prozent der Personen, bei denen vor dem fünfzigsten Geburtstag eine CRC-Diagnose gestellt wurde, weisen keine diesbezügliche familiäre Vorgeschichte auf oder sind erblich einschlägig belastet.[171] 2020 starben etwa 3640 Amerikaner an Darmkrebs, bevor sie fünfzig wurden – und da die Krankheit langsam fortschreitet, waren von denen, die später starben, vermutlich viele an ihrem fünfzigsten Geburtstag schon erkrankt.[172] Aus diesem Grund aktualisierte die American Cancer Society ihre Richtlinien im Jahr 2018 und senkte das Alter für Personen mit durchschnittlichem Risiko auf fünfundvierzig Jahre.
In meiner Praxis gehen wir noch weiter und empfehlen Patienten mit durchschnittlichem Risiko eine Koloskopie schon im Alter von vierzig Jahren – sogar noch früher, wenn etwas dafür spricht, dass sie einem höheren Risiko ausgesetzt sein könnten. Danach wiederholen wir die Untersuchung alle zwei bis drei Jahre, je nach den Befunden aus der vorhergehenden Koloskopie. Wenn zum Beispiel ein sessiler (flacher) Polyp entdeckt wird, erfolgt die nächste Untersuchung meist eher. Ein Abstand von zwei oder drei Jahren erscheint bei einem solch komplizierten Verfahren vielleicht sehr kurz, doch Dickdarmkrebs kann sich in einem Zeitraum von nur sechs Monaten bis zwei Jahren nach einer normalen Koloskopie entwickeln. Lieber einmal zu viel als einmal zu wenig.[173]
Warum empfehle ich gewöhnlich, eine Koloskopie früher vornehmen zu lassen, als die Richtlinien es vorgeben? Vor allem weil Darmkrebs unter den häufigsten Krebsarten mit am leichtesten zu entdecken ist und man das Risiko demnach besonders wirkungsvoll reduzieren kann. Er gehört nach wie vor zu den fünf tödlichsten Krebsarten in den Vereinigten Staaten, nach Lungenkrebs und danach Brustkrebs/Prostatakrebs bei Frauen/Männern sowie knapp vor Bauchspeicheldrüsen- und Leberkrebs. Von diesen fünf Krebsarten ist aber bei Darmkrebs die Chance am größten, ihn frühzeitig zu entdecken. Da er sich an einem relativ gut zugänglichen Ort, dem Dickdarm, entwickelt, können wir ihn sehen, ohne auf bildgebende Verfahren oder Biopsien zurückgreifen zu müssen. Weil er sich so gut beobachten lässt, ist seine Entwicklung von normalem Gewebe über Polyp zum Tumor so gut erforscht. Ihn früh aufzuspüren macht einen großen Unterschied, weil man Polypen oder Ausstülpungen dann sofort entfernen kann. Wäre das nur auch bei Arterienablagerungen möglich!
Ich denke, dass ein frühes Screening unter dem Strich viel besser ist, als eine zu späte Untersuchung zu riskieren. Bedenken Sie das asymmetrische Risiko: Möglicherweise ist der Verzicht auf frühe und häufige Vorsorgeuntersuchungen die gefährlichste Option.[174]
Zu weiteren Krebsarten, die bei einer visuellen Untersuchung relativ leicht zu erkennen sind, gehören Hautkrebs beziehungsweise Melanome. Auch der Pap-Abstrich zur Diagnose von Gebärmutterhalskrebs ist ein bewährter minimalinvasiver Test; ich empfehle meinen Patientinnen, ihn jährlich vornehmen zu lassen. Krebsarten, die sich in den inneren Organen entwickeln, sind hingegen schwieriger zu entdecken. Da wir sie nicht unmittelbar sehen können, müssen wir auf bildgebende Verfahren wie etwa eine Niedrigdosis-CT zur Entdeckung von Lungenkrebs zurückgreifen. Diese Untersuchungen werden zurzeit (früheren) Rauchern empfohlen, doch wie immer finde ich, dass man sie breitflächiger durchführen sollte, weil Lungenkrebs in etwa 15 Prozent der Fälle bei Personen diagnostiziert wird, die nie geraucht haben. Insgesamt fordert Lungenkrebs die meisten Krebstoten, doch schon an siebter Stelle der Rangliste stehen Todesfälle durch Lungenkrebs bei absoluten Nichtrauchern.
Gegenüber CT-Scans hat die MRT den Vorteil, dass sie keine ionisierende Strahlung erzeugt, aber trotzdem eine gute Auflösung liefert. Ein neueres Verfahren, das noch besser zwischen Krebs und Nichtkrebs unterscheiden kann als MRT-Screening, nennt sich diffusionsgewichtete Bildgebung mit Hintergrundsubtraktion (diffusion-weighted imaging, kurz DWI). Dabei beobachtet man in sehr kurzen Zeitabständen (von meist 10 bis 50 Mikrosekunden) die Bewegung von Wassermolekülen in und um Gewebe. Wird die Bewegung gestoppt oder eingeschränkt, könnte das auf einen dicht gedrängten Zellhaufen, einen Tumor, hindeuten. Je höher die Zelldichte ist, desto heller erscheint das Signal in der DWI-Sequenz der MRT, was die DWI funktional zu einem radiografischen »Geschwulstdetektor« macht. Zurzeit eignet sich die DWI besonders gut für Aufnahmen vom Gehirn, weil es dort am seltensten zu Bewegungsartefakten kommt.
Ich gehe davon aus, dass sich dieses Verfahren durch Optimierung der Software und Standardisierung der Technik mit der Zeit noch verbessern lässt. Doch trotz allem ist selbst die beste diffusionsgewichtete MRT nicht unproblematisch, wenn man sie isoliert verwendet. Die Sensitivität dieser Untersuchung ist zwar sehr hoch (was bedeutet, dass sie sehr gut im Aufspüren von Krebs ist, wenn jemand Krebs hat, und es deshalb sehr wenige falsch negative Befunde gibt), aber die Spezifität ist relativ gering (sie erkennt also nicht sehr gut, wenn jemand keinen Krebs hat, und liefert demzufolge viele falsch positive Befunde). Wieder einmal geht es um den unvermeidlichen Kompromiss zwischen Sensitivität und Spezifität, um Yin und Yang der Diagnose, wenn man so will. Je mehr man sie auf der einen Seite verbessert, desto mehr Defizite hat sie auf der anderen.[175]
Wie ich meinen Patienten erkläre, ist es bei einem Ganzkörper-MRT-Screening sehr gut möglich, dass ein harmloser Schilddrüsenknoten (oder ein anderes Knötchen) aufgespürt wird. Das ist der Preis dafür, dass man einen solch guten Einblick in die Organe erhält. Demzufolge entscheidet sich rund ein Viertel meiner Patienten verständlicherweise gegen ein derartiges Screening. Das bringt mich zum nächsten Instrument im Werkzeugkasten der Krebsfrüherkennung, das in der Lage ist, das Problem der bildgebenden Verfahren mit ihrer hohen Sensitivität und geringen Spezifität wettzumachen.
Ich bin vorsichtig optimistisch, was die Entwicklung sogenannter Flüssigbiopsien betrifft, die das Vorkommen von Krebs mittels Bluttest nachweisen sollen.[176] Dieses sich schnell entwickelnde und faszinierende Verfahren der sogenannten Multi-Krebs-Früherkennung (multicancer early detection, MCED) wird in zwei verschiedenen Situationen eingesetzt – zur Entdeckung von Rezidiven im Anschluss an die Behandlung von Krebspatienten und als Vorsorgeuntersuchung bei ansonsten gesunden Personen.
Max Diehn, einer meiner Kommilitonen an der medizinischen Hochschule und heute Onkologieprofessor in Stanford, beschäftigt sich seit 2012 an vorderster Front mit entsprechenden Forschungen. Zu Beginn wollten Max und seine Kollegen eine scheinbar einfache Frage beantworten: Lässt sich vielleicht bei einem Lungenkrebspatienten, dem ein Tumor operativ entfernt wurde, per Bluttest feststellen, ob der Krebs zurückgekehrt ist?
Früher wurden zu diesem Zweck bildgebende Verfahren wie ein CT verwendet, die einen Tumor »sichtbar« machen. Abgesehen von der Strahlungsbelastung ist das größte Problem dabei die eher schlechte Auflösung. Mit diesen Verfahren lassen sich Tumoren mit einem Durchmesser von weniger als einem Zentimeter nur sehr schlecht erkennen. Selbst wenn man davon ausgeht, dass dieser kleine Knoten die einzige Ansammlung von Krebszellen im Körper des Patienten ist (nicht sehr überzeugend – wenn eine Maus in der Falle sitzt, laufen meistens noch ein paar mehr im Haus herum), sprechen wir nichtsdestoweniger von über einer Milliarde Krebszellen, sobald ein Tumor mit herkömmlichen Screeningverfahren zu erkennen ist. Könnten wir diese Rezidive früher aufspüren, hätten die Patienten eine größere Chance, vom Krebs geheilt zu werden.
Max und seine Kollegen ließen sich etwas ganz Neues einfallen. Weil Krebszellen ständig wachsen, geben sie Zellmaterial, darunter Bruchstücke von Tumor-DNA, in den Blutkreislauf ab. Was wäre, wenn ein Bluttest diese sogenannte zellfreie DNA aufspüren könnte? Von der OP würde man die Gensignatur des Tumors bereits kennen, das heißt, man würde wissen, inwiefern sich die Lungenkrebszellen von normalen Lungenzellen unterscheiden. Es sollte also möglich sein, im Blutplasma eines Patienten nach dieser zellfreien DNA zu suchen und auf diese Weise festzustellen, ob eine Krebserkrankung vorliegt.
Man sollte sich nichts vormachen – das ist nach wie vor eine Suche nach der Nadel im Heuhaufen. Bei Krebs im Frühstadium, den wir mit Flüssigbiopsien in erster Linie aufspüren wollen, reden wir nur von einem etwa 0,01 bis 0,001 Prozent betragenden Anteil der zellfreien DNA im Körper, der tatsächlich von diesem Tumor abstammt (anders gesagt, von einem Zehntausendstel oder Hunderttausendstel). Das ist höchstens von einer Next-Generation-Technologie für Hochdurchsatz-DNA-Screening (high-throughput DNA screening) zu erwarten. Nach Krebsoperationen kommen diese Tests zunehmend zur Anwendung, aber die Technik ist noch nicht sehr ausgereift. Vor allem muss man wissen, wonach man sucht – nach den Mutationsmustern, die Krebs von normalen Zellen unterscheiden.
Einige Wissenschaftler erforschen bereits Möglichkeiten, Bluttests generell zur Krebsfrüherkennung einzusetzen. Das ist um eine Größenordnung komplizierter – man sucht in zehn Heuhaufen nach einer Nadel und weiß nicht einmal, wie die Nadel aussieht. Man kennt keinerlei Mutationsmuster, denn noch ist man ja gar nicht sicher, ob der betreffende Patient überhaupt Krebs hat. Also muss man sich auf die Suche nach anderen potenziellen Markern machen. Ein hierbei federführendes Unternehmen ist Grail, ein Spin-off des Gentechnikunternehmens Illumina. Der von Grail entwickelte Test namens Galleri sucht nach Methylierungsmustern der zellfreien DNA. Dabei handelt es sich im Wesentlichen um chemische Veränderungen der DNA-Moleküle, die auf das Vorkommen von Krebszellen hindeuten. Mittels »very-high-throughput screening« und eines äußerst leistungsstarken KI-Systems ermittelt der Galleri-Test zwei entscheidende Informationen aus einer Blutprobe: Liegt eine Krebserkrankung vor? Und wenn ja, wo? Von welchem Körperteil ist sie höchstwahrscheinlich ausgegangen?
Bei jedem diagnostischen Test gilt es zu entscheiden, wie man ihn kalibrieren soll. Soll mehr Gewicht auf Sensitivität oder auf Spezifität gelegt werden? Galleri ist im Abgleich mit der Datenbank Circulating Cell-free Genome Atlas (CCGA) validiert worden, die Blutproben von über 15 000 Patienten mit und ohne Krebs enthält.[177] In dieser Studie wurde dem Galleri-Test eine sehr hohe Spezifität von rund 99,5 Prozent bescheinigt, was bedeutet, dass nur 0,5 Prozent der Tests einen falsch positiven Befund erbrachten. Wenn der Test zu dem Ergebnis kommt, dass irgendwo in Ihrem Körper Krebszellen stecken, dann ist das wahrscheinlich wirklich der Fall. Die Sensitivität kann allerdings je nach Krebsstadium gering sein. (Das heißt, selbst wenn Sie laut Test keinen Krebs haben, sind Sie nicht unbedingt auf der sicheren Seite.)
Hier ist jedoch Folgendes zu bedenken: Dieser Test hat eine viel höhere Auflösung als radiografische Tests wie die MRT oder Mammografie. Diese auf Bildgebung basierenden Untersuchungen müssen den Tumor »sehen«, was erst möglich ist, wenn er eine gewisse Größe erreicht hat. Der Galleri-Test untersucht zellfreie DNA, die von Tumoren beliebiger Größe stammen kann – auch von denen, die den Bildgebungsverfahren verborgen bleiben.
Die CCGA-Studie erbrachte schon früh, dass die Erkennbarkeit von Krebs nicht nur vom Krebsstadium abhängt, was zu erwarten wäre (je weiter sich der Tumor entwickelt hat, desto größer ist die Wahrscheinlichkeit, im Blut zellfreie DNA zu finden), sondern auch vom Subtyp eines Tumors. So liegt die Entdeckungsrate von Hormonrezeptor-positivem Brustkrebs im Stadium I/II bei etwa 25 Prozent, während sie bei Hormonrezeptor-negativem Brustkrebs im Stadium I/II etwa 75 Prozent beträgt. Was sagt uns dieser Unterschied? Wir wissen, dass Brustkrebs keine einheitliche Krankheit ist und dass Hormonrezeptor-negative Tumoren tödlicher sind als Hormonrezeptor-positive. Demzufolge erweist sich der Test beim Entdecken des tödlicheren Subtyps von Brustkrebs als zuverlässiger.
Flüssigbiopsien haben gewissermaßen zwei Funktionen: Zum einen sollen sie feststellen, ob Krebs vorliegt oder nicht – eine Ja-Nein-Frage; zum anderen, und das ist vielleicht noch wichtiger, sollen sie uns Einblick in die Biologie des jeweiligen Krebses vermitteln. Wie gefährlich wird er wahrscheinlich sein? Zudem scheinen die Krebsarten, die mehr zellfreie DNA abgeben, aggressiver und todbringender zu sein und sind somit diejenigen, die wir so schnell wie möglich entdecken und behandeln wollen. Auch wenn diese Technologie noch in den Kinderschuhen steckt, bin ich zuversichtlich, dass wir mit der Kombination verschiedener diagnostischer Tests, von radiografischen Untersuchungen (etwa MRT) über visuelle Untersuchungen (etwa Koloskopie) bis hin zu biologisch-genetischen Tests (etwa Flüssigbiopsie), den Krebs, der am dringlichsten behandelt werden muss, korrekt identifizieren und dabei zu möglichst wenigen falsch positiven Ergebnissen kommen.
Ich glaube, dass dies bahnbrechende Folgen haben wird. Wenn Flüssigbiopsien halten, was sie versprechen, könnten wir bei einer Krebserkrankung routinemäßig bereits so früh eingreifen, dass wir die Chance haben, den Krebs zu kontrollieren oder sogar zu eliminieren – ganz anders als heute, wo die Behandlung normalerweise erst in einem späten Stadium beginnt und die Chancen für den Patienten bereits so schlecht stehen, dass wir auf ein Wunder hoffen müssen.
Von den vier apokalyptischen Reitern des Alterns kann man dem Krebs wohl am schlechtesten vorbeugen. Vermutlich ist er auch derjenige, bei dem unglückliche Umstände verschiedener Art die größte Rolle spielen, etwa in der Form gehäufter somatischer Mutationen. Die einzigen beeinflussbaren Risiken, die aus den Daten herausstechen, sind Rauchen, Insulinresistenz und Fettleibigkeit, was sich allesamt vermeiden lässt – und möglicherweise Umweltverschmutzung (von Luft, Wasser und so weiter), wobei die Daten hier nicht so eindeutig sind.
Allerdings verfügen wir bei Krebs über einige Behandlungsoptionen – im Gegensatz zur Alzheimer-Krankheit (wie wir im nächsten Kapitel sehen werden). Insbesondere die Immuntherapie ist Erfolg versprechend. Dennoch sind unsere Behandlungs- und Präventionsstrategien viel weniger effektiv als die Instrumente, die uns zur Bekämpfung von Herz-Kreislauf-Krankheiten und dem Spektrum der Stoffwechselstörungen von Insulinresistenz bis Typ-2-Diabetes zur Verfügung stehen.
Bis wir lernen, Krebs vorzubeugen oder ihn vollständig zu »heilen«, was ohne höchst außergewöhnliche Durchbrüche zu unserer Lebenszeit wohl nicht gelingen wird, müssen wir sehr viel mehr Energie auf die Früherkennung von Krebs verwenden, damit man spezifische Krebserkrankungen mit spezifischen Behandlungen besser ins Visier nehmen kann, während sie besonders gut zu bekämpfen sind. Die erste Regel lautet: »Bekomme keinen Krebs«, die zweite: »Entdecke ihn so früh wie möglich.«
Darum trete ich so vehement für frühes Screening ein. Es ist nun einmal so, dass kleinere Tumoren mit weniger Mutationen viel besser zu behandeln sind. Und die einzige Möglichkeit, sie früh aufzuspüren, ist aggressives Screening.
Da dies erhebliche Kosten verursacht, übt Medizin 2.0 in dieser Hinsicht eher Zurückhaltung. Natürlich entstehen finanzielle Kosten, aber die emotionalen sind auch zu berücksichtigen – vor allem, wenn Tests falsch positive Befunde liefern. Und es gibt Nebenrisiken, wie etwa das geringe Verletzungsrisiko bei einer Koloskopie oder das signifikantere Risiko einer unnötigen Biopsie. Diese drei Kostenarten sind gegen die Kosten durch das Übersehen oder zu späte Entdecken einer Krebserkrankung abzuwägen.
Niemand hat gesagt, dies sei ein Kinderspiel. Wir haben noch einen langen Weg vor uns. Doch endlich gibt es Hoffnung an mehreren Fronten – viel mehr als damals zur Zeit meiner Ausbildung zum Krebschirurgen. Mehr als fünfzig Jahre nachdem der War on Cancer ausgerufen wurde, zeichnet sich endlich ein Weg in eine Welt ab, in der eine Krebsdiagnose das frühe Aufspüren eines behandelbaren Problems bedeutet und nicht mehr die späte Entdeckung einer höchst bedrohlichen Krankheit. Dank besserer Screenings und wirkungsvollerer Behandlungen wie Immuntherapie könnte Krebs eines Tages eine beherrschbare Erkrankung sein und sogar seinen Status als apokalyptischer Reiter des Alterns verlieren.
Kapitel 9
Die Jagd nach Erinnerungen
Alzheimer und andere neurodegenerative Erkrankungen
Das größte Hindernis für Entdeckungen ist nicht Ignoranz – es ist die Illusion von Wissen.
Daniel J. Boorstin
Die meisten Leute gehen zum Arzt, wenn sie krank sind oder wenn sie befürchten, krank zu sein. Fast alle meine Patienten kommen zu mir, wenn sie mehr oder weniger gesund sind oder sich dafür halten. Das war auch bei Stephanie der Fall, die Anfang 2018 mit vierzig Jahren zum ersten Mal mein Sprechzimmer betrat. Sie hatte kein ernstes Anliegen, sondern »interessierte sich« einfach nur für das Thema Langlebigkeit.
Ihre Familiengeschichte war unspektakulär. Von ihren vier Großelternteilen waren drei mit Ende siebzig oder Anfang achtzig an den Folgen von Atherosklerose gestorben und der vierte an Krebs. Nichts Besonderes für Angehörige der »Greatest Generation«[178]. Das einzige Warnsignal war, dass ihre Mutter, die mit siebzig Jahren ansonsten noch fit war, neuerdings an leichten Erinnerungslücken litt, was Stephanie ihrem »fortgeschrittenen Alter« zuschrieb.
Wir machten für die nächste Woche einen weiteren Termin aus, um ihr Blutbild zu besprechen. Weil ich größten Wert auf die Analyse von Biomarkern lege, führten wir eine umfassende Reihe von Tests durch. Wenn die Ergebnisse einer Blutuntersuchung von neuen Patienten vorliegen, überprüfe ich einige Dinge sofort. Dazu gehört der Spiegel von Lp(a), dem so gefährlichen Lipoprotein, über das wir bereits in Kapitel 7 gesprochen haben, sowie der ApoB-Wert. Drittens schaue ich immer nach dem ApoE-Genotyp. ApoE ist das in Kapitel 4 erwähnte Gen, das mit dem Risiko einhergeht, an Alzheimer zu erkranken.
Aus Stephanies Laborwerten ging hervor, dass sie das ε4-Allel von ApoE besaß, das mit einem größeren Alzheimer-Risiko assoziiert ist – und zwar nicht nur eine Kopie, sondern gleich zwei (ε4/ε4). Das bedeutete, dass ihr Risiko, an Alzheimer zu erkranken, bis zu zwölfmal größer war als bei jemandem, der zwei Kopien des üblichen ε3-Allels besitzt. Die ε2-Variante von ApoE scheint ihre Träger vor der Alzheimerkrankheit zu schützen: Sie bedeutet ein um 10 Prozent geringeres Risiko für Personen mit ε2/ε3 und ein um 20 Prozent geringeres bei ε2/ε2.[179] Stephanie hatte Pech gehabt.
Sie war erst der vierte Patient, bei dem ich diesen sehr ungewöhnlichen Genotyp, den nur etwa 2 bis 3 Prozent der Bevölkerung aufweisen, festgestellt hatte. Und sie hatte keine Ahnung von der Gefahr, in der sie schwebte – obwohl man rückblickend sagen kann, dass die Vergesslichkeit ihrer Mutter ein Symptom ihrer beginnenden Alzheimer-Erkrankung war. Nun stand ich vor einer zweifachen Herausforderung: Ich musste ihr die Nachricht unmissverständlich, aber schonend beibringen und ihr, noch schwieriger, erklären, was sie zu bedeuten hatte und was nicht.
Unter solchen Umständen halte ich es gemeinhin für das Beste, gleich zur Sache zu kommen. Nachdem wir uns gesetzt hatten, sagte ich also ungefähr Folgendes: »Stephanie, wir haben in Ihrem Blutbild etwas entdeckt, was mir ein wenig Sorgen bereitet – nicht weil zum jetzigen Zeitpunkt etwas nicht in Ordnung ist, sondern weil es in zwanzig oder dreißig Jahren Probleme bereiten könnte. Sie weisen eine Genkombination auf, die das Risiko erhöht, dass Sie an Alzheimer erkranken. Wichtig ist aber auch zu verstehen, dass wir hier lediglich über einen Risikomarker und nicht über eine feststehende Tatsache reden. Ich bin überzeugt, dass wir dieses Risiko gemeinsam verringern können.«
Stephanie war am Boden zerstört. Sie befand sich ohnehin in einer sehr belastenden Situation – Scheidung, schwierige Arbeitsbedingungen und nun auch noch diese Nachricht. Es ist hart, Details über Gene und Risiken zu erläutern, wenn dich dein Gegenüber mit angsterfüllten Augen ansieht und nur denken kann: »Ich bin verloren.« Wir brauchten mehrere Wochen mit Gesprächen, bevor Stephanie auch den Rest der Botschaft aufnehmen konnte, der lautete, dass sie durchaus noch nicht verloren war.
Von den apokalyptischen Reitern des Alterns ist die Alzheimerkrankheit vielleicht die komplizierteste und therapieresistenteste. Wir wissen viel weniger darüber, wie und warum sie sich entwickelt und wie sie zu verlangsamen oder zu verhindern ist, als bei Atherosklerose. Anders als bei Krebs gibt es derzeit keine Möglichkeit, sie zu behandeln, sobald sich die ersten Symptome zeigen. Und im Gegensatz zu Typ-2-Diabetes und Stoffwechselstörungen scheint sie nicht ohne Weiteres reversibel zu sein (obwohl zu diesem Aspekt das letzte Wort noch nicht gesprochen ist). Aus diesem Grund fürchten meine Patienten Demenz fast ausnahmslos mehr als jede andere Folge des Alterns, den Tod eingeschlossen. Sie würden lieber an Krebs oder einer Herz-Kreislauf-Erkrankung sterben, als den Verstand, und damit sich selbst, zu verlieren.
Alzheimer ist die am weitesten verbreitete neurodegenerative Erkrankung, aber auch andere bereiten uns Sorgen. Am häufigsten von diesen sind die Lewy-Körper-Demenz (auch Lewy-Körperchen- oder Lewy-Body-Demenz) und die Parkinson-Krankheit, die eigentlich verschiedene Formen einer verwandten Erkrankung sind, die man mitunter (verwirrenderweise) als »Demenz mit Lewy-Körpern« bezeichnet. Der wichtigste Unterschied besteht darin, dass bei Lewy-Körper-Demenz in erster Linie kognitive Fähigkeiten beeinträchtigt sind, während es sich bei Parkinson in erster Linie (wenn auch nicht nur) um eine Bewegungsstörung handelt, wobei aber auch kognitive Defizite auftreten können. In den Vereinigten Staaten leiden etwa sechs Millionen Menschen an Alzheimer, etwa 1,4 Millionen an Lewy-Körper-Demenz und eine Million an Parkinson, der am schnellsten um sich greifenden neurodegenerativen Krankheit. Daneben gibt es eine Vielzahl seltenerer, aber ebenfalls schwerwiegender neurodegenerativer Erkrankungen, wie amyotrophe Lateralsklerose (ALS oder Lou-Gehrig-Syndrom) und Chorea Huntington.
Alle diese Krankheiten resultieren aus einer Degeneration der Nervenzellen, und bislang lassen sie sich noch nicht heilen – trotz der Abermilliarden an Dollar, die bereits zur Bekämpfung dieser komplexen Leiden aufgewendet wurden. Vielleicht wird es in naher Zukunft einen Durchbruch geben, doch momentan können wir bestenfalls versuchen, ihnen vorzubeugen. Eine einzige gute Nachricht gibt es allerdings. Während man früher davon ausgegangen ist, dass diese Erkrankungen völlig eigenständig und voneinander unabhängig sind, spricht immer mehr dafür, dass zwischen ihnen doch ein größerer Zusammenhang besteht. Das bedeutet auch, dass sich einige präventive Strategien für mehrere von ihnen eignen würden.
Viele Ärzte schrecken davor zurück, einen Gentest auf ApoE durchzuführen. Nach herkömmlicher Meinung sei es alles andere als sicher, dass jemand mit dem riskanten ε4-Allel tatsächlich an Alzheimer erkrankt, und außerdem könne man eh nichts für ihn tun. Warum also sollte man den Patienten mit diesem schrecklichen Wissen belasten?
Weil es zweierlei schlechte Nachrichten gibt: zum einen über Dinge, die wir ändern können, und zum anderen über Dinge, die wir nicht ändern können. Und anzunehmen, dass man für Träger des ε4-Allels nichts tun könne, ist in meinen Augen verkehrt. Es stimmt zwar, dass über die Hälfte der Personen mit Demenz infolge einer Alzheimer-Erkrankung mindestens eine Kopie des ε4-Allels trägt, aber dieses Risiko-Gen zu besitzen ist keine Garantie dafür, die Diagnose »Demenz infolge einer Alzheimer-Erkrankung« zu erhalten. Es gibt hundertjährige ε4/ε4-Träger ohne jedes Anzeichen für Demenz. Das liegt wahrscheinlich daran, dass sie auch Gene besitzen, die sie vor ε4 schützen – zum Beispiel scheint eine spezielle Variante des Gens Klotho (KL), kl-vs, ihre Träger vor Demenz zu bewahren.[180] Dagegen erkranken zahlreiche Träger der »normalen« Allele ε3/ε3 trotzdem an Alzheimer. Die ε4-Genvariante zu besitzen bedeutet lediglich ein erhöhtes Risiko. Nicht mehr und nicht weniger.
Was ich Stephanie außerdem klarzumachen versuchte, war: Die Zeit arbeitete für sie. Vor dem fünfundsechzigsten Geburtstag erreicht die Krankheit selten ein klinisches Stadium, auch nicht bei Patienten mit zwei Kopien von ε4. Somit hatten wir rund fünfundzwanzig Jahre Zeit zu versuchen, mit den derzeit verfügbaren Mitteln den Ausbruch dieser schrecklichen Krankheit abzuwenden oder hinauszuzögern. Bis dahin würde es der Forschung hoffentlich gelingen, wirksamere Behandlungen zu entwickeln. Es war eine klassische asymmetrische Situation, in der Nichtstun letztlich das größte Risiko bedeutete.
Was genau ist die Alzheimerkrankheit?
Obwohl die Alzheimerkrankheit erst Anfang des 20. Jahrhunderts beschrieben und benannt wurde, erwähnten bereits die Menschen der Antike das Phänomen der »Senilität«. Platon war der Ansicht, dass ältere Männer für Führungspositionen, die Scharfsinn oder Urteilsvermögen fordern, ungeeignet sein könnten, da zunehmendes Alter anscheinend alle Arten von Vergesslichkeit wie auch Dummheit hervorbringe. In King Lear schuf William Shakespeare das unvergessliche Porträt eines alten Mannes, der gegen die fortschreitende Umnachtung seines Geistes ankämpft.
Dass es sich um eine Krankheit handeln könnte, wurde erstmals von dem Psychiater und Neuroanatom Alois Alzheimer zur Sprache gebracht. Zunächst arbeitete er als Assistenzarzt in der Städtischen Anstalt für Irre und Epileptische in Frankfurt am Main und später als Privatdozent und Oberarzt in München. Dort untersuchte er 1906 das Gehirn der zuvor verstorbenen Auguste Deter, einer Frau Mitte fünfzig, die in ihren letzten Lebensjahren an Gedächtnisschwund, Wahnvorstellungen, Aggressivität und Verwirrung gelitten hatte. Alzheimer stellte fest, dass mit ihrem Gehirn eindeutig etwas nicht stimmte. Bündel aus verknäulten und verdickten Nervenfasern hatten die Nervenzellen teilweise zerstört, und dazwischen hatte sich eine merkwürdige Substanz abgelagert. Das seltsame Erscheinungsbild der Nervenzellen verblüffte ihn so sehr, dass er Zeichnungen davon anfertigte.
Ein Kollege von ihm prägte später die Bezeichnung »Alzheimerkrankheit«, doch nach Alzheimers Tod (er starb 1915 mit einundfünfzig Jahren nach einer Infektion) geriet die von ihm entdeckte Krankheit für fünfzig Jahre mehr oder weniger in Vergessenheit – genau wie andere, weniger verbreitete neurologische Erkrankungen wie Chorea Huntington, Parkinson und die Lewy-Körper-Demenz. Patienten mit Symptomen, die wir heute mit diesen Krankheiten verbinden, wie Stimmungswechsel, Depressionen, Gedächtnisschwund, Reizbarkeit und Irrationalität, wurden, so wie Auguste Deter, routinemäßig in eine Anstalt eingewiesen. Man betrachtete die »Alterssenilität« nach wie vor als unvermeidbare Begleiterscheinung des Alterns, so wie es schon zu Platons Zeiten gewesen war.
Erst Ende der 1960er-Jahre erkannten Wissenschaftler zunehmend an, dass »senile Demenz« nicht bloß eine normale Alterserscheinung, sondern eine Erkrankung war. Die drei britischen Psychiater Garry Blessed, Bernard Tomlinson und Martin Roth untersuchten die Gehirne von siebzig verstorbenen Patienten mit Demenz und fanden heraus, dass sie die gleichen Plaques und Faserbündel aufwiesen, wie sie Alois Alzheimer beobachtet hatte. Laut weiteren Studien schien eine Korrelation zwischen dem Grad der kognitiven Beeinträchtigung eines Patienten und der Menge der in seinem Gehirn vorgefundenen Plaques zu bestehen. Die drei Psychiater kamen zu dem Schluss, dass die Betroffenen ebenfalls an der Alzheimerkrankheit gelitten hatten. Ein gutes Jahrzehnt später, Anfang der 1980er-Jahre, identifizierten andere Forscher die Substanz in den Plaques als das Peptid Beta-Amyloid. Unter den möglichen Ursachen der Alzheimerkrankheit galt es sofort als Hauptverdächtiger, weil es häufig am Tatort vorgefunden wird.
Beta-Amyloid entsteht als Nebenprodukt, wenn das natürlicherweise vorkommende Amyloid-Vorläufer-Protein, oder Amyloid-Precursor-Protein (APP), in drei Teile aufgespalten wird. APP ist ein Membranprotein, das die Membran von Nervenzellen durchspannt und normalerweise in zwei Teile zerschnitten wird. Erfolgt jedoch eine Dreiteilung, bewirkt dies die »Fehlfaltung« eines der dabei entstehenden Fragmente, was heißt, dass dieses seine normale Struktur (und somit seine Funktion) einbüßt und »klebrig« wird, sodass es leicht Klumpen bildet – Beta-Amyloid, ein wirklich übles Zeug. Labormäuse, die gentechnisch so modifiziert werden, dass sich in ihren Nervenzellen Beta-Amyloid ablagert (was normalerweise nicht passiert), haben Probleme bei sonst leichten kognitiven Aufgaben, etwa beim Finden von Futter in einem einfachen Labyrinth. Zugleich löst Amyloid die Anhäufung sogenannter Tau-Proteine aus, die ihrerseits letztlich zur Gehirnschrumpfung führt. Aus Tau-Proteinen bestanden vermutlich die »Faserbündel«, die Alois Alzheimer in Auguste Deters Gehirn entdeckt hatte.
Wissenschaftler haben einige Genmutationen identifiziert, die eine sehr rasche Anhäufung von Beta-Amyloid fördern und alle so gut wie sicher bewirken, dass ihre Träger die Krankheit, oft schon in recht jungen Jahren, entwickeln. Diese Mutationen – die häufigsten treten in den Genen APP, PSEN1 und PSEN2 auf – beeinflussen typischerweise die Aufspaltung von APP. In Familien mit diesen Genmutationen kommt es gehäuft zu Alzheimer-Erkrankungen, die oft schon sehr früh, in den Dreißigern oder Vierzigern, ausbrechen. Glücklicherweise sind die Mutationen ausgesprochen selten, aber sie sind in 10 Prozent der früh einsetzenden Alzheimerfälle (oder in etwa 1 Prozent der gesamten Fälle) zu beobachten.[181] Auch Menschen mit Downsyndrom neigen zur großflächigen Anhäufung von Amyloid-Plaques, weil sich die betreffenden Gene auf Chromosom 21 befinden.
Aufgrund der verfügbaren Indizien war es keine gewagte Schlussfolgerung, dass diese Ablagerung von Beta-Amyloid im Gehirn die Alzheimerkrankheit unmittelbar verursacht. Seit den 1980er-Jahren ist die sogenannte Amyloid-Hypothese die führende Theorie der Alzheimer-Forschung, die die wissenschaftlichen Prioritäten der National Institutes of Health und der Pharmaindustrie gleichermaßen bestimmt hat. Man hat sich gedacht, wenn man das Amyloid beseitigen könnte, könne man auch das Fortschreiten der Krankheit zum Stillstand bringen oder sogar umkehren. Das hat jedoch nicht funktioniert. Dutzende Medikamente wurden entwickelt, die Beta-Amyloid auf die eine oder andere Weise angreifen. Doch selbst wenn das Amyloid dadurch verschwindet oder seine Produktion verlangsamt wird, gelingt es diesen Medikamenten nicht, die kognitiven Funktionen der Patienten zu verbessern oder das Fortschreiten der Krankheit einzudämmen. Das hat bisher kein einziges von ihnen geschafft.[182]
Beim Suchen nach einer Erklärung kam die Hypothese auf, dass den Patienten die Medikamente zu spät verabreicht wurden, also zu einem Zeitpunkt, an dem die Krankheit sich bereits festgesetzt hatte. Man weiß, dass sich Alzheimer langsam, über Jahrzehnte hinweg, entwickelt. Was wäre, wenn man früher mit dem Verabreichen der Medikamente beginnen würde? Diese vielversprechende Hypothese testete man in großen und viel veröffentlichten klinischen Studien an Personen mit einer erblichen Mutation, die sie für eine früh einsetzende Alzheimer-Erkrankung anfällig machte, aber auch das blieb ohne Erfolg. 2022 starteten Roche und Genentech eine breit angelegte Studie, bei der die frühe Verabreichung eines Anti-Amyloid-Präparats an Personen getestet wird, die weder Genmutationen besitzen noch eindeutige Symptome einer Demenz zeigen, in deren Gehirn aber Amyloid-Ablagerungen nachgewiesen wurden; Ergebnisse werden für das Jahr 2026 erwartet. Einige Forscher vermuten, dass sich der Krankheitsprozess möglicherweise umkehren lässt, wenn zwar schon Amyloidablagerungen, aber noch keine geschädigten Tau-Proteine existieren, was immer erst später passiert. Diese Theorie wird in einer weiteren noch nicht abgeschlossenen Studie untersucht.
Im Juni 2021 erteilte die FDA die Zulassung für ein Medikament mit dem Wirkstoff Aducanumab, das Beta-Amyloid angreift. Der Hersteller Biogen hatte zuvor zweimal Daten zur Zulassung vorgelegt und eine Absage erhalten. Erst beim dritten Anlauf klappte es. Der beratende Ausschuss der Behörde sprach sich auch dieses Mal dagegen aus, das Medikament zuzulassen, weil sein Nutzen nicht eindeutig belegt oder umstritten sei, doch die FDA genehmigte es trotzdem. Die Reaktion des Arzneimittelmarktes fiel verhalten aus, weil sich Medicare und einige Versicherungen weigerten, die jährlichen Kosten von 28 000 Dollar zu zahlen, solange das Medikament nicht in einer klinischen Studie an einer Universität erprobt worden sei.
Diese fortgesetzten Misserfolge bei der Suche nach Arzneimitteln gegen Alzheimer sorgten für Frustration und Verwirrung, weil seit Langem davon ausgegangen wird, dass Beta-Amyloid einen maßgeblichen Anteil an der Krankheit hat. So ließ Dr. Ronald Petersen, Direktor des Alzheimer’s Disease Research Center der Mayo Clinic, die New York Times 2020 wissen: »Amyloid und Tau bestimmen die Erkrankung. … Nichts gegen Amyloid zu unternehmen macht keinen Sinn.«[183]
Manche Wissenschaftler stellen jedoch immer öfter infrage, dass Beta-Amyloid für alle Alzheimer-Fälle verantwortlich ist, und führen in diesem Zusammenhang insbesondere die gescheiterten Versuche mit den Medikamenten an. Ihre Skepsis schien sich im Juli 2022 zu bestätigen, als Science einen Artikel veröffentlichte, der eine häufig zitierte Studie von 2006 in Zweifel zog. Diese Studie hatte der Amyloid-Theorie neuen Auftrieb gegeben, als ihr Stern bereits zu sinken schien. Sie hatte den Fokus auf einen speziellen Amyloid-Subtyp gelegt, der die Degeneration von Nervenzellen angeblich unmittelbar verursachte, was wiederum zahlreiche Untersuchungen über diesen Subtyp angestoßen hatte. Doch laut dem Artikel in Science waren in dieser Studie wesentliche Bilder gefälscht worden.
Es gab bereits eine Menge anderer Belege dafür, die bezweifeln ließen, dass tatsächlich eine kausale Beziehung zwischen Amyloid und Neurodegeneration existiert, wie man lange Zeit angenommen hatte. Bei Autopsien stellte sich heraus, dass mehr als 25 Prozent von kognitiv unauffälligen Personen zum Zeitpunkt ihres Todes großflächige Amyloidablagerungen im Gehirn aufwiesen – bei einigen war die Plaquebildung sogar genauso umfangreich wie bei Patienten, die mit schwerer Demenz gestorben waren. Aus irgendeinem Grund hatten die Personen jedoch keine kognitiven Beeinträchtigungen davongetragen. Das war im Grunde nichts Neues. Schon 1968 erwähnten Blessed, Tomlinson und Roth Beobachtungen anderer Forscher von »Bildungen von Plaques und weiteren Veränderungen, [die] bei normalen Personen mitunter ebenso stark ausgeprägt waren wie bei Fällen seniler Demenz«.[184]
Einige Experten behaupten, dass diese Patienten tatsächlich an der Krankheit litten, aber ihre Symptome langsamer in Erscheinung getreten seien oder sie ihre Hirnschädigung auf irgendeine Weise verborgen oder kompensiert hätten. Neuere Studien haben jedoch erbracht, dass auch der umgekehrte Fall möglich ist: Das Gehirn mancher Patienten mit allen Symptomen der Alzheimerkrankheit, einschließlich signifikanter kognitiver Beeinträchtigungen, weist nur wenige oder gar keine Ablagerungen von Amyloid auf, wie zwei gebräuchliche Diagnoseverfahren, die Amyloid-PET-Untersuchung und/oder die Untersuchung von Biomarkern im Liquor (Gehirn-Rückenmark-Flüssigkeit), zeigen konnten. Forscher des Memory and Aging Center der University of California San Francisco stellten mittels PET-Scans fest, dass es bei fast einem Drittel von Patienten mit milder bis mäßiger Demenz keine Anzeichen von Amyloid im Gehirn gab.[185] Andere Studien entdeckten eine nur schwache Korrelation zwischen der Menge an Amyloidablagerungen und der Schwere der Erkrankung. Es hat also den Anschein, als sei das Vorhandensein von Beta-Amyloid-Plaques weder notwendig für die Entwicklung der Alzheimerkrankheit noch hinreichend, um sie hervorzurufen.
Damit ergibt sich eine weitere Möglichkeit: Die 1906 von Alois Alzheimer beobachtete Erkrankung war nicht die gleiche wie die Alzheimerkrankheit, die weltweit Millionen Menschen heimsucht. Einen wichtigen Hinweis gibt uns das Alter beim Ausbruch der Erkrankung. Was wir als Alzheimerkrankheit bezeichnen (oder auch als Spätform der Alzheimerkrankheit oder late-onset Alzheimer’s disease), ist erst ab einem Alter von fünfundsechzig Jahren signifikant häufig zu beobachten. Auguste Deter, Dr. Alzheimers »Patient Zero«, zeigte jedoch schon mit fünfzig schwere Symptome, was eher zum Verlauf der Frühform der Alzheimerkrankheit (early-onset Alzheimer’s disease) passt als zu der Demenz, die Personen mit Ende sechzig, siebzig oder achtzig schleichend befällt. Eine 2013 vorgenommene Analyse von Auguste Deters Hirngewebe erbrachte, dass sie tatsächlich Trägerin der PSEN1-Mutation war, welche sich typischerweise bei früh an Demenz Erkrankten findet.[186] (Wie gesagt, spielt sie eine Rolle bei derjenigen Aufspaltung des Amyloid-Precursor-Proteins, die Beta-Amyloid erzeugt.) Auguste Deter litt tatsächlich an Alzheimer, aber an einer Form, an der man nur erkrankt, wenn man Träger eines dieser mutierten Gene ist. Wir sind vielleicht fälschlich davon ausgegangen, dass die übrigen 99 Prozent von Alzheimer-Fällen den gleichen Verlauf nehmen wie bei ihr.
So etwas ist in der Medizin keineswegs ungewöhnlich – der Indexfall erweist sich als Ausnahme von der Regel. Wenn man von diesem Fall auf alle anderen schließt, kann das eine Kette von Problemen und Missverständnissen nach sich ziehen. Wäre Auguste Deter andererseits erst mit fünfundsiebzig Jahren erkrankt, so hätte dem möglichwerweise niemand Beachtung geschenkt.
So wie die Alzheimerkrankheit (zu Recht oder Unrecht) über die Anhäufung von Beta-Amyloid und Tau-Proteinen definiert wird, werden Lewy-Körper-Demenz und die Parkinsonkrankheit mit der Anhäufung des neurotoxischen Proteins Alpha-Synuclein in Verbindung gebracht, das sich in Aggregaten, den sogenannten Lewy-Körpern, bildet (welche erstmals von Friedrich Lewy, einem Kollegen Alois Alzheimers, beobachtet wurden). Die ε4-Variante von ApoE erhöht nicht nur das Risiko, an Alzheimer zu erkranken, sondern steigert auch signifikant das Risiko für Lewy-Körper-Demenz sowie Parkinson mit Demenz, was die Annahme bestätigt, dass diese Erkrankungen in gewisser Hinsicht verwandt sind.[187]
All dies versetzt Patienten wie Stephanie in eine schreckliche Lage: Sie bekommen mit erhöhter Wahrscheinlichkeit eine Krankheit, deren Ursachen noch nicht vollständig erforscht sind und für die es keine wirksamen Behandlungen gibt. Das bedeutet, dass wir uns verstärkt einem Thema widmen müssen, das im Zusammenhang mit neurodegenerativen Erkrankungen bis vor Kurzem noch als tabu galt: der Prävention.
Kann man neurodegenerativen Erkrankungen vorbeugen?
Stephanie war außer sich vor Entsetzen. Ich hatte schon vorher Patienten mit zwei Kopien des ε4-Gens gehabt, aber von ihnen hatte niemand so panisch reagiert. Wir benötigten zwei Monate mit vier langen Gesprächen, bis Stephanie den ersten Schock überwunden hatte. Danach war es an der Zeit zu besprechen, was zu tun war.
Bisher gab es keine offensichtlichen Anzeichen von kognitiven Beeinträchtigungen oder Gedächtnisverlust. Noch nicht. Nebenbei bemerkt: Einige meiner Patienten flippen schon aus, wenn sie mal den Autoschlüssel oder ihr Handy nicht finden können. Dann muss ich ihnen immer wieder erklären, dass sie deswegen nicht gleich an Alzheimer leiden. Meistens waren sie einfach nur gestresst oder abgelenkt (woran ironischerweise oft genau das verlegte Handy schuld ist). Bei Stephanie war es anders. Ihr Risiko war real, und das wusste sie jetzt.
Bei der Behandlung von Hochrisikopatienten wie Stephanie arbeitete ich zu jener Zeit gewöhnlich mit Dr. Richard Isaacson zusammen, der 2013 die erste Klinik für Alzheimer-Prävention in den USA gegründet hatte. Wie sich Richard erinnert, war die Dekanin des Weill Cornell Medical College bei ihrem ersten Gespräch, in dem er ihr von seinem Vorhaben erzählte, entgeistert über dieses damals revolutionäre Ansinnen – man ging nicht davon aus, dass man der Alzheimerkrankheit vorbeugen konnte. Außerdem sah Richard mit seinen knapp dreißig Jahren nicht unbedingt glaubwürdig aus. »Sie hatte jemanden wie Oliver Sacks erwartet«, erzählte er mir. »Stattdessen saß ihr nun Doogie Howser[188] gegenüber.«[189]
Isaacson war mit siebzehn aufs College gegangen, um an der University of Missouri in Kansas City einen kombinierten Studiengang mit Bachelor-Abschluss und Medizinstudium zu absolvieren. Mit dreiundzwanzig Jahren hatte er sein Medizinexamen in der Tasche. Er wollte so viel wie möglich über die Alzheimerkrankheit in Erfahrung bringen, weil er befürchtete, dass seine Familie eine erbliche Veranlagung dafür hatte.
Richard wuchs in Commack auf Long Island auf. Damals hatte er miterlebt, wie sein geliebter Großonkel Bob der Krankheit erlag. Als Richard drei war, hatte Onkel Bob ihn bei einer Familienfeier vor dem Ertrinken in einem Swimmingpool gerettet. Doch bereits ein gutes Jahrzehnt später begann sich der geliebte Onkel zu verändern. Er erzählte immer dasselbe. Er war nicht mehr so lustig. Er starrte oft ins Leere und brauchte länger, um zu verarbeiten, was um ihn herum passierte. Schließlich wurde bei ihm Alzheimer diagnostiziert – aber da war er geistig schon nicht mehr anwesend. Es war, als sei er verschwunden.
Richard ertrug es nicht, mit anzusehen, wie sein lieber Onkel zugrunde ging. Außerdem machte er sich Sorgen, weil er wusste, dass es eine genetisch bedingte Anfälligkeit für die Alzheimerkrankheit gibt. War er auch in Gefahr? Oder seine Eltern? Ließ sich der Ausbruch der Krankheit irgendwie verhindern?
Als er an der University of Miami eine Stelle als Arzt annahm, sammelte er alle möglichen Berichte über Studien und Empfehlungen, die Möglichkeiten aufzeigten, das Alzheimer-Risiko zu verringern. Er machte Fotokopien davon und verteilte sie als Infomaterial an seine Patienten. 2010 veröffentlichte er das Material als Buch mit dem Titel Alzheimer’s Treatment, Alzheimer’s Prevention: A Patient and Family Guide.
Bald wurde ihm klar, dass in den wissenschaftlichen Kreisen, die sich mit der Alzheimerkrankheit beschäftigten, allein schon der Begriff Vorbeugung ein Unwort war. »Laut der Alzheimer’s Association kann man davon nicht sprechen«, erinnert er sich. Im selben Jahr erklärte ein Expertengremium bei den National Institutes of Health: »Derzeit lassen sich keine gültigen Schlussfolgerungen über den Zusammenhang zwischen irgendwelchen veränderbaren Risikofaktoren und kognitivem Verfall oder der Alzheimerkrankheit ziehen.«[190]
Das brachte Isaacson zu der Erkenntnis, dass er nur in einem größeren akademischen Umfeld die Chance hatte, die Wirksamkeit präventiver Maßnahmen vor einer breiteren medizinischen Gemeinschaft unter Beweis zu stellen. Cornell war bereit, das Risiko einzugehen, und so eröffnete er 2013 seine Klinik. Es war die erste ihrer Art in den USA, doch mittlerweile gibt es ein halbes Dutzend ähnlicher Zentren, darunter eines in Puerto Rico. (Isaacson ist inzwischen für ein Privatunternehmen in New York tätig. Seine Kollegin, Dr. Kellyann Niotis, arbeitet nun in meiner Praxis; sie ist auf die Arbeit mit Patienten spezialisiert, die ein erhöhtes Risiko haben, eine neurodegenerative Krankheit zu bekommen.)
Gleichzeitig erhielt die Idee der Alzheimer-Prävention zunehmend wissenschaftlichen Rückhalt. Eine zweijährige randomisierte kontrollierte Studie in Finnland, die 2015 veröffentlicht wurde, kam zu dem Ergebnis, dass Interventionen rund um Ernährung, sportliche Betätigung und kognitives Training in einer Gruppe von über tausendzweihundert älteren Erwachsenen mit Alzheimer-Risiko dazu beitrugen, geistige Funktionen zu erhalten und geistigem Verfall entgegenzuwirken.[191] Laut zwei weiteren großen europäischen Studien haben Änderungen der Lebensweise in verschiedenen Bereichen die kognitiven Leistungen von Erwachsenen mit Alzheimer-Risiko verbessert.[192] Es gab also Grund zur Hoffnung.
Ein traditioneller Arzt hätte Stephanie wieder nach Hause geschickt. Sie hatte keine Symptome und war noch relativ jung. Mit Anfang vierzig hatte sie noch gut zwanzig Jahre Zeit, bis sich möglicherweise eine klinische Demenz entwickeln würde. Medizin 2.0 hätte ihr erklärt, dass es keinen Anlass für eine Behandlung gab. Für Medizin 3.0 war sie jedoch die ideale Patientin, und ihr Fall duldete keinen Aufschub. Wenn es jemals eine Erkrankung gegeben hat, die einen Medizin-3.0-Ansatz erfordert – bei der Prävention nicht nur wichtig, sondern die einzige Option ist –, dann die Alzheimerkrankheit sowie verwandte neurodegenerative Erkrankungen.
Offen gestanden mag es seltsam anmuten, dass eine so kleine Praxis wie unsere eine präventive Neurologin wie Kellyann Niotis in Vollzeit beschäftigt. Warum tun wir das? Weil wir glauben, dass wir wirklich etwas bewirken können, wenn wir früh ansetzen und die Risiken für jeden Patienten sehr konsequent quantifizieren und dann versuchen, dagegen anzugehen. Bei einigen Patienten, beispielsweise Stephanie, besteht offenkundig ein höheres Risiko. Doch generell sind wir alle in gewissem Maß in Gefahr, Alzheimer und andere neurodegenerative Erkrankungen zu entwickeln.
Vom Blickwinkel der Prävention aus betrachtet war die Tatsache, dass Stephanie den ApoE-ε4/ε4-Genotyp besaß, eigentlich eine gute Nachricht. Natürlich war sie viel stärker gefährdet als jemand mit ε3/ε3, doch zumindest kannten wir die Gene, mit denen wir es aufnehmen mussten, und den vermeintlichen Verlauf der Krankheit, falls sie ausbrechen würde. Es ist beunruhigender, wenn in der Familie eines Patienten zahlreiche Fälle von Demenz zu verzeichnen sind oder er erste Anzeichen eines geistigen Verfalls zeigt, ohne Träger eines bekannten Alzheimer-Risikoallels wie ApoE-ε4 zu sein. Das heißt nämlich, dass irgendwelche anderen Risikogene im Spiel sein könnten, und wir wissen nicht, welche das wären. Stephanie war wenigstens mit einem Risiko, das sie kannte, konfrontiert. Da konnten wir ansetzen.
Zusätzlich gab es zwei Risikofaktoren, die sie nicht kontrollieren konnte: Sie war weiß, und sie war eine Frau. Für Menschen afrikanischer Abstammung ist das Risiko, an Alzheimer zu erkranken, aus unbekannten Gründen gemeinhin größer, aber ApoE-ε4 ist für sie anscheinend mit einer geringeren Gefahr verbunden als für Menschen europäischer, asiatischer und hispanischer Abstammung. Abgesehen vom Genotyp betrifft die Alzheimer-Erkrankung jedoch doppelt so viele Frauen wie Männer. Die Vermutung liegt nahe, dass dies an der höheren Lebenserwartung von Frauen liegt, die häufiger fünfundachtzig Jahre oder älter werden, denn in diesem Alter nimmt die Inzidenz um 40 Prozent zu. Das allein erklärt den Unterschied aber nicht. Einige Wissenschaftler vermuten, dass das plötzlich ansteigende Risiko für Neurodegeneration bei älteren Frauen irgendetwas mit der Menopause und den damit zusammenhängenden abrupten hormonellen Veränderungen zu tun hat. Insbesondere scheint ein rapider Abfall des Estradiolspiegels bei Frauen mit einem ε4-Allel das Risiko zu erhöhen.[193] Das wiederum legt eine mögliche Hormonersatztherapie in der Übergangszeit vor der Menopause bei ihnen nahe.
Die Menopause ist hier aber nicht das einzige Problem. Weitere Faktoren aus der Reproduktionsgeschichte, wie die Zahl der Kinder, die eine Frau zur Welt gebracht hat, das Alter bei der ersten Menstruation und die Einnahme von Verhütungsmitteln können ebenfalls einen wichtigen Einfluss auf das Alzheimer-Risiko und die kognitiven Fähigkeiten im späteren Leben haben. Zudem lassen jüngere Forschungen vermuten, dass Frauen eher zur neurotoxisch wirkenden Anhäufung des oben erwähnten Proteins Tau neigen.[194] Unter dem Strich bedeutet dies, dass Frauen ein höheres altersadjustiertes Risiko aufweisen, an Alzheimer zu erkranken, und dass die Krankheit bei ihnen, unabhängig von Alter und Bildungsniveau, allgemein schneller fortschreitet.
Während es doppelt so viele weibliche Alzheimer-Patienten gibt wie männliche, ist es bei der Lewy-Körper-Demenz und Parkinson genau umgekehrt – beide sind zweimal so häufig bei Männern. Aus noch unbekannten Gründen scheint die Parkinsonkrankheit jedoch ebenfalls schneller bei Frauen voranzuschreiten als bei Männern.[195]
Parkinson ist auch aus genetischer Sicht kompliziert. Es wurden zwar schon mehrere Genvarianten identifiziert, die das Risiko für die Krankheit erhöhen – etwa LRRK2 und SNCA –, aber 15 Prozent der Patienten mit einer Parkinson-Diagnose haben eine einschlägige Familiengeschichte – was eine genetische Komponente nahelegt –, ohne jedoch bekannte Risikogene oder Einzelnukleotid-Polymorphismen (single nucleotide polymorphisms, SNPs), also Variationen einzelner Basenpaare im Genom, aufzuweisen.
So wie die anderen apokalyptischen Reiter des Alterns hat auch die Demenz eine extrem lange Vorlaufzeit.[196] Sie bahnt sich so unmerklich an, dass die Erkrankung sehr häufig erst erkannt wird, wenn ihre ersten Stadien schon durchlaufen sind. Das erkennt man daran, dass aus gelegentlichen Missgeschicken und Erinnerungslücken ein auffälliger Gedächtnisverlust wird, sodass man gebräuchliche Wörter vergisst und häufig wichtige Dinge verlegt (auch das Vergessen von Passwörtern wird zum Problem). Freunde und Verwandte bemerken Veränderungen, und bei kognitiven Tests schneidet man nicht mehr so gut ab.
Medizin 2.0 hat diese frühe klinische Phase der Alzheimerkrankheit zunehmend im Blick. Bezeichnet wird sie mit dem Begriff »leichte kognitive Beeinträchtigung« (LKB) oder auch »leichte kognitive Störung«. Gebräuchlicher ist aber die englische Abkürzung MCI für mild cognitive impairment. MCI ist jedoch nicht die erste Etappe auf dem langen Weg zur Demenz. 2011 erbrachte eine umfangreiche Datenanalyse der britischen Kohortenstudie Whitehall II, dass Patienten schon lange, bevor sie die MCI-Kriterien erfüllen, kaum merkliche Anzeichen von kognitiven Veränderungen zeigen. Dann spricht man von der präklinischen Alzheimer-Erkrankung (Phase I). In dieser Phase, in der sich schleichend das pathologische Gerüst in den und um die Nervenzellen bildet, aber kaum gravierende Symptome auftreten, befinden sich Schätzungen zufolge allein in den USA über 46 Millionen Menschen.[197] Wie viele dieser Patienten tatsächlich Alzheimer entwickeln, ist unklar, aber klar ist, dass die Demenz jahrelang unbemerkt, ohne erkennbare Symptome voranschreiten kann, so wie sich der größte Teil eines Eisbergs unter der Meeresoberfläche verbirgt.
Das Gleiche gilt für andere neurodegenerative Erkrankungen, auch wenn ihre Warnsignale jeweils unterschiedlich aussehen. Die Parkinsonkrankheit kann sich durch leichte Veränderungen von Bewegungsmustern bemerkbar machen, einen starren Gesichtsausdruck, eine vornübergebeugte Haltung oder schlurfende Schritte, leichtes Zittern oder auch eine veränderte Handschrift (die manchmal kleiner und verkrampft wird). Bei Personen in den frühen Phasen der Lewy-Körper-Demenz können ähnliche körperliche Symptome auftreten, aber auch milde kognitive Beeinträchtigungen. In beiden Fällen kann es zu Wesensveränderungen kommen, wie Depressionen oder Ängstlichkeit. Irgendetwas scheint »nicht zu stimmen«, ist aber für Laien kaum greifbar.
Darum ist ein wichtiger erster Schritt für Patienten mit etwaigen kognitiven Problemen, sich einer strapaziösen Reihe von Tests zu unterziehen. Dabei arbeite ich gern mit einer präventiven Neurologin zusammen, weil diese Tests so komplex und schwer durchzuführen sind, dass ich sie lieber Spezialisten überlasse. Zudem sind sie für eine korrekte Diagnose unerlässlich – für die Einschätzung, ob ein Patient bereits auf eine Alzheimer-Erkrankung oder eine andere Form neurodegenerativer Demenz zusteuert und wie weit sie vermutlich schon fortgeschritten ist. Es handelt sich um klinisch validierte, hochkomplexe Tests, die jeden Aspekt der Kognition und des Gedächtnisses abdecken. Dazu gehören exekutive Funktionen, Aufmerksamkeit, Verarbeitungsgeschwindigkeit, verbale Flüssigkeit und Wortgedächtnis (Einprägen einer Wortliste), logisches Gedächtnis (Erinnern an eine Phrase in der Mitte eines Absatzes), assoziatives Gedächtnis (Verknüpfen eines Namens mit einem Gesicht), räumliches Gedächtnis (Anordnung von Gegenständen in einem Raum) und semantisches Gedächtnis (zum Beispiel, wie viele Tiere man in einer Minute nennen kann). Meine Patienten beklagen sich hinterher fast immer darüber, wie schwierig die Tests gewesen seien. Dann lächle ich nur und nicke.
Die Feinheiten und Abstufungen der Tests liefern uns wichtige Hinweise auf die Abläufe im Gehirn von Patienten, die sich noch ganz am Anfang des Prozesses kognitiver Veränderungen befinden, der mit zunehmendem Alter fortschreitet. Vor allem versetzen sie uns in die Lage, zwischen normaler Hirnalterung und Veränderungen, die zu Demenz führen können, zu unterscheiden. In einem wichtigen Testabschnitt wird der Geruchssinn der Patienten geprüft. Können sie zum Beispiel Kaffee am Geruch erkennen? Olfaktorische Neuronen gehören zu den ersten, die von Alzheimer betroffen sind.
Spezialisten wie Richard und Kellyann erkennen auch noch andere, nicht so leicht quantifizierbare Veränderungen, beispielsweise im Gang, im Gesichtsausdruck während eines Gesprächs oder sogar bei Augenbewegungen. Von ungeschulten Personen werden sie kaum oder gar nicht bemerkt, aber Experten fallen sie auf.
Die schwierigste Aufgabe bei der Interpretation der Testergebnisse ist, sie den verschiedenen Arten von neurodegenerativen Erkrankungen und Demenz zuzuweisen. Kellyann analysiert die Ergebnisse, um zu bestimmen, wo sich vermutlich betroffene Hirnareale befinden und welche Neurotransmitter dabei eine Rolle spielen, weil sich an ihnen typische Krankheitsmerkmale festmachen lassen. Frontotemporale und vaskuläre Demenz betreffen primär den Stirnlappen (Frontallappen). Diese Hirnregion ist für exekutive Funktionen wie Organisation und Problemlösen sowie Aufmerksamkeit und Verarbeitungsgeschwindigkeit verantwortlich. Diese Demenzformen beeinträchtigen demnach solche höheren kognitiven Funktionen. Die Alzheimer-Erkrankung betrifft in erster Linie die Schläfenlappen (Temporallappen); die deutlichsten Symptome zeigen sich demnach in Gedächtnis, Sprache und auditiver Verarbeitung (Produzieren und Verstehen von gesprochener Sprache). Neuerdings identifizieren Forscher jedoch auch verschiedene mögliche Unterarten der Alzheimerkrankheit, je nach den jeweils am stärksten geschädigten Hirnbereichen. Bei der Parkinsonkrankheit sieht es etwas anders aus, weil sie sich vor allem in Bewegungsstörungen äußert, die (zum Teil) aus einer verminderten Produktion von Dopamin, einem zentralen Neurotransmitter, resultieren. Während sich Alzheimer durch einen Test auf Beta-Amyloid in der Gehirn-Rückenmark-Flüssigkeit diagnostizieren lässt, ist man bei diesen anderen Formen der Neurodegeneration überwiegend auf klinische Diagnosen unter Rückgriff auf Tests und deren Interpretation angewiesen – hier handelt es sich also um eher subjektive Diagnosen. Trotzdem ist es in jedem Fall entscheidend, die betreffende Krankheit möglichst schnell zu identifizieren, damit man mehr Zeit für vorbeugende Maßnahmen hat.
Alzheimer und verwandte Demenzarten sind auch deshalb so schwer zu diagnostizieren, weil unser hochkomplexes Gehirn so geschickt darin ist, Schädigungen zu kompensieren und damit die frühen Stadien der Neurodegeneration zu verschleiern. Bei einem Gedanken oder einer Wahrnehmung ist nicht nur ein einziges neuronales Netz für Erkenntnis oder Entscheidung zuständig. Laut Francisco Gonzalez-Lima, Verhaltensneurowissenschaftler an der University of Texas in Austin, bearbeiten viele einzelne Netzwerke gleichzeitig ein und dasselbe Problem.[198] Diese parallelen Netzwerke können zu unterschiedlichen Schlussfolgerungen gelangen. Wenn man also sagt, man sei »hin- und hergerissen« oder »weiß nicht, was man will«, ist das aus wissenschaftlicher Sicht gar nicht so verkehrt. Das Gehirn wählt dann die gebräuchlichste Reaktion aus. In das System ist eine gewisse Redundanz, also ein gewisses Übermaß an Möglichkeiten, eingebaut.
Je mehr dieser Netze und Teilnetze im Lauf unseres Lebens durch Bildung oder Erfahrung oder auch den Erwerb komplexer Fertigkeiten wie das Sprechen einer Fremdsprache oder das Spielen eines Instruments entstanden sind, desto besser sind wir im Allgemeinen gegen geistigen Verfall gerüstet. Das Gehirn funktioniert weiterhin mehr oder weniger normal, auch wenn einige dieser Netze ihre Arbeit einstellen. Man hat festgestellt, dass diese »kognitive Reserve« bei einigen Patienten dazu beigetragen hat, die Symptome der Alzheimerkrankheit zu bekämpfen. Es scheint länger zu dauern, bis die Erkrankung Funktionen beeinträchtigt. »Bei Menschen mit Alzheimer, die geistig sehr gefordert werden und über gute Ersatzverknüpfungen verfügen, schreitet der geistige Verfall nicht so schnell fort«, sagt Richard.
Bei Parkinson kommt ein paralleles Konzept zum Tragen – die »motorische Reserve«. Menschen mit besseren Bewegungsmustern, die sich zeitlebens viel bewegen, weil sie beispielsweise regelmäßig Sport treiben, haben bessere Chancen, das Fortschreiten der Krankheit zu stoppen oder zu verlangsamen, als Menschen, die viel sitzen. Aus diesem Grund eignen sich Bewegung und sportliche Betätigung, und zwar nicht nur Gymnastik, sondern auch komplexere Aktivitäten wie Box-Work-outs, besonders gut zur Behandlung oder Prävention von Parkinson. Sportliche Betätigung ist die einzige Intervention, die erwiesenermaßen das Fortschreiten der Parkinson-Erkrankung verlangsamt.
Es ist jedoch schwierig, die kognitive Reserve von anderen Faktoren wie dem sozioökonomischen Status und Bildung zu trennen, die ihrerseits mit einer besseren Stoffwechselgesundheit und weiteren Faktoren verknüpft sind. (Man spricht auch vom healthy user bias, der »Verzerrung durch gesunde Teilnehmer«, was bedeutet, dass Studienergebnisse oft auf den allgemein guten Gesundheitszustand der Versuchspersonen zurückzuführen sind und nicht auf den speziell untersuchten Faktor).[199] Ob es Belege dafür gibt, dass sich eine kognitive Reserve »antrainieren« lässt oder sich als Präventionsstrategie eignet, indem man etwa lernt, ein Instrument zu spielen, oder andere Formen des »Hirntrainings« anwendet, ist demzufolge äußerst umstritten und zweifelhaft. Schaden kann es allerdings kaum – also warum nicht?
Es spricht einiges dafür, dass Aufgaben oder Aktivitäten, die vielfältigere Herausforderungen bieten, weil sie schnelleres Denken und Verarbeiten erfordern, mehr zum Aufbau und Erhalt einer kognitiven Reserve beitragen. Jeden Tag ein Kreuzworträtsel zu lösen scheint dagegen nur den Effekt zu haben, dass man im Lösen von Kreuzworträtseln immer besser wird. Für die motorische Reserve gilt das Gleiche: Um die Symptome der Parkinsonkrankheit hinauszuzögern, scheint Tanzen effektiver als Gehen zu sein – wahrscheinlich, weil es komplexere Bewegungen erfordert.
Genau das war etwas, was zugunsten von Stephanie sprach. Sie war gebildet und in ihrem Beruf erfolgreich. Sie verfügte über eine sehr solide kognitive Reserve, und ihre Testergebnisse waren noch sehr gut. Das bedeutete, dass uns einerseits vermutlich viel Zeit blieb – vielleicht Jahrzehnte –, um für sie eine Präventionsstrategie zu entwickeln, aber aufgrund ihres erhöhten genetischen Risikos konnten wir uns keinen Aufschub leisten. Wir brauchten einen Plan. Wie konnte der aussehen? Wie lässt sich diese scheinbar unaufhaltsame Krankheit verhindern?
Sehen wir uns zunächst einmal diejenigen Veränderungen genauer an, die sich im Gehirn von jemandem abspielen, dem die Alzheimerkrankheit näher rückt. Inwiefern tragen diese Veränderungen zum Fortschreiten der Erkrankung bei, und können wir irgendetwas tun, um sie zu stoppen oder den Schaden zu begrenzen?
Sobald wir uns nicht mehr ausschließlich auf die Amyloid-Hypothese fokussieren, werden uns gewisse andere typische Merkmale der Demenz ins Auge fallen, die Möglichkeiten zur Prävention bieten – Schwachstellen in der Rüstung unseres Gegners.
Alternativen zu Beta-Amyloid
Schon seit Jahrzehnten, nahezu im Gleichschritt mit der Beobachtung von Plaques und Faserbündeln, vermerken Forscher bei Demenzkranken Probleme mit der Hirndurchblutung. Bei Autopsien sind im Gehirn von Alzheimer-Patienten häufig ausgeprägte Verkalkungen[200] der Blutgefäße und Kapillaren, die das Gehirn versorgen, zu sehen. Dies ist keine neue Entdeckung: In ihrem wegweisenden Artikel von 1968, der die Alzheimerkrankheit als ein verbreitetes Altersleiden beschrieb, hatten Blessed, Tomlinson und Roth auch auf gravierende Gefäßschädigungen im Gehirn der verstorbenen Patienten hingewiesen.[201] Jahrzehntelang, schon seit 1927, hatte man das Phänomen beiläufig erwähnt, doch gemeinhin als eine Folge der Neurodegeneration betrachtet und nicht etwa als eine mögliche Ursache.
Anfang der 1990er-Jahre befand sich Jack de la Torre, ein Neurologe der Case Western Reserve University, auf dem Flug nach Paris. Er wollte an einer Tagung teilnehmen und dachte über die Ursachen der Alzheimerkrankheit nach. Die Amyloid-Hypothese war noch recht neu, aber wegen der Beobachtungen, die er in seinem eigenen Labor gemacht hatte, konnte sich de la Torre nicht wirklich mit ihr anfreunden. Plötzlich fiel es ihm wie Schuppen von den Augen. »Die Ergebnisse von Dutzenden Experimenten mit Ratten offenbarten sich mir mit einem Mal als schlagende Beweise«, schrieb er später. In jenen Experimenten hatte er die Blutversorgung der Rattengehirne eingeschränkt, und mit der Zeit hatten die Ratten Symptome entwickelt, die denen von menschlichen Alzheimer-Patienten bemerkenswert ähnelten: Gedächtnisverlust sowie eine schwere Atrophie des Cortex und des Hippocampus. Die Wiederherstellung der Durchblutung konnte weitere Schädigungen vermeiden oder sie bis zu einem gewissen Maß rückgängig machen, aber bei älteren Tieren schienen sie schwerwiegender und länger andauernd zu sein als bei jüngeren. Die wichtigste Erkenntnis lautete: Eine ungehinderte Durchblutung schien für ein gesundes Gehirn von entscheidender Bedeutung zu sein.
Das Gehirn ist ein gefräßiges Organ.[202] Es macht zwar nur 2 Prozent unseres Körpergewichts aus, aber beansprucht etwa 20 Prozent unseres Gesamtenergiebedarfs. Seine 86 Milliarden Neuronen besitzen jeweils zwischen 1000 und 10 000 Synapsen, die die Verbindung zu anderen Neuronen oder Zielzellen herstellen und auf diese Weise unsere Gedanken, unsere Persönlichkeit, unsere Erinnerungen sowie die Schlussfolgerungen erzeugen, die unseren guten und schlechten Entscheidungen zugrunde liegen. Es gibt zwar Computer, die größer und schneller sind, aber bislang kann es noch keine menschengemachte Maschine mit den Intuitionen und der Lernfähigkeit eines Menschengehirns aufnehmen, von Gefühlen oder Kreativität ganz zu schweigen. Kein Computer kommt auch nur annähernd an die Multidimensionalität des menschlichen Geistes heran. Während ein Computer seine Energie aus Strom gewinnt, benötigt die wunderbare Maschine namens Menschenhirn den steten Zufluss von Glucose und Sauerstoff, den ein weitverzweigtes und filigranes Netzwerk aus Blutgefäßen gewährleistet. Schon eine kleine Störung dieses vaskulären Netzes kann zu einem lähmenden oder gar tödlichen Schlaganfall führen.
Überdies verstoffwechseln Hirnzellen Glucose anders als der Rest des Körpers. Sie brauchen kein Insulin, sondern absorbieren die Glucose aus dem Blutkreislauf direkt über Transporter, die im Prinzip ein Tor in der Zellmembran öffnen. Das versetzt das Gehirn bei einem niedrigen Blutzuckerspiegel in die Lage, für seine Energieversorgung oberste Priorität zu beanspruchen. Wenn Mangel an frischen Glucosequellen herrscht, wandelt die Leber unser Fett in Ketonkörper um. Diese fungieren als alternative Energiequelle, die uns, je nach dem Umfang unserer Fettreserven, über einen sehr langen Zeitraum hinweg ernähren können. (Im Gegensatz zu Muskeln oder der Leber speichert das Gehirn keine Energie.) Wenn die Fettdepots schwinden, ernährt uns unser Muskelgewebe, danach die anderen Organe und selbst unsere Knochen – alles, damit das Gehirn weiter funktionieren kann, koste es, was es wolle. Das Gehirn schaltet sich als Letztes ab.
Während sein Flugzeug den Atlantik überquerte, kritzelte de la Torre seine Ideen auf die einzige verfügbare Schreibfläche – eine Spucktüte. Die Flugbegleiterinnen warfen ihm strafende Blicke zu, als er eine weitere Tüte und dann noch eine verlangte. Seine »Kotzbeutel-Theorie«, wie er sie scherzhaft nannte, lautete: Die Alzheimerkrankheit ist in erster Linie eine Gefäßerkrankung des Gehirns.[203] Die für uns sichtbaren Demenzsymptome werden durch eine allmählich abnehmende Durchblutung verursacht, die letztlich zu einer »neuronalen Energiekrise« führt, wie er es nennt. Diese wiederum löst eine Kaskade unglückseliger Ereignisse aus, die die Nervenzellen schädigt und schließlich eine Neurodegeneration herbeiführt. Danach erst kommen die Amyloid-Plaques und Faserbündel – nicht ursächlich, sondern als Folge. »Wir haben geglaubt und glauben weiterhin, dass Beta-Amyloid ein bedeutendes pathologisches Produkt der Neurodegeneration ist«, schrieb de la Torre vor einigen Jahren, »… [aber] es ist nicht die Ursache der Alzheimerkrankheit.«[204]
Es gab bereits Belege, die seine Theorie stützten. Alzheimer wird häufiger bei Patienten diagnostiziert, die einen Schlaganfall erlitten haben, was typischerweise durch eine plötzliche Durchblutungsstörung in spezifischen Regionen des Gehirns hervorgerufen wird. In diesen Fällen treten urplötzlich Symptome auf, als habe man einen Schalter umgelegt. Zudem hat sich herausgestellt, dass Personen, die bereits mehrfach mit Herz-Kreislauf-Erkrankungen zu tun hatten, ein höheres Risiko aufweisen, an Alzheimer zu erkranken. Und es besteht erwiesenermaßen eine lineare Beziehung zwischen geistigem Verfall und erhöhter Intima-Media-Dicke der Arteria carotis (Halsschlagader), einem großen Blutgefäß, das das Hirn mit Blut versorgt. Mit zunehmendem Alter nimmt die Hirndurchblutung ohnehin natürlicherweise ab, und die altersbedingte Verdickung der Arterie könnte die Blutversorgung des Gehirns weiter einschränken. Allerdings sind vaskuläre Probleme nicht der alleinige Übeltäter. Insgesamt gibt es etwa zwei Dutzend bekannte Risikofaktoren für Alzheimer, die ebenfalls die Durchblutung behindern; zu ihnen gehören hoher Blutdruck, Rauchen, Kopfverletzungen und Depressionen. Die Indizienbeweise sind zahlreich.
Mit verbesserter Neuroimaging-Technologie ließ sich nicht nur bestätigen, dass die Hirndurchblutung bei Alzheimer-Patienten eingeschränkt ist, sondern auch, dass ein Abfall der Durchblutung anscheinend ankündigt, wann der Übergang von einer präklinischen Alzheimer-Erkrankung zu MCI und dann zu voll ausgeprägter Demenz erfolgt. Derzeit geht man zwar davon aus, dass sich eine vaskuläre Demenz, die etwa 15 bis 30 Prozent der Demenzdiagnosen in Nordamerika und Europa sowie bis 30 Prozent in Asien und den Entwicklungsländern ausmacht, von einer durch Alzheimer bedingten Demenz unterscheidet. Dennoch überschneiden sich ihre Symptome und Pathologie so signifikant, dass sie für de la Torre verschiedene Manifestationen von ein und derselben Grunderkrankung sind.[205]
Nach einer weiteren überzeugenden und vielleicht parallelen Theorie ist die Alzheimerkrankheit auf einen abnormen Glucosestoffwechsel im Gehirn zurückzuführen. Wissenschaftler und Ärzte verweisen schon lange auf einen Zusammenhang zwischen Alzheimer und Stoffwechselstörungen. Bei Patienten mit Typ-2-Diabetes verdoppelt oder verdreifacht sich das Risiko für eine Alzheimer-Erkrankung, also etwa so stark wie beim Auftreten einer Kopie des ApoE-ε4-Gens.[206] Rein mechanisch kann ein chronisch erhöhter Blutzuckerspiegel, wie er bei Typ-2-Diabetes und Prädiabetes/Insulinresistenz auftritt, das Gefäßsystem im Gehirn unmittelbar schädigen. Doch schon allein eine Insulinresistenz genügt, um das Alzheimer-Risiko zu erhöhen.[207]
Insulin scheint eine entscheidende Rolle für die Erinnerungsfunktion zu spielen. Im Hippocampus, einem wichtigen Gedächtniszentrum des Gehirns, kommen Insulinrezeptoren in hoher Konzentration vor. Laut mehreren Studien verbessert es umgehend die kognitive Leistung und das Gedächtnis, wenn man Versuchspersonen per Nasenspray Insulin verabreicht – womit es auf möglichst kurzem Weg ins Gehirn gelangt –, selbst wenn bei den Personen bereits eine Alzheimer-Erkrankung diagnostiziert wurde.[208] Eine Studie kam zu dem Ergebnis, dass intranasal appliziertes Insulin dazu beitrug, das Hirnvolumen von Alzheimer-Patienten zu erhalten.[209] Offenkundig ist es hilfreich, Neuronen mit Glucose zu versorgen, was durch Insulinresistenz blockiert wird. So schreiben die Autoren: »Die Hinweise verdichten sich, dass eine Insulinresistenz im zentralen Nervensystem zur Entwicklung und Progression der Alzheimerkrankheit beiträgt.«
Das Signal hierfür scheint (erneut) ein Abfall der Energiezufuhr zum Gehirn zu sein, wie es ähnlich auch zu Beginn einer vaskulären Demenz zu beobachten ist.[210] Hirnuntersuchungen mit bildgebenden Verfahren haben Jahrzehnte vor dem Einsetzen anderer Symptome vaskulärer Demenz einen reduzierten Glucosestoffwechsel im Gehirn nachgewiesen.[211] Faszinierenderweise scheint diese Reduzierung in Hirnregionen, die auch infolge einer Alzheimer-Erkrankung geschädigt werden, besonders heftig auszufallen – etwa im Parietallappen, der bei der Verarbeitung und Integration von Sinnesinformationen eine wichtige Rolle spielt, sowie im Hippocampus des Temporallappens, der für das Gedächtnis relevant ist.[212] So wie eine eingeschränkte Durchblutung lässt auch ein eingeschränkter Glucosestoffwechsel die betreffenden Neuronen nach Energie hungern und ruft kaskadenartige Reaktionen hervor, wie Entzündungsprozesse, oxidativen Stress, mitochondriale Dysfunktion – und letzten Endes auch Neurodegeneration.
Welche Rolle spielt ApoE-ε4?
Es ist immer noch nicht ganz klar, wie oder warum – aber ε4 scheint andere Risikofaktoren für Alzheimer und die Krankheit fördernde Mechanismen zu forcieren, insbesondere metabolische Faktoren wie einen reduzierten Glucosestoffwechsel im Gehirn, den wir soeben erörtert haben. Einfach ausgedrückt, scheint das Allel alles noch schlimmer zu machen – auch den bei Alzheimer auftretenden Geschlechterunterschied: Bei einer Frau mit einer ε4-Kopie ist die Wahrscheinlichkeit zu erkranken viermal größer als bei einem Mann mit dem gleichen Genotyp.[213]
Das Protein ApoE (Apolipoprotein E), für das das Gen codiert, spielt eine bedeutende Rolle beim Cholesterintransport wie auch beim Glucosestoffwechsel. Es dient als wichtigster Cholesterinträger im Gehirn, indem es Cholesterin über die Blut-Hirn-Schranke transportiert, um den Heißhunger der Neuronen zu stillen. Hussein Yassine, Neurowissenschaftler an der University of Southern California, der die Bedeutung von ApoE für die Alzheimer-Krankheit untersucht, vergleicht das Protein mit einem Orchesterdirigenten. Wie er sagt, sehe es so aus, dass Menschen mit dem ε4-Allel sowohl Probleme beim Cholesterintransport als auch mit dem Glucosestoffwechsel hätten, und zwar in einem größeren Ausmaß als Menschen mit ε2 oder ε3. Obwohl sich das risikoreichere ApoE-ε4 vom harmlosen ε3 nur in einer einzigen Aminosäure unterscheide, scheine es beim Transport von Cholesterin ins Gehirn und vor allem auch wieder hinaus weniger effektiv zu sein. Es gebe auch einige Hinweise darauf, dass ApoE-ε4 eine frühe Öffnung der Blut-Hirn-Schranke bewirke, was das Gehirn anfälliger für Verletzungen und letztlich Degeneration mache.[214]
Seltsamerweise war ApoE-ε4 nicht immer ein Bösewicht. Über Millionen Jahre waren alle unsere frühen Vorfahren auf dem Hominini-Ast des Evolutionsstammbaums ε4/ε4-Träger. Dies entsprach dem ursprünglichen menschlichen Genotyp.[215] Die ε3-Mutation tauchte vor etwa 225 000 Jahren auf, wohingegen ε2 eher ein Nachzügler ist, der erst in den letzten 10 000 Jahren in Erscheinung trat. Daten aus heutigen Populationen mit einem häufigen Vorkommen von ε4 lassen vermuten, dass das Allel in Umgebungen mit vielen Infektionskrankheiten von Nutzen sein könnte. So sind Kinder mit ApoE-ε4, die in brasilianischen Favelas leben, weniger anfällig für Diarrhö und geistig weiter entwickelt.[216] In Umgebungen, in denen Infektionskrankheiten zu den häufigsten Todesursachen zählten, waren ApoE-ε4-Träger möglicherweise diejenigen, die länger lebten.
Dieser Überlebensvorteil hat vielleicht dafür gesorgt, dass ApoE-ε4 Entzündungsprozesse begünstigt, was in einigen Situationen (zum Beispiel beim Bekämpfen einer Infektion) nützlich sein kann, in anderen (zum Beispiel im modernen Leben) eher schädlich. Wie wir in Kapitel 7 gesehen haben, fördern Entzündungsvorgänge atherosklerotische Schädigungen unserer Blutgefäße und bereiten auf diese Weise der Alzheimerkrankheit und Demenz den Weg. Alzheimer-Patienten weisen im Gehirn häufig einen hohen Spiegel von Zytokinen wie TNF-alpha und IL-6 auf, die an Entzündungsprozessen beteiligt sind, und laut Studien sind bei ε4-Trägern vermehrt Entzündungen von Nervengewebe zu beobachten.[217] Natürlich ist nichts davon der langfristigen Gesundheit des Gehirns zuträglich; wie schon gesagt, scheint ε4 sämtliche Risikofaktoren für Alzheimer noch zu forcieren.
Offensichtlich richtet die ε4-Variante noch in anderer Hinsicht Schaden an, zum Beispiel, wenn es um Ernährungsgewohnheiten unserer modernen Zeit geht. Träger von ε4 entwickeln nicht nur mit größerer Wahrscheinlichkeit das metabolische Syndrom – es kann sogar sein, dass das Protein ApoE-ε4 zum Teil eigens dafür verantwortlich ist, indem es die Fähigkeit des Gehirns zerstört, den Insulinspiegel zu regulieren und die Glucosehomöostase (Blutzuckerregulation) im Körper aufrechtzuerhalten. Dieses Phänomen offenbart sich, wenn bei betroffenen Patienten eine kontinuierliche Glucosemessung (continuous glucose monitoring, CGM) vorgenommen wird (worauf wir in Kapitel 15 ausführlicher eingehen). Selbst bei jungen Patienten mit ε4 kommt es nach dem Verzehr von kohlenhydratreichen Lebensmitteln zu dramatischen Glucosespitzen, obwohl unklar ist, welche klinische Signifikanz dies hat.
Demzufolge könnte ε4 genau diejenige Stoffwechselstörung vorantreiben, die auch das Demenzrisiko erhöht. Zugleich scheint es den Schaden, der dem Gehirn durch die Stoffwechselstörung unmittelbar zugefügt wird, zu vergrößern. Forscher haben herausgefunden, dass in Arealen mit hohem Glucosespiegel die von ApoE-ε4 codierte aberrante Proteinform bewirkt, dass Insulinrezeptoren im Gehirn blockiert werden, sodass sich klebrige Klumpen oder Aggregate bilden, die Nervenzellen an der Energieaufnahme hindern.
Nicht jeder mit dem ApoE-ε4-Genotyp ist jedoch von den gleichen Beeinträchtigungen betroffen. Seine Auswirkungen auf Erkrankungsrisiken und den Verlauf von Krankheiten sind äußerst variabel. Faktoren wie Geschlecht, Ethnie und Lebensstil spielen eindeutig eine Rolle, aber mittlerweile nimmt man an, dass das Alzheimer-Risiko und der Effekt von ApoE auch sehr stark von anderen Genen abhängen, die ebenfalls mit dem Risiko, an Alzheimer zu erkranken, zu tun haben. Zu ihnen gehört Klotho, dessen Schutzfunktion wir oben schon erwähnt haben. So ließe sich vielleicht erklären, warum manche ε4-Träger nie Alzheimer entwickeln, andere hingegen sehr früh.
All dies spricht dafür, dass sich metabolische und vaskuläre Ursachen von Demenz in gewisser Hinsicht überschneiden, so wie Patienten mit Insulinresistenz auch anfällig für Gefäßkrankheiten sind. Und wir lernen daraus, dass wir bei Hochrisikopatienten wie Stephanie besonders sorgfältig auf die Stoffwechselgesundheit achten müssen.
Der Präventionsplan
Trotz allem bleibe ich vorsichtig optimistisch, was Patienten wie Stephanie angeht – selbst angesichts ihrer sehr hohen genetischen Vorbelastung. Das Konzept der Alzheimer-Prävention an sich ist noch relativ jung – wir haben gerade erst begonnen, an der Oberfläche der Möglichkeiten zu kratzen. Wenn wir die Krankheit besser verstehen, können unsere Behandlungen und Interventionen ausgeklügelter werden und zeigen hoffentlich Wirkung.
Eigentlich denke ich, dass wir mittlerweile mehr über die Vorbeugung der Alzheimerkrankheit wissen als über die Vorbeugung von Krebs. Unsere wichtigste vorbeugende Maßnahme gegen Krebs ist, nicht zu rauchen und auf unsere Stoffwechselgesundheit zu achten. Das ist jedoch ein sehr allgemein gehaltener Ansatz, der uns nicht allzu weit bringt. Wir brauchen aggressives Screening und hoffen, Krebs irgendwie aufzuspüren, bevor es zu spät ist. Bei Alzheimer steht uns ein viel größeres Instrumentarium zur Verfügung und auch viel bessere Diagnoseverfahren. Geistiger Verfall in einem frühen Stadium ist relativ leicht zu entdecken, wenn wir wissen, wo wir zu suchen haben. Außerdem lernen wir immer mehr über genetische Faktoren – auch über diejenigen, die die schädliche Wirkung von Hochrisikogenen wie ApoE-ε4 zumindest teilweise aufheben.
Weil der Stoffwechsel bei ε4-Trägern mit hohem Risiko, wie etwa Stephanie, eine so entscheidende Rolle spielt, müssen wir bei ihnen zunächst etwaige metabolische Probleme in Angriff nehmen. Unser Ziel ist die Verbesserung des Glucosestoffwechsels sowie die Bekämpfung von Entzündungsprozessen und oxidativem Stress. Eine mögliche Empfehlung für jemanden wie Stephanie lautet, zu einer mediterranen Ernährung mit mehr einfach ungesättigten Fettsäuren und weniger raffinierten Kohlenhydraten zu wechseln und regelmäßig fettreichen Fisch zu essen. Es gibt Belege dafür, dass eine Nahrungsergänzung mit der Omega-3-Fettsäure DHA, die in Fischöl enthalten ist, zur Erhaltung der Hirngesundheit, insbesondere bei ε4/ε4-Trägern, beiträgt.[218] Bei ihnen sind möglicherweise höhere DHA-Dosen erforderlich, weil ε4 Stoffwechselveränderungen und Störungen der Blut-Hirn-Schranke hervorrufen kann.
Hier kann auch eine ketogene Diät von Vorteil sein. Im Zustand der Ketose nutzt das Gehirn zur Energiezufuhr eine Mischung aus Ketonen und Glucose. Laut Studien über Alzheimer-Patienten ist ihr Gehirn weiterhin in der Lage, Ketone zu verstoffwechseln, auch wenn es Glucose nicht mehr so gut nutzen kann. Es könnte demnach sinnvoll sein, dem Gehirn nicht ausschließlich Glucose, sondern Glucose und Ketone als Energiequelle zur Verfügung zu stellen. Ein systematischer Überblick über randomisierte kontrollierte Studien erbrachte, dass ketogene Therapien bei Versuchspersonen mit leichter kognitiver Beeinträchtigung und Alzheimer im Frühstadium eine allgemeine Verbesserung der kognitiven Leistungen und des Gedächtnisses zur Folge hatten.[219] Man könnte also von einer »Flexible-Fuel-Strategie« sprechen.
Stephanie beschloss, nicht nur auf Zuckerzusatz und raffinierte Kohlenhydrate, sondern auch auf Alkohol zu verzichten. Wie genau sich Alkohol im Hinblick auf die Alzheimerkrankheit auswirkt, ist umstritten. Einiges weist darauf hin, dass Alkohol einen gewissen Schutz vor Alzheimer bietet, aber andere Belege sprechen dafür, dass ein stärkerer Alkoholkonsum auch ein Risikofaktor sein kann, und ε4-Träger sind möglicherweise noch anfälliger für die schädliche Wirkung des Alkohols.[220] Ich bleibe da lieber auf der sicheren Seite und Stephanie ebenfalls.
Das wirkungsvollste Instrument in unserem präventiven Werkzeugkasten ist sportliche Betätigung, denn sie beeinflusst das Alzheimer-Risiko gleich auf zweierlei Weise: Sie trägt zur Aufrechterhaltung der Glucosehomöostase bei und fördert die Gesundheit des Gefäßsystems. Wir stellten also nicht nur Stephanies Ernährung um, sondern entwickelten auch ein Programm mit regelmäßiger sportlicher Betätigung für sie, mit einem Fokus auf konstanter Ausdauer, um die Leistungsfähigkeit ihrer Mitochondrien zu steigern. Das wirkte sich auch positiv auf ihren stressbedingt viel zu hohen Cortisonspiegel aus. Gesundheitliche Risiken aufgrund von Stress und Angst treten bei Frauen anscheinend signifikant häufiger auf.[221] Wie wir in Kapitel 11 sehen werden, produziert Ausdauertraining Faktoren, die unmittelbar Hirnregionen ansprechen, welche für Kognition und Gedächtnis zuständig sind. Zudem hilft es beim Bekämpfen von Entzündungsvorgängen und oxidativem Stress.
Krafttraining ist vermutlich genauso wichtig. Laut einer Studie mit fast 500 000 Patienten in Großbritannien bestand eine starke negative Korrelation zwischen der Handkraft, einem ausgezeichneten Gradmesser für die Gesamtstärke, und dem Vorkommen einer Demenz (siehe Abbildung 8).[222] Personen im unteren Quartil der Handkraft (also die schwächsten) wiesen eine um 72 Prozent höhere Inzidenz von Demenz auf als die im oberen Quartil. Die Autoren stellten fest, dass diese Korrelation auch nach Bereinigung hinsichtlich der üblichen Störfaktoren wie Alter, Geschlecht, sozioökonomischem Status, Krankheiten wie Diabetes und Krebs, Rauchen sowie Lebensstilfaktoren wie Schlafmustern, Gehgeschwindigkeit und Zeit vor dem Fernseher Bestand hatte. Und es schien keine Obergrenze oder ein »Plateau« für diese Relation zu geben – je größer die Handkraft, desto niedriger das Demenzrisiko.
Man ist versucht, Ergebnisse wie diese aus den gleichen Gründen abzutun, aus denen wir gegenüber Resultaten aus der Epidemiologie skeptisch sein sollten. Doch im Gegensatz zur Ernährungsepidemiologie (mehr dazu in Kapitel 14) spricht die Epidemiologie, die einen Zusammenhang zwischen Kraft sowie kardiorespiratorischer Fitness und einem geringeren Risiko von Neurodegeneration herstellt, eine so eindeutige und überzeugende Sprache, dass meine eigenen, etwa 2012 gehegten, Zweifel bezüglich der positiven Wirkung von sportlicher Betätigung nach und nach schwanden. Heute erkläre ich meinen Patienten, dass sportliche Betätigung ohne jeden Zweifel das beste uns zur Verfügung stehende Mittel ist, um neurodegenerativen Erkrankungen vorzubeugen. Basta! (Das erörtern wir in allen Einzelheiten in Kapitel 11 und 12.)
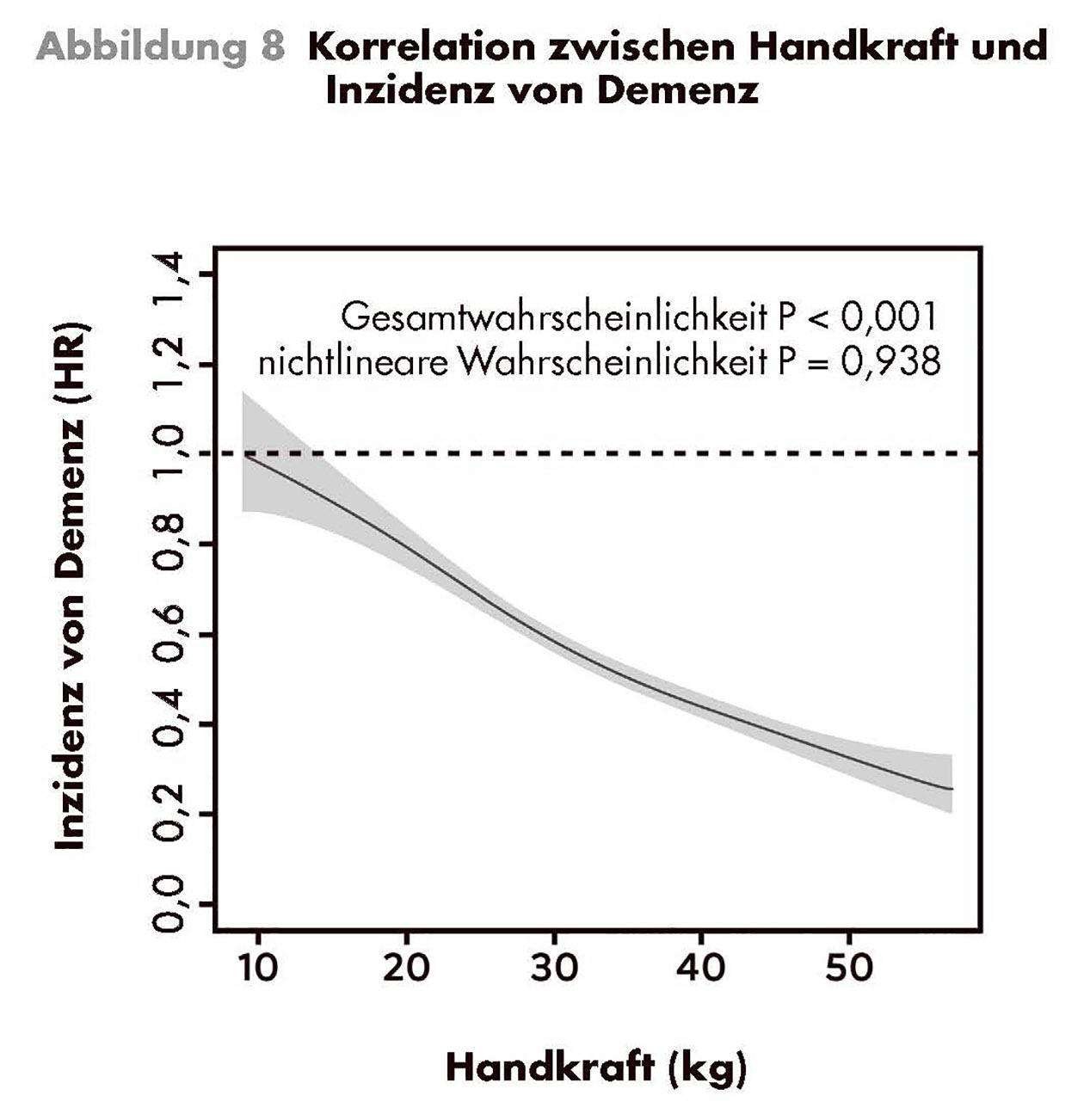
Dieses Diagramm zeigt, dass die Inzidenz von Demenz mit zunehmender Handkraft abnimmt. Die Daten sind als Hazard Ratios (Verhältnis von jeweils zwei Inzidenzdichten) im Vergleich zur schwächsten Gruppe dargestellt, z. B. 0,4 = 40 Prozent. Bei einer Person mit einer Handkraft von 40 kg entspricht das Demenz-Risiko also ungefähr 40 Prozent des Demenz-Risikos einer Person mit einer Handkraft von 10 kg.
Quelle: Esteban-Cornejo et al. (2022)
Auch der Schlaf ist ein hochwirksames Mittel gegen die Alzheimerkrankheit, wie wir in Kapitel 16 sehen werden. Im Schlaf heilt sich unser Gehirn selbst; im Tiefschlaf ist es im Wesentlichen mit »Großreinemachen« beschäftigt und beseitigt intrazellulären Müll, der sich zwischen den Nervenzellen anlagern kann. Schlafunterbrechungen und schlechter Schlaf sind potenzielle Förderer eines erhöhten Demenz-Risikos.[223] Kommt zu schlechtem Schlaf noch großer Stress und ein erhöhter Cortisonspiegel hinzu, wie in Stephanies Fall, vervielfacht dies quasi das Risiko, weil es eine Insulinresistenz begünstigt und zugleich den Hippocampus schädigt. Darüber hinaus beeinträchtigt Hypercortisolämie (überhöhter Cortisonspiegel durch Stress) die Ausschüttung von Melatonin, dem Hormon, das normalerweise unserem Gehirn signalisiert, dass es Zeit zum Schlafengehen ist (und das zudem dazu beitragen kann, den Verlust von Nervenzellen und kognitive Beeinträchtigungen zu verhindern). Es war also dringend notwendig, Stephanies Schlafprobleme in den Griff zu bekommen. Wegen ihrer Scheidung und ihrer beruflichen Situation schlief sie nachts kaum einmal vier Stunden am Stück durch.
Wie sich gezeigt hat, ist, etwas überraschend, auch Hörverlust ein Risikofaktor. Laut Studien besteht eine eindeutige Verbindung zwischen Hörverlust und der Alzheimerkrankheit, obwohl er kein direktes Symptom ist.[224] Vielmehr scheint Hörverlust in einem Kausalzusammenhang mit geistigem Verfall zu stehen, weil Menschen, die schlecht hören, dazu neigen, sich zurückzuziehen und den Austausch mit anderen zu meiden. Wenn dem Gehirn Input entzogen wird – in diesem Fall akustischer Input –, verkümmert es. Den Patienten mit Hörverlust fehlen soziale Kontakte, geistige Stimulation und das Gefühl dazuzugehören; Hörgeräte können einige der Symptome möglicherweise lindern. Was bislang noch eine Hypothese ist, untersucht zurzeit eine klinische Studie namens ACHIEVE (Aging and Cognitive Health Evaluation in Elders, »Altern und Einschätzung der geistigen Gesundheit bei älteren Menschen«).
Depression wird zwar auch mit Alzheimer in Verbindung gebracht, scheint aber eher ein Symptom als ein Risikofaktor oder Antreiber der Krankheit zu sein. Dennoch hilft die Behandlung von Depressionen bei Patienten mit MCI oder der Frühform der Alzheimerkrankheit offenkundig, andere Symptome geistigen Verfalls zu lindern.
Eine weitere verblüffende Intervention zur Reduzierung systemischer Entzündungsprozesse und möglicherweise auch des Alzheimer-Risikos ist das Reinigen der Zähne mit Zahnbürste und Zahnseide. (Ja, Sie haben richtig gelesen, Zahnseide.) Es gibt immer mehr wissenschaftliche Untersuchungen, die die Mundgesundheit, vor allem den Zustand des Zahnfleischs, mit der Gesamtgesundheit in Verbindung bringen. Forscher haben herausgefunden, dass insbesondere ein Erreger, das Bakterium P. gingivalis, das häufig für Erkrankungen des Zahnfleischs verantwortlich ist, einen starken Anstieg von Entzündungsmarkern wie IL-6 bewirkt. Noch merkwürdiger ist, dass man P. gingivalis auch im Gehirn von Alzheimer-Patienten gefunden hat, obwohl Wissenschaftler unsicher sind, ob dieses Bakterium unmittelbar Demenz herbeiführt – so Dr. Patricia Corby, Professorin für Zahngesundheit an der New York University.[225] Trotzdem ist die Verbindung zu stark, um ignoriert zu werden. (Weil zudem eine starke Korrelation zwischen Mundgesundheit und Gesamtgesundheit, insbesondere im Hinblick auf das Risiko für Herz-Kreislauf-Erkrankungen, besteht, achte ich heute viel mehr auf die Benutzung von Zahnseide und die Gesundheit des Zahnfleischs als früher.)
Ein weiterer Aspekt der Prävention von Demenz (und wo wir schon dabei sind, auch Atherosklerose), über den ich seit relativ kurzer Zeit ebenfalls nachdenke, ist der Besuch einer Trockensauna. Bis etwa 2019 war ich äußerst skeptisch, was Daten betraf, die auf eine Verbindung zwischen Saunieren und der Gesundheit von Herz und Gehirn hindeuteten. Je intensiver ich mich jedoch mit Literatur zu diesem Thema beschäftige, desto mehr überzeugen mich die Menge der Vorteile, die Übereinstimmung der Forschungsergebnisse und die zugrunde liegenden physiologischen Mechanismen, die die Daten glaubwürdig machen. Ich bin zwar nicht so fest davon überzeugt, dass ein regelmäßiger Saunabesuch das Risiko verringert, an Alzheimer zu erkranken, wie ich das bei sportlicher Betätigung bin, aber doch sehr viel sicherer als zu Beginn meiner Reise. Das beste Resümee, das ich aus der wissenschaftlichen Literatur zum Thema ziehen konnte, lautet: Mindestens vier Saunagänge pro Woche von jeweils mindestens zwanzig Minuten bei 82 Grad Celsius oder mehr sind ideal, um das Risiko einer Alzheimer-Erkrankung um etwa 65 Prozent[226] (und das von Atherosklerose um 50 Prozent)[227] zu senken.
Weitere mögliche Interventionen, die laut Studien einigermaßen erfolgversprechend sind, sind die Senkung des Homocysteinspiegels durch die Gabe von B-Vitaminen[228] bei gleichzeitiger Optimierung der Versorgung mit Omega-3-Fettsäuren.[229] Bei Patienten mit dem ε4/ε4-Genotyp wurde eine Korrelation von einem höheren Vitamin-D-Spiegel mit besseren Gedächtnisleistungen festgestellt.[230] Aus der aktuellen Literatur geht jedoch nicht hervor, ob die zusätzliche Gabe von Vitamin D das Alzheimer-Risiko senkt. Und wie bereits erwähnt, verspricht eine Hormonersatztherapie für Frauen im Übergang zur Menopause Erfolge – vor allem bei Frauen mit wenigstens einer ε4-Kopie.
Am beängstigendsten an der Alzheimerkrankheit ist, kurz gesagt, dass Medizin 2.0 hier nicht helfen kann. Überhaupt nicht. Der Punkt, an dem Medizin 2.0 eingreift – der Zeitpunkt der Diagnose – entspricht mehr oder weniger dem Punkt, an dem es für die meisten Alzheimer-Patienten kein Zurück mehr gibt. Danach kann man nur noch wenig oder nichts mehr für sie tun. Sobald eine Demenz diagnostiziert wurde, ist es extrem schwierig, ihr Fortschreiten zu verlangsamen, und wahrscheinlich unmöglich, sie rückgängig zu machen (obwohl wir das nicht mit Sicherheit sagen können). Demzufolge sind wir gezwungen, das vertraute Terrain der uns bekannten Medizin zu verlassen, das uns Gewissheit verspricht, und uns den Konzepten von Medizin 3.0 zur Prävention und Risikoreduktion anzuvertrauen.
Nach heutigem Stand ist die Alzheimerkrankheit der letzte apokalyptische Reiter des Alterns, den wir auf dem Weg zu einem Leben als Hundertjährige passieren müssen – das letzte Hindernis, mit dem wir konfrontiert werden. Typischerweise wird Alzheimer erst spät im Leben diagnostiziert – und Hundertjährige erkranken, wenn überhaupt, viel später daran. Je länger es uns gelingt, demenzfrei zu bleiben, desto größer sind unsere Chancen, länger und gesünder zu leben. (Sie wissen ja, einer der drei Vektoren der gesunden Lebenszeit sind unsere geistigen Fähigkeiten.) Doch solange die Wissenschaft keine wirksameren Behandlungen entwickelt, bleibt Prävention unsere einzige Option. Darum müssen wir sehr früh einen umfassenden Ansatz zur Vorbeugung der Alzheimerkrankheit und anderer neurodegenerativer Erkrankungen wählen.
Grob gesagt, sollte unsere Strategie auf den folgenden Prinzipien basieren:
WAS GUT FÜRS HERZ IST, IST AUCH GUT FÜRS GEHIRN. Das heißt: Ein gesundes Gefäßsystem (niedriger ApoB-Spiegel, niedrige Entzündungswerte und geringer oxidativer Stress) ist entscheidend für die Hirngesundheit.
WAS GUT FÜR DIE LEBER (UND die BAUCHSPEICHELDRÜSE) IST, IST AUCH GUT FÜRS GEHIRN. Stoffwechselgesundheit ist entscheidend für die Hirngesundheit.
ZEIT IST DER SCHLÜSSEL. Wir müssen früh an Vorbeugung denken, und je ungünstiger die Zeichen in puncto genetischer Veranlagung stehen, desto härter müssen Sie arbeiten und desto früher müssen Sie damit beginnen. Genau wie bei Herz-Kreislauf-Erkrankungen brauchen wir einen langen Atem.
UNSER WIRKUNGSVOLLSTES MITTEL ZUR VORBEUGUNG VON GEISTIGEM VERFALL IST SPORTLICHE BETÄTIGUNG. Wir haben viel über Ernährung und den Stoffwechsel gesprochen, doch sportliche Betätigung scheint auf vielfache Weise (vaskulär, metabolisch) zur Erhaltung der Hirngesundheit beizutragen. In Teil III gehen wir noch ausführlicher darauf ein, doch sportliche Betätigung – und zwar ausgiebige – ist eine tragende Säule unseres Programms zur Alzheimer-Prävention.
Ich bin sehr optimistisch, dass wir in Zukunft noch viel mehr darüber in Erfahrung bringen, wie wir allen Formen der Demenz vorbeugen und sie behandeln können. Doch dafür sind harte Arbeit und Kreativität von den betreffenden Wissenschaftlern gefragt, beträchtliche Investitionen in neue Theorien und Ansätze sowie Mut von Patienten wie Stephanie, die sich mit diesem gefürchtetsten und rätselhaftesten der vier apokalyptischen Reiter des Alterns konfrontiert sehen.
Teil III
Kapitel 10
Taktisches Denken
Grundsätze für ein besseres Leben
Nimm an, was nützlich ist, lass weg, was unnütz ist,
und füge hinzu, was dein Eigenes ist.
Bruce Lee
Mitte des 19. Jahrhunderts beobachtete der französische Arzt Stanislas Tanchou, dass Krebserkrankungen in den schnell wachsenden Großstädten Europas immer häufiger auftraten. Die industrielle Revolution schritt rasant voran und veränderte die Gesellschaft in nie da gewesener Weise. Tanchou sah eine Verbindung zwischen beiden: »Offenbar nimmt der Krebs, wie der Wahnsinn, mit der Fortentwicklung der Zivilisation zu.«[231]
Damit war er seiner Zeit voraus. Letztlich wurden Krebserkrankungen neben Herz-Kreislauf-Erkrankungen, Typ-2-Diabetes, Demenz und einigen weiteren unter dem Begriff »Zivilisationskrankheiten« zusammengefasst, weil sie sich offensichtlich mit der Industrialisierung und Urbanisierung in Europa und den USA ausgebreitet hatten.
Das bedeutet nicht, dass Zivilisation etwas Schlechtes wäre und wir alle wieder als Jäger und Sammler leben sollten. Ich bin dankbar, in unserer modernen Welt leben zu dürfen, in der ich keine tödlichen Krankheiten, willkürliche Gewalt und Gesetzlosigkeit erdulden muss, so wie unsere Urahnen es über Jahrtausende mussten (und Menschen in vielen Teilen der Welt heute noch müssen). Doch auch wenn der moderne Lebensstil dazu beigetragen hat, unsere Lebenserwartung und unseren Lebensstandard zu erhöhen, schuf er doch auch Bedingungen, die unserer Langlebigkeit auf bestimmte Weise Grenzen setzen.
Heute stecken wir in dem Dilemma, dass sich unsere Umwelt in den letzten ein, zwei Jahrhunderten in praktisch jeder Hinsicht – Nahrungsversorgung und Ernährungsgewohnheiten, Aktivität, Struktur der sozialen Netzwerke – verändert hat, unsere Gene aber praktisch dieselben geblieben sind. Ein klassisches Beispiel dafür haben wir in Kapitel 6 kennengelernt, nämlich die veränderte Rolle, die Fructose in unserer Ernährung spielt. Unsere Urahnen konsumierten Fructose fast nur in Form von Obst und Honig; damals half sie dabei, Energie in Form von Fett zu speichern, um den Winter oder Zeiten des Nahrungsmangels zu überstehen. Die Fructose war unsere Freundin. Heute ist sie auf unserem Speiseplan übermäßig stark vertreten, und dies zu viel in flüssiger Form, was unseren Stoffwechsel und unsere Energiebilanz durcheinanderbringt. Wir können zu leicht viel mehr Fructose-Kalorien zu uns nehmen, als unser Körper vertragen kann.
Diese von uns geschaffene veränderte Umwelt ist potenziell toxisch – im Hinblick auf das, was wir essen (lang-, nicht kurzfristig),[232] wie (oder ob) wir uns bewegen, wie gut oder schlecht wir schlafen und wie sie sich auf unsere seelische Gesundheit auswirkt (etwa wenn wir ein paar Stunden in den sozialen Medien unterwegs waren). Sie ist für unser Genom, das Ergebnis unserer Evolution, so fremd wie, sagen wir einmal, es ein Flughafen für Hippokrates wäre. In Kombination mit unserer recht neu erworbenen Fähigkeit, einst lebensbedrohliche Epidemien, Verletzungen und Krankheiten zu überleben, bewirkt dies nahezu ein Außer-Kraft-Setzen der natürlichen Selektion. Unsere Gene und unsere Umwelt passen nicht mehr zusammen. Daher müssen wir klug und taktisch vorgehen, um uns dieser neuen Welt mit ihren Gefahren anzupassen und in ihr zu gedeihen.
Aus diesem Grund haben wir uns in den bisherigen Kapiteln dieses Buches mit unserem Ziel und unserer Strategie befasst. Wenn wir wissen wollen, was zu tun ist, müssen wir unsere Gegner in- und auswendig kennen, ungefähr so, wie Muhammad Ali George Foreman kannte. Inzwischen sollte uns unsere Strategie weitgehend vertraut sein – ich hoffe, Ihnen wenigstens einen Teil der biologischen Mechanismen nahegebracht zu haben, die dazu beitragen, uns für bestimmte Krankheiten anfällig zu machen, und ebenso die Art, wie diese Krankheiten voranschreiten.
Wenden wir uns nun unserer Taktik zu, den Mitteln und Methoden, mit denen wir in dieser seltsamen und manchmal gefährlichen neuen Umwelt navigieren wollen. Wie werden wir unsere alten Erwartungen überwinden und unsere besten Bonusdekaden (er-)leben? Welche konkreten Maßnahmen können wir ergreifen, um unser Risiko für Krankheit und Tod zu verringern und unsere Lebensqualität im Älterwerden zu verbessern?
Die Medizin 3.0 kennt fünf Gebiete, auf denen wir taktisch ansetzen können, um unsere Gesundheit zu beeinflussen. Der erste Ansatzpunkt ist das Gebiet von Bewegung bzw. Sport, welches meiner Ansicht nach das größte Potenzial, den größten Einfluss auf die Lebensspanne und die gesunde Lebenszeit hat. Natürlich hat Sport verschiedene Aspekte, darum betrachte ich die einzelnen Komponenten aerobe Effizienz, maximale Sauerstoffaufnahme (VO2max), Kraft und Stabilität, auf die ich später noch im Detail eingehen werde. Der zweite Ansatzpunkt ist die Ernährung, oder besser: die Biochemie der Ernährung. Der dritte Ansatzpunkt ist der Schlaf, dessen Bedeutung von der Medizin 2.0 bis vor relativ kurzer Zeit völlig unterschätzt wurde. Der vierte Ansatzpunkt umfasst verschiedene Werkzeuge und Techniken, um die emotionale Gesundheit zu beeinflussen und zu verbessern. Der fünfte Ansatzpunkt schließlich entspricht den verschiedenen Medikamenten, Nahrungsergänzungsmitteln und Hormonen, über die Wissen nicht nur im Medizinstudium vermittelt wird. Ich werfe diese allesamt in einen Topf mit der Bezeichnung exogene Moleküle, womit ich alle Wirkstoffmoleküle meine, die wir von außen aufnehmen.
In diesem Abschnitt werde ich nicht besonders auf andere exogene Moleküle eingehen wie auf jene, die ich bereits eingehend erwähnt habe (wie Lipidsenker, Rapamycin und Metformin, jenes Diabetesmedikament, das auf mögliche Langlebigkeitseffekte überprüft wird). Stattdessen liegt mein Schwerpunkt auf den anderen vier Ansatzpunkten, die allesamt im Medizinstudium und in den ersten Berufsjahren nicht wirklich abgedeckt, teils nicht einmal erwähnt wurden. Wir lernten praktisch nichts über Sport, Ernährung, Schlaf oder seelische Gesundheit. Das mag sich allmählich ändern, aber wenn heute Ärzte etwas von diesen Dingen wissen und Ihnen tatsächlich helfen können, dann wahrscheinlich deshalb, weil sie sich ihr Wissen selbst angeeignet haben.
Manche unserer Taktiken scheinen auf den ersten Blick naheliegend zu sein. Bewegung. Ernährung. Schlaf. Seelische Gesundheit. Natürlich wollen wir all das optimieren. Aber der Teufel (für mich eher: das Vergnügen) steckt im Detail. Auf welche Weise(n) sollten wir uns bewegen? Wie verbessern wir unsere Ernährung? Wie gelingt es uns, länger und besser zu schlafen?
In all diesen Fällen sind die groben Ziele zwar klar, die Einzelheiten und Nuancen aber nicht. Wir haben fast unendlich viele Möglichkeiten. Deshalb müssen wir exakt ermitteln, wie wir einen effektiven taktischen Plan entwickeln können – und wie es uns gelingt, unseren Kurs entsprechend zu ändern. Wir müssen mehr in die Tiefe gehen.
Was macht eine effektive Taktik aus?
Dies erkläre ich gern am Beispiel von Autounfällen, die auch eine kleine Obsession von mir sind. Viel zu viele Menschen aller Altersgruppen kommen bei Autounfällen ums Leben – in den USA laut National Highway Traffic Safety Administration alle zwölf Minuten einer –,[233] und ich glaube, dass viele dieser Todesfälle mit der richtigen Taktik vermeidbar wären.
Was können wir tun, um unser Risiko, hinter dem Steuer zu sterben, zu verringern? Und kann man Autounfälle überhaupt vermeiden, da sie sich doch offensichtlich zufällig ereignen?
Naheliegende Taktiken, die wir bereits kennen, sind: den Sicherheitsgurt anlegen, während der Fahrt keine Textnachrichten verschicken (was vielen offenbar schwerfällt), nicht fahren, wenn man Alkohol getrunken hat, denn Alkohol ist bei bis zu einem Drittel der Todesfälle im Straßenverkehr im Spiel. Statistiken zum Thema belegen auch, dass fast 30 Prozent der Todesfälle mit zu hoher Geschwindigkeit zusammenhängen. All dies sind hilfreiche Hinweise, aber weder überraschend noch besonders aufschlussreich.
Der erste Schritt hin zu einer guten Taktik besteht darin, sich Gefahrenpunkte bewusst zu machen. Ich war beispielsweise immer automatisch davon ausgegangen, dass Autobahnen die lebensgefährlichsten Fahrstrecken wären, weil dort hohe Geschwindigkeiten herrschen. Doch Jahrzehnte abdeckende Unfallstatistiken lassen erkennen, dass sich ein sehr hoher Anteil der Unfälle an Kreuzungen ereignet.[234] Wenn man als Autofahrer zu Tode kommt, dann meist durch ein anderes Auto, das von links (also der Fahrerseite) aufprallt, eine rote Ampel überfahren hat oder zu schnell unterwegs war. Meist erfolgt der Aufprall im rechten Winkel, und oft kommt der Fahrer zu Tode, der den Unfall nicht verursacht hat.
Die gute Nachricht ist, dass wir an Kreuzungen eine Wahl haben. Wir haben es in der Hand. Wir können entscheiden, ob und wann wir die andere Straße queren. Dies eröffnet die Möglichkeit für eine bestimmte Taktik, um Zusammenstöße auf einer Kreuzung zu vermeiden. Am gefährlichsten sind somit Autos, die (bei Rechtsverkehr) von links auf unsere Fahrerseite zukommen, daher sollten wir dieser Seite besondere Aufmerksamkeit schenken. Bei stark befahrenen Kreuzungen ist es also durchaus sinnvoll, nach links, nach rechts und wieder nach links zu schauen, falls man beim ersten Blick etwas übersehen hat. Ein Studienfreund von mir, der Fernfahrer mit einem großen Truck ist, bestätigt mir dies: Bevor er auf irgendeine Kreuzung fährt (selbst wenn er Vorfahrt oder grünes Licht hat), schaut er immer erst nach links, dann nach rechts, um genau diese Art Unfall zu vermeiden. Und wie gesagt, er sitzt dabei in einem großen LKW!
Dies ist eine spezifische, umsetzbare Taktik, die wir bei jeder Fahrt anwenden können. Auch wenn sie keine hundertprozentige Sicherheit bietet, senkt sie unser Risiko in zwar überschaubarem, aber doch nachweisbarem Maße. Überdies hat unsere Taktik eine Art Hebelwirkung: Mit relativ geringem Aufwand können wir das Risiko erheblich verringern.
Unseren Taktiken wollen wir uns auf ähnliche Weise nähern, indem wir vom Vagen, Allgemeinen kommend zu spezifischen, zielgerichteten Maßnahmen gelangen. Auf Daten gestützt und unserer Intuition folgend entscheiden wir, welche Ansatzpunkte wir wählen, und nutzen Feedback, um zu beurteilen, was funktioniert und was nicht. Scheinbar kleine Tricks können dabei im Laufe der Zeit signifikante Verbesserungen bewirken.
Meine Veranschaulichung am Beispiel Autounfälle mag etwas abwegig erscheinen, aber tatsächlich ist dies gar nicht so verschieden von der Lage, in der wir uns in unserem Streben nach einem langen Leben befinden. Das Auto ist in unserer Gesellschaft allgegenwärtig, eine Bedrohung von außen, mit der zu leben wir lernen müssen. Desgleichen müssen wir uns, um gesund älter zu werden, in einer Welt zurechtfinden können, in der sogar noch mehr Gefahren und Risiken für unsere Gesundheit lauern. In diesem dritten und letzten Abschnitt des vorliegenden Buches werden wir verschiedene Methoden erlernen, mit denen wir jene Risiken mindern oder eliminieren und unsere gesunde Lebenszeit verbessern und verlängern können – und wie sie bei den Patienten jeweils anzuwenden sind.
Die komplexesten taktischen Gebiete sind Ernährung sowie Sport und Bewegung. Nach meiner Beobachtung müssen die meisten Menschen auf beiden Gebieten Veränderungen vornehmen, und zwar recht massive. Bei der Aufnahme und Beurteilung neuer Patienten stelle ich stets drei Schlüsselfragen:
a)Sind sie über- oder unterernährt, nehmen sie also zu viele oder zu wenige Kalorien zu sich?
b)Sind sie zu schwach oder angemessen bemuskelt?
c)Ist ihr Stoffwechsel gesund oder nicht?
Wie nicht anders zu erwarten, gibt es große Überschneidungen zwischen der Gruppe der überernährten und derjenigen der metabolisch nicht gesunden Personen, doch ich hatte auch schon viele dünne Patienten mit Stoffwechselproblemen. Fast immer jedoch geht ein schlechter metabolischer Gesundheitszustand mit einer zu schwachen Bemuskelung einher, was auf den Zusammenhang zwischen Ernährung und Sport hindeutet.
Wir werden auf diese unterschiedlichen Konstellationen noch genauer eingehen; kurz gesagt verdeutlicht dies, warum es so wichtig ist, alle unterschiedlichen taktischen Maßnahmen miteinander zu koordinieren. Bei überernährten Patienten etwa wollen wir einen Weg finden, ihre Kalorienaufnahme zu reduzieren (dafür gibt es drei Möglichkeiten; mehr dazu in Kapitel 15). Sind sie jedoch auch zu schwach bemuskelt, was häufig der Fall ist, wollen wir überdies sicherstellen, dass sie weiterhin genügend Protein aufnehmen, denn das Ziel ist nicht der Gewichtsverlust, sondern der Verlust an Körperfett, gekoppelt mit Muskelaufbau. Eine oft komplizierte Angelegenheit.
Keiner unserer taktischen Ansatzpunkte lässt sich ganz von den anderen trennen. In Kapitel 16 etwa beschäftigen wir uns mit dem großen Einfluss von Schlaf auf unsere Insulinempfindlichkeit und unsere sportliche Leistungsfähigkeit (und übrigens auch auf unser seelisches Wohlbefinden). Bei den meisten Patienten widme ich daher ihrer Fitness und ihrer Ernährung viel Aufmerksamkeit, da beide eng miteinander verknüpft sind. Bei unseren Entscheidungen und der Entwicklung unserer Taktiken greifen wir auf viele Daten zurück, darunter statische Biomarker wie Blutfettgehalt und Leberfunktionswerte, dynamische Biomarker wie orale Glucosetoleranz sowie anthropometrische Daten, etwa zu Zusammensetzung des Körpers, Viszeralfettgewebe, Knochendichte und Muskelmasse.
Vieles von dem, was Sie im Folgenden lesen werden, spiegelt die Gespräche wider, die ich Tag für Tag mit meinen Patienten führe. Wir sprechen darüber, was sie erreichen wollen, und über die wissenschaftlichen Hintergründe unserer Strategie. Im Hinblick auf die jeweilige Taktik leite ich sie darin an, ihren eigenen Plan zu erarbeiten. So gut wie nie stelle ich ein Rezept aus, an das sie sich blind zu halten haben, denn ich möchte sie in die Lage bringen, dass sie selbst aktiv werden, um ihre Fitness, ihren Ernährungszustand, ihren Schlaf und ihre seelische Gesundheit zu verbessern. (Wie Sie sicher bemerkt haben, brauche ich für die meisten der beschriebenen Punkte auch gar kein Rezept.) Das Handeln selbst liegt dann in ihrer Verantwortung, und das ist selten leicht. Schließlich erfordert es, dass sie ihre Gewohnheiten ändern und an sich arbeiten.
Es folgt nun keineswegs ein Plan, an den man sich blind halten kann, denn es gibt keine Lösung, die für jeden Menschen passt. Sehr kleinteilige Anleitungen zu Bewegung, Ernährung oder Lebensführung erfordern individuelles und wiederholtes Feedback, etwas, das mit einem Buch nicht zu leisten ist. Ich erhoffe mir vielmehr, Ihnen einen Rahmen vermitteln zu können, der Ihnen hilft, sich besser zu bewegen und zu ernähren, besser zu schlafen und emotional gesünder zu werden; das wird Ihnen mehr helfen als eine lange und breite Anleitung dazu, wie viel Gramm von diesem oder jenem Makronährstoff jeder einzelne Erdenbewohner zu sich nehmen sollte. Meiner Überzeugung nach ist dies das Beste, was wir aktuell nach heutigem Stand der wissenschaftlichen Erkenntnis und nach meiner persönlichen klinischen Erfahrung (hier kommt die »Kunst« ins Spiel) tun können. Ich bin ständig dabei, herumzutüfteln, zu experimentieren und Dinge zu verändern, bei meiner eigenen Lebensführung und bei der meiner Patienten. Und meine Patienten tun dies selbst auch.
Wir sind an keinerlei spezifische Ideologie, Lehre oder Bezeichnungen gebunden. Wir sind weder »Keto« noch »Low Fat«, wir ziehen auch nicht aerobes Training dem Krafttraining vor oder umgekehrt. Wir haben einen breiten Ansatz und wählen und testen Taktiken, die hoffentlich die gewünschte Wirkung erzielen. So habe ich früher beispielsweise vielen meiner Patienten längere Phasen des Wasserfastens empfohlen und es auch selbst praktiziert. Inzwischen tue ich das nicht mehr, weil ich zu der Überzeugung gelangt bin, dass die Nachteile (die vor allem mit Muskelabbau und mangelnder Nährstoffversorgung zu tun haben) bei meinen Patienten – abgesehen von jenen, die stark überernährt sind – gegenüber seinem metabolischen Nutzen überwiegen. Wir passen unsere Taktiken im Hinblick auf unsere veränderten Bedürfnisse und nach neuestem wissenschaftlichem Kenntnisstand permanent an.
Unser einziges Ziel ist es, länger und besser zu leben – Outlive. Dafür müssen wir das Narrativ des Niedergangs, den so viele vor uns erduldet haben, überschreiben und einen Plan entwickeln, sodass jedes Lebensjahrzehnt ein bisschen besser wird als das davor.
Kapitel 11
Sport
Das wirksamste Mittel für ein langes Leben
Ich habe keinen einzigen Kampf im Ring gewonnen.
Ich habe sie alle in der Vorbereitung gewonnen.
Muhammad Ali
Vor einigen Jahren fragte mich mein Freund John Griffin per Mail, welche Art von Training er machen solle: mehr Kardio oder mehr Gewichte? Was ich empfehlen könnte? »Ich bin wirklich verwirrt von all dem widersprüchlichen Zeug«, schrieb er.
Für mich klang diese scheinbar einfache Frage wie ein Hilferuf. John ist ein intelligenter Mann mit messerscharfem Verstand, und doch war sogar er frustriert angesichts all der einander widersprechenden Ratschläge von »Experten«, die dieses oder jenes als den sichersten Weg zu vollendeter Gesundheit anpriesen. Er konnte einfach nicht herausfinden, was er im Fitnessstudio machen sollte und warum.
Das war, bevor ich wieder in Vollzeit als Mediziner arbeitete. Damals war ich noch tief in die Ernährungsforschung involviert, die womöglich noch verwirrender war als die Sportwissenschaft, voller widersprüchlicher Befunde und leidenschaftlich verfochtener Lehren, die mit fadenscheinigen Daten belegt waren. Sind Eier gut oder schlecht? Wie ist es mit Kaffee? Das Ganze trieb mich auch in den Wahnsinn.
Ich schrieb John eine Antwort – und schrieb und schrieb. Als ich auf »Versenden« klickte, hatte ich fast 2000 Wörter geschrieben, viel mehr als von ihm erbeten. Der arme Kerl wollte einfach nur eine kurze Antwort, kein Memorandum. Doch ich war nicht zu mehr zu bremsen. Später erweiterte ich den Text dieser E-Mail zu einem 10 000-Wörter-Manifest zur Langlebigkeit, aus dem schließlich das Buch entstand, das Sie gerade in Händen halten.[235]
Johns Frage hatte ganz klar etwas in mir ausgelöst. Nicht, dass ich ein leidenschaftlicher Verfechter von Krafttraining und gegen Ausdauertraining gewesen wäre oder umgekehrt. Ich reagierte auf die binäre Fragestellung. Falls Sie es noch nicht bemerkt haben: Ich schätze es überhaupt nicht, wie wir diese komplexen, nuancierten Fragen von entscheidender Bedeutung auf ein einfaches Entweder-oder reduzieren. Kardiotraining oder Gewichte? Low Carb oder pflanzenbasierte Ernährung? Olivenöl oder Rindertalg?
Ich weiß es nicht. Müssen wir uns denn wirklich für eins von beiden entscheiden?
Das Problem besteht, wie wir auch in den Ernährungskapiteln noch sehen werden, darin, dass wir offenbar alles in eine Art Religionskrieg über die einzig wahre Lehre verwandeln müssen. Manche Experten beharren darauf, dass Krafttraining dem Kardiotraining überlegen sei, doch ebenso viele behaupten, es sei genau andersherum. Dieser Streit ist endlos wie sinnlos, denn er opfert die Wissenschaft auf dem Altar der verschiedenen Interessen. Das Grundproblem ist, dass wir diese für das Leben so enorm wichtigen Gebiete – Bewegung bzw. Sport, aber auch Ernährung – viel zu detailliert betrachten. Es geht nicht darum, welcher Teil des Fitnessstudios Ihnen besser gefällt. Es geht um viel grundlegendere Fragen.
Sport kann mehr als alle anderen taktischen Ansatzpunkte, die wir in diesem Buch behandeln, darüber entscheiden, wie Sie den Rest Ihres Lebens leben werden. Zahllose Daten belegen, dass schon ziemlich wenig Bewegung Ihr Leben um mehrere Jahre verlängern kann. Bewegung bewirkt, dass praktisch alle chronischen Krankheiten später einsetzen, ist aber auch extrem effektiv darin, die gesunde Lebenszeit zu verlängern und zu verbessern. Bewegung kehrt nicht nur den körperlichen Verfall um, sondern kann auch den kognitiven Abbau verlangsamen oder sogar umkehren. (Zudem wirkt sie sich positiv auf die seelische Gesundheit aus, doch das ist schwieriger quantitativ zu erfassen.)
Sollten Sie sich also nach der Lektüre dieses Buches nur eine Art von neuen Gewohnheiten zulegen wollen, dann müssen Sie sich für das Gebiet der Bewegung entscheiden. Wenn Sie bereits Sport treiben, könnten Sie Ihr bisheriges Programm überdenken und modifizieren. Und wenn Bewegung bisher eher nicht Teil Ihres Lebens ist, sind Sie damit nicht allein – 77 Prozent der US-Bevölkerung geht es genauso.[236] Jetzt ist der richtige Augenblick, das zu ändern. Genau jetzt. Schon ein bisschen tägliche Aktivität ist viel besser, als nichts zu tun. Der Wechsel von null Sport auf wöchentlich gerade einmal 90 Minuten kann Ihr Risiko, aufgrund einer beliebigen Ursache zu sterben, bereits um 14 Prozent senken.[237] Das schafft wohl kaum ein Medikament.
Meine Antwort auf Fragen wie die, die mir mein Freund John Griffin gestellt hat, lautet also: ja und ja. Ja, Sie sollten mehr Kardio-training machen, und ja, Sie sollten mehr Gewichte stemmen.
Wenn Sie am anderen Ende des Spektrums stehen und, so wie ich selbst, seit dem Kindergartenalter Sport treiben, verspreche ich Ihnen, dass die in diesem Kapitel vorgestellten Erkenntnisse Ihnen dabei helfen werden, Ihr Programm besser zu strukturieren – nicht, um schneller einen Marathon zu laufen oder im Fitnessstudio mehr Eindruck zu schinden, sondern für ein längeres und besseres Leben, in dem Sie vor allem auch im höheren Alter körperlich aktiv bleiben können.
Die Erkenntnis, dass Bewegung gut für uns ist, ist ungefähr so neu wie die, dass Hühnersuppe uns guttut, wenn wir erkältet sind. Doch nur die wenigsten Menschen sind sich im Klaren darüber, welch grundlegende Effekte Sport tatsächlich hat. Eine Studie nach der anderen belegt, dass Menschen, die regelmäßig Sport treiben, bis zu einem Jahrzehnt länger leben als Menschen, die ihre Zeit vorwiegend sitzend verbringen.[238] Wer regelmäßig läuft oder Fahrrad fährt, lebt nicht nur meist länger, sondern erfreut sich auch besserer Gesundheit und zeigt eine geringere Morbidität aufgrund von Ursachen, die mit einer metabolischen Dysfunktion zu tun haben.[239] Und wer (noch) nicht regelmäßig Sport treibt, kann sich auch glücklich schätzen, denn die guten Wirkungen von Sport setzen ein, sobald man sich überhaupt bewegt – und sei es strammes Gehen –, und steigern sich dann.[240] So wie praktisch jede Ernährungsform einen großen Vorteil gegenüber der reinen Ernährung mit Fast Food birgt, ist praktisch jede Bewegung besser, als auf dem Sofa sitzen zu bleiben.
Meine Mitstudenten und ich lernten zwar so gut wie nichts über Sport und schon gar nicht, wie man ihn Patienten »verordnen« kann, doch die Medizin 2.0 erkennt zumindest seine Bedeutung an. Leider bleibt es fast immer bei dem allgemeinen Rat, sich mehr zu bewegen und weniger herumzusitzen. Die Empfehlungen der US-Regierung zur körperlichen Bewegung lauten dahingehend, dass »aktive Erwachsene« fünfmal wöchentlich mindestens 30 Minuten lang (oder insgesamt 150 Minuten) einer »aeroben Aktivität von moderater Intensität« nachgehen sollten.[241] Das soll noch durch Krafttraining an zwei Tagen in der Woche ergänzt werden, wobei »alle größeren Muskelgruppen« beansprucht werden sollten.
Man stelle sich vor, Ärzte würden sich bei der Krebsbehandlung genauso vage ausdrücken:
ARZT: »Frau Schmidt, ich muss Ihnen leider mitteilen, dass Sie Dickdarmkrebs haben.«
FRAU SCHMIDT: »Das ist ja furchtbar, Herr Doktor. Was soll ich machen?«
ARZT: »Sie brauchen eine Chemotherapie.«
FRAU SCHMIDT: »Was für eine Chemotherapie? Welche Dosierung? Wie oft? Wie lange? Was gibt es für Nebenwirkungen?«
ARZT: (Zuckt die Achseln.)
Wir benötigen exaktere Anleitungen, um unsere Ziele auf effektive, sichere Art zu erreichen. Zunächst einmal aber möchte ich darauf eingehen, warum Sport so wichtig ist, denn die Datenlage ist in meinen Augen rundum überzeugend. Wenn ich meinen Patienten die Daten präsentiere, sind sie selten überrascht von der Tatsache, dass aerobe (kardiorespiratorische) Fitness und Kraft mit einer längeren Lebensspanne und gesunden Lebenszeit assoziiert sind – aber wie stark die positive Wirkung ist, das überrascht sie durchaus. Die Daten zum Sport zeigen klipp und klar, dass wir umso mehr profitieren, je mehr wir uns bewegen.
Beginnen wir mit der kardiorespiratorischen oder aeroben Fitness. Sie steht dafür, wie effizient unser Körper Sauerstoff in die Muskeln transportieren und wie effizient die Muskeln diesen Sauerstoff aufnehmen können, damit wir längere Strecken laufen (oder gehen), mit dem Rad fahren oder schwimmen können. Im Alltag zeigt sie sich als unsere körperliche Kondition. Je größer unsere kardiorespiratorische Fitness, desto mehr Energie haben wir für jegliche Aktivität, der wir gern nachgehen – und wenn es Shopping ist.
Wie sich zeigt, ist die maximale kardiorespiratorische Fitness, angegeben als VO2max, der vielleicht aussagekräftigste Marker für Langlebigkeit.[242] VO2max steht für die maximale Sauerstoffaufnahme, zu der eine Person in der Lage ist. Sie wird gemessen, während diese Person Sport an ihrer körperlichen Belastungsgrenze treibt. (Wenn Sie diesen Test schon einmal absolviert haben, wissen Sie, wie unangenehm das ist.) Je mehr Sauerstoff unser Körper nutzen kann, desto höher der VO2max-Wert.
Unser Körper hat eine bemerkenswerte Fähigkeit, auf Anforderungen zu reagieren. Angenommen, ich sitze einfach nur auf dem Sofa und schaue einen Film. In Ruhe braucht eine Person meiner Größe rund 300 Milliliter Sauerstoff pro Minute, um genügend ATP (Adenosintriphosphat, der »Treibstoff« in unseren Zellen) für die lebenserhaltenden physiologischen Prozesse und das Filmgucken zu bilden. Das ist ein recht niedriger Energiebedarf. Gehe ich aber nach draußen und laufe eine Runde in meinem Viertel, steigt der Energiebedarf rasant an. Meine Atmung und Herzfrequenz beschleunigen sich, damit ich mehr Sauerstoff aus meiner Umgebung aufnehmen und nutzen kann und meine Muskeln arbeiten können. Bei solcher Bewegungsintensität braucht ein Mensch meiner Größe 2500 bis 3000 Milliliter Sauerstoff pro Minute, also das Acht- bis Zehnfache des Bedarfs beim Filmgucken auf dem Sofa. Laufe ich nun einen Hügel so schnell hinauf, wie ich kann, steigt der Sauerstoffbedarf meines Körpers noch einmal auf 4000, 4500 oder gar 5000 Milliliter an, je nachdem, wie schnell und wie fit ich bin. Je besser mein Trainingszustand, desto mehr Sauerstoff kann ich nutzen, um ATP zu bilden, und desto schneller kann ich den Hügel hinauflaufen.
Irgendwann erreiche ich den Punkt, an dem ich über aerobe Stoffwechselwege keine weitere Energie mehr bilden kann. Dann bin ich gezwungen, auf weniger effiziente, weniger nachhaltige Wege der Energiebildung umzuschalten, so wie beim Sprint. Die Menge Sauerstoff, die ich bei dieser Maximalbelastung nutze, entspricht meinem VO2max-Wert. (Bei anhaltender Belastung werden meine Kräfte dann bald »versagen«, ich kann dann also den Hügel nicht weiter in diesem Tempo hinauflaufen.) Der VO2max-Wert wird meist als das von einer Person nutzbare Sauerstoffvolumen pro Kilogramm Körpergewicht pro Minute angegeben. Ein durchschnittlich trainierter, fünfundvierzig Jahre alter Mann hat einen VO2max-Wert von rund 40 ml/kg/min, ein Hochleistungs-Ausdauersportler dagegen hat einen Wert, der auf siebzig zugeht oder noch darüber liegt. Eine untrainierte Person über dreißig oder über vierzig wiederum schafft vielleicht nur einen Wert knapp unter 30, so Mike Joyner, Sportphysiologe und -wissenschaftler der Mayo Clinic in Rochester. Diese Personen kämen den Hügel gar nicht hinauf.[243] Je höher jemandes VO2max-Wert ist, desto mehr Sauerstoff kann der oder die Betreffende aufnehmen und für die ATP-Bildung nutzen und desto schneller kann die Person fahren oder laufen, kurz: desto mehr kann sie leisten.
Dieser Wert ist nicht nur für Sportler relevant, sondern korreliert, wie sich gezeigt hat, stark mit der Langlebigkeit. Wie eine 2018 im Journal of the American Medical Association (JAMA) veröffentlichte Studie ergab, die mehr als 120 000 Personen beobachtet hatte, war ein höherer VO2max-Wert (gemessen auf dem Laufband) mit einer durchweg geringeren Mortalität korreliert.[244] Die Personen mit der größten Fitness zeigten die geringste Mortalitätsrate, und zwar überraschend deutlich. Ein Beispiel: Eine Person, die raucht, hat eine um 40 Prozent höhere Gesamtmortalität (also das Risiko, zu einem beliebigen Zeitpunkt zu sterben) als jemand, der nicht raucht, was einer Hazard Ratio von 1,40 entspricht. (Hazard bezeichnet die Inzidenzdichte, in diesem Fall die aktuelle Sterberate einer Personengruppe. Die Hazard Ratio oder HR besagt, um wie viel höher die Sterberate in der einen Gruppe ist als in der anderen.) Die Studie ergab, dass Personen, die einen für ihr Alter und ihr Geschlecht unterdurchschnittlichen (also zwischen dem 25. und dem 50. Perzentil angesiedelten) VO2max-Wert aufweisen, eine doppelt so hohe Gesamtmortalität haben wie Personen im oberen Quartil (im Bereich zwischen dem 75. und 97,6. Perzentil). Eine geringe kardiorespiratorische Fitness birgt also ein größeres relatives Sterberisiko als das Rauchen.[245]
Und das ist nur der Anfang. Eine Person im unteren Quartil der VO2max-Werte (also im Bereich der 25 Prozent mit der geringsten Fitness) hat ein fast viermal so hohes Sterberisiko wie jemand im oberen Quartil – und ein fünfmal höheres als jemand mit einem VO2max-Höchstwert (im Bereich der obersten 2,3 Prozent).[246] Das ist durchaus erstaunlich. Die Vorteile beschränken sich zudem keineswegs nur auf die Personen mit der größten Fitness; schon ein Aufstieg vom unteren Quartil auf den Bereich zwischen dem 25. und dem 50. Perzentil (also von der geringsten Fitness zu einer unterdurchschnittlichen Fitness) bedeutet eine annähernde Halbierung des Sterberisikos, so das Ergebnis dieser Studie.
Eine viel umfangreichere und neuere Studie bestätigte diese Befunde.[247] Sie wurde 2022 im Journal of the American College of Cardiology veröffentlicht und fußte auf der Auswertung von Daten von 750 000 Veteranen der US-Armee im Alter von dreißig bis fünfundneunzig Jahren (siehe Abbildung 9). Dies war eine ganz andere Studienpopulation, die beide Geschlechter und alle Bevölkerungsgruppen umfasste; dennoch kamen die Forscher zu einem fast identischen Ergebnis: Jemand, dessen Fitness in den unteren 20 Prozent angesiedelt ist, hat ein 4,09-mal höheres Sterberisiko als eine Person in den obersten zwei Prozent ihrer Alters- und Geschlechtergruppe. Selbst eine Person mit moderater Fitness (40. bis 60. Perzentil) hat immer noch eine mehr als doppelt so hohe Gesamtmortalität wie die Gruppe mit maximaler Fitness, so das Ergebnis dieser Studie. »Fehlende Fitness barg ein größeres Risiko als alle Herz-Kreislauf-Risikofaktoren, die untersucht wurden«, so die Autoren.
Natürlich gibt es hier, wie bei praktisch allen Beobachtungsstudien, mit Sicherheit manche Störfaktoren, darunter auch die Ernährung. Doch mindestens fünf Faktoren[248] tragen dazu bei, dass ich zumindest auf eine teilweise Kausalität in diesem Zusammenhang vertraue.
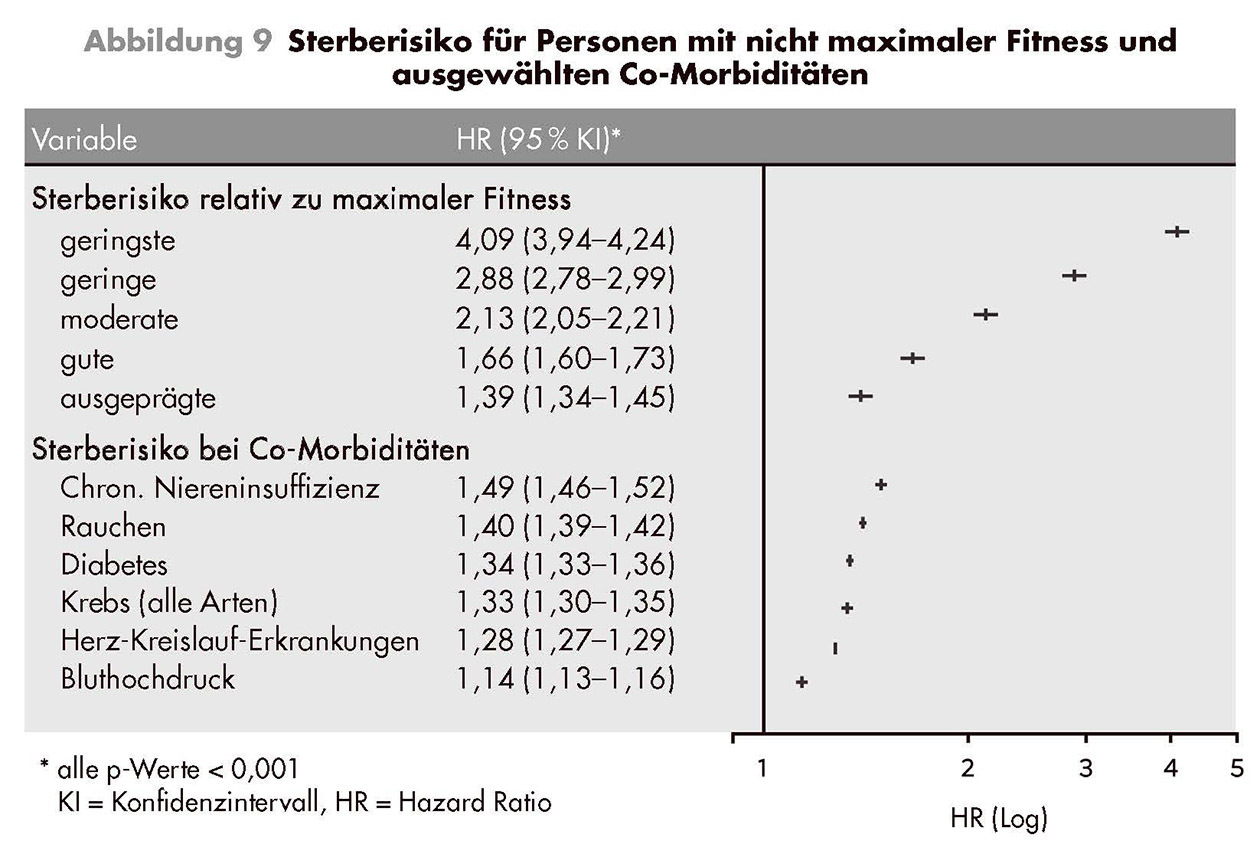
Die Tabelle gibt das Gesamtsterberisiko für unterschiedliche Fitnesszustände im Vergleich zu Individuen in den obersten zwei Prozent der VO2max-Werte ihrer Alters- und Geschlechtsgruppe (»maximale Fitness«) wieder (oben) sowie bei verschiedenen Co-Morbiditäten, also den Vergleich von Personen mit den und ohne die angegebenen Krankheiten (unten). Die Fitnesszustände sind in Perzentilgruppen eingeteilt: geringste (< 20. Perzentil), geringe (21.–40. Perzentil), moderate (41.–60. Perzentil), gute (61.–80. Perzentil) und ausgeprägte Fitness (81.–97. Perzentil).
Quelle: Kokkinos et al. (2022)
Zunächst einmal ist die Stärke des Effekts sehr ausgeprägt. Zum Zweiten sind die Daten konsistent, und es besteht eine Reproduzierbarkeit über zahlreiche Studien mit unterschiedlichsten Populationen. Drittens gibt es eine dosisabhängige Reaktion (je größer Ihre Fitness, desto länger leben Sie). Viertens hat dieser Effekt über die bekannten Wirkungen von Bewegung bzw. Sport auf die Lebensspanne und die gesunde Lebenszeit eine hohe biologische Plausibilität. Und als fünfter Faktor weisen praktisch alle Daten aus Experimenten zu Sport beim Menschen darauf hin, dass dieser die Gesundheit fördert.
Die Autoren der JAMA-Studie folgerten: »Kardiorespiratorische Fitness korreliert negativ mit der Langzeitmortalität, ohne dass eine Obergrenze des positiven Einflusses beobachtet wurde [meine Kursivierung]. Eine maximale aerobe Fitness war mit den größten Überlebensraten assoziiert.«[249]
Aus diesen Daten kann ich nicht die Aussage ableiten, dass ein hoher VO2max-Wert allein Ihren Bluthochdruck oder Ihre Rauchgewohnheiten ausgleichen wird, so sehr die genannten Hazard Ratios dies auch nahelegen. Ohne randomisierte kontrollierte Studien kann ich mir zwar nicht sicher sein, aber ich bezweifle es irgendwie. Was ich jedoch sagen kann, ist, dass mit sehr hoher Gewissheit ein höherer VO2max-Wert für Ihre allgemeine Gesundheit und Lebenserwartung besser ist als ein niedriger VO2max-Wert. Punkt.
Eine für unser Anliegen noch bessere Nachricht ist, dass sich der VO2max-Wert durch Training vergrößern lässt. Wir können dieses Maß für unsere Fitness sehr stark beeinflussen, wie wir noch erfahren werden.
Die starke Assoziation zwischen kardiorespiratorischer Fitness und Langlebigkeit ist schon lange bekannt. Es dürfte Sie aber (wie mich auch) überraschen zu erfahren, dass die Muskulatur fast ebenso stark mit einem längeren Leben korreliert. Eine über zehn Jahre laufende Beobachtungsstudie mit rund 4500 Testpersonen im Alter von fünfzig Jahren an aufwärts ergab, dass diejenigen mit einer geringen Muskelmasse über die Studiendauer ein 40 bis 50 Prozent höheres Mortalitätsrisiko hatten als die Kontrollgruppe.[250] Wie die weitere Analyse zeigte, ist es nicht die reine Muskelmasse, die zählt, sondern vielmehr die Stärke dieser Muskeln, ihre Fähigkeit, Kraft zu entwickeln. Es genügt also nicht, im Fitnessstudio Muskelpakete aufzubauen – die Muskeln müssen auch stark sein. Sie müssen imstande sein, Kraft zu entwickeln. Versuchspersonen mit geringer Muskelkraft hatten ein doppelt so hohes Sterberisiko; solche mit geringer Muskelmasse und/oder Muskelkraft plus metabolischem Syndrom hatten eine 3- bis 3,33-mal höhere Gesamtmortalität.
Die Muskelkraft könnte sogar die kardiorespiratorische Fitness übertrumpfen, das legt zumindest eine Studie nahe.[251] Die Forscher begleiteten eine Gruppe von nahezu 1500 Männern im Alter von 40 Jahren an aufwärts über einen Zeitraum von durchschnittlich 18 Jahren. Ein Ergebnis war, dass ein Mann, dessen kardiorespiratorische Fitness in den unteren 50 Prozent, dessen Muskelkraft aber im oberen Drittel der Gruppe angesiedelt war, immer noch ein um 48 Prozent niedrigeres Gesamtmortalitätsrisiko hatte als das bezüglich Muskelkraft untere Drittel der Gruppe.[252]
Es gilt praktisch dasselbe wie beim VO2max-Wert: Je größer Ihre Fitness, desto geringer Ihr Sterberisiko. Auch hier kann keine andere Behandlung, ob medikamentös oder sonst wie, einen ähnlichen Nutzen erzielen. Sport ist derart wirksam gegen Alterskrankheiten – die apokalyptischen Reiter –, dass er oft mit Medizin verglichen wird.
John Ioannidis, ein Stanford-Forscher mit der Neigung zu provokanten Fragen, beschloss, diese Metapher auf ihre Richtigkeit zu überprüfen, und verglich Studien zur Wirkung von Sport mit solchen zur Wirkung von Medikamenten.[253] Dabei fand er heraus, dass bei zahllosen randomisierten klinischen Studien Behandlungen auf sportlicher Basis genauso gut oder besser abschnitten als zahlreiche pharmazeutische Wirkstoffgruppen, wenn es um die Absenkung der Mortalität durch koronare Herzkrankheit,[254] Prädiabetes oder Diabetes sowie Schlaganfall ging.
Das Beste an der Sache: Sie brauchen sich Sport nicht vom Arzt verschreiben zu lassen.
Der Effekt geht, so glaube ich, größtenteils auf eine verbesserte Mechanik zurück: Sport stärkt das Herz und unterstützt somit das Herz-Kreislauf-System. Wie wir in diesem Kapitel noch erfahren werden, verbessert er auch die Gesundheit der Mitochondrien, jener unersetzlichen Organellen, die in unseren Zellen (unter anderem) Energie zur Verfügung stellen. Das wiederum verbessert unsere Fähigkeit zur Verstoffwechselung von Glucose und Fett. Mehr Muskelmasse und stärkere Muskeln stützen und schützen den Körper; außerdem erhalten sie die Stoffwechselgesundheit, weil die Muskeln Energie effizient verbrauchen. Die Liste ließe sich noch beliebig verlängern, aber in Kürze ausgedrückt hilft Sport der »Maschine« Mensch dabei, längere Zeit viel besser zu funktionieren.
Biochemisch betrachtet wirkt Sport durchaus wie ein Medikament. Um genauer zu sein: Er bringt den Körper dazu, eigene (endogene) Wirkstoffe zu produzieren. Wenn wir Sport treiben, bilden unsere Muskeln sogenannte Zytokine, die als Signale an andere Körperteile dienen und dazu beitragen, unser Immunsystem zu stärken und das Muskel- und Knochenwachstum anzuregen. Ausdauertraining wie Laufen oder Radfahren fördert die Bildung eines weiteren wirksamen Moleküls, des Wachstumsfaktors BDNF (Brain-derived neurotrophic factor), der die Gesundheit und Funktion des Hippocampus unterstützt.[255] Dieser Teil des Gehirns spielt eine essenzielle Rolle für das Gedächtnis. Sport fördert zudem die Blutgefäßversorgung des Gehirns,[256] und er kann zum Erhalt des Hirnvolumens beitragen. Darum ist Sport für mich ein besonders wichtiger Teil der Behandlung von Patienten mit dem Risiko, eine Alzheimerkrankheit zu entwickeln – so wie Stephanie, die Frau mit den Alzheimer-Hochrisikogenen, die wir in Kapitel 9 kennengelernt haben.
Die Daten, welche die Wirksamkeit von Bewegung bzw. Sport hinsichtlich der Lebensspanne aufzeigen, sind so unwiderlegbar wie nur irgendetwas in der Humanbiologie. Ich glaube jedoch, dass Sport noch effektiver darin ist, die Lebensspanne zu bewahren, als sie zu verlängern. Hierfür gibt es weniger belastbare Beweise, aber ich denke, dass Sport genau hier seine magische Wirkung zeigt, wenn er richtig praktiziert wird. Meinen Patienten jedenfalls sage ich, dass sich Sport selbst dann, wenn er das Leben um ein Jahr verkürzen würde (was er ganz klar nicht tut), lohnen würde, weil er das Leben besonders im mittleren und höheren Alter so sehr verbessert.
Eines der wichtigsten Anzeichen des Alterns ist das Nachlassen der körperlichen Leistungsfähigkeit. Unsere kardiorespiratorische Fitness geht aus verschiedenen Gründen zurück, unter anderem durch ein geringeres Herzzeitvolumen, das vor allem auf eine geringere maximale Herzfrequenz zurückgeht. Wir büßen mit jedem Lebensjahrzehnt an Kraft und Muskelmasse ein, unsere Knochen werden brüchiger, unsere Gelenke weniger beweglich und unser Gleichgewichtssinn lässt nach, eine Tatsache, die vielen dann bewusst wird, wenn sie von einer Leiter stürzen oder am Bordstein ins Straucheln kommen.
Dieser Prozess geht, um Hemingway zu zitieren, auf zwei Arten vor sich: erst allmählich, dann plötzlich. Tatsächlich setzt das Alter unserem Körper stark zu. Längs- und Querschnittstudien ergaben, dass fettfreie Körpermasse (die größtenteils der Muskelmasse entspricht) und Aktivitätslevel vom dritten und vierten Lebensjahrzehnt bis ins mittlere Alter relativ konstant bleiben.[257] Etwa ab dem fünfundsechzigsten Lebensjahr jedoch lassen die körperliche Aktivität und die Muskelmasse rasant nach; noch stärker ist der Abbau etwa nach dem fünfundsiebzigsten Lebensjahr. Es ist so, als fielen die Leute irgendwann mit Mitte siebzig einfach von einer Klippe.
Im Alter von achtzig Jahren hat ein Durchschnittsmensch acht Kilogramm Muskelmasse weniger als zu Spitzenzeiten. Personen, die aktiver bleiben, verlieren weniger Muskulatur, durchschnittlich nur drei bis vier Kilogramm. Zwar sind die Ursächlichkeiten hier nicht ganz eindeutig, doch ich vermute, dass sie in zwei Richtungen gehen: Die Menschen sind weniger aktiv, weil sie schwächer sind, und sie sind schwächer, weil sie weniger aktiv sind.
Anhaltender Muskelschwund und Inaktivität sind für uns buchstäblich lebensbedrohlich. Senioren mit der geringsten Muskelmasse (oder fettfreien Körpermasse) haben das höchste Gesamtmortalitätsrisiko. Eine chilenische Studie untersuchte rund 1000 Männer und 400 Frauen, die bei Studienbeginn ein durchschnittliches Alter von vierundsiebzig Jahren hatten.[258] Die Forscher teilten die untersuchten Personen je nach ihrer appendikulären fettfreien Körpermasse (technisch betrachtet der Muskelmasse ihrer Extremitäten, normalisiert auf die Körpergröße) in Quartile auf und beobachteten sie über den Studienverlauf. Nach zwölf Jahren waren nahezu 50 Prozent der Personen im untersten Quartil gestorben, jedoch nur 20 Prozent der Personen aus dem obersten Quartil für fettfreie Körpermasse. Zwar lässt sich allein daraus keine Kausalität ableiten, doch die Ausgeprägtheit und Reproduzierbarkeit von Befunden wie diesen deuten darauf hin, dass dies mehr ist als eine bloße Korrelation. Muskeln helfen uns im Alter beim Überleben.
Auch dies ist also ein Gebiet, auf dem sich Lebensspanne und gesunde Lebenszeit weit überschneiden. Ich vermute nämlich, dass eine größere Muskelmasse den Tod genau deshalb hinauszögert, weil sie auch die gesunde Lebenszeit verlängert. Darum lege ich so viel Wert darauf, unsere Skelettmuskulatur (die ich in Ermangelung eines besseren Begriffs als »Exoskelett« à la Terminator bezeichne) zu erhalten.
Ihr »Exoskelett« (die Muskulatur) hält Ihr eigentliches Skelett (die Knochen) aufrecht und intakt. Mehr Muskelmasse im »Exoskelett« scheint Sie vor allen möglichen Übeln zu bewahren,[259] sogar vor ungünstigen Verläufen nach einer Operation. Vor allem aber korreliert sie stark mit einem niedrigeren Sturzrisiko,[260] einer bedeutenden, aber oft übersehenen Ursache für Todesfälle und körperliche Einschränkungen im Alter. Wie Abbildung 10 zeigt, sind Stürze die bei Weitem häufigste Ursache von tödlichen Unfällen bei Personen ab fünfundsechzig Jahren – und da sind jene noch gar nicht mitgezählt, die drei oder sechs oder zwölf Monate nach ihrem nicht tödlichen, aber schwerwiegenden Sturz versterben, der bei ihnen einen langen und schmerzhaften Niedergang eingeleitet hat. Laut der US-Gesundheitsbehörde CDC werden alljährlich 800 000 ältere Personen aufgrund von Stürzen ins Krankenhaus eingeliefert.[261]
Ich vermute, dass diese Assoziation in beide Richtungen wirkt: Eine Person mit mehr Muskelmasse wird mit geringerer Wahrscheinlichkeit stürzen und sich verletzen, während jene, die aus anderen Gründen ein geringes Sturzrisiko haben (besserer Gleichgewichtssinn, besseres Körperbewusstsein), durch den Erhalt ihrer Muskelmasse ebenfalls eine bessere Zeit haben werden. Muskelatrophie und Sarkopenie (altersbedingter Muskelabbau) dagegen erhöhen unser Risiko, zu stürzen und womöglich eine Operation zu benötigen, und verschlechtern zugleich unsere Aussicht, besagte Operation ohne Komplikationen zu überleben.[262] So wie beim VO2max-Wert ist es wichtig, die Muskelmasse um jeden Preis zu erhalten.
Sport in all seinen Varianten ist unsere mächtigste Waffe im Kampf gegen dieses Elend und das allgemeine Risiko zu sterben. Er verlangsamt den Verfall, nicht nur den physischen, sondern denjenigen hinsichtlich aller drei Vektoren der gesunden Lebenszeit, also auch der kognitiven und seelischen Gesundheit. Eine neuere Studie mit älteren Erwachsenen in Großbritannien ergab, dass jene, die schon am Beginn der Studie eine Sarkopenie zeigten, ein Jahrzehnt später mit fast sechsmal höherer Wahrscheinlichkeit über eine schlechte Lebensqualität berichteten als jene, die mehr Muskelmasse bewahrt hatten.[263]
Genau dies wollen wir vermeiden. Und wir können es vermeiden – mithilfe jener machtvollen »Medizin« namens Sport, die auf wundersame Weise die Lebensspanne verlängert und die gesunde Lebenszeit verbessert. Allerdings erfordert er mehr Anstrengung und Wissen als das bloße Einnehmen einer Pille. Je mehr wir jedoch zu unternehmen gewillt sind, desto mehr werden wir in der Zukunft davon profitieren.
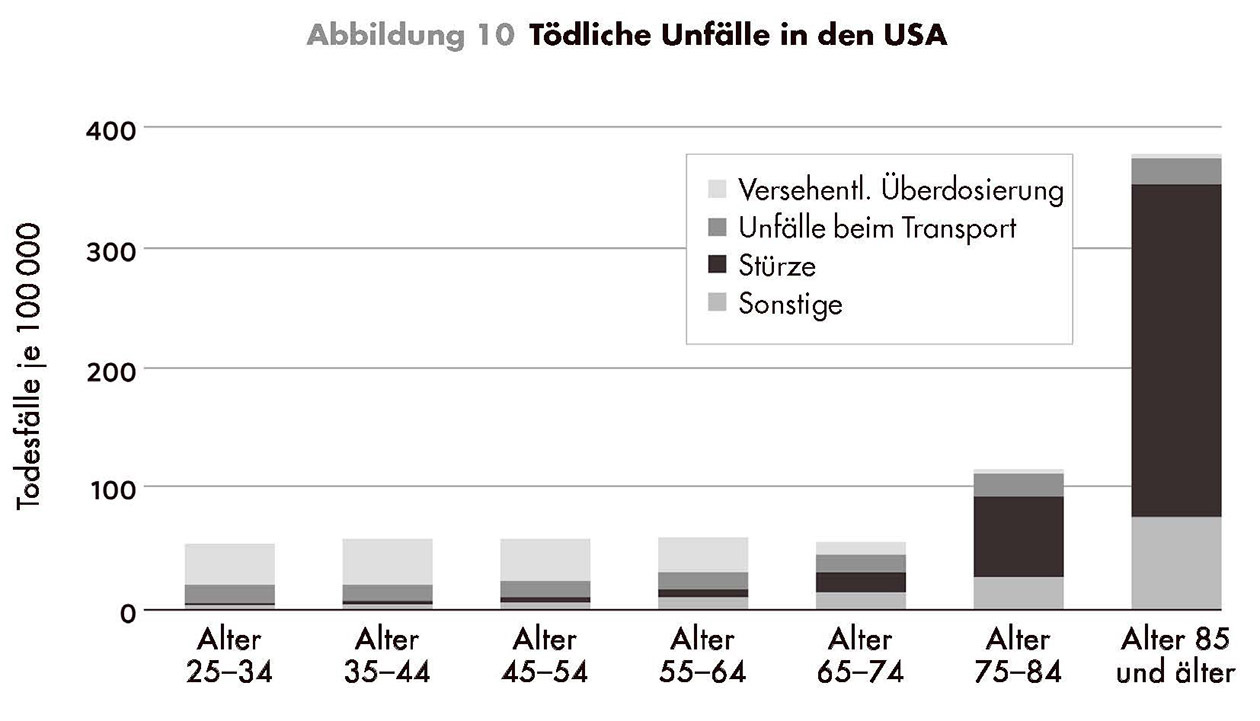
Quelle: CDC (2021)
Darum lege ich so viel Wert auf Training mit Gewichten – ab sofort, egal, wie alt Sie sind. Es nie zu spät, damit anzufangen; meine Mutter begann erst mit siebenundsechzig Jahren damit, und es hat ihr Leben verändert. Dutzende von Studien belegen, dass Krafttrainingsprogramme die Mobilität und körperlichen Funktionen von fettleibigen Testpersonen signifikant verbessern können;[264] Gleiches gilt für Personen, die sich von einer Krebstherapie erholen,[265] und sogar für solche, die bereits älter und fragiler sind.[266] Darum finde ich stets einen Weg, um viermal die Woche schwere Gewichte zu heben, ganz gleich, welcher Art, was ich gerade mache oder wo ich gerade bin.
Von der Medizin 2.0 gibt es im Hinblick auf Sport kaum mehr als Lippenbekenntnisse. Hat Ihre Ärztin schon einmal geprüft, wie stark Sie zupacken können, oder Sie explizit nach Ihrem Krafttraining gefragt? Kennt Ihr Arzt Ihren VO2max-Wert? Oder hat er Trainingsvorschläge zu dessen Verbesserung gemacht? Ich vermute, dass Sie alle Fragen mit einem klaren Nein beantworten können, denn so gut wie nichts von dem, was wir hier oder in den Kapiteln zum Thema Ernährung beschreiben, wird (zumindest im US-Gesundheitssystem) als »medizinische Behandlung« eingestuft. Zwar bieten viele Krankenkassen Zuschüsse oder Bonuspunkte für den Besuch von Fitnesskursen und Ähnlichem, aber ein angemessener Fokus auf diesen Ansatzpunkten, wie wir alle (mich eingeschlossen) ihn meiner Meinung nach brauchen, ist bei den meisten Medizinern nicht zu finden.
Erst nachdem wir uns eine Verletzung zugezogen haben oder so schwach geworden sind, dass wir womöglich auf die Hilfe anderer angewiesen sind, kommen wir in den Genuss einer Physiotherapie oder Rehabilitationsmaßnahme. Betrachten Sie also das, was ich auf den folgenden Seiten beschreibe, als eine »Prähabilitation« – als eine Physiotherapie, bevor Sie sie nötig haben.
Wenn ich mit meinen Patienten über Sport spreche, erzähle ich Ihnen oft von Sophie, der Mutter meiner Freundin Becky, die wir in Kapitel 3 kennengelernt haben. Sie war stets relativ aktiv gewesen, auch als Rentnerin. Sie spielte ein- oder zweimal die Woche Golf und arbeitete fast jeden Tag in ihrem Garten. Es war kein strukturiertes »Übungsprogramm«; sie machte einfach das, was ihr Freude bereitete. Dann jedoch verletzte sie sich erst die Schulter, dann das Knie, und beides erforderte eine Operation. Selbst nach den Eingriffen erholte sie sich nicht wieder vollständig. Ihre Aktivität kam nahezu zum Erliegen. Wie mir Becky berichtete, saß ihre Mutter meist im Haus herum und war niedergeschlagen. Schon bald setzte bei ihr der kognitive Verfall ein.
Als ich bei ihrer Beerdigung saß, dachte ich darüber nach und wurde unglaublich traurig. Doch ihre Geschichte war nur eine von vielen dieser Art. Wir alle haben wohl ältere Freunde und Verwandte, bei denen es ähnlich lief, die langsam (oder auch rasch) dahinschwächelten, bis sie keine Freude mehr an den Dingen empfanden, die sie einst liebten. Was hätte man tun können, so fragte ich mich, um Sophies Schicksal abzuwenden?
Hätte sie einfach mehr »Sport« treiben müssen? Ins Fitnessstudio gehen und den Crosstrainer benutzen? Hätte sie das retten können?
Es war nicht klar, dass die Antwort so einfach war. Ich hatte in meinem Leben jede Menge Sport getrieben, doch zur Zeit von Sophies Beerdigung pflegte ich selbst einige Wehwehchen, die sich im Laufe der Jahre eingestellt hatten. So fit ich auch sein mochte, es war durchaus nicht klar, dass ich auf einem besseren Weg war als Sophie.
Die meiste Zeit meines Lebens war ich ziemlich auf meine Fitness erpicht, wobei ich mich immer auf eine bestimmte Sportart fokussierte und diese unweigerlich auf die Spitze trieb. Nachdem ich mich beim Boxen, Laufen und schließlich Freiwasserschwimmen (Langstreckenschwimmen) verausgabt hatte, wandte ich mich dem Radfahren zu. Und ich ging gleich in die Vollen: Mein oberstes Ziel war es, das örtliche Zeitfahren zu gewinnen, ein 20-Kilometer-Einzelrennen, für das sich praktisch niemand interessierte. Ich verbrachte Stunden damit, Daten zu analysieren und meinen Luftwiderstand zu berechnen, denn ich wollte mein Ergebnis mithilfe von idiotischen Modellen, die ich in Excel konstruierte, um kostbare Sekunden verbessern.
In Wahrheit war ich für alles andere, außer über 20 Kilometer so schnell wie möglich in die Pedale zu treten, fast gar nicht mehr zu gebrauchen. Ich hatte einen hohen VO2max-Wert und konnte über die Pedale viel Kraft entwickeln, aber ich war nicht wirklich kräftig oder beweglich, und mein Gleichgewicht und meine Stabilität waren nicht besonders gut. Ich war ein eindimensionaler Athlet, und wenn ich dabei geblieben wäre, wäre meine Wirbelsäule womöglich in der Haltung verwachsen, die ich beim Zeitfahren einnahm, sodass ich zwar immer noch Rad fahren, aber (vor allem mit dem Oberkörper) ansonsten nichts Nützliches hätte anstellen können. Letztlich gab ich den Radrennsport auf, denn mir wurde klar, dass dieses obsessive Herangehen bei praktisch jeder Aktivität nicht haltbar war. Wie viele alte Marathonläufer kennen Sie, die noch aktiv sind? Wahrscheinlich nicht allzu viele.
Danach wechselte ich eine Weile ziemlich ziellos zwischen unterschiedlichen Fitnessaktivitäten. Ich versuchte es wieder mit dem Laufen. Ich besuchte mit meiner Frau einen Pilates-Kurs. Eine Zeit lang machte ich Bootcamp-Training. Ich probierte schlichtweg alles aus. Dann wurde ich Mitglied in einer Fitnesskette, deren Spezialität hochintensives Intervalltraining (HIIT) war. Mir machten die schnellen Work-outs dort Spaß, etwa Sprints auf dem Laufband und 30-Sekunden-Blocks mit Liegestützsprüngen, und es nahm viel weniger Zeit in Anspruch als das Radfahren, also war ich zufrieden. Aber ich hatte kein richtiges Ziel, nur das, »Sport zu machen«.
All das änderte sich, als ich bei Sophies Beerdigung saß. Offiziell war sie an einer Lungenentzündung gestorben, aber was sie wirklich umgebracht hatte, war, wie mir klar wurde, das Altern ihres Körpers, das sie langsam nach unten zog. Dieses hatte nicht in ihrem letzten Lebensjahr, ja nicht einmal in ihrer letzten Lebensdekade eingesetzt. Es hatte schon Jahrzehnte früher angefangen, gegen sie zu arbeiten, lange bevor ich sie kannte. Und es würde auch uns andere umbringen: Ihrer Tochter Becky, meinen Patienten, mir selbst und all meinen Leserinnen und Lesern stand wahrscheinlich dieses Schicksal bevor.
Dieser Gedanke stimmte mich zutiefst traurig. Doch dann kam mir die zündende Idee: Wir konnten dem nur etwas entgegensetzen, indem wir uns die Philosophie von Zehnkämpfern zulegten – angepasst an unser Alter.
Zehnkämpfer genießen unter den olympischen Athleten wohl das höchste Ansehen. Die Gewinnerinnen und Gewinner der Goldmedaille werden zu den größten Athleten der Welt erklärt. Doch sie sind nicht bei jeder der zehn einzelnen Disziplinen die Besten, in manchen würden sie vielleicht nicht einmal eine Medaille gewinnen. Dennoch gelten sie als die Größten, weil sie in so vielen Disziplinen so bemerkenswert gut sind. Sie sind wahre Generalisten – aber sie trainieren wie Spezialisten.
Dem Altern müssen wir auf ähnliche Weise entgegentreten, beschloss ich. Wir alle sollten für den Zehnkampf der Hundertjährigen trainieren.
Der Zehnkampf der Hundertjährigen
Was in aller Welt soll das sein?
Die Rede ist nicht von einem echten Wettkampf zwischen Hundertjährigen, obwohl es ähnliche Veranstaltungen durchaus gibt – bei den National Senior Games (Senior Olympics) in den USA etwa treffen sich alljährlich bemerkenswerte ältere Athletinnen und Athleten, manche davon neunzig Jahre und älter. Der Altersrekord beim 100-Meter-Lauf der Damen liegt bei hundert Jahren; die Läuferin schaffte die Strecke in etwa 41 Sekunden.
Der Zehnkampf der Hundertjährigen ist eine Überschrift, unter der ich die physischen Bestrebungen meiner Patienten für ihre späteren Lebensjahrzehnte einordne. Der Begriff klingt natürlich ein bisschen morbide und lässt an den eigenen körperlichen Verfall denken. Aber dieser wird nun einmal nicht weniger unausweichlich, wenn wir nicht an ihn denken.
Stellen Sie sich den Zehnkampf der Hundertjährigen als eine Liste der zehn wichtigsten körperlichen Aufgaben vor, zu denen Sie für den Rest Ihres Lebens in der Lage sein wollen. Ein paar der unten aufgeführten Punkte ähneln tatsächlich athletischen Übungen, andere sind eher Aktivitäten des täglichen Lebens, und wieder andere spiegeln unsere persönlichen Interessen wider. Ich finde diese Liste nützlich, denn sie hilft dabei, präzise zu visualisieren, welche Art von Fitness wir mit dem Älterwerden aufbauen und erhalten müssen. Sie ist eine Art Vorlage für unser Training.
Am Anfang präsentiere ich meinen Patienten immer eine lange Liste physischer Aufgaben, die unter anderem Folgendes umfassen kann:
Wandern Sie 2,5 Kilometer auf einem hügeligen Weg.
Stehen Sie aus eigener Kraft vom Fußboden auf, und stützen Sie sich dabei höchstens auf einen Arm.
Heben Sie ein kleines Kind hoch.
Tragen Sie zwei 2,5 Kilogramm schwere Einkaufstüten fünf Straßenblocks weit.
Heben Sie eine zehn Kilogramm schwere Tasche in
das Handgepäckfach im Zug oder Flugzeug.Balancieren Sie 30 Sekunden lang mit offenen Augen
auf einem Bein.
(Bonuspunkte: Augen geschlossen, 15 Sekunden)Haben Sie Sex.
Gehen Sie in drei Minuten vier Treppen hinauf.
Öffnen Sie ein Einmachglas.
Machen Sie 30 Seilsprünge am Stück.
Die gesamte Liste ist viel länger und umfasst mehr als fünfzig Punkte, aber Sie haben jetzt einen Eindruck davon, worum es geht. Nach der Lektüre der Liste sollen meine Patienten auswählen, welche Aufgaben davon sie auch in ihrem neunten, oder besser noch: ihrem zehnten Lebensjahrzehnt noch ausführen können wollen. Wofür entscheiden sie sich?
Meistens für alle. Sie möchten 2,5 Kilometer wandern, ihren Einkauf selber tragen, ein Urenkelkind auf den Arm nehmen und nach einem Sturz allein wieder auf die Beine kommen können. Oder auf dem Golfplatz 18 Löcher spielen oder mit dem Flugzeug verreisen können. Natürlich möchten sie das.
Und das ist großartig. Ihre Urenkelin freut sich furchtbar, wenn Sie sie auf den Arm nehmen. Wir wollen einmal ein wenig nachrechnen. Angenommen, das Kind wiegt 12,5 oder 15 Kilogramm. Dann entspricht das Hochheben einer Kniebeuge, bei der Sie eine 15-Kilogramm-Hantel vor sich halten. Können Sie das heute auch, im Alter von, sagen wir einmal, vierzig Jahren? Vermutlich ja. Blicken wir aber in die Zukunft. In den kommenden 30 oder 40 Jahren wird Ihre Muskelkraft pro Lebensjahrzehnt um acht bis siebzehn Prozent nachlassen – im Laufe der Zeit immer schneller.[267] Wollen Sie also das 15-Kilogramm-Enkel- oder -Urenkelkind mit achtzig Jahren hochheben, müssen Sie mit vierzig Jahren schadlos 25 bis 27,5 Kilogramm heben können. Können Sie das?
Nächster Punkt: Sie möchten auch einen hügeligen Weg entlangwandern können? Um das bequem zu schaffen, brauchen Sie einen VO2max-Wert von rund 30 ml/kg/min. Schauen wir uns doch einmal Ihren zuletzt gemessenen VO2max-Wert an – aha, der lag nur bei 30. Damit liegen Sie im Durchschnitt Ihrer Altersgruppe, doch das reicht leider nicht aus, denn auch Ihr VO2max-Wert wird mit den Jahren geringer. Wir müssen also die Wanderung von Ihrer Liste streichen. Sie könnten sie jetzt noch schaffen, nicht aber, wenn Sie schon älter sind.
Und weiter geht’s. Im höheren Alter eine zehn Kilogramm schwere Tasche über den Kopf heben zu können bedeutet, mit vierzig dasselbe mit einer 20 oder 25 Kilogramm schweren Tasche tun zu können. Vier Treppen mit achtzig hinaufzukommen bedeutet, mit vierzig diese Treppen hinaufsprinten zu können. Bei jedem Beispiel müssen wir jetzt viel mehr machen, um uns gegen den natürlichen und vorzeitigen Kräfteverfall und den Rückgang unserer Sauerstoffaufnahme mit zunehmendem Alter zu wappnen.
Letztlich verstehen meine Patienten, worum es geht. Zusammen erstellen wir eine Liste mit zehn oder fünfzehn Aufgaben für ihren persönlichen Zehnkampf der Hundertjährigen, die für ihre Ziele in späteren Lebensjahrzehnten stehen. Diese bestimmt dann über die Art ihres Trainings.
Das Schöne am Zehnkampf der Hundertjährigen ist, dass er breit gefächert und zugleich hoch individuell ist. Und er ist keineswegs auf zehn Aufgaben beschränkt; die meisten Menschen haben am Ende mehr auf ihrer Liste stehen, je nachdem, welche Ziele sie haben. Meine eigene Version des Zehnkampfs ist auf meine Interessen zugeschnitten, wie Schwimmen und Bogenschießen. Sie ist, wie ich zugeben muss, auch ein wenig aggressiv, was die Bedeutung einer sehr ausgeprägten Fitness in meinem Leben widerspiegelt. Ich würde also für mich wahrscheinlich noch ein paar dieser Aufgaben ergänzen:
800 Meter in 20 Minuten schwimmen.
Eine Minute lang mit einer 15-Kilogramm-Hantel in
jeder Hand gehen.Einen Compoundbogen mit einem Zuggewicht von 50 Pfund spannen und damit einen Pfeil abschießen.
Fünf Klimmzüge machen.
90 Stufen in zwei Minuten hinaufgehen (VO2max = 32).
Eine Minute lang an ausgestreckten Armen hängen
(Dead Hang).Ein Rennauto mit fünf bis acht Prozent der Geschwindigkeit fahren, die ich heute schaffe.
Eine Stunde lang mit einem 20-Kilogramm-Rucksack wandern.
Mein Gepäck selbst tragen.
Einen steilen Abhang hinaufgehen.
Letztlich werden beim Zehnkampf der Hundertjährigen die Aufgaben der meisten Menschen wohl gewisse Überschneidungen zeigen. Wer beispielsweise Stand-up-Paddling mag, wählt vielleicht solche, die die tiefe Haltemuskulatur und die Muskulatur beider Körperseiten kräftigen. Wahrscheinlich trainiert die Person aber dieselben Muskelgruppen, die ich für das Bogenschießen trainiere, und bewahrt sich Schwung und Gleichgewicht in ganz ähnlichem Maße.
Der Zehnkampf der Hundertjährigen ist ambitioniert, ganz klar. Eine Neunzigjährige, die ohne Hilfe an Bord eines Flugzeugs kommt und sogar noch ihr Handgepäck selbst verstaut, ist äußerst fit. Doch der Wahnsinn hat Methode. Diese individuellen Aufgaben sind durchaus zu bewältigen. Es gibt Achtzig-, Neunzig- und inzwischen sogar Hundertjährige, die Marathon laufen, Radrennen fahren, Gewichte heben, Flugzeuge steuern, aus Flugzeugen springen, Ski fahren, echten Zehnkampf betreiben und alle möglichen anderen wunderbaren Dinge tun. Alle oben genannten Aufgaben liegen also im Bereich des Machbaren.
Der Zehnkampf der Hundertjährigen soll uns unter anderem dabei helfen, neu zu definieren, was in unseren späteren Lebensjahren möglich ist, und mit der verbreiteten Vorstellung aufzuräumen, dass die meisten Menschen an diesem Punkt ihres Lebens schwach und zu wenig imstande seien. Wir müssen uns von diesem altersschwachen Stereotyp verabschieden und ein neues Bild kreieren – vielleicht nach dem Vorbild des klassischen Fitnessgurus Jack LaLanne, der bis zu seinem Tod mit sechsundneunzig Jahren täglich ein rigoroses Work-out absolvierte. Anders als die meisten, die ein sehr hohes Alter erreichen, tat er dies nicht zufällig. Sein ganzes Leben hindurch erarbeitete und bewahrte er sich ein hohes Fitnesslevel, beginnend in den 1930er-Jahren, als nur wenige Menschen regelmäßig trainierten und es überhaupt noch keine »Fitnesszentren« gab. Als er älter wurde, tat er bewusst alles, um der stereotypen Vorstellung vom Alter als Phase der Schwäche und des Verfalls entgegenzuwirken. Er arbeitete hart und erfolgreich daran zu zeigen, wozu ein älterer Mensch tatsächlich imstande ist und was er erreichen kann.
Wollen wir in seine Fußstapfen treten, müssen wir damit aufhören, einfach nur »Sport zu machen«, weil wir es sollten, und beispielsweise die Mittagspause auf dem Crosstrainer zu verbringen. Ich kann Ihnen versprechen: Das geht besser! Mein Vorschlag: Beginnen Sie, genau wie ich, zu trainieren, und das mit einem ganz speziellen Ziel, nämlich knackige Hundertjährige zu werden. Wenn mir meine Patienten sagen, sie hätten mehr Interesse daran, knackige Fünfzigjährige als hundertjährige Zehnkämpfer zu werden, antworte ich ihnen, dass es keinen besseren Weg dazu gibt, als sich das langfristige Ziel zu setzen, mit hundert (oder neunzig oder achtzig) Jahren kräftig und dynamisch zu sein. Ähnlich ist es beim Bogenschießen: Ein Schütze, der auf 90 Meter Distanz trainiert, wird auf der 50-Meter-Distanz genauer schießen. Indem wir unser Ziel im Zehnkampf der Hundertjährigen festlegen, können wir außerdem jedes Lebensjahrzehnt bis dorthin besser machen.
Mit meiner Zielsetzung beim Zehnkampf der Hundertjährigen trainiere ich jetzt mit dem Fokus, den ich damals ausschließlich auf das Radfahren, Schwimmen oder Boxen richtete. Es geht nicht darum, bei jeder Aufgabe großartig zu sein – ganz ordentlich genügt schon. Als Zehnkämpfer dieser Art trainieren wir nicht mehr für ein bestimmtes Ereignis, sondern werden zu ganz besonderen Athleten: zu Athleten des Lebens.
Kapitel 12
Training 101
Vorbereitung für den Zehnkampf der Hundertjährigen
Eine überragende Wertentwicklung erzielt man nur dann, wenn man etwas anders macht als die Mehrheit.
Sir John Templeton
Die meisten Trainingsanleitungen haben entweder eine sehr spezifische (z. B. das Trainieren für den ersten Marathon) oder zu vage (z. B. »in Bewegung bleiben«) Ausrichtung. Oder sie betonen »Kardio« zuungunsten von Training mit Gewichten, oder umgekehrt. In diesem Kapitel wollen wir unser Bewegungstraining am Prinzip der Langlebigkeit ausrichten. Welche Kombination von Trainingsformen hilft uns dabei, chronische Krankheiten und den Tod hinauszuzögern und zugleich so viel gesunde Lebenszeit wie möglich zu haben?
Dies zu erreichen ist durchaus komplizierter als die Senkung des eigenen Risikos für Herz-Kreislauf-Erkrankungen, denn es gibt mehr Variablen und mehr Optionen innerhalb jeder Variablen. Das Problem ist nicht ein-, sondern dreidimensional. Die drei Dimensionen, innerhalb derer wir unsere Fitness optimieren wollen, sind aerobe Ausdauer und Effizienz (»Kardio-«), Kraft und Stabilität. Alle drei tragen entscheidend zu unserer Gesundheit und Kraft im Älterwerden bei. (Und wie wir inzwischen wissen, verlängern sie auch unsere Lebensspanne.) Aber sowohl Kardio- als auch Krafttraining sind weitaus nuancierter, als es den meisten Menschen bewusst ist – und die Stabilität ist womöglich die am wenigsten verstandene Komponente von allen.
Mit Kardiotraining ist ein ganzes physiologisches Kontinuum gemeint, vom lockeren Spaziergang bis hin zum intensiven Sprint. Die verschiedenen Intensitätslevels gelten allesamt als Kardiotraining, obwohl die Energie dafür aus unterschiedlichen Systemen bezogen wird. Wir interessieren uns hier vor allem für zwei Abschnitte des Kontinuums: lange, beständige, moderate Ausdauerarbeit wie Laufen, Radfahren oder Schwimmen, bei der wir die von Physiologen sogenannte »Zone 2« trainieren, und maximale aerobe Belastungen, bei denen die VO2max, also die maximale Sauerstoffaufnahme, ins Spiel kommt.
Der Aspekt des Krafttrainings erscheint auf den ersten Blick einfacher: Wenn Sie Ihre Muskeln gegen einen Widerstand in Form von Gewichten oder anderen Kräften (etwa der Schwerkraft, elastischen Bändern oder Ähnlichem) einsetzen, passen sie sich dem an und werden stärker. So funktionieren Muskeln, und das ist wirklich wunderbar. Es gibt einige spezifische Bewegungen, die ich für grundlegend wichtig halte, aber hier ist unser vorrangiges Ziel, nicht nur Kraft und Muskelmasse aufzubauen; ebenso wichtig ist es, Verletzungen zu vermeiden.
An diesem Punkt kommt die Stabilität ins Spiel. Auf sie werden wir im nächsten Kapitel noch genauer eingehen, doch sei schon gesagt, dass ich die Stabilität für genauso wichtig halte wie kardiorespiratorische (aerobe) Fitness und Kraft. Es fällt ein wenig schwer, sie zu definieren, aber für mich ist Stabilität das solide Fundament, das uns ermöglicht, alles Sonstige zu tun, ohne uns zu verletzen. Stabilität macht uns quasi unverwundbar. Sophie war relativ fit für ihr Alter, aber es mangelte ihr wahrscheinlich an Stabilität, was sie verletzungsanfällig machte. Vielen Menschen geht es genauso, ohne dass ihnen das bewusst ist – auch mir, im Alter zwischen zwanzig und dreißig Jahren. Es spielt fast keine Rolle, wie groß Ihre Fitness ist, Sie können trotzdem ein Verletzungsrisiko haben. Darum muss unser Trainingsansatz nicht nur die herkömmlichen Indikatoren von Fitness (wie den VO2max-Wert und unsere Muskelkraft) im Blick haben, sondern vor allem unsere Widerstandsfähigkeit gegen Verletzungen.
In den folgenden Abschnitten erarbeiten wir uns einen Rahmen um jeden dieser Aspekte, damit Sie das Trainingsprogramm für Ihren ganz persönlichen Zehnkampf der Hundertjährigen aufstellen können.
Aerobe Effizienz: Zone 2
Ein Begriff ist in unserer bisherigen Diskussion zum Thema Sport noch gar nicht aufgetaucht: Kalorien. Die meisten Menschen glauben, einer der größten Vorteile von Sport, wenn nicht sogar der größte, sei es, dass dabei »Kalorien verbrannt« werden. Das werden sie, aber wir wollen hier genauer unterscheiden – uns interessieren nicht die Kalorien, sondern die Brennstoffe. Wie wir unterschiedliche Energielieferanten, Glucose und Fettsäuren, nutzen, ist nicht nur für unsere Fitness entscheidend, sondern auch für unsere metabolische und allgemeine Gesundheit. Aerobes Training kann, wenn es auf bestimmte Weise durchgeführt wird, unsere Fähigkeit verbessern, Glucose und vor allem Fett als Brennstoff zu nutzen.
Die Zone 2 ist eine von fünf Ebenen der Trainingsintensität,[268] mit deren Hilfe Trainer im Ausdauersport die Trainingsprogramme ihrer Sportlerinnen und Sportler konzipieren. Manchmal werden die Intensitätszonen anhand der Herzfrequenz definiert, manchmal anhand der Kraftentwicklung, und um die Verwirrung noch zu steigern, unterscheiden manche Trainingsmodelle fünf, andere aber sechs oder sieben Zonen. Meist aber entspricht die Zone 1 einem lockeren Spaziergang und Zone 5 (oder 6 oder 7) einem maximal intensiven Sprint. Die Zone 2 ist bei allen Modellen ungefähr gleich: Gehen in einem Tempo, das langsam genug ist, um sich noch zu unterhalten, aber schnell genug, um die Unterhaltung etwas mühsam zu machen. Das entspricht einem leichten bis moderaten aeroben Training.
Zu meiner Zeit als Radsportler habe ich reichlich Zone-2-Workouts gemacht; diese Art von Training ist für jeden Ausdauersport unerlässlich. Die Bedeutung von Zone-2-Trainingseinheiten hatte ich jedoch nie ganz begriffen, bis ich 2018 zufällig den blitzgescheiten Sportwissenschaftler Iñigo San Millán kennenlernte. Ich war zu einer Tagung in die Vereinigten Arabischen Emirate geflogen und wurde schon kurz nach der Landung, um elf Uhr an einem kühlen Dezemberabend, mit San Millán bekannt gemacht. Er war Assistant Professor an der University of Colorado School of Medicine und erst kürzlich als Director of Performance bei den Radprofis vom Team Emirates angestellt worden. Er hielt sich vor Ort auf, um bei einigen Fahrern des Teams vor der Saison Tests durchzuführen, und als er hörte, dass ich ein ehemaliger Radsportler war, setzte er mich sofort, mitten in der Nacht, auf ein Fahrradergometer, um meinen VO2max-Wert zu ermitteln. Ich mochte ihn sofort.
San Millán ist gebürtiger Spanier und war selbst Radprofi. Er hat mit den verschiedensten Athleten und Trainern vieler Sportarten zusammengearbeitet, darunter Hunderte Spitzenprofis des Radsports. Er ist zudem der persönliche Trainer von Tadej Pogačar, der 2020 und 2021 die Tour de France gewann und 2022 Zweiter wurde. Trotz seiner beeindruckenden Sportlerlaufbahn liegt San Milláns wahre Leidenschaft in der Erforschung des Zusammenhangs zwischen Sport, der Gesundheit der Mitochondrien und Krankheiten wie Krebs und Diabetes vom Typ 2. Er hofft, so erklärte er mir, seine Erkenntnisse über die Menschen mit der größten Fitness auf diesem Planeten – Radprofis und andere Ausdauer-Spitzensportler – nutzen zu können, um den Menschen mit der geringsten Fitness zu helfen, also jenem Drittel oder gar jener Hälfte der Bevölkerung, die unter Störungen oder Erkrankungen des Stoffwechsels leiden.
Nach San Milláns Ansicht sind gesunde Mitochondrien entscheidend für die athletische Leistungsfähigkeit und die metabolische Gesundheit. In unseren Mitochondrien können sowohl Glucose als auch Fettsäuren in Energie umgewandelt werden, doch während Glucose noch auf vielen weiteren Wegen verstoffwechselt werden kann, ist dies mit Fettsäuren ausschließlich in den Mitochondrien möglich. Normalerweise verbrennt jemand, der sich mit geringerer relativer Intensität betätigt, mehr Fett, während bei höherer Intensität mehr Glucose genutzt wird. Je gesünder und effizienter unsere Mitochondrien, desto größer unsere Fähigkeit, Energie aus Fett zu gewinnen, das die bei Weitem effizienteste und häufigste Energiequelle des Körpers ist. Diese Fähigkeit, beide Brennstoffe – Fett und Glucose – zu nutzen, bezeichnet man als »metabolische Flexibilität«. Und auf genau diese zielen wir ab: In den Kapiteln 6 und 7 erfuhren wir, wie die unaufhörliche Ansammlung und das Übermaß an Fett Leiden wie Diabetes und Herz-Kreislauf-Erkrankungen befeuert. Gesunde Mitochondrien (begünstigt durch Zone-2-Training) helfen uns dabei, die Ansammlung von Fett in Grenzen zu halten.
Vor einigen Jahren veröffentlichten San Millán und sein Kollege George Brooks eine faszinierende Studie, die diese Zusammenhänge beleuchtet.[269] Darin verglichen sie drei Gruppen von Versuchspersonen: Radprofis, moderat aktive gesunde Männer und solche mit vorwiegend sitzender Lebensweise, die die Kriterien für das metabolische Syndrom erfüllten, in erster Linie also insulinresistent waren. Die Forscher ließen die Teilnehmer aus allen Gruppen mit einer bestimmten, ihrer Fitness angepassten Intensität (bei etwa 80 Prozent ihrer maximalen Herzfrequenz) auf dem Fahrradergometer fahren und bestimmten dabei, wie viel Sauerstoff sie aufnahmen und wie viel Kohlendioxid sie abatmeten. Auf diese Weise ermittelten sie, wie effizient die Männer Kraft entwickelten und welche primären Brennstoffe sie nutzten. Dabei fanden sie bemerkenswerte Unterschiede. Die Radsportler konnten rasant in die Pedale treten und viel Kraft entwickeln, während sie immer noch Fett verbrannten. Die Versuchspersonen mit metabolischem Syndrom jedoch griffen fast ausschließlich auf Glucose als Energielieferant zurück, und das vom ersten Pedaltritt an. Sie hatten praktisch keine Möglichkeit, ihre Fettspeicher anzugreifen, waren also metabolisch unflexibel. Sie konnten nur Glucose nutzen, kein Fett.
Ganz offensichtlich waren diese beiden Gruppen – Profisportler und nicht gesunde Personen, die ihre Zeit hauptsächlich sitzend zubrachten – so unterschiedlich, wie man es sich nur vorstellen konnte. San Milláns Erkenntnis bestand darin, dass die eher »sesshaften« Versuchspersonen ähnlich trainieren sollten wie die Tour-de-France-Teilnehmer, mit denen er arbeitete. Ein Radprofi trainiert 30 bis 35 Stunden in der Woche auf dem Fahrrad, 80 Prozent davon in Zone 2. Für die Athleten schafft das die Grundlage für jegliches intensiveres Training. (Der Kniff dabei: Die Zone-2-Leistung eines Radprofis fühlt sich für die meisten Menschen an wie Zone 5.)
So fundamental das Zone-2-Training für professionelle Radsportler auch sein mag, in San Milláns Augen ist es sogar noch wichtiger für Nichtathleten, und das aus zwei Gründen. Erstens baut es eine Grundausdauer auf, die allem, was wir tun, zugutekommt, ob es nun ein 100-Kilometer-Radrennen ist oder Spielen mit den Enkeln oder Urenkeln. Zweitens glaubt er, dass es eine entscheidende Rolle bei der Prävention chronischer Krankheiten spielt, indem es die Gesundheit und Effizienz unserer Mitochondrien verbessert. Darum ist das Trainieren der aeroben Ausdauer und Effizienz (z. B. Zone-2-Training) das erste Element meines Zehnkampf-Trainingsprogramms.
Wenn wir Sport in Zone 2 treiben, wird die meiste Arbeit von unseren Muskelfasern vom Typ 1, den langsam zuckenden (»roten«) Fasern, geleistet. Diese sind extrem dicht mit Mitochondrien gepackt und somit bestens ausgestattet für effiziente Ausdauerarbeit in gemäßigtem Tempo. Wir können sehr lange gehen, ohne uns erschöpft zu fühlen. Wenn wir das Schritttempo jedoch erhöhen, beginnen immer mehr Muskelfasern vom Typ 2, die schnell zuckenden (»weißen«) Fasern, zu arbeiten; sie sind weniger effizient, aber kräftiger. Sie bilden bei diesem Prozess auch mehr Lactat, ein Abfallprodukt ihrer ATP-Bildungsmethode. Das Lactat ist an sich nicht schlimm; trainierte Athleten sind sogar imstande, es als eine Art Brennstoff wieder zu verwerten. Allerdings wird aus Lactat plus Wasserstoffionen Milchsäure, und diese bewirkt ein akutes Gefühl des Brennens in ihren Muskeln[270] während starker Anstrengung.
Technisch ausgedrückt, beschreibt San Millán die Zone 2 als maximale Leistung, die wir aufrechterhalten können, ohne Lactat anzureichern. Dieses wird zwar gebildet, aber im gleichen Maße auch wieder abgebaut. Je effizienter unser »Mitochondrienmotor«, desto schneller können wir Lactat abbauen und desto mehr Leistung können wir in Zone 2 erbringen. Wenn wir bei diesem Work-out aber Brennen in den Muskeln spüren, haben wir es ganz offensichtlich übertrieben und bilden mehr Lactat, als wir abbauen können.
Da ich nicht nur Zahlen liebe, sondern auch Biomarker und direktes Feedback, teste ich oft meinen Lactatwert während meines Zone-2-Trainings. Ich benutze ein kleines Lactat-Handmessgerät, um sicherzugehen, dass ich nicht zu intensiv trainiere. Ziel ist es, den Lactatwert konstant zu halten, idealerweise zwischen 1,7 und 2,0 Millimol pro Liter. Hier liegt für die meisten Menschen der Schwellenwert für Zone 2. Trainiere ich zu hart, steigt der Lactatwert an; dann lasse ich es langsamer angehen. (Manchmal ist man versucht, zu intensiv zu trainieren, weil sich das Work-out in Zone 2 an guten Tagen ziemlich »leicht« anfühlt.) Alles dreht sich darum, den Lactatwert konstant in diesem Bereich zu halten und nachhaltig zu trainieren.
Wenn Sie (wie die meisten Menschen) kein tragbares Lactat-Messgerät zur Hand haben, können Sie Ihren Zone-2-Bereich auch auf anderem Wege recht genau ermitteln. Wenn Sie Ihre maximale Herzfrequenz kennen – keinen Schätzwert, sondern Ihr wirkliches Maximum, den höchsten Wert, der bei Ihnen je gemessen wurde –, entspricht Ihre Zone 2 ungefähr dem Bereich zwischen 70 und 85 Prozent dieses Maximalwerts, je nachdem, wie fit Sie sind. Das ist ein ziemlich weiter Bereich, daher empfehle ich Menschen zu Beginn des Trainings gern, ihren »Grad der empfundenen Anstrengung« (RPE, von englisch rate of perceived exertion) zu nutzen; man spricht hier auch vom »Talk Test«. Wie sehr strengen Sie sich an? Wie gut können Sie sich noch unterhalten? Im oberen Bereich von Zone 2 sollten Sie sich noch unterhalten können, ohne aber an einem Gespräch besonders interessiert zu sein. Wenn Sie keine ganzen Sätze mehr sprechen können, sind Sie wahrscheinlich bereits in Zone 3, das heißt, Sie trainieren zu intensiv. Können Sie sich aber ganz locker unterhalten, trainieren Sie vermutlich in Zone 1, was nicht intensiv genug ist.
Die Leistung in Zone 2 ist sehr unterschiedlich, je nach Fitnesszustand der Betreffenden. Bei der Studie von San Millán und Brooks brachten es die Radprofis in Zone 2 auf rund 300 Watt Leistung, während die metabolisch nicht gesunden, sich wenig bewegenden Testpersonen bei etwa vergleichbarer Intensität nur rund 100 Watt Leistung schafften. Das ist ein gewaltiger Unterschied. Wenn wir die Leistung in Watt pro Kilogramm Körpergewicht ausdrücken, tritt dieser noch deutlicher zutage: Die rund 70 Kilogramm schweren Radsportler leisteten mehr als vier Watt pro Kilogramm Körpergewicht, während die mehr als 100 Kilogramm schweren »sesshaften« Testpersonen nur etwa ein Watt pro Kilogramm Körpergewicht schafften.
Diese deutliche Differenz verweist wiederum auf die Tatsache, dass die Mitochondrien, die »Motoren«, der nicht gesunden Personen weit weniger effizient arbeiteten als diejenigen der Sportler und darum sehr schnell von der aeroben Energiegewinnung, bei der Fett und Glucose mit Sauerstoff in den Mitochondrien verbrannt werden, zur deutlich weniger effizienten Glycolyse wechseln, einem Energiegewinnungsweg, der ausschließlich Glucose verwertet und jede Menge Lactat produziert (auf ähnliche Weise produzieren Krebszellen Energie, bezeichnet als Warburg-Effekt). Sobald wir mit dieser Art der Energiegewinnung beginnen, reichert sich Lactat an, und wir können unsere Leistung schnell nicht mehr aufrechterhalten. Es gibt auch (zum Glück seltene) Gendefekte, bei denen die Mitochondrien geschädigt werden und die noch weitaus schwerere Folgeschäden verursachen, doch unter den weit verbreiteten chronischen Krankheiten hat der Diabetes vom Typ 2 eine wirklich üble Wirkung auf die Mitochondrien. San Milláns Daten belegen sehr elegant, welche Schäden diese Krankheit anrichtet.
Selbst in Ruhe verrät uns unser Lactatspiegel viel über unsere metabolische Gesundheit. Personen, die unter Fettleibigkeit oder anderen Stoffwechselproblemen leiden, haben in Ruhe meist deutlich erhöhte Lactatspiegel, ein klarer Hinweis darauf, dass ihre Mitochondrien nicht optimal arbeiten, da sie zu sehr damit beschäftigt sind, einfach nur die Basisenergie bereitzustellen. Das bedeutet, dass sie für ihren gesamten Energiebedarf fast ausschließlich auf Glucose (oder deren Speicherform Glycogen) zurückgreifen müssen und überhaupt keinen Zugriff auf ihre Fettreserven haben. Es erscheint wirklich ungerecht, aber ausgerechnet die Menschen, die am dringendsten ihr Körperfett verbrennen sollten, nämlich die, die davon am meisten haben, können praktisch nichts davon als Energiequelle nutzen, während die schlanken, durchtrainierten Profisportler dies ganz leicht bewerkstelligen, weil ihr Stoffwechsel flexibler ist (und ihre Mitochondrien gesünder sind).[271]
Die Gesundheit der Mitochondrien wird besonders dann bedeutsam, wenn wir älter werden, denn eines der wichtigsten Zeichen des Alterns ist der Rückgang von Zahl und Qualität der Mitochondrien in unseren Zellen. Der Rückgang ist jedoch nicht zwingend eine Einbahnstraße. Mitochondrien sind unglaublich plastisch; aerobes Training stimuliert die Bildung vieler neuer und effizienterer Mitochondrien. Diesen Prozess nennt man mitochondriale Biogenese, während die Eliminierung von nicht mehr funktionstüchtigen Mitochondrien in einem Recyclingprozess namens Mitophagie (ähnlich der in Kapitel 5 erwähnten Autophagie, aber eben bei Mitochondrien) erfolgt.[272] Eine Person, die regelmäßig in Zone 2 trainiert, verbessert den Zustand ihrer Mitochondrien mit jedem Lauf, jeder Schwimmstrecke und jeder Radfahrt. Werden sie jedoch nicht gebraucht, gehen sie wieder verloren.
Auch dies ist ein Grund dafür, dass die Zone 2 eine so starke Mittlerin zwischen Stoffwechselgesundheit und dem Glucose-Gleichgewicht ist.[273] Die Muskulatur ist der größte Glycogenspeicher im Körper, und durch die Bildung weiterer Mitochondrien steigern wir unsere Fähigkeit zum Abbau dieses gespeicherten Brennstoffs enorm, sodass dieser nicht letztlich in Form von Fett gespeichert wird oder in unserem Blutplasma verbleibt. Ein chronisch erhöhter Glucose-Blutspiegel schädigt Herz, Gehirn, Nieren und praktisch alles, was dazwischen liegt – und kann beim Mann auch zu Erektionsstörungen beitragen. Verschiedene Studien ergaben, dass während des Sports unsere Gesamtaufnahme von Glucose gegenüber der Aufnahme in Ruhe um fast das Hundertfache ansteigt.[274] Interessant ist, dass diese Glucoseaufnahme auf unterschiedlichen Wegen erfolgt. Da wäre zunächst der übliche durch Insulin regulierte Weg, den wir gut kennen. Sport aktiviert aber auch weitere Stoffwechselwege,[275] darunter die nicht insulinvermittelte Glucoseaufnahme (englisch non-insulin-mediated glucose uptake, NIMGU). Bei dieser wird Glucose direkt durch die Zellmembran transportiert, ohne dass Insulin beteiligt ist.
Das erklärt wiederum, warum Sport, besonders solcher in Zone 2, so effektiv beim Umgang mit Diabetes sowohl vom Typ 1 als auch vom Typ 2 ist. Er befähigt den Körper, in den Muskeln die Insulinresistenz zu umgehen und so den Blutzuckerspiegel zu senken. Einer meiner Patienten, der unter Typ-1-Diabetes leidet, also kein Insulin bildet, hält seinen Glucosespiegel fast ausschließlich dadurch in Schach, dass er Tag für Tag rund zehn bis fünfzehn Kilometer stramm geht, manchmal sogar mehr. Während des Gehens saugen seine Muskelzellen per NIMGU Glucose aus seinem Blut. Er muss immer noch Insulin spritzen, aber nur einen Bruchteil dessen, was er ohne seinen Sport benötigen würde.
Ein weiterer Pluspunkt der Zone 2 ist der, dass sie sehr niederschwellig ist, selbst für jemanden, der seine Zeit bislang überwiegend sitzend verbracht hat. Manche Menschen kommen schon durch einen strammen Spaziergang in ihre Zone 2; wer besser trainiert ist, muss dazu einen Hügel hinaufsteigen. Es gibt vielerlei Möglichkeiten: Sie können im Fitnessstudio auf den Heimtrainer steigen, auf dem örtlichen Sportplatz einige Runden auf der Bahn joggen oder im Schwimmbad ein paar Bahnen ziehen. Vielen Gesprächen mit San Millán und anderen Sportphysiologen zufolge scheint es, dass etwa drei Stunden oder vier 45-Minuten-Einheiten in Zone 2 pro Woche bei den meisten Menschen das Minimum sind, um einen positiven Effekt zu erzielen, wenn man denn die Hemmschwelle erst einmal überwunden hat. (Wer auf eine größere Ausdauerleistung hin trainiert, etwa einen Marathon, muss natürlich mehr tun.) Ich bin von den Vorteilen des Zone-2-Trainings so überzeugt, dass es inzwischen eine wichtige Größe meines Trainingsplans ist. Viermal pro Woche verbringe ich rund eine Stunde auf meinem Heimtrainer an der Obergrenze meiner Zone 2.
Ihre Fortschritte in der Zone 2 können Sie unter anderem anhand der von Ihnen bei dieser Intensität erbrachten Leistung in Watt ersehen. (Viele Heimtrainer zeigen Ihnen während des Trainings an, wie viel Watt Sie gerade erbringen. Wenn Sie Ihre durchschnittliche Leistung in Watt bei einer Zone-2-Trainingseinheit durch Ihr Körpergewicht in Kilogramm teilen, erhalten Sie einen Wert für Watt pro Kilogramm Körpergewicht, und das ist die Zahl, die uns interessiert. Wiegen Sie beispielsweise 60 Kilogramm und können Sie 125 Watt in Zone 2 erzeugen, entspricht das etwas mehr als zwei Watt pro Kilogramm Körpergewicht. Diesen Wert darf man von einer Person mit relativ guter Fitness erwarten. Es sind nur ungefähre Größenordnungen, aber jemand mit ausgeprägter Fitness schafft ungefähr drei Watt pro Kilogramm Körpergewicht, Radprofis erreichen vier Watt und mehr. Auf die eigentliche Zahl kommt es dabei weniger an als darauf, wie sehr Sie sich im Laufe der Zeit verbessern. (Dasselbe gilt, wenn Sie laufen oder gehen: Verbessern Sie sich, werden Sie in Ihrer Zone 2 schneller.)
Das Training in der Zone 2 kann ein bisschen langweilig sein, darum nutze ich die Zeit oft, um Podcasts oder Hörbücher zu hören oder um über Dinge nachzudenken, die mich gerade bei der Arbeit beschäftigen – eine positive Begleiterscheinung des Trainings besteht darin, dass es auch die Kognition fördert, indem es die Durchblutung des Gehirns steigert und die Bildung des Brain-derived Neurotrophic Factor (BDNF) stimuliert,[276] den wir an früherer Stelle schon kennengelernt haben. Dies ist ein weiterer Grund dafür, dass das Zone-2-Training ein äußerst wichtiger Teil unseres Alzheimer-Präventionsprogramms ist.
Training in Zone 2 ist für mich wie das Errichten eines Fundaments. Die meisten Menschen bekommen es nie zu Gesicht, und dennoch leistet es einen wichtigen Beitrag zu praktisch allem, was wir tun, im Training oder im Leben.
Maximale aerobe Leistung: VO2max
Wenn die Zone 2 einen gleichbleibenden Zustand darstellt, in dem man in vertretbarer Geschwindigkeit umherschweift, dann entspricht Sport am Punkt der maximalen Sauerstoffaufnahme (VO2max) praktisch dem Gegenteil. Hier ist die Intensität weit ausgeprägter – eine heftige, minutenlange Anstrengung, wenn auch noch nicht im Bereich eines ultimativen Sprints. Bei der VO2max bilden wir mithilfe einer Kombination von aeroben und anaeroben Stoffwechselwegen Energie, aber dabei sind wir beim Maximum unserer Sauerstoffaufnahme. Die Sauerstoffaufnahme ist somit entscheidend.
Zusätzlich zur Verbesserung unserer Mitochondriengesundheit, Glucoseaufnahme und metabolischen Flexibilität erhöht das Zone-2-Training auch unseren VO2max-Wert etwas. Wollen Sie diesen jedoch wirklich steigern, müssen Sie diese Zone spezifischer trainieren. Bei Patienten, die noch Sportanfänger sind, beginnen wir mit dem VO2max-Training nach etwa fünf oder sechs Monaten beständigen Zone-2-Trainings.
Ich lege unter anderem deshalb besonderes Augenmerk auf den VO2max-Wert, weil dieses Maß für die maximale aerobe Kapazität stark mit der Lebenserwartung korreliert, wie wir bereits aus Kapitel 11 wissen.[277] Ich lasse alle meine Patienten einen VO2max-Test absolvieren und dann trainieren, um den Wert zu verbessern. Selbst wenn Sie keinen Hochleistungs-Ausdauersport betreiben, ist Ihr VO2max-Wert eine wichtige Maßzahl, die Sie kennen sollten.
Tests werden vielfach angeboten, sogar von einigen großen Fitnessstudios. Leider ist ein VO2max-Test eine ziemlich unangenehme Sache. Dabei fährt man auf einem Fahrradergometer oder läuft auf einem Laufband und steigert die Intensität immer weiter, während man eine Maske trägt, mit deren Hilfe Sauerstoffverbrauch und CO2-Abgabe gemessen werden. Der Spitzenwert Ihrer Sauerstoffaufnahme, der meist erreicht wird, kurz bevor Sie »nicht mehr können«, entspricht Ihrem VO2max-Wert. Wir schicken all unsere Patienten mindestens einmal jährlich zum VO2max-Test, und fast alle hassen ihn. Dann vergleichen wir ihre Ergebnisse, normalisiert auf Körpergewicht, Altersgruppe und Geschlecht.
Warum ist dies wichtig? Weil unser VO2max-Wert ein ziemlich genaues Abbild unserer körperlichen Leistungsfähigkeit ist. Er sagt uns, was wir schaffen können – und was nicht. Betrachten wir einmal Abbildung 11, in der niedrige, durchschnittliche und hohe VO2max-Werte nach Altersgruppen aufgeführt sind. Zwei Dinge fallen hier auf. Erstens gibt es einen gewaltigen Abstand zwischen der Fitness der Spitze und der der untersten fünf Prozent aller Altersgruppen (oberste bzw. untere Linie). Und zweitens zeigt sich deutlich, wie stark der VO2max-Wert mit dem Alter sinkt und wie dieses Absinken mit einer geringeren funktionalen Kapazität einhergeht. Je niedriger der Wert, desto weniger können Sie leisten.
Ein fünfunddreißigjähriger Mann mit einer für sein Alter durchschnittlichen Fitness – bei einem VO2max-Wert um 35 – sollte mit ungefähr zehn Stundenkilometern laufen können. Im Alter von siebzig Jahren jedoch schaffen das nur noch die fünf Prozent mit der größten Fitness. Desgleichen wird ein durchschnittlicher fünfundvierzig- bis fünfzigjähriger Mann in der Lage sein, flott eine Treppe hinaufzusteigen (VO2max = 32), doch mit fünfundsiebzig muss man dazu zur Spitzengruppe seiner Altersgenossen zählen. Aktivitäten, die uns in jungen oder mittleren Jahren leichtfallen, werden mit zunehmendem Alter schwierig oder unmöglich. Das erklärt, warum es vielen Menschen in ihrer Randdekade so schlecht geht. Sie können einfach nicht mehr viel tun.
Ich dränge meine Patienten immer dazu, auf einen möglichst hohen VO2max-Wert hin zu trainieren, damit sie sich mit dem Älterwerden eine gute körperliche Leistungsfähigkeit bewahren. Idealerweise sollten sie anstreben, in der Spitzengruppe für ihr Alter und ihr Geschlecht (also ungefähr die obersten zwei Prozent) zu stehen. Wenn sie das erreichen, lobe ich sie – und setze sie dann darauf an, die Spitzengruppe für ihr Geschlecht bei den zwanzig Jahre Jüngeren ins Visier zu nehmen. Das erscheint extrem, aber ich setze gern extreme Ziele, wie Sie vermutlich schon bemerkt haben.
Dahinter verbirgt sich eine Logik. Angenommen, Sie sind eine fünfzigjährige Frau und lieben das Bergwandern; damit möchten Sie einmal Ihren Ruhestand verbringen. Eine solche Aktivität erfordert einen VO2max-Wert von etwa 30. Nehmen wir zur Verdeutlichung der Sache auch an, dass Sie sich im 50. Perzentil Ihrer Altersgruppe befinden, also bei etwa 32 ml/kg/min. Heute können Sie also eine Bergwanderung machen!
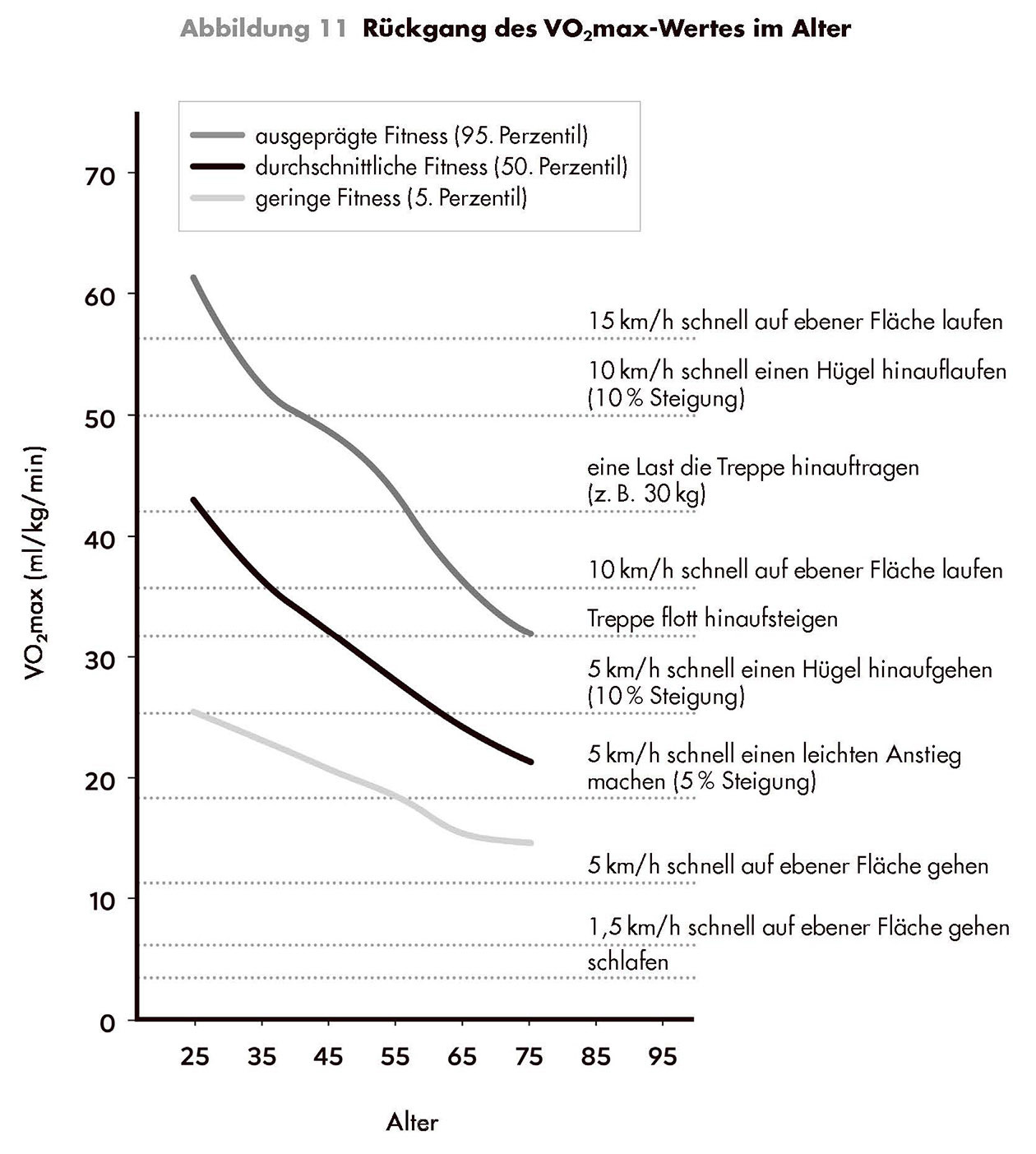
Quelle: Grafik von Jayson Gifford, Brigham Young University, nach Daten von Ligouri (2020)
Das klingt gut – ist es aber nicht wirklich. Studien ergaben, dass unser VO2max-Wert pro Lebensdekade offenbar um rund zehn Prozent zurückgeht, nach dem fünfzigsten Lebensjahr sogar um bis zu 15 Prozent.[278] Ein durchschnittlicher oder sogar leicht überdurchschnittlicher VO2max-Wert genügt also nicht. Unser Plan ist, dass Sie noch weitere dreißig oder vierzig Jahre leben. Wenn Sie jetzt, mit fünfzig, mit 32 ml/kg/min starten, dürfte Ihr Wert, wenn Sie achtzig sind, etwa bei 21 ml/kg/min liegen. Das sind keine abstrakten Zahlen; sie spiegeln einen tief greifenden Funktionsabbau wider. Dies unterscheidet das leichtfüßige Erklimmen einer Treppe vom mühseligen Gehen auf einer leicht ansteigenden Fläche. Vom Wandern in den Dolomiten ganz zu schweigen. Wenn unsere Fünfzigjährige ihr Fitnessziel jenseits der neunzig erreichen will, muss sie jetzt einen VO2max-Wert von 45 bis 49 haben – den Spitzenwert für ihr Geschlecht, aber für das Alter von 30.
Es ist bei alldem wichtig, dass Ihre Ziele Ihren eigenen Prioritäten entsprechen, den Aktivitäten, die Sie mögen und denen Sie auch im höheren Alter nachgehen möchten. Je aktiver Sie im Alter sein möchten, desto mehr müssen Sie heute dafür trainieren.
Vergessen wir nicht: Das Erhöhen des eigenen VO2max-Wertes, ganz gleich, um wie viel, wird Ihr Leben verbessern, nicht nur im Hinblick auf Ihre Lebenserwartung, sondern auch auf Ihre Lebensqualität, heute und in Zukunft. Wenn Sie Ihren VO2max-Wert vom untersten auf das nächsthöhere (und immer noch unterdurchschnittliche) Quartil verbessern, ist das mit einem Rückgang der Gesamtmortalität um fast 50 Prozent assoziiert, wie wir bereits erfahren haben. Ich bin mir sicher, dass praktisch jeder das erreichen kann – und auch sollte, denn die Alternative ist in der Tat inakzeptabel. Sinkt die maximale Sauerstoffaufnahme oder VO2max unter eine bestimmte Grenze (bei Männern meist 18 ml/kg/min, bei Frauen 15), bedroht dies Ihre Fähigkeit, selbstständig zu leben.[279] Ihr Motor schickt sich an zu versagen.
Darum ist es so wichtig, zusätzlich zum Zone-2-Training auch für den VO2max-Wert zu trainieren. Dies ist entscheidend für ein auch im Alter erfüllendes, unabhängiges Leben. Allerdings bedeutet es harte Arbeit über lange Zeit, dies aufzubauen und zu bewahren.
Inwieweit kann man die VO2max trainieren? Nach herkömmlicher Meinung, die den Großteil der Literatur widerspiegelt, ist es vermutlich möglich, die aerobe Kapazität älterer Menschen mit acht bis zehn Wochen Training um etwa 13 Prozent zu verbessern und mit 24 bis 52 Wochen Training um etwa 17 Prozent, so eine Übersichtsstudie. Das ist ein guter Anfang, repräsentiert aber meiner Ansicht nach nur den Beginn dessen, was möglich ist. Derlei Studien sind in der Medizin 2.0 üblicherweise zu kurz angelegt. Wir sprechen von einem lebenslangen Trainingsprogramm, nicht von einem, das über acht Wochen läuft. Jeder Mensch ist hinsichtlich seines Fitnesspotenzials und der Wirkung, die Training bei ihm zeigt, unterschiedlich, aber Mike Joyner glaubt, dass ein längerfristiges und gezielteres Training über längere Zeitspannen – in der Größenordnung von Jahren, nicht Wochen – stärkere Effekte erzielen kann. Meinen Patienten sage ich immer, dass dies kein Zweimonats-, sondern ein Zweijahresprojekt ist.
Welche Steigerung letztlich möglich ist, wissen wir nicht, doch die Literatur deutet darauf hin, dass sich anhaltendes, gewissenhaftes Training auszahlt. Eine kleine Studie mit neun achtzigjährigen gut trainierten Ausdauersportlern (Langlauf-Skiläufern) kam zu dem Ergebnis, dass ihr VO2max-Wert bei durchschnittlich 38 lag; der einer Kontrollgruppe untrainierter achtzigjähriger Männer dagegen lag bei 21, eine Differenz von mehr als 80 Prozent.[280] Das ist gewaltig. Die Sportler hatten die aerobe Kapazität von Personen, die Jahrzehnte jünger waren als sie,[281] während die Männer in der Kontrollgruppe so stark abgebaut hatten, dass sie dabei waren, ihre Fähigkeit, eigenständig zu leben, einzubüßen. Es stimmt, die Testpersonen waren lebenslang aktive Athleten – aber das ist auch ein Teil der Erkenntnis. Unser Ziel ist es, Spitzenathleten des Alterns zu werden.
Der Lohn: Die Steigerung unserer VO2max macht uns funktional jünger.[282] Eine Studie ergab, dass eine Steigerung des VO2max-Wertes bei älteren Versuchspersonen um 6 ml/kg/min (oder etwa 25 Prozent) einer Reduktion ihres Alters um zwölf Jahre gleichkam.[283] Wenn Sie ein Mann zwischen sechzig und siebzig sind und mit einem VO2max-Wert von 30 anfangen, entsprechen Sie ungefähr dem Durchschnitt Ihrer Altersgruppe (siehe Abbildung 12). (Bei Frauen liegt der VO2max-Wert im Alter aus unterschiedlichen Gründen meist etwas niedriger, eine »durchschnittliche« Sechzigjährige läge also bei rund 25 ml/kg/min.) Wenn Sie diesen durch Training auf 35 steigern können, sind Sie deutlich in den obersten 25 Prozent Ihrer Altersgruppe. Gute Arbeit. Und so kann man die Sache auch betrachten: Als Sechzigjähriger haben Sie somit die kardiorespiratorische Fitness eines durchschnittlichen Fünfzigjährigen erlangt, also eines Mannes, der zehn Jahre jünger ist als Sie. Mit einem Wert von 38 oder 39 entsprechen Sie sogar einem durchschnittlichen Dreißigjährigen. Sie haben sich somit eine Phasenverschiebung erarbeitet, ganz ähnlich wie im Falle der Hundertjährigen: Sie haben nun die Fitness einer Person, die Jahrzehnte jünger ist.[284] Klopfen Sie sich ruhig auf die Schulter, Sie haben es verdient!
Das Schöne daran ist, dass sich der VO2max-Wert immer durch Training verbessern lässt, ganz gleich, wie alt Sie sind. Sie glauben mir nicht? Dann darf ich Ihnen einen erstaunlichen Franzosen namens Robert Marchand vorstellen, der 2012 einen Rekord für seine Altersgruppe aufstellte, indem er 24,25 Kilometer in einer Stunde mit dem Rad fuhr, und das im Alter von hunderteins Jahren.[285] Offensichtlich war er mit dieser Leistung nicht zufrieden, denn er beschloss, dass er härter trainieren müsse. Mit einem strengen Trainingsprogramm, das von Spitzentrainern und Physiologen erarbeitet worden war, konnte er seinen VO2max-Wert von bereits beeindruckenden 31 ml/kg/min auf 35 ml/kg/min steigern, was den obersten 2,5 Prozent bei den Achtzigjährigen entsprach. Zwei Jahre später, im Alter von nunmehr hundertdrei Jahren, kam er wieder und brach seinen eigenen Rekord, indem er in einer Stunde fast 27 Kilometer radelte. Das ist beeindruckend und zeigt, dass es nie zu spät ist, seine VO2max zu verbessern.
Selbst wenn wir keine Weltrekorde aufstellen wollen, gleicht die Methode zum Trainieren der VO2max stark derjenigen, mit der Spitzensportler trainieren, nämlich der Ergänzung der Zone-2-Arbeit um ein oder zwei VO2max-Work-outs in der Woche.
Die Einheiten beim hochintensiven Intervalltraining (HIIT) sind sehr kurz und messen oft nur Sekunden. VO2max-Intervalle sind ein wenig länger, zwischen drei und acht Minuten, und etwas weniger intensiv. Ich mache diese Work-outs auf meinem Rennrad, das ich auf einen Heimtrainer montiert habe, oder an der Rudermaschine, doch Laufen auf dem Laufband (oder einer Laufbahn) dürfte auch funktionieren. Eine erprobte Formel für diese Intervalle ist, vier Minuten lang so schnell wie möglich zu laufen oder zu fahren, wie Sie es durchhalten können – kein intensiver Sprint, aber doch schon eine große Anstrengung. Es folgen vier Minuten lockeren Laufens oder Fahrens, in denen Ihre Herzfrequenz wieder unter 100 fallen sollte. Wiederholen Sie dies vier- bis sechsmal, und regeln Sie sich dann herunter.[286]
Stellen Sie sicher, dass Sie sich möglichst vollständig erholen, bevor Sie die nächste Einheit beginnen. Wenn Sie sich zwischen den Einheiten nicht ausreichend erholen, können Sie nicht Ihre Höchstleistung und folglich auch nicht die angestrebte Anpassung erreichen. Achten Sie außerdem darauf, sich ausreichend aufzuwärmen und nach dieser intensiven Trainingseinheit wieder abzukühlen.
Die gute Nachricht ist, dass Sie, wie ich vermute, nicht viel Zeit in Ihrem Pain Cave, Ihrem privaten »Folterkeller« für das intensive Training, zubringen müssen. Wenn Sie nicht gerade für einen Wettkampf in den Ausdauer-Spitzensportarten wie Radfahren, Schwimmen, Laufen, Triathlon oder Skilanglauf trainieren, genügt im Allgemeinen ein einziges Work-out pro Woche in dieser Zone. Sie werden rasch bemerken, dass dieses Ihre Leistung beim Rest Ihres Sportprogramms ebenfalls verbessern wird – und, was noch wichtiger ist, den Rest Ihres Lebens.
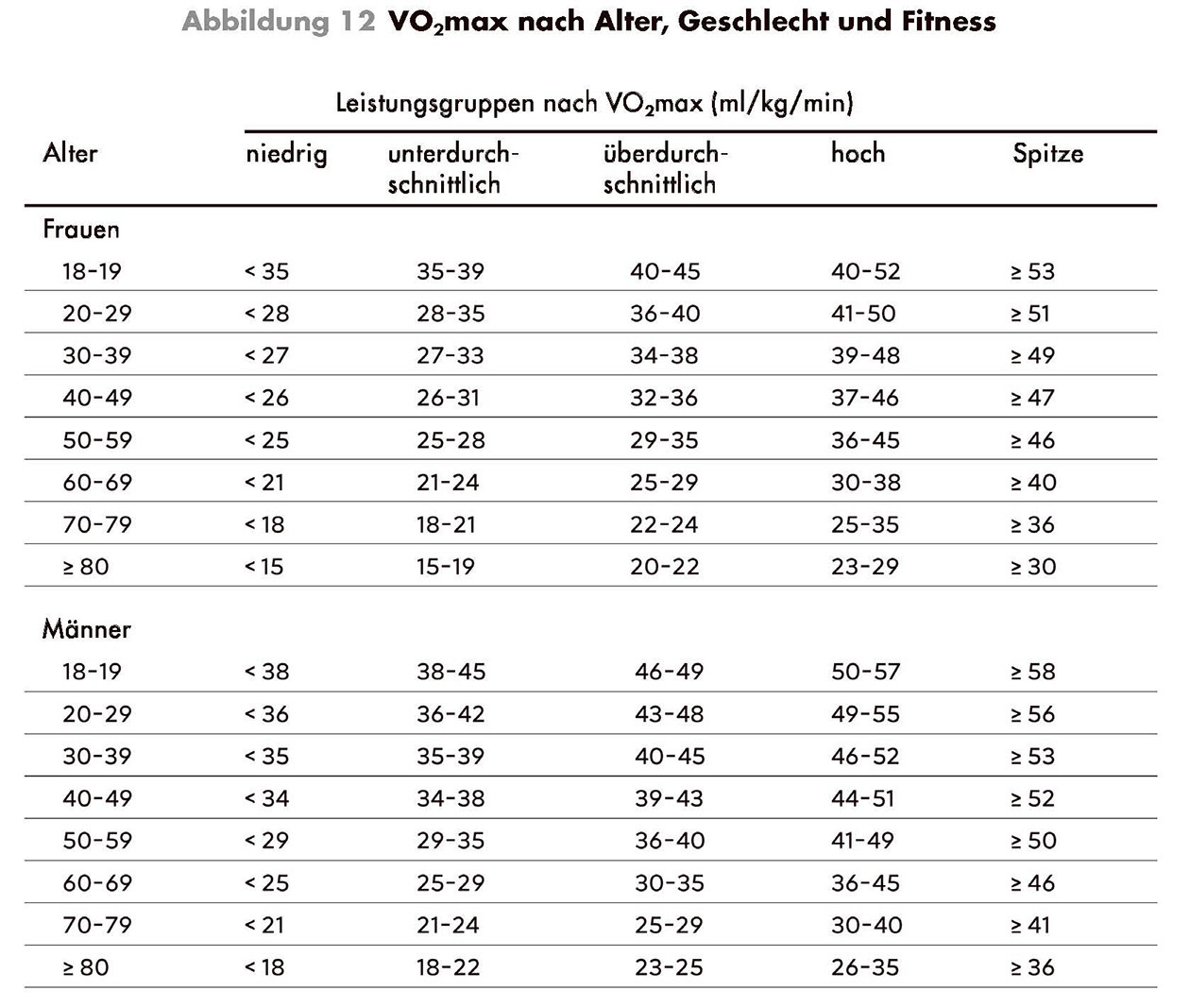
Vergleichsgruppen nach VO2max-Wert: niedrig (unterste 25 %), unterdurchschnittlich (26. bis 50. Perzentil), überdurchschnittlich (51. bis 75. Perzentil), hoch (76. bis 97,6. Perzentil) und Spitzengruppe (oberste 2,3 %).
Quelle: Mandsager et al. (2018)
Diese Wirkung wurde mir vor gar nicht langer Zeit sehr deutlich vor Augen geführt, als meine Frau und ich in London-Heathrow innerhalb kürzester Zeit einen Anschlussflug erreichen mussten. Jeder, der an diesem Flughafen schon einmal umgestiegen ist, weiß, dass der Weg von Terminal 5 zu Terminal 3 geradezu eine Reise für sich ist. Wir konnten unseren Anschluss nur erwischen, indem wir ungefähr anderthalb Kilometer in weniger als acht Minuten rannten, wobei wir noch je einen zehn Kilogramm schweren Koffer dabeihatten. Das war keine Zone-2-Trainingseinheit; wir mussten uns viel mehr anstrengen, und das für acht lange Minuten. Wir mussten ein Mehr an Leistung weit jenseits unserer Zone 2 bringen, das eher an unsere VO2max heranreichte.
Diese Situation ähnelte in gewisser Weise (bis auf die Umgebung natürlich) dem, was unsere Urahnen als Jäger und Sammler oft erlebten. Eine echte Jagd ist natürlich stimmungsvoller als eine Hetzjagd durch den Flughafen; ansonsten aber erfordert auch sie 95 Prozent beständige Aktivität in maßvollem Tempo und fünf Prozent Aktivität von höchster Intensität. Wer auch nur eine Chance haben wollte, die Antilope oder das Mammut oder welches Tier auch immer zu erlegen, brauchte diese Extrakraft, um sein Ziel zu erreichen.
Die Form von kardiorespiratorischer (aerober) Fitness, die wir im Leben wirklich brauchen, ist also letztlich eine sehr gute Ausdauerleistung in mäßigem Tempo, aber auch die Fähigkeit, bei Bedarf »Vollgas« zu geben. Das Trainieren und Bewahren einer ausgeprägten aeroben Fitness – und zwar jetzt – ist unerlässlich, um dieses Leistungsspektrum auch in späteren Jahren zu erhalten.
Die maximale aerobe Leistung ist ein bisschen wie der Verstärker von Leadgitarrist Nigel Tufnel in dem Kultfilm This Is Spinal Tap: Bei den meisten Verstärkern lässt sich die Lautstärke nur bis 10 aufdrehen, bei seinem jedoch bis 11. Er ist »eins lauter«, so seine berühmten Worte.
Hin und wieder ist es gut, wenn man den Regler weiter aufdrehen kann. Wir jedenfalls erwischten unser Flugzeug gerade noch.
Kraft
Das Training mit Gewichten ist ein fester Bestandteil meines Lebens, seit ich mit vierzehn Jahren gemeinsam mit meinem Freund John, beide Möchtegernboxer, zum ersten Mal das Studio im Scarborough-Campus der University of Toronto betrat. Dieses miefige Verlies im zweiten Untergeschoss war von schwitzenden Kerlen bevölkert, deren Leben es war, schwere Gewichte zu stemmen. Es gab weder Heizung noch Fenster noch Strom, darum war es im Winter bitterkalt und im Sommer so heiß, dass nicht selten einer der Sportler nach einer maximal intensiven Trainingseinheit einfach umkippte. Wir liebten es. Es war für uns genau so ein Mythos wie das Gold’s Gym in Venice Beach.
Ich ging damals ins Fitnessstudio, weil ich Ambitionen als Boxer hatte. Und ich verschwendete keinen Gedanken daran, wie mein Leben jenseits der dreiundzwanzig aussehen könnte. Heute bin ich ein Mann mittleren Alters und verstehe die Ernsthaftigkeit, mit der jene älteren Männer ihr Training verfolgten. Ich habe ein anderes Traumziel – den Zehnkampf der Hundertjährigen, falls es Ihnen entfallen sein sollte –, aber ich vermute, dass ich in derselben Situation bin wie sie damals.
Es ist eine traurige Tatsache, dass unsere Muskelmasse mit Überschreiten des dreißigsten Lebensjahres allmählich zurückgeht. Ein achtzig Jahre alter Mann hat etwa 40 Prozent weniger Muskelgewebe (gemessen als Querschnitt des Musculus vastus lateralis, der einen Teil des »Quadrizeps« bildet, also des großen Muskels am vorderen Oberschenkel) als mit fünfundzwanzig.[287] Aber die Muskelmasse ist vielleicht gar nicht so wichtig. Laut Andy Galpin, Professor für Kinesiologie an der California State University in Fullerton und eine der absoluten Autoritäten zu den Themen Kraft und Leistung, büßen wir etwa zwei- bis dreimal schneller an Muskelkraft ein als an Muskelmasse. Und unsere Leistung (Kraft × Geschwindigkeit) schwindet zwei- bis dreimal schneller dahin als unsere Kraft. Grund dafür ist die größte im alternden Muskel stattfindende Veränderung, nämlich der Abbau unserer schnell zuckenden (»weißen«) Muskelfasern (Muskelfasern vom Typ 2). Unser Training muss also darauf abzielen, diese durch Training mit hohen Widerständen zu verbessern. Bewegung im Alltag und Ausdauerarbeit in der Zone 2 mögen ausreichen, um den Abbau der Muskelfasern vom Typ 1 zu verhindern, doch nur die Arbeit gegen größere Widerstände kann das Verschwinden der Muskelfasern vom Typ 2 aufhalten.
Muskelmasse und -kraft sind viel schneller verloren als aufgebaut, besonders, wenn wir im Alltag viel sitzen. Selbst wenn jemand stets gewissenhaft trainiert hat, kann eine kurze Phase der Inaktivität vieles vom Trainingseffekt zunichtemachen. Rührt diese Inaktivität von einem Sturz oder Knochenbruch her und währt sie länger als ein paar Tage, kann sie oft einen steilen Niedergang auslösen, von dem man sich womöglich nie wieder ganz erholt. Genau das war Sophie passiert. Eine Studie mit zwölf gesunden Freiwilligen mit einem Durchschnittsalter von siebenundsechzig Jahren ergab, dass nach nur zehn Tagen Bettruhe, wie sie bei einer schwereren Erkrankung oder Verletzung des Bewegungsapparats typisch ist, die fettfreie Körpermasse (Muskulatur) bei den Teilnehmenden im Mittel um etwa 3,3 Pfund zurückgegangen war.[288] Das ist schon substanziell und zeigt, wie gefährlich Inaktivität sein kann. Bewegt sich jemand wenig und nimmt dabei noch zu viele Kalorien auf, beschleunigt sich der Muskelabbau, denn angesetztes Fett verdrängt vor allem Muskeln.
Die extremste Form dieses Muskelschwunds bezeichnet man als Sarkopenie,[289] wie bereits in Kapitel 11 beschrieben. Eine Person mit Sarkopenie hat wenig Energie, fühlt sich schwach und hat Probleme mit dem Gleichgewicht. Die Sarkopenie ist ein Leitsymptom für das Syndrom der Gebrechlichkeit.[290] Diese liegt vor, wenn mindestens drei der folgenden Kriterien erfüllt sind: unfreiwilliger Gewichtsverlust, Erschöpfung oder Energiemangel, verminderte körperliche Aktivität, langsamer und unsicherer Gang sowie Muskelschwäche (überprüft anhand der Handkraft, dazu im Folgenden mehr). Gebrechlichen Personen fällt es schwer, zu stehen oder zu gehen, und sie haben ein hohes Risiko für Stürze und Knochenbrüche.
Einen Muskel wieder aufzubauen, wenn dieses Stadium einmal erreicht ist, fällt sehr schwer. Eine Studie untersuchte 62 gebrechliche Seniorinnen und Senioren (Durchschnittsalter achtundsiebzig), die an einem Krafttrainingsprogramm teilnahmen, und kam zu dem Ergebnis, dass selbst nach sechs Monaten reinen Krafttrainings die Hälfte der Versuchspersonen überhaupt keine Muskelmasse aufgebaut hatte.[291] Sie verloren auch keine Muskelmasse, was wahrscheinlich dem Training mit Gewichten zu verdanken war, doch macht dies deutlich, wie schwer es ist, in späten Lebensjahren Muskelmasse aufzubauen.
Ein anderes Maß, das wir bei unseren Patienten genau beobachten, ist die Knochendichte (oder Knochenmineraldichte). Wir bestimmen sie jedes Jahr bei jedem Patienten, indem wir mithilfe von Dual-Röntgen-Absorptiometrie (englisch dual-energy x-ray absorptiometry, DEXA) sowohl beide Hüftgelenke als auch ihre Lendenwirbelsäule untersuchen. Mit dieser Methode lassen sich auch Körperfett und fettfreie Körpermasse bestimmen, sie ist also in allen Fragen zur Zusammensetzung des Körpers eine hilfreiche Technik.
Die drei Knochenregionen werden meist betrachtet, wenn es um die Diagnose von Osteopenie oder Osteoporose geht. Viele Leitlinien empfehlen hier ein Screening für Frauen ab fünfundsechzig, für Männer ab siebzig (die Leitlinie des Dachverbandes für Osteologie von 2017 empfiehlt es für Frauen sogar erst ab siebzig, für Männer ab achtzig, wenn keine sonstigen Befunde oder Komplikationen vorliegen), was typisch für die Medizin 2.0 ist: Erst einmal abwarten, bis jemand wirklich in Gefahr ist, und erst dann handeln. Wir halten es dagegen für wichtig, viel früher einzugreifen, noch bevor irgendwelche Probleme entstehen.
Tatsächlich sinkt die Knochendichte parallel zur Muskelmasse; mit Anfang zwanzig hat sie ihren höchsten Wert, dann beginnt ein langsamer, stetiger Rückgang. Bei Frauen schreitet dieser deutlich schneller voran, sobald sie die Menopause hinter sich haben, wenn sie keine Hormonersatztherapie (HET) bekommen (auch dies ein Grund dafür, dass wir diese Behandlung sehr empfehlen), denn Östrogene sind für starke Knochen entscheidend, sowohl bei Frauen als auch bei Männern. Weitere Risikofaktoren sind genetische Veranlagung (familiäre Häufung), Rauchen über lange Zeit, langfristiger Gebrauch von Corticosteroiden (etwa bei Asthma oder Autoimmunerkrankungen), Arzneien, die Östrogen blockieren (die beispielsweise von manchen Frauen gegen Brustkrebs eingenommen werden), eine geringe Muskelmasse (wieder einmal) und Unterernährung.
Warum interessiert uns das so sehr? Wie bei den Muskeln geht es auch hier letztlich um Schutz. Wir wollen diesen Niedergang verlangsamen, uns vor Verletzungen und Gebrechlichkeit schützen. Die Mortalität bei Hüft- oder Oberschenkelbrüchen ist jenseits des fünfundsechzigsten Lebensjahres enorm. Sie variiert je nach Studie zwischen 15 und 36 Prozent innerhalb eines Jahres – was bedeutet, dass bis zu ein Drittel der Menschen über fünfundsechzig, die sich Hüfte oder Oberschenkel brechen, in diesem Zeitraum sterben. Selbst wenn eine Person an der Verletzung nicht stirbt, kann der Rückschlag funktional dem Tod gleichwertig sein, wenn man betrachtet, wie viel Muskelmasse und somit physische Kapazität durch die Bettruhe verloren ging (wir erinnern uns, wie schnell Menschen dieses Alters durch Bettruhe an Muskelmasse einbüßen).
Wir wollen dieses Problem, wenn es denn aufkommt, schon Jahrzehnte vor einer möglichen Fraktur aufspüren. Wenn wir eine langsam oder rasant sinkende Knochendichte entdecken, verfolgen wir vier Strategien:
Optimieren der Ernährung, mit Schwerpunkt auf Protein und Gesamtenergiebedarf (siehe Ernährungskapitel)
Aktivität mit Heben oder Tragen schwerer Gewichte: Krafttraining, besonders mit schweren Gewichten, fördert das Knochenwachstum – mehr als Impact-Sportarten wie Laufen (obwohl dieses wiederum besser ist als Schwimmen oder Radfahren). Knochen reagieren auf mechanische Beanspruchung, und Östrogen ist das Schlüsselhormon zur Übersetzung des mechanischen Signals (Belastung durch Gewicht) in ein chemisches, das dem Körper meldet, er solle mehr Knochen bilden.
Hormonersatztherapie, wenn indiziert
Medikamente zur Erhöhung der Knochendichte, wenn indiziert
Idealerweise lösen wir das Problem schon mit den ersten beiden Maßnahmen, aber scheuen Sie nicht vor der Anwendung von Hormonen und Medikamenten zurück, wenn dies angemessen ist. Die Erkenntnis für Sie als Leser ist, dass Ihre Knochendichte wichtig ist und mindestens so viel Aufmerksamkeit verdient wie die Muskelmasse, darum sollten Sie sie mindestens alle paar Jahre prüfen lassen. (Besonders wenn Ihre Hauptsportart keine Belastung durch Gewichte mit sich bringt, wie Radfahren oder Schwimmen.)
Krafttraining sehe ich als eine Art Rücklage für den Ruhestand. So wie wir mit genügend Erspartem in Rente gehen wollen, um den Rest unseres Lebens versorgt zu sein, wollen wir das höhere Alter mit einer ausreichend großen Reserve an Muskeln (und Knochendichte) erreichen, die uns vor Verletzungen schützt und uns erlaubt, die Dinge zu tun, an denen wir Freude haben. Es ist viel besser, im Voraus zu sparen, zu investieren und zu planen, sodass sich Ihr Vermögen im Laufe der Jahrzehnte allmählich aufbaut, als zu versuchen, mit Ende fünfzig einen individuellen Rentenvertrag abzuschließen und zu hoffen, dass Ihnen überdies die Börsenkurse in die Hände spielen. Wie das Investieren ist auch das Krafttraining kumulativ, seine Vorteile addieren sich. Je mehr Reserven Sie schon früh aufbauen, desto besser sind Sie auf lange Sicht gestellt.
Anders als manchen Leuten im Fitnessstudio ist es mir ziemlich egal, wie groß mein Bizeps ist oder wie viel ich beim Bankdrücken schaffe. Derlei ist interessant, wenn Sie Bodybuilder oder Gewichtheber sind, aber meiner Ansicht nach weniger für den Zehnkampf der Hundertjährigen (oder das richtige Leben). Ein weitaus wichtigeres Maß für die Kraft ist, so meine Schlussfolgerung, wie viel Sie tragen können. Das sage ich meiner Intuition folgend, aber auch aufgrund von Forschungen zu Jägern und Sammlern sowie der menschlichen Evolution. Das Tragen ist eine Superkraft unserer Art. Es ist ein Grund dafür, dass wir opponierbare Daumen sowie lange Beine (und Arme) besitzen. Kein anderes Tier ist imstande, große Objekte effizient von hier nach dort zu tragen. (Und die Tiere, die es doch können, wie Pferde und anderes Vieh, tun es nur, weil wir sie entsprechend gezüchtet, trainiert und in Geschirre gesteckt haben.) Dies verdeutlicht wiederum, wie ich Krafttraining generell sehe. Es dreht sich größtenteils darum, Sie »tragfähiger« zu machen.
Ich war schon immer begeistert davon, schwere Objekte mit meinen Händen zu tragen. Als Teenager arbeitete ich im Sommer auf dem Bau und meldete mich immer wieder freiwillig, um Werkzeuge und Material kreuz und quer über die Baustelle zu tragen. Noch heute baue ich das Tragen in irgendeiner Form, meist mit Hanteln oder Sandsäcken, in die meisten meiner Work-outs ein. Außerdem bin ich inzwischen fast besessen von einer Aktivität, die als Rucking bezeichnet wird und im Grunde nichts anderes ist als Wandern oder Walking in schnellem Tempo mit schwerem Gepäck auf dem Rücken. An drei oder vier Tagen die Woche bin ich so für eine Stunde in meinem Heimatort unterwegs, hügelauf- und -abwärts. Meist überwinde ich dabei auf circa fünf, sechs Kilometern Strecke zig Höhenmeter. Der 25 bis 30 Kilogramm schwere Rucksack ist dabei eine ziemliche Erschwernis, sodass ich meine Beine und meinen Rumpf trainiere und zugleich eine schöne Herz-Kreislauf-Einheit absolviere. Das Beste daran ist, dass ich auf diesen Touren niemals mein Mobiltelefon mitnehme; ich bin allein in der Natur unterwegs, oder mit Freund oder Freundin, einem Familienmitglied oder einem Gast (für die Rucking bei mir ein Muss ist; ich habe zwei Reserverucksäcke in meiner Garage).
Auf diese Betätigung bin ich in dem Buch The Comfort Crisis von Michael Easter gestoßen, das mir wahrlich die Augen geöffnet hat. Easters einleuchtende These ist, dass wir, weil wir jegliche Beschwerlichkeiten aus unserem modernen Leben verbannt haben, den Bezug zu jenen grundlegenden Fertigkeiten (von häufigen Leiden ganz zu schweigen) verloren haben, die einst das Menschsein ausmachten. Das Tragen von Dingen über weite Entfernungen ist eine dieser Fertigkeiten; unsere Urahnen mussten wahrscheinlich große Strecken zurücklegen, um Nahrung für ihre Familien zu finden und ihre (Jagd-)Beute dann zurück ins Lager zu tragen, wo sie unter allen aufgeteilt wurde. Das Tragen ist so effektiv, dass das Militär es in sein Training mit einbezieht.
»Das Tragen hat unsere Art geformt«, so Easter.[292] »Unsere Urahnen trugen oft etwas. Es verlieh ihnen eine robuste funktionale Kraft und Ausdauer, die wahrscheinlich eine gute Schutzwirkung hatte. Mit unserem technischen Fortschritt aber haben wir das Tragen aus unserem Leben verbannt, wie so viele andere Unannehmlichkeiten. Rucking ist eine praktische Art, das Tragen wieder zum Teil unseres Lebens zu machen.«
Der Unterschied besteht hauptsächlich darin, dass ich in meinem Rucksack nicht 15 Kilogramm Antilopenfleisch trage, sondern Metallgewichte, die natürlich weniger schmackhaft sind. Beim Rucking konzentriere ich mich vor allem auf hügelige Wege. Bergauf zu gehen bietet mir Gelegenheit, meine VO2max zu trainieren; wer zum ersten Mal »ruckt«, wird staunen, wie anstrengend schon ein 15-prozentiger Anstieg ist, wenn man nur zehn Kilogramm auf dem Rücken trägt – und anschließend wieder bergab läuft. (Ein gutes Ziel ist es, ein Viertel bis ein Drittel des eigenen Körpergewichts tragen zu können, sobald man genug Kraft und Kondition entwickelt hat. Meine Tochter und meine Frau tragen immer so viel, wenn sie mich begleiten.)
So großartig Rucking ist, ich nutze auch noch andere Methoden, um mehr Kraft aufzubauen. Mein Training strukturiere ich mit Übungen, die Folgendes fördern:
Handkraft, also die Kraft, mit der Sie mit den Händen zugreifen können. Sie umfasst alles von den Händen bis zum dem großen Rückenmuskel Musculus latissimus dorsi. Fast jede Aktion beginnt mit Greifen.
Belastung bei konzentrischer und exzentrischer Bewegung, also wenn sich die Muskeln verkürzen (konzentrisch arbeiten) und verlängern (exzentrisch arbeiten). Wir müssen somit imstande sein, das Gewicht zu heben und wieder abzusenken, langsam und kontrolliert. Beim Rucking bietet sich bergab hierzu die beste Gelegenheit, weil man gezwungen ist, die »Bremsen zu ziehen«.
Zugbewegungen in allen Winkeln von oberhalb des Kopfes bis vor der Brust; diese erfordern auch Handkraft
(z. B. Klimmzüge, Rudern).Hüftbeugende Bewegungen wie Kreuzheben und Kniebeuge, aber auch Step-ups, Hip Thrusts und zahllose nur mit einem Bein ausgeführte Übungen, die Beine, Po und unteren Rücken stärken (Hip Hinges).
Ich konzentriere mich auf diese vier grundlegenden Elemente der Kraft, weil sie die höchste Relevanz für den Zehnkampf der Hundertjährigen haben – und auch für ein erfülltes, aktives Leben in späteren Jahrzehnten. Wenn Sie fest zugreifen können, können Sie leicht ein Marmeladenglas öffnen. Wenn Sie kräftig ziehen können, können Sie Einkäufe tragen und schwere Gegenstände anheben. Wenn Sie die Hüfte richtig beugen können, können Sie problemlos von einem Stuhl aufstehen. Sie sorgen dafür, dass Sie gut älter werden. Es geht nicht darum, wie viel Gewicht Sie heute heben können, sondern darum, wie gut Sie in 20 oder 30 oder 40 Jahren funktionieren werden.
Die Handkraft habe ich als Erstes genannt, weil sie zu den Dingen zählt, an die viele keinen Gedanken verschwenden. Ich war selbst überrascht darüber, wie viel wissenschaftliche Literatur eine bessere Handkraft im mittleren und höheren Alter mit einer geringeren Gesamtsterblichkeit in Verbindung bringt.[293], [294] Diese Daten sind sogar ebenso robust wie diejenigen für die VO2max und die Muskelmasse. Etliche Studien deuten darauf hin, dass die Handkraft – also wie stark Sie mit einer Hand zudrücken können – etwas darüber aussagt, wie lange Sie wahrscheinlich leben werden.[295] Eine geringe Handkraft bei älteren Menschen gilt wiederum als ein Symptom der Sarkopenie, jener altersbedingten Muskelatrophie, auf die wir oben eingegangen sind. Bei diesen Studien gibt die Handkraft quasi Aufschluss über die Stärke der gesamten Muskulatur, aber sie ist auch ein grober Indikator für die allgemeine Robustheit und die Fähigkeit, sich zu schützen, falls man ausrutscht oder das Gleichgewicht verliert. Wenn Sie die Kraft haben, sich an einem Geländer oder einem Ast festzuhalten, könnten Sie einen Sturz verhindern.
Wenn man bedenkt, wie verbreitet der Fitnessgedanke und Besuche im Studio seit Jahrzehnten in unserer Kultur sind, dann überrascht es doch, dass erwachsene US-Amerikaner heute offenbar eine viel geringere Handkraft – und somit weniger Muskelmasse – haben als noch vor einer Generation. Noch 1985 hatten Männer im Alter von zwanzig bis fünfundzwanzig Jahren im Durchschnitt rechtsseitig eine Handkraft von rund 60 Kilogramm, 2015 dagegen lag der Durchschnitt in dieser Altersgruppe nur noch bei gut 50 Kilogramm.[296] Das lässt darauf schließen, dass Menschen, die heute zwischen dreißig und vierzig Jahre alt sind, mit viel weniger Kraft in das mittlere Lebensalter eintreten als ihre Eltern. Das könnte im höheren Alter zu Problemen führen.
Die Handkraft ist in jedem Alter bedeutsam. Jede unserer Interaktionen beginnt mit unseren Händen (oder unseren Füßen, doch dazu später mehr). Unser Griff ist bei praktisch jeder unserer physischen Aufgaben der erste Kontakt, ob beim Golfen oder beim Holzhacken; er ist unsere Schnittstelle mit der Außenwelt. Ist unser Griff schwach, wird alles andere ebenfalls beeinträchtigt.
Die Handkraft lässt sich recht einfach trainieren. Eine meiner Lieblingsmethoden ist der klassische Farmer’s Carry, bei dem man eine Minute oder länger mit einer Hex-Bar mit Gewichten oder aber einer Hantel in jeder Hand läuft. (Bonuspunkte gibt es, wenn Sie die Hantel senkrecht emporhalten, bei absolut geradem Handgelenk und bei 90 Grad gewinkeltem Ellbogen, so als würden Sie sie durch einen Raum voller Menschen tragen.) Eine Standardanforderung an unsere männlichen Patienten ist, dass sie ihr halbes Körpergewicht in jeder Hand (also insgesamt ihr ganzes Körpergewicht) mindestens eine Minute lang tragen können; bei weiblichen Patienten zielen wir auf 75 Prozent dieses Gewichts. Das ist natürlich ein hehres Ziel – bitte probieren Sie das nicht gleich bei Ihrem nächsten Besuch im Fitnessstudio. Manche unserer Patienten brauchen ein volles Jahr Training, bis sie es auch nur versuchen können.
Generell raten wir unseren Patienten, mit deutlich weniger Gewicht zu beginnen als dem, was sie früher gehoben haben; manchmal trainieren wir anfangs sogar nur mit dem eigenen Körpergewicht. Wie wir im folgenden Kapitel zum Thema Stabilität noch erfahren werden, ist es weitaus wichtiger, optimale Bewegungsmuster zu erlernen und zu praktizieren, als jedes Mal schwere Gewichte zu stemmen. Der Farmer’s Carry etwa ist ziemlich einfach (Gewichte in beide Hände, Arme an die Seite, losgehen). Der wichtigste Tipp hierzu ist, die Schulterblätter dabei unten und hinten zu halten, nicht hochgezogen oder nach vorn gekrümmt. Wenn Sie erst mit dem Krafttraining beginnen, fangen Sie mit leichten Gewichten (vielleicht sogar nur fünf oder 7,5 Kilogramm) an und steigern Sie sich langsam.
Eine andere Methode, die Handkraft zu testen, ist das »Dead Hanging« (Hängen an den ausgestreckten Armen) an einer Stange, so lange wie möglich. (Dies ist keine Übung für jeden Tag, sondern eher ein Test für ab und zu.) Man greift die Reckstange, lässt sich einfach hängen und trägt so das eigene Körpergewicht. Diese Übung ist einfach, aber doch vertrackt und unterstützt die enorm wichtigen Muskeln, die das Schulterblatt stabilisieren (mehr dazu im folgenden Kapitel). Hier möchten wir, dass im Alter von circa vierzig Jahren die Männer mindestens zwei Minuten und Frauen mindestens 90 Sekunden so hängen können. (Mit jeder Dekade jenseits der vierzig reduzieren wir das Ziel ein wenig.)
Zum Thema Kraft gehört unbedingt auch die Erwähnung der Belastung bei konzentrischer und insbesondere exzentrischer Bewegung. Exzentrische Arbeit bedeutet, dass der Muskel belastet wird, wenn er sich verlängert, etwa beim Absenken der Hantel beim Bizepstraining. Rein intuitiv fokussieren wir uns beim Heben von etwas auf die konzentrische Phase, beispielsweise beim Heben der Hantel beim Bizepstraining, also der Arbeit bei sich verkürzendem Muskel. Einer der beiden Tests, denen wir unsere Patienten unterziehen, besteht darin, auf einen 50 Zentimeter hohen Block hinauf- und wieder hinabzusteigen (Step-up und Step-down). Dabei soll der Step-down drei volle Sekunden dauern (vorwärts, als würde man eine sehr hohe Stufe hinabsteigen). Das Aufsteigen fällt vergleichsweise leicht, doch die meisten Personen tun sich anfangs schwer mit einem kontrollierten Drei-Sekunden-Step-down. Dieser erfordert einen kontrollierten exzentrischen Kraftaufwand. (Mehr zu Step-ups und Step-downs am Ende von Kapitel 13.)
Die exzentrische Kraft ist im Leben, und besonders im fortschreitenden Alter, oft der Punkt, an dem viele schwächeln. Exzentrische Kraft im Quadrizeps-Muskel gibt uns die nötige Kontrolle, wenn wir eine Steigung oder eine Treppe hinabgehen. Sie ist sehr wichtig, da sie uns vor Stürzen und Verletzungen des Bewegungsapparates schützen kann. Durch exzentrische Belastung unserer Muskeln entlasten wir zudem unsere Gelenke, besonders das Kniegelenk – etwa wenn wir einen sehr steilen Hang langsam hinabsteigen, statt unkontrolliert hinunterzustürmen. Der Unterschied bei den auf unsere Knie einwirkenden Kräften ist dabei enorm (und das Ergebnis vermutlich auch – entweder ein sicherer Abstieg oder eine Landung auf dem Gesicht und wahrscheinlich eine Knieverletzung).
Das Trainieren der exzentrischen Kraft ist relativ einfach. Im Großen und Ganzen bedeutet es, sich auf die »Senkphase« von Hebeübungen zu fokussieren, sei es bei Klimmzügen, beim Kreuzheben oder bei Ruderübungen. Bergab-Rucking, also Gehen mit Gewichtsrucksack, ist wunderbar, um sowohl exzentrische Kraft als auch räumliche Achtsamkeit und Kontrolle zu stärken, beide sind wichtig für das Stabilitätstraining (siehe nächstes Kapitel). Exzentrische Kraft schützt auch vor Knieschmerzen. Sie brauchen sie nicht bei jeder Trainingseinheit zu berücksichtigen. Manchmal möchte man sich einfach darauf konzentrieren, das Gewicht schnell zu bewegen oder ein schwereres Gewicht zu heben. Achten Sie aber darauf, sich bei jedem Work-out auch die Zeit für das Trainieren der exzentrischen Phase bei Hebeübungen zu nehmen.
Als Nächstes folgen die Zugbewegungen, die mit der Handkraft in engem Zusammenhang stehen. Durch Zug üben wir unseren Willen aus, ob wir nun eine Tasche mit Einkäufen aus dem Kofferraum heben oder den El Capitan erklimmen. Im Fitnessstudio trainieren wir die Zugkraft meist mit der Ruderübung, bei der wir das Gewicht zum Körper ziehen, oder mit Klimmzügen. Das Rudergerät, welches ich besonders für das VO2max-Training bevorzuge, ist ebenfalls eine einfache und effektive Methode, um die Zugkraft zu trainieren.
Das letzte grundlegende Element der Kraft sind hüftbeugende Bewegungen, bei denen wir uns in den Hüftgelenken – nicht in der Wirbelsäule – beugen (Hip Hinges), um einige der größten Muskeln des Körpers zu stärken, den Musculus glutaeus maximus (Gesäßmuskel) und die ischiocrurale Muskulatur (rückseitige Oberschenkelmuskeln). Ich wiederhole: das Ganze bei geradem Rücken! Diese sehr kraftvolle Bewegung ist für uns unerlässlich. Ob beim Ansprung von einer Olympia-Sprungschanze, dem Aufheben eines Centstücks vom Boden oder einfach dem Aufstehen von einem Stuhl, immer beugen bzw. strecken wir unser Hüftgelenk.
Hip Hinges unter starker axialer Belastung, etwa beim Kreuzheben oder bei Kniebeugen mit schwerem Gewicht, sollten gut vorbereitet sein, denn hier besteht die Gefahr einer Wirbelsäulenverletzung. Darum lassen wir unsere Patienten sehr langsam auf hüftbeugende Bewegungen unter Last hinarbeiten, meist mit Step-ups auf einem Bein (siehe Beschreibung unten) und rumänischem Kreuzheben im leichten Ausfallschritt, entweder ganz ohne Gewichte oder mit nur leichten Gewichten in den Händen.
Normalerweise würde ich in diesem Abschnitt ausführlich erläutern, worauf bei Klimmzügen und Hip Hinges genau zu achten ist. Ich bin jedoch zu dem Schluss gekommen, dass es für ihre richtige Ausführung Dutzende Bilder und Tausende Wörter brauchen würde, und das in einem Buch, das schon jetzt allzu umfangreich ist. Aus zwei Gründen habe ich mich also gegen detaillierte Erläuterungen entschieden. Erstens glaube ich, dass derlei am besten direkt von einer anderen Person erlernbar ist, die die Bewegungen anleiten kann. Die größte Schwierigkeit besteht beispielsweise nicht darin, die richtige Haltung der Wirbelsäule relativ zum Bein oder die Winkelung des Hüftgelenks bildlich darzustellen. Die größte Schwierigkeit besteht vielmehr darin zu wissen, wie man vor der Hüftbeugung die Gesäß- und rückseitige Oberschenkelmuskulatur exzentrisch belastet und wie es sich anfühlt, die Füße mit der gesamten Sohle gleichmäßig gegen den Boden zu drücken.
Wenn es schwierig für Sie ist, sich das vorzustellen, können Sie nachvollziehen, warum ich der Meinung bin, dass Ihnen all das besser gezeigt als mit Worten beschrieben werden sollte. Und die beste Art, wie ich es Ihnen zeigen kann (außer direkt mit Ihnen zu arbeiten), ist ein Video, das Sie sich anschauen können und in dem ich die Übungen unter Anleitung meiner Kollegin Beth Lewis durchführe. (Den Link zu diesen Videos und eine kurze Beschreibung finden Sie am Ende des folgenden Kapitels.)
Der zweite Grund, warum ich mich gegen die genaue Beschreibung all dieser Übungen entschieden habe, ist, dass wir neu zu uns gekommene Patienten meist erst einmal vom Krafttraining abhalten, zumindest von solchem mit schweren Gewichten. Als ersten Schritt unterziehen wir sie einer Reihe von Kraft- und Bewegungstests, um nicht nur ihre körperliche Verfassung, sondern auch ihre Stabilität einschätzen zu können. Bevor Sie sich also ins Fitnessstudio begeben, bitte ich Sie dringend, das nächste Kapitel zu lesen, um das so wichtige und komplexe Konzept der Stabilität zu verstehen.
Kapitel 13
Das Hohelied der Stabilität
Bewegung neu lernen, um Verletzungen zu vermeiden
Je erhabener das Gebäude, desto tiefer muss sein Fundament sein.
Thomas von Kempen
Inzwischen dürfte klar sein, wie wichtig es ist, mit zunehmendem Alter in guter körperlicher Verfassung zu bleiben. Die Frage ist nur: Warum gelingt das so wenigen?
Eine typische Siebzigjährige wird weniger als halb so viel »moderate bis intensive« körperliche Aktivität zeigen wie mit vierzig Jahren – und ab siebzig beschleunigt sich der Niedergang noch. Bei Siebzig- und Achtzigjährigen ist Fitness die Ausnahme, nicht die Regel.
Es ist verlockend, das dem Alter an sich zuzuschreiben, den Wehwehchen und Beschwerden, die sich ab dem mittleren Lebensalter anhäufen, vom steten Rückgang der aeroben Kapazität und Kraft ganz zu schweigen. Weitere Faktoren wie Gewichtszunahme und Schlafstörungen können ebenfalls zu einer schlechten Verfassung beitragen. Ich vermute aber, dass der rätselhafte Faktor, der erklärt, warum so viele Menschen einfach aufhören, sich zu bewegen, noch ein anderer ist, nämlich Verletzungen. Will sagen: Ältere Menschen betätigen sich weniger oder gar nicht mehr körperlich, weil sie es schlichtweg nicht mehr können. Sie haben sich in irgendeiner Weise irgendwann in ihrem Leben verletzt und haben nie wieder zur Normalität zurückgefunden. Darum ging es mit ihnen immer weiter bergab.
Das traf ganz sicher auf Sophie zu, die Mutter meiner Freundin Becky; ich selbst hätte allerdings auch durchaus diesen Weg einschlagen können. Als Zwanzigjähriger, noch während meines Medizinstudiums, trainierte ich intensiv und hob fast täglich Gewichte. Damals erlitt ich eine mysteriöse Rückenverletzung, die zwei Operationen erforderte (von denen eine verpfuscht wurde). Es folgte eine lange und schwierige Erholungsphase. Monatelang konnte ich mich kaum rühren und kam nur mit großen Mengen an Schmerzmitteln über den Tag. Selbst das Zähneputzen verursachte mir heftige Rückenschmerzen, und die meiste Zeit des Tages verbrachte ich auf dem Boden liegend. Es ging mir derart schlecht, dass meine Mutter nach Palo Alto kommen und sich um mich kümmern musste. Nun, wenn einem Zwanzigjährigen so etwas passiert, denkt jeder, wie furchtbar das doch ist (und das ist es), aber bei jemandem in Sophies Alter erwartet man solche Vorkommnisse fast.
Sophie und ich waren keine Einzelfälle: Derlei Verletzungen und chronische Schmerzen sind erschreckend weit verbreitet. Nach Angaben der US-amerikanischen Gesundheitsbehörde CDC leiden mehr als 27 Prozent der Amerikaner jenseits der fünfundvierzig unter chronischen Schmerzen, und etwa zehn bis zwölf Prozent sagen, dass Schmerzen ihre Aktivität in den letzten sechs Monaten »an den meisten Tagen oder jeden Tag« eingeschränkt haben.[297] An den meisten Tagen oder sogar jeden Tag! Vor allem Rückenschmerzen sind ein Grund für die Verschreibung von Opioiden und für operative Eingriffe von oft zweifelhaftem Wert.[298] Sie sind weltweit eine führende Ursache für Arbeitsunfähigkeit[299] und verursachen geschätzt allein in den USA sage und schreibe 635 Milliarden Dollar an Kosten für medizinische Behandlungen und durch Produktionsausfälle.
Wie ich am eigenen Leib erfahren musste, hilft Ihnen alle kardiorespiratorische (aerobe) Fitness oder Kraft dieser Welt nicht weiter, wenn Sie sich verletzen und einige Monate – oder für immer – mit dem Training aussetzen müssen. Studien mit Athleten im Studentenalter, die während ihrer Sportkarriere Verletzungen erlitten, ergaben, dass diese durchgängig über eine geringere Lebensqualität im mittleren und höheren Alter berichteten.[300] Ihre Verletzungen machen ihnen nicht nur körperlich, sondern auch psychisch weiter zu schaffen, für Jahrzehnte ihres Lebens. Während meiner langen Leidenszeit wurde mir klar, wie wichtig unsere körperliche Funktionsfähigkeit für unser allgemeines Wohlbefinden ist.
Alles bisher Beschriebene, Forschungsergebnisse und meine persönliche Erfahrung stützen meine wichtigste Fitnessempfehlung: Achten Sie vor allem anderen darauf, sich nicht zu verletzen.
Wie können wir das? Meiner Ansicht nach ist Stabilität der wichtigste Faktor, doch es braucht auch ein Umdenken. Wir müssen uns von der Einstellung verabschieden, dass wir all unsere Work-outs bei jedem Besuch im Fitnessstudio immer weiter steigern sollen – Tag um Tag die meisten Wiederholungen, die schwersten Gewichte. Wie ich lernen musste, führt dieser ständige Leistungszwang ohne eine angemessene Stabilität fast unweigerlich zu Verletzungen. Wenn Sie kaum durch Ihr Work-out kommen, greifen Sie letztlich womöglich auf Ihre ganz eigenen körperlichen Schummeleien zurück, potenziell gefährliche Bewegungsmuster, die zur Gewohnheit geworden sind.
Stattdessen müssen wir uns darauf fokussieren, die Dinge richtig zu machen und sichere, optimale Bewegungsmuster zu kultivieren, die unserem Körper seinem Bau entsprechende Bewegungen erlauben und das Risiko von Verletzungen reduzieren. Besser smart – als zu hart. Doch wie ich aus eigener Erfahrung weiß, ist es nicht leicht, sich neue Bewegungsmuster anzueignen.
Stabilität wird oft mit den Core-Muskeln (englisch core, »Kern«) in Verbindung gebracht, doch es gehört mehr dazu als kräftige Bauchmuskeln (die sowieso nicht allein die Core-Muskulatur bilden). Meiner Ansicht nach ist Stabilität für jede Form von Bewegung unerlässlich, besonders wenn man diese Bewegung noch jahrzehntelang ausüben möchte. Stabilität ist das Fundament, auf dem die beiden Säulen kardiovaskuläre Fitness und Kraft stehen. Ohne sie stehen Sie im Wortsinne schlecht da. Vielleicht wird es nicht sofort passieren, aber früher oder später werden Sie wahrscheinlich eine Verletzung erleiden, die Sie in Ihrer Bewegung einschränkt, Ihnen mit zunehmendem Alter die täglichen Aktivitäten erschwert und für Sie vielleicht den Zehnkampf der Hundertjährigen vorzeitig beendet.
Eines hat mich das Stabilitätstraining gelehrt: Die meisten »akuten« Verletzungen, wie ein Riss des vorderen Kreuzbandes oder ein Riss in der ischiocruralen Muskulatur, treten nicht unvermittelt auf. Mag sein, dass sie sich plötzlich bemerkbar machen – durch heftige Rücken- oder Nacken- oder Knieschmerzen –, aber dem ging wahrscheinlich eine chronische Schwäche oder mangelnde Stabilität an der Basis des Gelenks voraus, und das ist der eigentliche Übeltäter. Ein Eisberg, der im Wasser treibt. Die »akute« Verletzung ist nur das, was wir sehen, die Manifestation der zugrunde liegenden Schwäche. Wenn wir also die Ziele erreichen wollen, die wir uns in unserem Zehnkampf der Hundertjährigen gesetzt haben, müssen wir alle möglichen Verletzungen, die wie treibende Eisberge auf uns lauern, vorausahnen und umschiffen. Dazu müssen wir verstehen, was Stabilität bedeutet, und sie in unsere Trainingsroutine einbauen.
Es fällt schwer, Stabilität präzise zu definieren, aber intuitiv wissen wir, was damit gemeint ist. Eine technische Definition könnte so lauten: Stabilität ist die unbewusste Fähigkeit, eine Kraft zu zügeln, abzubremsen oder zum Halten zu bringen. Eine stabile Person kann auf interne oder externe Stimuli reagieren, indem sie ihre Haltung und Muskelspannung entsprechend anpasst, und das überwiegend unbewusst.
Ich erkläre Stabilität gern mit einer Analogie aus meiner Lieblingssportart, dem Autorennsport. Vor ein paar Jahren fuhr ich zu einer Rennstrecke in Südkalifornien, um dort ein paar Tage mit meinem Coach zu trainieren. Zum Aufwärmen drehte ich ein paar Runden mit meinem damaligen Privatwagen, einem modifizierten BMW M3 Coupé mit einem starken 460-PS-Motor. Nach Monaten des Kriechens über verstopfte Autobahnen in Südkalifornien war es herrlich, die Kurven auszufahren und die Geraden entlangzujagen.
Dann wechselte ich zu dem Rennauto, das wir gemietet hatten, im Grunde eine abgespeckte, renntaugliche Version des beliebten BMW 325i. Dessen Motor war zwar mit 165 PS um zwei Drittel weniger stark als mein Privatauto, aber meine Rundenzeiten waren mit ihm trotzdem mehrere Sekunden besser, und das ist im Autorennsport eine Ewigkeit. Was bewirkte diesen Unterschied? Das um 20 Prozent geringere Gewicht des Rennwagens spielte eine Rolle, aber viel wichtiger noch waren sein kompakteres Fahrgestell und seine stärker haftenden Rennreifen. Zusammen brachten sie mehr Motorkraft auf die Strecke, sodass wir mit diesem Auto viel schneller durch die Kurven kamen. Mein Privatwagen war zwar auf den langen Geraden schneller, insgesamt aber langsamer, weil er die Kurven nicht so effizient nehmen konnte. Das Rennauto war schneller, weil es stabiler war.
Ohne Stabilität nützte mir der stärkere Motor meines Privatwagens nichts. Wenn ich versuchte, mit ihm so schnell durch die Kurven zu kommen wie mit dem Rennwagen, driftete ich regelmäßig aus der Strecke. Auf das Fitnessstudio übertragen, ist mein Privatwagen der Typ mit den dicken Muskelpaketen, der die schwersten Gewichte auf die Stange packt, aber irgendwie dauernd verletzt ist (und kaum etwas anderes machen kann, als im Studio Gewichte zu stemmen). Das Rennauto ist der unauffällige Typ, der im Kreuzheben sein doppeltes Körpergewicht schafft, beim Tennis einen schnellen Aufschlag hat und am nächsten Tag noch einen Berglauf macht. Er sieht nicht unbedingt stark aus. Aber weil er nicht nur seine Kraft, sondern auch seine Stabilität trainiert hat, können seine Muskeln über seinen gesamten Körper viel mehr Kraft entfalten, von den Schultern bis zu den Füßen, und dabei seinen empfindlichen Rücken und die Kniegelenke schützen. Er ist wie ein streckentaugliches Rennauto: stark, schnell, stabil – und gesund, weil seine ausgeprägte Stabilität ihm erlaubt, all diese Dinge zu tun, und er sich dabei nur selten, wenn überhaupt, verletzt.
Natürlich ist mein Straßenwagen bei einer langen Fahrt viel bequemer; keine Analogie ist vollkommen. Aber der Vergleich funktioniert dennoch, weil er uns dazu bringt, Stabilität im dynamischen Zusammenhang zu sehen. Leider werden die Wörter stabil und Stabilität allzu oft mit statischen Begriffen wie stark und im Gleichgewicht benutzt. Ein Baum ist stabiler als ein Setzling. Ein Jenga-Turm bleibt nur stehen, solange er stabil ist. Doch im Zusammenhang mit Sport und Bewegung interessiert uns nicht, wie starr etwas ist. Wir wollen lieber darüber nachdenken, wie Kraft effizient und sicher durch etwas weitergeleitet werden kann.
Sicher – das ist das entscheidende Wort. Fehlt die Stabilität, muss die ganze Extrakraft irgendwohin. Wenn der starke Motor meines Straßenwagens nur einen Teil seiner Kraft über die Reifen auf die Straße überträgt, verschwindet der Rest der ganzen Energie irgendwo, in erster Linie in der Reibung und in nicht produktiver Bewegung. Teile des Autos, die sich eigentlich nicht gegeneinander bewegen sollten, tun genau das. Es mag Spaß machen, mit einem Auto durch die Kurve zu driften, aber die verlorene Energie schädigt die Reifen und belastet die Aufhängung. Beide werden nicht lange halten. Passiert dies mit unserem Körper, erfolgt diese sogenannte Dissipation (»Zerstreuung«) der Kraft über den Weg des geringsten Widerstandes – meist über Gelenke, wie Knie, Ellbogen und Schultern, und/oder die Wirbelsäule. Sie alle werden irgendwann versagen. Gelenkverletzungen sind fast immer die Folge eines solchen »Energielecks«.
Insgesamt hilft uns Stabilität dabei, die größte Kraft in der denkbar sichersten Weise aufzubringen, indem sie die unterschiedlichen Muskelgruppen unseres Körpers verbindet und so das Verletzungsrisiko für unsere Gelenke, unser Weichgewebe und besonders unsere empfindliche Wirbelsäule deutlich senkt. Unser Ziel ist es, sich kraftvoll, flüssig, flexibel und agil in der Welt zu bewegen.
Stabilität in Bewegung ist manchmal ein großartiger Anblick. Stabilität lässt einen dünnen Pitcher beim Baseball einen wuchtigen Ball werfen. Stabilität erlaubt Kai Lenny, am Surfspot Jaws auf Maui haushohe Wellen zu reiten. Aber Stabilität erlaubt auch einer Frau von fünfundsiebzig Jahren, verletzungsfrei Tennis zu spielen. Stabilität bewahrt eine achtzigjährige Großmutter davor zu stürzen, wenn sie einen unerwartet hohen Bordstein hinuntersteigt. Stabilität gibt einem Fünfundneunzigjährigen das Selbstvertrauen, mit seinem geliebten Hund im Park spazieren zu gehen. Sie lässt uns das weitermachen, was wir lieben. Und wenn uns Stabilität fehlt, werden unweigerlich üble Folgen eintreten – wie es bei mir war, bei Sophie und bei Millionen von Menschen mit einstmals guter Fitness.
Meine schmerzhafte Rücken-Episode markierte nur den Anfang meiner Verletzungskarriere. Einmal absolvierte ich ein Langstreckenschwimmen zwischen Catalina und dem kalifornischen Festland mit angerissener Knorpellippe (Labrum) des Schultergelenks, was zweifellos dadurch verschlimmert worden war, dass ich vier Stunden täglich im Pool und im Meer trainiert hatte, auch als ich die Schmerzen bereits wahrgenommen hatte.[301] Mehr als 15 Jahre später musste ich die Sache operativ behandeln lassen. Das war der Preis dafür, dass ich es in einer bestimmten Sportart so übertrieben hatte. Ich brauchte allerdings noch einige Jahrzehnte, bis ich allmählich begriff, warum ich mir den Rücken verletzt hatte.
Diese Erkenntnis verdanke ich Beth Lewis, einer früheren Profitänzerin und Kraftdreikämpferin, die inzwischen als Trainerin und Rundum-Bewegungsgenie arbeitet und damals in New York lebte. (Inzwischen habe ich sie überredet, nach Austin zu ziehen.) Wir hatten uns kaum begrüßt, da forderte sie mich schon auf, mein Hemd auszuziehen und Kniebeugen zu machen. Ich gehorchte – und sie war nicht gerade beeindruckt. Ich war geknickt. Ich hatte mich immer als jemand gesehen, der wusste, was er im Studio tat. Nun wurde mir gesagt, dass ich nicht einmal eine einfache Kniebeuge richtig hinbekam.
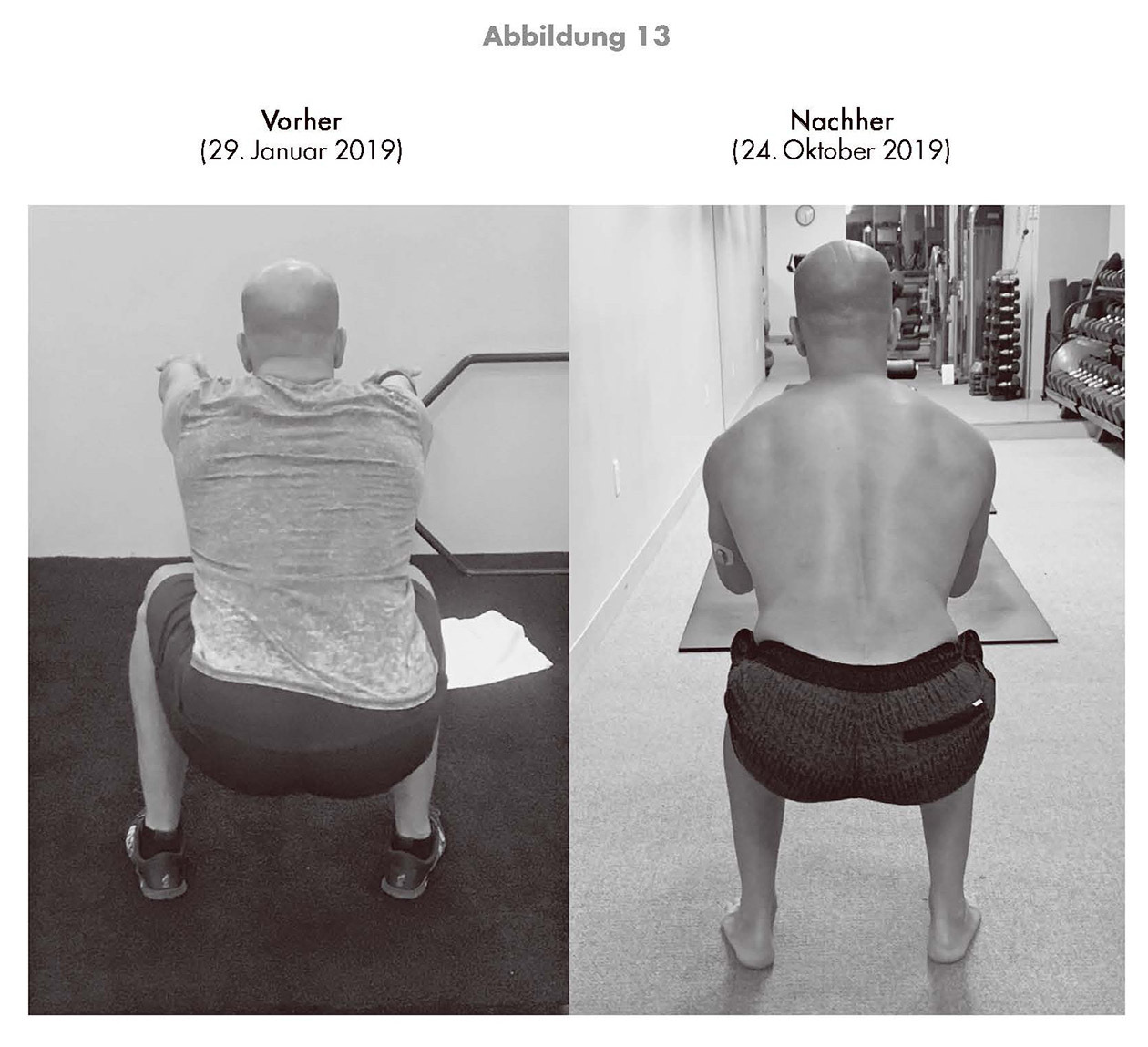
Ihr Handyvideo erzählte eine traurige Geschichte, wie Sie dem »Vorher«-Foto links in Abbildung 13 entnehmen können: Während ich meine Hüften anspannte und herunterging, verlagerte ich automatisch meinen ganzen Körper nach rechts. Ich sehe aus, als würde ich gleich umkippen. Mein Problem bestand, wie diese Bilder schmerzhaft deutlich machen, darin, dass mir die Stabilität fehlte. Noch heute tut es mir weh, das Bild anzuschauen, denn es erinnert mich an Tausende von grauenhaften, belastenden Kniebeugen, die ich in dieser merkwürdigen Haltung durchgeführt habe.
Mir war damals nicht einmal bewusst, dass ich es so machte, aber wahrscheinlich kompensierte ich auf diese Weise verschiedene Verletzungen und Schwächen, die ich im Laufe der Jahre angesammelt hatte. Ich lernte, wie das läuft: Wir versuchen, unsere bestehenden Verletzungen und Einschränkungen zu umgehen oder uns um sie herumzumogeln, und am Ende stehen wir vor neuen Problemen. Diese Verlagerung nach rechts könnte sogar meine Rückenverletzung als Zwanzigjähriger erklären; selbst damals hatte ich bereits seit Jahren schwere Gewichte gehoben. Es sollte neun Monate dauern, die Sache wieder in Ordnung zu bringen, doch letztlich ging ich gestärkt daraus hervor, wie Sie im »Nachher«-Foto rechts sehen können. Ich musste nicht nur meinen Körper umtrainieren, sondern auch mein Gehirn.
Sowohl Beth als auch Michael Stromsness, ein Trainer, mit dem ich in Kalifornien gearbeitet und der mich mit Beth bekannt gemacht hatte, beherrschten eine Methode, von der ich noch nie gehört hatte. Die dynamische neuromuskuläre Stabilisation, kurz DNS, klingt kompliziert, basiert aber auf unseren einfachsten, natürlichsten Bewegungen: jenen Bewegungen, die wir als Babys machten.
Hinter DNS steckt die Theorie, dass die Abfolge von Bewegungen, die kleine Kinder beim Laufenlernen absolvieren, nicht zufällig ist, sondern Teil eines neuromuskulären Entwicklungsprogramms, das für unsere Fähigkeit zur korrekten Bewegung unerlässlich ist.[302] Während wir nach und nach diese Bewegungen durchführen, lernt unser Gehirn, unseren Körper zu steuern und optimale Bewegungsmuster zu entwickeln.
Die DNS wurde von einer Gruppe tschechischer Neurologen entwickelt, die in den 1960er-Jahren in einer Prager Klinik mit Kindern arbeiteten, welche unter infantiler Zerebralparese litten. Wie sie feststellten, durchliefen diese Kinder aufgrund ihrer Erkrankung nicht die üblichen Stadien der Bewegungsentwicklung wie Robben, Krabbeln und so fort. Darum hatten sie ihr Leben lang Bewegungsprobleme. Ließ man aber betroffene Kinder ein »Trainingsprogramm« durchlaufen, das eine bestimmte Abfolge von Bewegungen umfasste und die üblichen Lernstufen von Krabbeln, aufrechtem Sitzen und schließlich Stehen nachahmte, verbesserten sich ihre Symptome, und sie konnten mit dem Heranreifen ihre Bewegungen besser steuern. Die Forscher erkannten, dass die meisten gesunden Menschen im Heranwachsen eigentlich einen umgekehrten Prozess durchlaufen – wir verlieren nach und nach diese natürlichen, gesunden, tief in uns verwurzelten Bewegungsmuster.
Daher kommt es, dass mein jüngster Sohn Ayrton eine perfekte tiefe Kniebeuge hinbekommt, indem er seinen kleinen Po fast bis zum Boden senkt und die Knie extrem beugt, dabei aber vollkommen kraftvoll und im Gleichgewicht bleibt. Absolut meisterhaft. Als ich jedoch dieselbe Bewegung auszuführen versuchte, endete ich in derselben entwürdigend schiefen Position wie auf dem »Vorher«-Foto; ein Hüftgelenk wies zum Boden, die Schultern waren schief, und meine Füße kippten auswärts. Mein Kleinkind kann Kniebeugen, ich offensichtlich nicht.
Und auch nicht meine vierzehnjährige Tochter Olivia (jedenfalls nicht, bis Beth mit ihr arbeitete). Biegsam wie Plastilin, dünn, aber stark, hätte sie eigentlich genauso gut oder besser Kniebeugen machen sollen wie ihr jüngster Bruder. Aber sie konnte es nicht, denn schon in diesem Alter hatte sie zwei Drittel ihres Lebens in der Schule zugebracht, meist auf einem Stuhl sitzend. Die optimalen Bewegungsmuster, die sie als Klein- und Krabbelkind erlernt hatte, wurden wieder gelöscht, bevor sie die für richtige Kniebeugen erforderliche Stabilität in den Hüftgelenken entwickelt hatte. Wenn sie die nächsten 30, 40 oder 50 Jahre überwiegend auf Stühlen sitzend verbringt (was wahrscheinlich ist), wird sie im selben Boot sitzen wie so viele meiner Patienten und auch ich selbst. Wir haben allesamt vergessen, wie wir unsere Körper richtig bewegen.
Die meisten Erwachsenen bekommen keine korrekte Kniebeuge hin, selbst ohne zusätzliches Gewicht. Der einzige Weg, wie viele von uns die Kniebeuge eines Kleinkindes annähernd imitieren können, ist auf dem Rücken liegend, wie Michael Stromsness in einer unserer frühen Einheiten an mir demonstrierte. In dieser Position fällt es viel leichter, die Knie zu einer perfekten Kniebeuge zu heben, mit der richtigen Wölbung der Wirbelsäule von der Schädelbasis bis ins Steißbein. Es ist also nicht die Beweglichkeit an sich, die die meisten Erwachsenen von der richtigen Kniebeuge abhält; vielmehr gelingt es durchschnittlichen Erwachsenen bei Belastung durch ein Gewicht, und sei es nur das eigene Körpergewicht, nicht mehr, ihren Rumpf zu stabilisieren.
Bei der DNS geht es darum, unseren Körper – und unser Gehirn – neu zu trainieren, in jenen Bewegungsmustern, die wir einst als kleine Kinder erlernten. Michael Rintala, ein führender DNS-Praktiker in den USA, beschreibt es so: »DNS ergänzt ganz wunderbar all die gute Arbeit, die Sie schon machen – wie ein Software-Upgrade für alles, was Sie gerade tun.«[303]
Meine eigene Software brauchte dringend ein Upgrade.
Die Einzelheiten meiner Reise sind zu verwickelt, um sie hier in Gänze zu schildern, aber auf den restlichen Seiten dieses Kapitels möchte ich versuchen, wenigstens einige Grundprinzipien des Stabilitätstrainings zu erläutern. Diese mögen auf den ersten Blick etwas seltsam erscheinen, und wenn Sie sich von diesem Kapitel Tipps für ein Power-Work-out versprochen haben, werden Sie vielleicht enttäuscht. Eigentlich ist genau das unser Thema: In meiner Praxis ermuntern wir am liebsten erst dann zu richtigem Krafttraining (auch vielen der hier beschriebenen Selbsttests, wie Dead Hangs und Step-ups mit Gewichten), wenn wir einen gewissen Stabilitätsmodus erreicht haben. Denn wir denken, dass es das Risiko nicht wert ist. Wie beim Konstruktionswesen lohnt sich der Zeitaufwand, um ein solides Fundament zu errichten, auch wenn sich das Projekt daraufhin um ein paar Monate länger hinzieht.
Eine Anmerkung vorweg: Beim Trainieren von Kraft und aerober Kondition ist die Sache ziemlich eindeutig; hinsichtlich der Stabilität aber hat jeder so seine ganz eigenen Probleme. Und es ist unmöglich, eine Anleitung zu geben, die auf jeden passt. Daher möchte ich die restlichen Seiten dieses Kapitels nutzen, um Ihnen zu vermitteln, wie Ihr Körper mit der Welt interagiert – und worum es bei Stabilität letztlich überhaupt geht. Wenn Sie nach der Lektüre dieses Kapitels noch mehr erfahren wollen, empfehle ich Ihnen die Websites zur DNS (https://www.rehabps.com) und des Postural Restoration Institute (PRI, https://www.posturalrestoration.com), der beiden führenden Vertreter dessen, worum es hier geht. Stabilität ist ein integraler Bestandteil meines Trainingsprogramms. Zweimal wöchentlich mache ich eine Stunde lang gezieltes Stabilitätstraining nach den Prinzipien der DNS, des PRI und anderer Praktiken; an den übrigen Tagen widme ich ihm jeweils zehn bis fünfzehn Minuten.
Stabilitätstraining beginnt ganz unten an der Basis, nämlich mit der Atmung.
Beim Atmen geht es um viel mehr als nur den Gasaustausch oder gar kardiorespiratorische Fitness. Wir atmen täglich mehr als 20 000-mal ein und aus, und die Art, wie wir das tun, hat großen Einfluss darauf, wie wir uns bewegen und wie unser mentaler Zustand ist. Beth drückt es so aus: Wir sind, wie wir atmen.
Die Verbindung zwischen Körper, Geist und Atmung ist all jenen bereits bekannt, die schon mehrere Pilates- oder Yogakurse besucht haben oder meditieren. Bei diesen Praktiken ist die Atmung der Anker, der Prüfstein, unser Zeitmesser. Sie ist der Spiegel unserer mentalen Verfassung und beeinflusst diese auch. Wenn etwas mit unserer Atmung nicht stimmt, kann das unser mentales Gleichgewicht durcheinanderbringen und Ängste und Sorgen auslösen; Ängste aber können ihrerseits alle Atemprobleme verstärken, die wir schon haben. Das liegt daran, dass tiefe, gleichmäßige Atemzüge unser parasympathisches Nervensystem aktivieren, das beruhigend wirkt, während eine schnelle oder unregelmäßige Atmung dessen Gegenspieler aktiviert, das sympathische Nervensystem, das Teil der Kampf-oder-Flucht-Reaktion des Körpers ist.
Die Atmung ist außerdem wichtig für Stabilität und Bewegung, ja sogar für die Kraft. Eine schlechte oder gestörte Atmung kann unsere motorische Kontrolle beeinträchtigen und uns verletzungsanfällig machen, das belegen Studien. Bei einem Experiment kamen die Forscher zu dem Ergebnis, dass eine Reduktion des für die Atmung verfügbaren Sauerstoffs in Kombination mit einer Gewichtsbelastung bei den Versuchspersonen bewirkte, dass diese ihre Wirbelsäule weniger gut stabilisieren konnten. In den Alltag übersetzt heißt das: Jemand, der schwer (und unzureichend) atmet, während er Schnee schaufelt, hat ein erhöhtes Risiko für eine Rückenverletzung.
Die Art, wie jemand atmet, gibt subtile, aber enorm aufschlussreiche Hinweise darauf, wie die Person ihren Körper bewegt und, noch wichtiger, ihre Bewegungen stabilisiert. Wir führen mit unseren Patienten stets eine Reihe von Tests zur Atmung und Bewegung durch, um uns ein vollständiges Bild von ihrer Atmungsstrategie zu machen und davon, wie diese ihre Kraft und Stabilität beeinflusst.
Ein einfacher Test, dem wir jeden schon zu einem frühen Zeitpunkt unterziehen, verläuft so: Legen Sie sich auf den Rücken, mit einer Hand auf dem Bauch und einer auf der Brust, und atmen Sie ganz normal, ohne sich besonders zu bemühen oder darüber nachzudenken. Achten Sie nun darauf, welche Hand sich auf und ab bewegt – ist es die auf Ihrer Brust, die auf dem Bauch, oder sind es beide (oder keine von beiden)? Manche Menschen neigen dazu, den Brustkorb beim Einatmen zu weiten, während der Bauch flach ist oder sogar einsinkt. Das erzeugt eine Spannung im Oberkörper und um die Körpermitte, und wenn der Brustkorb geweitet bleibt, ist es schwierig, vollständig auszuatmen. Andere atmen vor allem »in den Bauch«, wodurch das Becken nach vorn kippt. Wieder andere nehmen eine komprimierte Haltung ein, haben also Schwierigkeiten, überhaupt Luft ein- und auszuatmen, weil sie den Brustkorb nicht mit jedem Einatmen weiten können.
Beth unterscheidet drei Typen von Atmungsformen und den entsprechenden Phänotypen, die sie scherzhaft als »Marshmallowmann« (Sie wissen schon, die Figur aus dem Film Ghostbusters), »traurige Type« und »Yogini« bezeichnet – alle mit unterschiedlichen Stabilitätsstrategien:
Der Marshmallowmann
Aufgebläht. Diese Personen sind Oberkörperatmer, die dazu neigen, sowohl zum Atmen als auch zum Stabilisieren ihre Wirbelsäule zu strecken. Die Lendenwirbelsäule ist überstreckt, das Becken nach vorn gekippt, sodass das Gesäß herausragt. Sie ziehen sich immer in sich selbst hoch und geben sich den Anschein, das Sagen zu haben. Sie haben nur begrenzt ein Empfinden dafür, sich mit den Füßen zu erden, und sind auch nur begrenzt dazu imstande, die Füße zur Stoßabsorption einzudrehen (stattdessen sind sie auswärtsgedreht). All dies macht sie sehr anfällig für Schmerzen im unteren Rücken sowie Anspannung von Waden und Hüfte.
Die traurige Type
Komprimiert. Alles an diesen Personen ist irgendwie zusammengedrückt und eng. Ihr Kopf ist vorgeneigt, ebenso ihre Schultern, die quasi nach vorn eingerollt sind, da die Betreffenden sie immer vorziehen, in dem Versuch, mehr Luft einzuatmen. Ihr mittlerer Rücken ist übermäßig gekrümmt oder kyphotisch, die Beweglichkeit von Hals und oberen Extremitäten ist eingeschränkt. Manchmal sind die Unterschenkel nach außen gedreht und die Füße ebenfalls. Die Schwerkraft zieht sie nach unten.
Die Yogini
Unkontrolliert. Diese Personen haben einen extremen passiven Bewegungsradius, also eine große Flexibilität – und eine extrem begrenzte Fähigkeit, diese aktiv zu kontrollieren. Sie können oft ihre Zehen anfassen und im Stehen die Hände flach auf den Boden legen, aber wegen ihrer mangelnden Kontrolle sind sie sehr anfällig für Gelenkverletzungen. Ständig versuchen sie, sich im Raum zu finden, sie zappeln und zucken; ihre übermäßige Flexibilität versuchen sie zu kompensieren, indem sie sich vor allem mit Hals und Kiefer stabilisieren. Es fällt ihnen sehr schwer, fettfreie Körpermasse (Muskulatur) aufzubauen. Manchmal sind sie sehr ängstlich, und möglicherweise haben sie eine gestörte Atmung.
Nicht jeder entspricht genau einem von diesen drei Typen; viele von uns werden aber zumindest einige dieser Merkmale bei sich selbst wiederfinden. Es gibt auch Überschneidungen; es ist beispielsweise durchaus möglich, gleichzeitig eine traurige Type oder ein Marshmallowmann und eine Yogini zu sein, denn bei der Yogini geht es vor allem um den Mangel an muskulärer Kontrolle.
Ich war ein aufgeblähter Marshmallowmann, so sagte es mir Beth: Wenn ich einatmete, spreizte sich mein Brustkorb, wie bei einem Gockel, der sich in die Brust wirft. Das brachte zwar Luft in meine Lunge, zog aber auch meinen Körperschwerpunkt nach vorn. Zum Ausgleich krümmte sich meine Wirbelsäule in eine Kyphose, und mein Gesäß ragte heraus (Beth nannte das »Entenpo«). Das überdehnte meine ischiocrurale Muskulatur und kappte de facto ihre Verbindung zum restlichen Körper, sodass ich keinen Zugriff auf diese Muskelgruppe hatte. All die Jahre, bevor mir dies klar wurde, hatte ich beim Kreuzheben nur meinen Rücken und meine Gesäßmuskeln benutzt, praktisch ohne Unterstützung meiner starken ischiocruralen Muskulatur. Was das Atmen anging, musste ich mich damit beschäftigen, die Luft loszuwerden, während jemand, der mehr in Richtung traurige Type tendiert, eher daran arbeiten sollte, Luft in die Lunge zu bekommen, etwa indem er durch die Nase und nicht durch den Mund einatmet.
Dem Atemtraining liegt die Vorstellung zugrunde, dass eine richtige Atmung viele weitere körperliche Parameter beeinflusst: die Position der Rippen, Streckung der Halswirbelsäule, Form der Wirbelsäule, ja sogar die Stellung unserer Füße auf dem Boden. Wie wir atmen, spiegelt wider, wie wir mit der Welt interagieren. »Dafür zu sorgen, dass dein Atem weit und dreidimensional und leicht sein kann, ist unerlässlich für das Entwickeln von guter, effizienter und koordinierter Bewegung«, so Beth.
Beth fängt gern mit einer Übung an, die die Atmung bewusst macht und das Zwerchfell stärkt; dieses ist nicht nur ein wichtiger Atemmuskel, sondern stabilisiert auch maßgeblich den Körper. Sie lässt die Patienten auf dem Rücken liegen, die Beine angewinkelt auf einer Bank oder einem Stuhl, und bittet sie, so ruhig und bewegungsarm wie möglich zu atmen. Eine optimale Einatmung dehnt den Brustkorb komplett nach vorne, zur Seite und nach hinten aus und zugleich auch den Bauch, sodass sich Zwerchfell und Beckenboden senken können. Entscheidend ist, dass die Atmung ruhig ist. Eine laute Einatmung sieht dramatisch aus und fühlt sich auch so an, da sich Hals, Brustkorb oder Bauch zuerst bewegen werden und sich das Zwerchfell nicht frei absenken kann; das erschwert das Einatmen.
Anschließend sollen die Patienten komplett mit gespitzten Lippen ausatmen, um Kompression und Luftwiderstand zu maximieren und das Zwerchfell zu kräftigen. Pusten sie so alle Luft hinaus und entleeren ihre Lunge vollständig, spüren sie, dass ein komplettes Ausatmen eine gute Vorbereitung für ein tiefes Einatmen ist und umgekehrt. Dies soll zwei- bis dreimal mit je fünf Atemzügen wiederholt werden. Dabei ist auf eine mindestens zwei Sekunden währende Pause nach dem Ausatmen zu achten, um die isometrische Kontraktion zu halten – das ist bei der DNS entscheidend.
Bei der DNS lernen Sie, sich den Bauch als einen Zylinder vorzustellen, umgeben von einer Wand aus Muskeln, mit dem Zwerchfell als Ober- und dem Beckenboden als Unterseite. Ist der Zylinder aufgebläht, spürt man den intraabdominalen Druck (intraabdominal pressure, kurz IAP). Dieser ist entscheidend für die echte Aktivierung der Core-Muskeln und für das DNS-Training von grundlegender Bedeutung. Für eine sichere Bewegung ist es wichtig zu lernen, den Zylinder komplett unter (intraabdominalen) Druck zu setzen, denn er stabilisiert wirksam die Wirbelsäule.
Noch eine schnelle Übung, um zu verdeutlichen, wie Sie IAP erzeugen können: Atmen Sie komplett ein, sodass es sich anfühlt, als blähten Sie den Zylinder auf allen Seiten auf und zögen die Luft bis hinunter zum Beckenboden, der Unterseite des Zylinders. Natürlich »atmen« Sie nicht bis dorthin in dem Sinne, dass Luft bis in Ihr Becken kommt; Sie streben eine maximale Lungenausdehnung an, die ihrerseits das Zwerchfell nach unten drückt. Fokussieren Sie sich mit jedem Einatmen darauf, den Zylinder in seinem gesamten Durchmesser auszudehnen, und heben Sie nicht nur die Bauchdecke. Wenn Sie dies korrekt ausführen, werden Sie bemerken, dass sich Ihr Hosenbund rundherum spannt, auch im Rücken und nicht nur am Bauch. Beim Ausatmen hebt sich das Zwerchfell wieder, und die Rippen sollten sich wieder einwärtsbewegen, während sich Ihr Hosenbund wieder zusammenzieht.
Dieses Einatmen erzeugt eine Spannung, und beim Ausatmen halten Sie diese Muskelspannung in Ihrer gesamten Zylinderwand. Dieser intraabdominale Druck ist die Grundlage für unser komplettes Stabilitätstraining, beim Kreuzheben, bei Kniebeugen, bei einfach allem. Es ist wie bei einer Plastikflasche: Ohne Deckel können Sie sie mit einer Hand zusammendrücken, ist der Deckel aber zugeschraubt, herrscht zu viel Druck im Inneren (also Stabilität), und die Flasche lässt sich nicht zusammendrücken. Ich praktiziere diese 360-Grad-Bauchatmung jeden Tag, nicht nur im Studio, sondern auch, wenn ich am Schreibtisch sitze.[304]
Ihr »Typ« gibt auch gewisse Hinweise darauf, wie Sie trainieren sollten. Marshmallowmann-Menschen brauchen oft mehr Erdung durch die Füße und mehr Arbeit mit einem Gewicht vor sich, um ihre Schultern und Hüften in eine neutralere Position zu bringen. Beth lässt Menschen wie mich meist ein Gewicht vor dem Körper halten, ungefähr eine Handbreit vor dem Brustbein. Das zwingt mich dazu, meinen Körperschwerpunkt nach hinten zu verlagern, mehr über meine Hüften. Versuchen Sie es einmal mit einer leichten Hantel oder einer Wasserflasche, dann verstehen Sie, was ich meine. Die Haltungsänderung ist gering, aber doch merklich.
Mit den traurigen Typen beiderlei Geschlechts arbeitet Beth eher an der Rotation quer über den gesamten Körper. Sie lässt sie die Arme quer über den Körper schwingen, um Brustkorb und Schultern zu öffnen. Vorsichtig ist sie mit der Gewichtsbelastung von Rücken und Schultern; hier beginnt sie lieber mit Übungen mit dem eigenen Körpergewicht und im Ausfallschritt, etwa einer Abfolge von Ausfallschritten (Walking Lunge) mit bei jedem Schritt nach oben oder quer vor dem Körper ausgestreckten Armen.
Den Yogini empfiehlt Beth angesichts ihrer mangelnden Gelenkkontrolle Übungen der »geschlossenen Kette«, bei denen das ausführende Körpersegment an beiden Enden fixiert ist. Das sind beispielsweise Liegestütze am Boden oder an der Wand, aber auch Trainingsgeräte mit definierter, begrenzter Bewegungsfreiheit. Geräte sind für diese Menschen wichtig, ebenso für Personen, die bislang nur wenig oder gar kein Training mit Gewichten gemacht haben, denn die Geräte lenken ihre Bewegungen in einem sicheren Rahmen. Für Yogini und Neulinge allgemein ist es wichtig, sich ihrer Position im Raum, auch im Bezug auf ihren Bewegungsradius, bewusster zu werden.
Allgemeiner betrachtet geht es darum, dass jemandes Atmung uns Einblicke in dessen generelle Strategie zur Stabilität verschafft, also jene Bewegungs- und Haltungsmuster, die er oder sie im Laufe der Jahre entwickelt hat, um mit der physikalischen Umwelt zurechtzukommen. Wir alle haben diese Strategien, und in 95 Prozent der Fälle funktionieren sie im Alltag wunderbar. Kommt aber dieser oder jener Stressor hinzu, etwa Geschwindigkeit, Gewicht oder Neuartigkeit und Nichtvertrautheit (etwa wenn man im Dunkeln eine Treppe hinabsteigt), können diese Strategien, diese instinktiven körperlichen Reaktionen, Probleme bereiten. Und wenn auch unsere Atmung strapaziert wird, verstärkt das die anderen Probleme noch.
Der Weg zur Stabilität beginnt mit der Atmung, aber wir beschreiten ihn mit den Füßen – der grundlegendsten Kontaktstelle zwischen unserem Körper und der Welt. Unsere Füße sind buchstäblich das Fundament für jede Bewegung, die wir machen. Ob wir etwas Schweres heben, gehen, laufen oder beim Rucking unterwegs sind, Treppen steigen oder an der Haltestelle auf den Bus warten, stets lenken wir Kraft durch unsere Füße. Leider haben viele von uns die grundlegende Kraft und das Bewusstsein für ihre Füße verloren, weil diese zu oft in Schuhen stecken – besonders in großen Schuhen mit dicken Sohlen.
Um auf meine Rennauto-Analogie zurückzukommen – unsere Füße sind quasi die Reifen, der einzige Kontaktpunkt zwischen Auto und Straße. Die Kraft des Motors, die Stabilität und Steifheit des Fahrwerks, das Können des Fahrers – all das ist nutzlos, wenn die Reifen keinen festen Grip auf der Fahrbahn haben. Ich sage sogar, dass die Füße für uns wichtiger sind als die Reifen für das Auto, denn sie spielen überdies noch eine wichtige Rolle als Stoßdämpfer, bevor eine einwirkende Kraft die Knie, Hüftgelenke und den Rücken erreicht. Sich nicht um seine Füße zu kümmern ist für mich so, als würde man sich einen McLaren Senna (mein Traumauto) kaufen und dann die billigsten Reifen aufziehen, die man bekommen kann. Genau das ist es, was viele Jahre in schlechtem Schuhwerk mit unseren Füßen machen.
Betrachten Sie noch einmal mein »Vorher«-Foto. Ja, meine Hüfte ist offensichtlich schief, aber schauen Sie sich einmal genau meine Füße an. Stehen sie flach auf dem Boden? Nein, das tun sie nicht. Wie Sie deutlich sehen können, sind sie auf die Außenkanten gekippt, also in der »Supination«, so die physiologische Bezeichnung. Sie sollten flach, geerdet, stabil und stark dastehen, um mein Gewicht zu tragen. Stattdessen sind sie eingedreht und wackelig. Kein Wunder, dass meine Kniebeuge mies aussieht.
Um uns wieder mit unseren Füßen vertraut zu machen, unterzieht Beth mich und unsere Patienten gern einer Routine, die sie »Zehenyoga« nennt. Dieses Zehenyoga (das ich übrigens nicht ausstehen kann) umfasst eine Reihe von Übungen, die die Geschicklichkeit und eigene Kraft unserer Zehen ebenso stärken soll wie unsere Fähigkeit, sie bewusst zu steuern. Wenn Sie ins Studio gehen, denken Sie vermutlich nicht an die Kraft Ihrer Zehen, doch das sollten Sie. Unsere Zehen sind unerlässlich für das Gehen, Laufen und Heben, insbesondere aber für das Abbremsen und Absenken des Körpers. Besonders die große Zehe ist für den Abstoß bei jedem Schritt notwendig. Ist sie nicht gestreckt, kann das zu Gangstörungen führen und sogar bewirken, dass wir mit zunehmendem Alter nicht mehr ohne Hilfe vom Boden aufstehen können. Ist die Zehenkraft eingeschränkt, sind alle oberhalb davon befindlichen Glieder der Kette – Knöchel, Knie, Hüfte, Wirbelsäule – verwundbarer.
Zehenyoga ist schwieriger, als es sich anhört, darum habe ich unter https://www.peterattiamd.com/outlive/videos ein Video mit Anleitung eingestellt. Beth rät ihren Schülern immer, sich vorzustellen, ihre Füße hätten vier Ecken, die alle vier jederzeit fest auf dem Boden ruhen sollten, wie die Beine eines Stuhls. Versuchen Sie, wenn Sie so dastehen, bei jeder »Ecke« jedes Fußes zu spüren, wie sie sich an den Boden drückt: die Basis der großen Zehe, die Basis der kleinen Zehe, die Innen- und die Außenseite der Ferse. Das ist einfach und erhellend: Wann haben Sie sich das letzte Mal so geerdet gefühlt?
Versuchen Sie einmal, alle zehn Zehen anzuheben und so weit zu spreizen, wie Sie können. Nun versuchen Sie, nur die große Zehe auf den Boden abzusenken, während die anderen angehoben bleiben. Gar nicht so leicht, nicht wahr? Jetzt umgekehrt: Belassen Sie jeweils vier Zehen auf dem Boden, und heben Sie nur die großen Zehen. Heben Sie nun alle fünf Zehen, und versuchen Sie, diese eine nach der anderen abzusenken, beginnend mit der großen Zehe. (Sie wissen jetzt, was gemeint ist.)[305]
Dies erfordert, wenn ich es denn überhaupt fertigbringe, enorme mentale Konzentration; das Gehirn muss der großen Zehe befehlen, dass sie sich senken oder anheben soll – und genau darum geht es. Eines der Ziele des Stabilitätstrainings ist es, die mentale Kontrolle – ob bewusst oder nicht – über entscheidende Muskeln und Körperteile wiederzuerlangen. Weil unsere Füße so viel Zeit in mehr oder weniger passende Schuhe gezwängt verbringen, die wahrscheinlich auch noch stark gepolsterte Sohlen aufweisen, haben viele den Kontakt zu ihren Füßen verloren oder diese mit der Zeit in missliche Fehlstellungen gebracht.
Bei meinem »Vorher«-Foto sind, wie schon angemerkt, meine beiden Füße auf der Außenkante nach innen gedreht (Supination). Häufig werden die Füße auch auf die Innenkante geknickt und dabei nach außen gedreht (Pronation). Wer sich schon einmal Laufschuhe im Fachhandel gekauft hat, kennt beide Begriffe vielleicht schon. Beth vergleicht die Pronation mit einem großen Auto, das zu wenig Luft in den Reifen hat; die Bewegungen sind dabei irgendwie platschend und übertragen die Kraft nur unzureichend auf den Boden. Die Supination dagegen erinnert an Autoreifen mit zu viel Druck, sodass man ins Schleudern und Springen kommt. Die Füße sind dann nicht imstande, Stöße abzufedern, und all das Hüpfen und Rütteln wird ungedämpft auf die Knöchel, Knie, Hüftgelenke und den unteren Rücken übertragen. Beide Syndrome, Pronation und Supination, bergen zudem das Risiko für eine Plantarfasziitis (Faszienentzündung der Fußsohle), Kniegelenksschäden und mehr. Wir müssen imstande sein, uns in die und aus der Pronation und Supination zu bewegen, um uns effizient fortzubewegen. Wenn ich heute Kniebeugen oder irgendeine Hebeübung im Stand mache, stelle ich zuerst meine Füße fest auf, mache mir ihre vier »Ecken« bewusst und verteile das Gewicht gleichmäßig. (Wichtig auch: Ich hebe am liebsten barfuß oder in minimalistischem Schuhwerk Gewichte, ohne große Polsterung an den Sohlen, sodass ich meine Fußsohlen die ganze Zeit komplett spüre.)
Die Füße sind auch für das Gleichgewicht entscheidend, ein weiteres wichtiges Element der Stabilität. Ein zentraler Test bei unserer Einschätzung der Bewegung läuft folgendermaßen: Unsere Patienten sollen sich so hinstellen, dass ein Fuß vor dem anderen steht, und nach Möglichkeit das Gleichgewicht halten. Dann sollen sie die Augen schließen und schauen, wie lange sie die Position halten können. Zehn Sekunden sind schon eine respektable Zeit; tatsächlich ist die Fähigkeit, im Alter von fünfzig oder mehr Jahren auf einem Bein stehen zu können, mit der Lebenserwartung korreliert, ebenso wie die Handkraft.[306] (Mein Tipp: Balancieren wird viel leichter, wenn man sich vorher auf das bewusste feste Aufstellen der Füße konzentriert, wie oben beschrieben.)
Die Struktur, die wir ganz besonders schützen wollen und der beim Stabilitätstraining ganz allgemein große Aufmerksamkeit gilt, ist die Wirbelsäule. Wir verbringen so viel von unserer Zeit in Autositzen, auf Schreibtischstühlen, vor Computern und auf unsere diversen Geräte blickend, dass das moderne Leben manchmal wie ein konzertierter Angriff auf die Integrität unserer Wirbelsäule erscheint.
Diese ist in drei Abschnitte geteilt, Lenden- (unterer Rücken), Brust- (mittlerer und oberer Rücken) und Halswirbelsäule. Radiologen sehen derart viele Degenerationen in der Halswirbelsäule, Folgen des jahrelangen Schauens auf Mobiltelefone mit gebeugtem Kopf, dass sie diese als »Tech Neck« (»Technik-Nacken«) bezeichnen.[307]
Darum ist es wichtig, erstens das Smartphone beiseitezulegen und zweitens zu versuchen, eine gewisse propriozeptive Achtsamkeit rund um die Wirbelsäule zu entwickeln, sodass man wirklich versteht, wie sich Streckung (Zurückbeugen) und Beugung (Vorbeugen) in jedem einzelnen Wirbel anfühlen. Am einfachsten gelingt dies, wenn Sie im Vierfüßerstand (auf Händen und Knien) extrem langsam zwischen Katzenbuckel und Hohlkreuz wechseln, ähnlich den Yoga-Positionen Katze und Kuh.[308]
Die Besonderheit besteht darin, dass Sie die Bewegung wirklich, wirklich langsam und bewusst von einem Ende Ihrer Wirbelsäule zum anderen ausführen sollen, sodass Sie spüren, wie jeder einzelne Wirbel seine Position verändert, vom Steißbein bis hinauf in den Nacken, bis Ihre Wirbelsäule im Hohlkreuz ist. Dann kehren Sie die Bewegung um, kippen Ihr Becken nach vorn und biegen die Wirbelsäule Wirbel für Wirbel auf, bis Ihr Rücken wieder gewölbt ist wie ein Katzenbuckel. (Beachten Sie bitte: einatmen beim Hohlkreuz, ausatmen beim Katzenbuckel.)
Bei dieser Übung geht es nicht darum, wie weit Sie den Rücken aufwölben oder durchdrücken können, sondern wie viel Kontrolle Sie über die einzelnen Segmente erlangen können, während Sie die Position vom einen Extrem ins andere wechseln. Sie sollten lernen, die Position jedes Wirbels zu spüren, was Ihnen wiederum dabei hilft, Belastungen und Kräfte besser über die gesamte Wirbelsäule zu verteilen. Heute erlaubt mir diese segmentale Kontrolle beim Kreuzheben, einen neutraleren Bogen zwischen Brust- und Lendenwirbelsäule zu beschreiben und die Last gleichmäßig zu verteilen; früher hatte meine Wirbelsäule dabei eine starke Wölbung nach vorn (Lordose oder Hohlkreuz), was bedeutete, dass ich zu viel Kraft aus ihren Scharnierpunkten bezog.
Als Nächstes kommen wir zu den Schultern, die sowohl komplex als auch evolutionär interessant sind. Die Schulterblätter (Scapulae) sitzen auf den Rippen und sind äußerst beweglich. Das Schultergelenk wird durch eine komplexe Muskulatur kontrolliert, die an verschiedenen Stellen des Schulterblatts und am oberen Teil des Oberarms (Humerus) entspringt bzw. ansetzt (darum wird das Gelenk auch Glenohumeralgelenk genannt). Wenn Sie dieses Kugelgelenk mit dem sehr viel stabileren und solideren Kugelgelenk der Hüfte vergleichen, wird deutlich, dass die Evolution des aufrechten Ganges bei unseren Urahnen einen großen Tribut forderte: Im Austausch für eine weitaus größere Beweglichkeit und, ganz praktisch gesehen, die lebenswichtige Fähigkeit, einen Speer zu werfen, büßten wir im Schultergelenk sehr viel Stabilität ein. Doch da an der Schulter sehr viel mehr Muskeln ansetzen (17 an der Zahl), ist das Gelenk viel anfälliger als das Hüftgelenk, wie ich während meiner Box- und Schwimmkarriere am eigenen Leib erlebte.
Beth brachte mir eine einfache Übung bei, um mir die Bedeutung der Position und Kontrolle des Schulterblatts zu verdeutlichen. Die Bewegung ist eine kontrollierte Gelenksrotation (controlled articular rotation, kurz CAR): Stellen Sie sich mit den Füßen in schulterbreitem Abstand hin und platzieren Sie ein Gymnastikband leichter oder mittlerer Stärke unter den Füßen, je ein Ende in einer Hand (eine sehr leichte Hantel tut es auch). Halten Sie die Arme neben dem Körper, heben Sie die Schulterblätter und schieben Sie diese dann nach hinten und zusammen; in dieser Retraktion wollen wir sie unter Belastung haben. Lassen Sie sie dann »herunterfallen« und bringen Sie sie schließlich wieder an den Ausgangspunkt. Wir beginnen die Bewegung in diesen »Vierecken«, doch das Ziel ist, so viel Kontrolle zu erlangen, dass wir unsere Schulterblätter geschmeidig kreisen lassen können. Beim Stabilitätstraining dreht sich viel um diese Form der neuromuskulären Kontrolle; es stellt die Verbindung zwischen unserem Gehirn und wichtigen Muskelgruppen und Gelenken wieder her.
Fast alles, was wir beim Fitnesstraining und im täglichen Leben tun, geht durch unsere Hände. Die Füße stehen in Kontakt mit dem Boden und absorbieren einwirkende Kräfte; über die Hände hingegen geben wir Kraft weiter. Sie sind unsere Schnittstelle mit dem Rest unserer Welt. Die Handkraft, also die Kraft, mit der wir zupacken können, ist dabei nur ein Teil der Gleichung. Unsere Hände sind schon erstaunlich – stark genug, um den Saft aus einer Zitrone zu pressen, und zugleich geschickt genug, um eine Beethovensonate auf dem Klavier zu spielen. Unser Griff kann fest und zugleich federleicht sein und Kraft auf raffinierte Weise übertragen.
Es dreht sich alles darum, wie Sie die Kraft verteilen. Wenn Sie Kraft über Ihre Hände weitergeben und modulieren können, dann können Sie effizient schieben und ziehen. Diese Kraft entspringt den starken Muskeln des Rumpfes und wird in einer Kette weitergeleitet, von der Rotatorenmanschette über Ellbogen und Unterarm bis ins Handgelenk. Eine schwache Rotatorenmanschette am Schultergelenk korreliert eng mit einer geringen Handkraft.
Am Anfang steht jedoch die Kraft der Finger – auch diese leider eines jener Dinge, die wir für Komfort und Bequemlichkeit geopfert haben. Als wir noch Dinge umhertrugen, waren starke Hände für uns überlebenswichtig. Diese Zeiten sind vorbei. Viele von uns benutzen ihre Hände fast nur noch zum Tippen und Wischen. Diese Schwäche bedeutet, dass Schub- und Zugbewegungen ein höheres Risiko für Ellbogen- und Schulterverletzungen mit sich bringen.
Da wir das Zugreifen nicht mehr im Alltag trainieren, müssen wir es bei unseren Work-outs bewusst tun und uns darauf fokussieren, Bewegungen mit den Händen zu initiieren und bei Bewegungen des Oberkörpers alle Finger zu benutzen. Training mit Gewichten ist sehr gut geeignet, um die Handkraft aufzubauen, doch ist es wichtig, sich dabei stets bewusst zu machen, was unsere Finger tun und wie Kraft durch sie übertragen wird.
Das verdeutlicht Beth gern mit einem einfachen Bizepscurl mit einer (leichten) Hantel. Versuchen Sie zunächst den Curl mit leicht zurückgebogenem Handgelenk, das nur ein bisschen von der Linie des Unterarms abweicht. Führen Sie dann wieder den Bizepscurl durch, aber diesmal mit geradem Handgelenk. Welche Variante fühlte sich stärker und kräftiger an? Bei welcher fühlte es sich so an, als ob die Finger beteiligt waren? Hier geht es darum, das Bewusstsein für die Bedeutung der Finger als letztes Glied der Kette zu schärfen.
Nicht zuletzt ist das Zugreifen auch in Situationen wichtig, in denen wir schnell reagieren müssen – wir müssen schnell nach der Leine eines Hundes greifen (oder sie loslassen) können, wenn es darauf ankommt, oder ein Geländer packen, um nicht zu stürzen. Unser Griff und unsere Füße verbinden uns mit der Welt, sodass unsere Muskeln tun können, was für uns nötig ist. Auch beim Kreuzheben: Beth brachte mir bei, dass es beim Kreuzheben genauso um die Füße und Hände geht wie um die ischiocrurale Muskulatur und die Gesäßmuskeln. Wir drücken den Boden von uns weg, wenn wir unsere Finger heben.
Die von mir bislang beschriebenen Bewegungen und Übungen sind nur Basiselemente der Stabilitätsarbeit. Sie mögen einfach erscheinen, doch sie erfordern eine enorme Fokussierung; in meiner Praxis erlauben wir unseren Patienten erst dann die Arbeit mit schweren Gewichten, wenn sie mindestens sechs Monate nach diesen grundlegenden Prinzipien gearbeitet haben.
Eines sei noch angemerkt: Trainer können manchmal sehr hilfreich sein, etwa wenn es um eine grundlegende Anleitung, Zuverlässigkeit und Motivation geht; wir raten unseren Patienten jedoch davon ab, sich zu sehr darauf zu verlassen, dass ein Trainer ihnen immer genau sagt, was sie bei jedem Work-out tun sollen. Ich vergleiche das mit Schwimmenlernen in einem Nassanzug. Anfangs hilft dieser mit seinem zusätzlichen Auftrieb dabei, Selbstvertrauen zu gewinnen. Langfristig aber nimmt er Ihnen die Notwendigkeit, Ihr Gleichgewicht im Wasser zu finden. Das Gleichgewicht ist die eigentliche Herausforderung beim Schwimmen, denn unser Körperschwerpunkt ist um einiges entfernt von unserem Volumenschwerpunkt, sodass unsere Hüfte absinkt. Gute Schwimmer lernen mit dem Training, dieses Ungleichgewicht zu überwinden. Wenn Sie aber nie den Nassanzug ausziehen, lernen Sie nicht, dieses Problem zu lösen.
Desgleichen können Trainer Ihnen helfen, indem Sie Ihnen die Grundlagen verschiedener Übungen vermitteln und Sie motivieren, sich das Work-out zur Gewohnheit zu machen. Aber wenn Sie nie lernen, Ihre Übungen alleine zu machen, werden Sie nie andere Varianten ausprobieren, und Sie werden nie die Propriozeption entwickeln, die Sie brauchen, um Ihre optimalen Bewegungsmuster zu meistern. Sie berauben sich selbst des Lernfortschritts, der ein so wichtiger Bestandteil des Stabilitätstrainings ist – der Prozess des allmählichen Überwindens der Kluft zwischen dem, was Sie zu tun glauben, und dem, was Sie tatsächlich tun.
Alles, worauf wir in diesem letzten Abschnitt eingegangen sind, dient zwei Zwecken: der Übung und der (Selbst-) Einschätzung. Ich rate Ihnen sehr, sich hin und wieder beim Training zu filmen, um das, was Sie zu tun glauben, mit dem zu vergleichen, was Sie tatsächlich mit Ihrem Körper tun. Ich tue das täglich – mein Smartphone auf dem Stativ ist eines meiner wertvollsten Geräte im Fitnessstudio. Ich filme jeden Tag meine zehn wichtigsten Durchgänge und schaue mir die Aufnahmen zwischen den Durchgängen an, um das Gesehene mit dem zu vergleichen, was ich zu tun glaubte. Mit der Zeit wird die Kluft immer schmaler.
Anfangs war es schwer zu akzeptieren, dass ich bis auf Weiteres keine schweren Gewichte mehr heben würde, aber Beth und Michael Stromsness überzeugten mich. Ich bekam keine vernünftige Kniebeuge hin und konnte keinen einfachen Klimmzug korrekt durchführen, darum hätte alles, was darüber hinausging, für mich ein (weiteres) Verletzungsrisiko bedeutet.
Eine Weile haderte ich damit. Wie sollte ich ohne Gewichtstraining leben? Es brauchte einige Monate Arbeit, doch endlich hatte ich genug gelernt, um wieder mit dem Kreuzheben anzufangen. Wo ich früher 200 Kilogramm und mehr gestemmt hatte, ließ mich Beth mit nur rund 50 Kilogramm anfangen, was mir fast wie gar kein Gewicht erschien.
Es half mir, als ich mich an etwas erinnerte, was mein Fahrtrainer Thomas Merrill oft sagte. Er ist ein unglaublicher Fahrer und hat 2022 den zweiten Platz in einem der angesehensten Autorennen der Welt gewonnen, dem 24-Stunden-Rennen von Le Mans. Er weiß also, wovon er spricht. Eines seiner Mantras ist, dass man, um schneller zu werden, erst einmal langsamer werden muss.
Das meint er so: Wenn man ein Auto zu stark ausfährt, als wolle man zu sehr so schnell wie möglich fahren, macht man Fehler. Und Fehler summieren sich beim Fahren. Wenn Sie in Kurve 5 ins Trudeln kommen, dann wahrscheinlich, weil Sie den Scheitelpunkt in Kurve 2 verfehlt und das in Kurve 3 und 4 nicht korrigiert haben. Sie müssen langsamer fahren und das Auto an die richtige Stelle lenken, dann wird es für den Rest sorgen.
Langsamer werden, schnell fahren. Ich glaube, mit dem Erlernen von Stabilität ist es genauso.
Das Einmaleins des Hüftbeugens:
Step-ups richtig machen
Statt Ihnen viele Übungen zu beschreiben, möchte ich eine einzelne Übung genauer erklären; das ist meines Erachtens aufschlussreicher. Aus drei Gründen habe ich mich für einen Step-up, also das einfache Aufsteigen auf eine Box oder einen Stuhl, entschieden. Erstens ist dies eine hüftbeugende Bewegung, eines der Kernelemente unseres Krafttrainings. Zweitens ist er eine einbeinige Übung, die nicht unbedingt viel axiale (Wirbelsäulen-)Belastung mit sich bringt, nicht einmal mit Hanteln in den Händen. Sie ist also ziemlich sicher, selbst für Anfänger (Sie fangen mit dem eigenen Körpergewicht an). Und drittens ist dies eine der besten Übungen, um sowohl die exzentrische als auch die konzentrische Phase der Bewegung anzugehen. Ich mag sie auch, weil sie einige der grundlegenden Stabilitätskonzepte veranschaulicht, die wir in diesem Kapitel schon kennengelernt haben.
Suchen Sie sich zunächst einen Kasten (oder einen niedrigen Stuhl). Die Höhe muss so beschaffen sein, dass Ihr Oberschenkel, wenn Sie den Fuß auf den Kasten setzen, waagerecht steht. Bei den meisten Menschen sollten Kasten oder Sitzfläche also eine Höhe von 40 bis 50 Zentimetern haben. Setzen Sie einen Fuß auf den Kasten, achten Sie darauf, dass große und kleine Zehe und auch die gesamte Ferse fest aufliegen. (Ich mache die Übung immer barfuß.) Der hintere Fuß bleibt am Boden, etwa 30 Zentimeter hinter dem Kasten. Etwa 40 Prozent des Körpergewichts sollen auf dem hinteren Bein lasten und 60 Prozent auf dem vorderen. Halten Sie das Hüftgelenk des vorderen Beins gebeugt, die Wirbelsäule gerade, den Brustkorb geschlossen (Rippen gesenkt), die Arme entspannt neben dem Körper und den Blick nach vorn gerichtet.
Schieben Sie nun Kopf, Brustkorb und Becken gleichzeitig leicht nach vorn und atmen Sie dabei ruhig, aber tief durch die Nase ein, sodass sich das Zwerchfell senken und einen intraabdominalen Druck erzeugen kann. Sie sollten Druck in der Mitte des vorderen Fußes in Richtung auf die Ferse verspüren; belassen Sie aber die Zehen auf dem Kasten. Gleiten Sie mit dem vorderen Oberschenkel ganz leicht nach hinten, sodass die ischiocrurale Muskulatur und der große Gesäßmuskel vorgespannt werden; sie sollten ganz leicht belastet sein. Dieses Empfinden ist bei der Hüftbeugung wesentlich. Die Führung soll von Gesäßmuskel und ischiocruraler Muskulatur kommen, nicht aus dem Becken oder Brustkorb. Alle Kraft kommt aus dem Zusammenspiel dieser Muskeln, nicht aus dem Rücken. Ihr Knie bleibt hinter den Zehen, Becken und Brustkorb sind in einer Linie. Belasten Sie den vorderen Fuß gleichmäßig, ohne einen Schwerpunkt auf Zehen, Mittelfuß oder Ferse.
Pressen Sie nun den vorderen Fuß von oben bewusst auf den Kasten, und stoßen Sie sich minimal mit dem hinteren Fuß ab. Heben Sie sich vom Boden ab, atmen Sie bei Beginn dieser Bewegung aus, strecken Sie das Hüftgelenk und stellen Sie sich gerade auf den Kasten. Kopf und Brustkorb sollten sich in einer Linie über dem Becken befinden. Führen Sie das hintere Bein ein wenig vor das Standbein. Alles sollte gleichzeitig seine Position erreichen, während Sie (bei bewusster Kompression des Brustkorbs) ausatmen. Halten Sie diese Position eine oder zwei Sekunden lang.
Führen Sie beim Hinabsteigen den Fuß des (nun vorderen) Spielbeins hinter den Kasten, und bewegen Sie gleichzeitig Kopf, Brustkorb und Schultern leicht vorwärts; das Hüftgelenk beugt sich (wieder), um ischiocrurale Muskulatur und Gesäßmuskel auf das Absenken Ihres Körpergewichts vorzubereiten. Belasten Sie den vorderen Teil des Standfußes, die Zehen sind aktiv in Richtung Kasten gekrümmt. Spüren Sie, wie sich das Gewicht, während Sie Ihren Körper nach unten und hinten bewegen, vom Vorder- in den Mittelfuß und schließlich auf die Ferse verlagert, in einer gleitenden, koordinierten Bewegung, die durch die ischiocrurale Muskulatur kontrolliert wird (nicht vergessen: langsam nach hinten schwingen).
Führen Sie alles so langsam und gleichmäßig wie möglich durch; streben Sie drei Sekunden vom Beginn des Absteigens bis zur »Landung« an (das ist schwer – zwei Sekunden sind auch schon gut). Während sich der hintere Fuß senkt, verlagert sich Ihr Gewicht kontinuierlich nach hinten, bis Sie ankommen. Belasten Sie den hinteren Fuß möglichst nicht mit mehr als 40 Prozent Ihres Körpergewichts, um nicht in Versuchung zu kommen, die nächste Wiederholung mit Schwung nach vorn zu starten. Wiederholen Sie das Ganze.
Führen Sie pro Seite sechs Wiederholungen durch. Beginnen Sie zunächst nur mit dem eigenen Körpergewicht. Haben Sie jedoch die Bewegung und das Empfinden verinnerlicht, können Sie mit Gewichten arbeiten, etwa einer Hantel in jeder Hand. (Der Bonus dabei: Sie trainieren gleichzeitig auch Ihre Handkraft.)
Die Abfolge und Positionen sind bei dieser Übung mit Gewichten im Grunde dieselben, doch gibt es hier ein paar Dinge zu beachten:
Die Belastung ist nun eine Funktion zweier Faktoren: Gewicht und Höhe des Kastens. Die Höhe kann ein Problem werden, wenn die Mobilität (Flexibilität und Belastungstoleranz) ein Faktor ist.
Die Gewichte müssen locker mit dem Arm herabhängen. Das Gehirn findet immer Wege, um Energie zu sparen und zu »schummeln«; unterdrücken Sie daher den unbewussten Drang, mit den Gewichten vorwärtszuschwingen oder die Schultern zu heben, um den Step-up einzuleiten (das passiert sehr wahrscheinlich, wenn die Gewichte zu schwer sind). Der Gesäßmuskel und die ischiocrurale Muskulatur sollen sämtliche Arbeit verrichten.
Wenn Sie die exzentrische Phase (Step-down) nicht kontrollieren können, sind die Gewichte zu schwer. Sie sollten nicht das Gefühl entwickeln, nach hinten zu fallen. Versuchen Sie es zunächst mit leichteren Gewichten oder einem kürzeren (zweisekündigen) Abstieg.
Es ist wichtig, Brustkorb und Kopf über oder leicht vor dem Becken zu halten, wenn Sie den Aufstieg einleiten. Geht das Becken vorneweg, biegen Sie den Rücken nach hinten, und es wird zu viel Druck auf das Knie ausgeübt.
Videoanleitungen für diese und weitere Übungen finden Sie auf meiner Website unter https://peterattiamd.com/outlive/videos/.
Was Sport bewirken kann: Barry
Als früherer Athlet und lebenslanger Sportler brachte ich schon eine grundlegende Fitness mit, auch wenn meine Bewegungen und meine Hebearbeit nicht immer ganz korrekt waren. Viele meiner Probleme rührten daher, dass ich zu viel Gewichte hob, mit dem Rad fuhr oder schwamm. Die meisten Menschen haben allerdings das gegenteilige Problem: Sie bewegen sich nicht genug. Oder sie haben nicht genug getan. Oder sie können nicht viel tun. Für die meisten ist das die eigentliche Herausforderung. Sie brauchen ein bisschen Starthilfe. Die gute Nachricht: Genau diese Menschen können von Bewegung und Sport am meisten profitieren. Sie haben am meisten zu gewinnen.
Und genau hier ist auch ersichtlich, was Sport tatsächlich bewirken kann – er hat die Fähigkeit, Menschen zu verwandeln, sie funktionell jünger zu machen. Es ist nahezu unglaublich. An früherer Stelle habe ich bereits beschrieben, dass meine Mutter ihr Leben veränderte, indem sie als Sechzigerin mit dem Gewichtstraining begann. Doch es gibt meiner Meinung nach kein besseres Beispiel als den wunderbaren, inspirierenden Barry.
Barry war ein Klient von Beth (aber keiner meiner Patienten), ein Unternehmer und Manager, der sein Berufsleben erfolgreich darauf verwandt hatte, eine Firma aufzubauen. Er verbrachte unzählige Stunden bei der Arbeit, nahm sich aber praktisch keine Zeit für irgendetwas anderes, auch nicht für seine Fitness. Gelegentlich unternahm er Fahrradausflüge, aber das war schon alles.
Ich sehe das oft bei meinen Patienten: Sie erkaufen sich Wohlstand mit ihrer Gesundheit. Dann erreichen sie ein bestimmtes Alter und erkennen, dass sie auf dem falschen Weg sind. Genau so war es bei Barry: Nachdem er praktisch 50 Jahre lang auf einem Stuhl gesessen hatte, ging er in den Ruhestand, und es dämmerte ihm, dass er in furchtbarer Verfassung war. Nicht nur war seine körperliche Leistungsfähigkeit sehr begrenzt, er hatte auch fast ständig Schmerzen. Er ging damals auf die achtzig zu und sah einige leidvolle Jahre auf sich zukommen – eine schlechte Randdekade.
Barry fragte sich: Warum habe ich so viel gearbeitet? In seinem damaligen Zustand erschien der Ruhestand alles andere als verlockend.
Irgendwann aber kam ihm die Erleuchtung: Statt sich zur Ruhe zu setzen, verpasste er sich einen neuen Job. Dieser »Job«, und das war er für ihn, bestand darin, seinen vernachlässigten Körper wieder aufzubauen, sodass er wieder mehr Freude am Leben hatte. Er begann, mit Beth zu arbeiten, und machte auch während der Pandemie weiter, als persönliches Training eine Zeit lang unmöglich war. Er war hoch motiviert. Beth muss normalerweise viele Klienten ermahnen, ihr Übungspensum einzuhalten, doch bei Barry hatte sie das entgegengesetzte Problem: Er wollte zu viel Zeit im Fitnessstudio verbringen. Sie musste ihn dazu anhalten, Pausen zu machen und sich auszuruhen.
Barry hatte ganz offensichtlich andere Ziele als ich, aber sie gingen weit über ein schwammiges »gesünder werden« hinaus. Er wollte einen Klimmzug schaffen – das war sein erklärtes Fitnessziel. Was er wirklich wollte, war, sich stark zu fühlen und sich wieder selbstbewusst in der Welt zu bewegen, ohne die Angst, zu stürzen, ganz so, wie er es als junger Mann getan hatte. Davon war er allerdings noch meilenweit entfernt; hätte Beth ihn an eine Klimmzugstange gehängt, hätte er sich wahrscheinlich eine Verletzung zugezogen. Er konnte kaum schmerzfrei gehen. Daher musste er auf viel grundlegenderer Ebene beginnen und erst einmal lernen, einfache Bewegungsmuster sicher durchzuführen.
Beth begann bei ihm mit einigen derselben Übungen wie bei mir: Bauchatmung, dann langsamer Übergang zu Katzenbuckel und Hohlkreuz. Um sein Sturzrisiko zu verringern, setzte sie den Schwerpunkt auf Bewegungen, die mit dem Gleichgewicht zu tun hatten, und fing dabei mit seinen Füßen an – er lernte wieder, seine Zehen zu bewegen und zu spüren, nachdem er sie jahrzehntelang in Schuhe gezwängt hatte. Weiter ging es mit einbeinigen Übungen im Gehen und Stehen. Beth ließ ihn sogar tanzen, damit er wieder lernte, wie er seine Füße bewegen und auf seine visuelle Wahrnehmung reagieren musste, um im Gleichgewicht zu bleiben.
Dann gingen die beiden dazu über, grundlegende Kraft aufzubauen, angefangen mit Walking Lunges, also einer Abfolge von Ausfallschritten, die seinen unteren Körper kräftigen sollte. Seine Bauchmuskeln waren von einer 20 Jahre zurückliegenden Operation noch immer geschwächt – nach meiner Beobachtung kommt es häufig vor, dass so etwas Menschen noch Jahrzehnte später beeinträchtigt. Sie arbeiteten also an seiner Bauchmuskelkraft, beginnend (wie bei mir) mit dem Aufbau von intraabdominalem Druck. Nach und nach arbeiteten sie sich weiter hoch und bauten die Kraft im mittleren und oberen Körper (und die Stabilität in den Schulterblättern) auf, die er brauchte. Es dauerte nicht lange, da konnte er besser Liegestütz machen als die meisten Zwanzigjährigen aus dem Studio.
Beth ließ ihn Übungen machen, die seine Reaktionsfähigkeit und sein Gleichgewicht verbessern sollten. Sie schickte ihn an die Koordinationsleiter, die auch Fußballer und andere Feldspieler benutzen, um Gleichgewicht, Schnelligkeit und Fußarbeit zu trainieren. Wenn Sie ein Athlet des Lebens werden wollen, dann trainieren Sie eben auch wie ein Athlet.
Zu guter Letzt ließ Beth Barry Sprungübungen machen, was definitiv außerhalb der Komfortzone der meisten Achtzigjährigen ist. Er war zunächst nervös, doch letztlich schaffte er es, dass er von ein paar Yogablöcken springen und in einer Kniebeuge landen – und diese halten – konnte. Dahinter steckte der Gedanke, ihn auf das Unerwartete vorzubereiten, sodass er sich, wenn er unvermittelt eine Stufe oder den Bordstein hinabging, auffangen konnte und nicht stürzte. Die meisten Menschen verspannen sich aus lauter Angst unbewusst; sie trauen ihren »Bremsen«, ihrer exzentrischen Kraft, nicht mehr. Das aber macht ihre Landung meist weniger sicher. Wer stabil sein will, muss sich flüssig bewegen und reaktionsbereit sein, fast wie ein Tänzer.
Eine weitere wichtige Bewegung, die sie erarbeiteten, war das selbstständige Aufstehen vom Boden, unter Zuhilfenahme nur eines Arms (im besten Falle sogar ganz ohne Zuhilfenahme der Arme). Dies gehört zu den Bewegungen, die wir in jüngeren Jahren als selbstverständlich erachten. Natürlich kommen wir vom Boden hoch – bis wir es irgendwann plötzlich nicht mehr schaffen. Kinder lernen ohne großes Nachdenken, wie man vom Boden aufsteht. Irgendwo unterwegs aber verlieren Erwachsene ihre Fähigkeit, diese grundlegende Bewegung auszuführen. Selbst wenn wir körperlich stark sind, fehlt uns die neuromuskuläre Kontrolle; die Botschaft von unserem Gehirn kommt einfach nicht bei unseren Muskeln an. Für jemanden, der einundachtzig Jahre alt ist wie Barry (während ich diese Zeilen schreibe), hat das große Bedeutung; es könnte den Unterschied bedeuten zwischen einem eigenständigen Leben und dem möglichen Umzug in ein Seniorenheim. Beth brachte ihm also eine durchchoreografierte Bewegungssequenz bei, mit der er aus einer sitzenden Position aufstehen konnte, und er arbeitete so lange daran, bis er sie beherrschte.
Dieser »Barry Get-Up« ist inzwischen Teil der Fitnessprüfung, der wir alle unsere Patienten unterziehen, und eine der zentralen Übungen im Zehnkampf der Hundertjährigen (sie sollte auch in Ihrem nicht fehlen). Es ist eine wichtige Bewegung, ob Sie nun nach einem Sturz wieder auf die Beine kommen wollen oder einfach mit Ihren Enkeln auf dem Fußboden gespielt haben. (Eine Videoanleitung des Barry Get-Up finden Sie unter https://peterattiamd.com/outlive/videos) Jeder und jede sollte dies können.
Die Übung steht aber auch für das, was man mit Sport (und natürlich Gleichgewichtstraining) erreichen kann. Menschen wie Barry helfen uns, das Narrativ des Niedergangs zu überschreiben, in dem Sophie, die Mutter meiner Freundin, und so viele andere gefangen waren und sind. Sport und Bewegung haben die Macht, uns von Grund auf zu verändern, selbst wenn wir, wie Barry, bei null anfangen. Sport gibt uns die Möglichkeit, uns – wörtlich und bildlich – vom Boden aufzurichten, stärker und fähiger zu werden. Es geht nicht darum, den Verfall aufzuhalten, es geht darum, immer besser und besser und besser zu werden.
Barry drückt das so aus: »Wenn du nicht vorwärtsgehst, dann gehst du rückwärts.«
Kapitel 14
Ernährung 3.0
Warum wir bessere Wissenschaft brauchen
Religion ist eine Kultur des Glaubens;
Wissenschaft ist eine Kultur des Zweifelns.
Richard Feynman, 1918–1988
Mittlerweile gehe ich nicht mehr gerne auf Partys, denn sobald die Leute wissen, womit ich wirklich meine Brötchen verdiene (weil sie mir meine üblichen Notlügen, ich sei Schafhirte oder Rennfahrer, nicht abnehmen), wollen sie mit mir über die Themen reden, die ich am meisten hasse: Diät und Ernährung.
Ich versuche dann, die Unterhaltung so schnell wie möglich zu beenden, um mir einen Drink zu holen, obwohl ich noch ein Glas in der Hand halte, oder ich tue so, als müsste ich dringend auf eine Nachricht auf meinem Smartphone reagieren, und wenn das alles nichts hilft, fingiere ich eine Ohnmacht. Wie Politik und Religion ist das Thema meiner Meinung nach nicht für Partykonversation geeignet. (Sollte ich Ihnen jemals auf einer Feier als Volltrottel aufgefallen sein, bitte ich um Entschuldigung.)
Diät und Ernährung sind wissenschaftlich immer noch so wenig verstanden, dafür aber so emotional aufgeladen und mit schlechter Information und vereinfachtem Denken durchsetzt, dass man auf einer Party oder in sozialen Medien unmöglich differenziert darüber sprechen kann. Außerdem sind die Leute heute darauf konditioniert, dass sie alles in Form von Schlagwortlisten mit Texthäppchen, aufklebertauglichen Slogans oder anderen oberflächlichen Darstellungsarten präsentiert bekommen wollen. Das erinnert mich an eine Anekdote über den großen Physiker (und einen meiner Wissenschaftshelden) Richard Feynman. Der wurde auf einer Party gebeten, kurz und in einfachen Worten zu erklären, wofür er den Nobelpreis erhalten hatte. Er antwortete, wenn er seine Arbeit kurz und einfach erklären könnte, hätte er den Nobelpreis wahrscheinlich nicht verdient.[309]
Feynmans Bonmot trifft auch auf Ernährung zu, mit einem Unterschied: Über diesen Gegenstand wissen wir aktuell noch wesentlich weniger als über subatomare Teilchen. Einerseits haben wir epidemiologische »Studien«, die allein zum Zweck des Clickbaits gemacht werden (also um mehr Seitenabrufe zu generieren) und so absurde Behauptungen aufstellen wie, dass der Verzehr von 30 Gramm Nüssen pro Tag das Krebsrisiko um exakt 18 Prozent senkt[310] (das habe ich mir nicht ausgedacht). Auf der anderen Seite stehen klinische Studien, die fast ausnahmslos schlecht konzipiert, durchgeführt und/oder statistisch ausgewertet sind. Wegen der mangelhaften wissenschaftlichen Qualität wissen wir tatsächlich nicht viel darüber, wie sich das, was wir essen, auf unsere Gesundheit auswirkt. Damit erhalten unzählige Möchtegerngurus und selbst ernannte Experten die großartige Gelegenheit, lautstark zu verkünden, dass sie und nur sie allein wissen, wie die wahre, richtige Ernährung der Menschen aussieht. Auf Amazon gibt es 40 000 Diätbücher; sie können nicht alle recht haben.
Das leitet zu meiner letzten Kritik an der Welt der Ernährung und der Diäten über: Sie betrifft das dort vorherrschende extreme »Stammesdenken«. Low-Fat, Veganismus, Fleischesser, Steinzeitdiät, Low-Carb, Atkins – jede dieser Ernährungsweisen hat ihre Vorkämpfer und engagierten Verfechter, die bis zum letzten Atemzug behaupten, die ihre sei allen anderen überlegen, obwohl sie dafür keinen schlüssigen Beweis liefern können.
Vor langer, langer Zeit gehörte auch ich zu diesen leidenschaftlichen Fürsprechern einer bestimmten Diät. Drei Jahre lang habe ich eine ketogene Diät gehalten und über meine Erfahrungen damit ausgiebig geschrieben, gebloggt und gesprochen. Ich bin auf ewig mit Low-Carb und ketogener Diät verbandelt – mit allen Vor- und Nachteilen. Auf zugesetzten Zucker zu verzichten – ich habe die Cola, die ich am 8. September 2009 in der Hand hielt, weggestellt, Sekunden nachdem meine liebe Frau mir vorgeschlagen hatte, daran zu arbeiten, »etwas weniger vollschlank zu werden« – war der erste Schritt einer langen, lebensverändernden, gelegentlich auch frustrierenden Reise durch die Welt der Diäten und der Ernährungswissenschaft. Das Gute daran: Mein metabolisches Syndrom im Anfangsstadium hat sich komplett zurückgebildet, und das rettete mir vermutlich das Leben. Außerdem brachte es mich dazu, dieses Buch zu schreiben. Das Schlechte daran: Meine Geduld für Diätdiskussionen ist erschöpft.
Betrachten Sie dieses Kapitel als meine Buße.
Insgesamt glaube ich, dass die meisten Leute entweder zu viel oder zu wenig über dieses Thema nachdenken. Auf der »Zu wenig«-Seite sind es wahrscheinlich mehr, wenn man die immer weiter steigenden Zahlen zu Adipositas und metabolischem Syndrom betrachtet. Aber die auf der »Zu viel«-Seite sind laut und penetrant (siehe nur auf Twitter, jetzt X, die Posts zum Thema »Nutrition« bzw. »Ernährung«). Ich bekenne mich schuldig, dasselbe getan zu haben – in der Vergangenheit. Rückblickend stelle ich fest, dass ich viel zu weit links auf der Dunning-Kruger-Kurve war, die unten in Abbildung 14 karikiert wird – mein maximales Selbstvertrauen und mein ziemlich minimales Wissen hatten mich dem »Gipfel der Ignoranz« schon recht nahe gebracht.
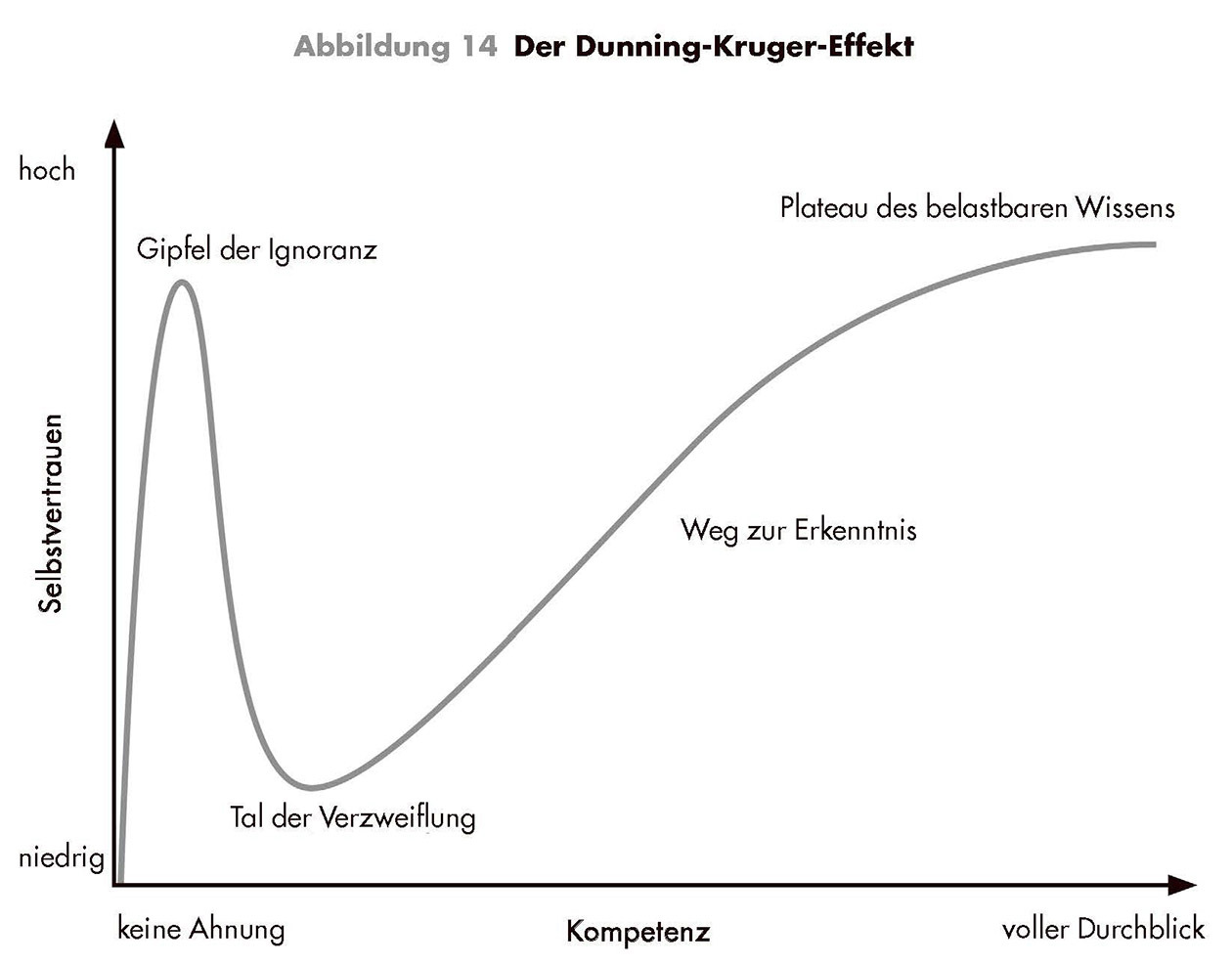
Quelle (Grafik): Wikimedia Commons (2020)
Den mühsamen Weg zur Erkenntnis habe ich nun vielleicht zur Hälfte bewältigt, wenn’s hoch kommt, aber eine wesentliche Veränderung ist bei mir eingetreten: Ich spreche mich nicht mehr dogmatisch für irgendeine Ernährungsweise aus, weder für die ketogene Diät noch für irgendeine Form des Fastens. Es hat lange gedauert, bis ich es verstanden hatte, aber die Grundannahme, die den Diätkriegen und dem größten Teil der ernährungswissenschaftlichen Forschung zugrunde liegt – dass es eine perfekte Ernährungsweise gibt, die für alle Menschen gleichermaßen hervorragend funktioniert –, diese Annahme ist grundfalsch. Mehr als alles andere verdanke ich diese Lektion meinen Patienten, deren persönliche Kämpfe mich eine Demut in Ernährungsdingen gelehrt haben, die ich allein durch das Lesen wissenschaftlicher Artikel nie erfahren hätte.
Ich ermutige meine Patienten, das Wort »Diät« möglichst nicht mehr in den Mund zu nehmen, und wenn ich ein Diktator wäre, würde ich es komplett verbieten. Wenn Sie eine Scheibe Schinken essen oder ein Marshmallow, nehmen Sie viele verschiedene chemische Substanzen zu sich. Ganz so, wie sich diese beiden Dinge aufgrund ihrer chemischen Zusammensetzung im Geschmack unterscheiden, haben die Moleküle in der Nahrung, die wir zu uns nehmen, auch unterschiedliche Auswirkungen auf Enzyme, Stoffwechselwege und -mechanismen in unserem Körper; viele davon haben wir bereits in den vorherigen Kapiteln diskutiert. Die Moleküle in der Nahrung – bei denen es sich im Wesentlichen nur um unterschiedlich angeordnete Kohlenstoff-, Stickstoff-, Sauerstoff-, Phosphor- und Wasserstoff-Atome handelt – interagieren ebenfalls mit unseren Genen, unserem Stoffwechsel, unserem Mikrobiom und unserem physiologischen Zustand. Außerdem reagiert ein jeder von uns anders auf diese Moleküle.
Statt über Diäten sollten wir über die Biochemie der Ernährung sprechen. Das bringt das Thema aus der Sphäre von Ideologie und Religion – und vor allem der Emotionen – heraus und platziert es wieder fest in der Sphäre der Wissenschaft. Wir können diesen neuen Ansatz als Ernährung 3.0 betrachten: streng wissenschaftlich, stark personalisiert und (wie wir gleich sehen werden) geleitet von Feedback und Daten statt von Ideologien und Schlagworten. Es geht nicht darum, Ihnen vorzuschreiben, was Sie essen sollen. Es geht darum herauszufinden, was mit Ihrem Körper und Ihren Zielen funktioniert und – ebenso wichtig – was Sie dauerhaft durchhalten können.
Welches Problem wollen wir hier lösen? Was wollen wir mit Ernährung 3.0 erreichen?
Das bringt uns, meiner Meinung nach, wieder zu den drei einfachen Fragen, die wir in Kapitel 10 gestellt haben:
Sind Sie unterernährt oder überernährt?
Ist Ihre Muskulatur schwach oder adäquat ausgebildet?
Sind Sie metabolisch gesund oder nicht?
Die Korrelation zwischen schlechter metabolischer Gesundheit, Überernährung und schwacher Muskulatur ist sehr hoch. Deshalb geht es für die meisten Patienten darum, die Energieaufnahme zu senken, während sie fettfreie Körpermasse aufbauen. Das heißt, sie müssen Mittel und Wege finden, weniger Kalorien zu verzehren und dabei gleichzeitig mehr Proteine aufzunehmen, das Ganze kombiniert mit der richtigen sportlichen Betätigung. Das ist das häufigste Problem, das wir im Zusammenhang mit Ernährung zu lösen haben.
Wenn Patienten unterernährt sind, liegt es meist daran, dass sie nicht genug Protein aufnehmen, um ihre Muskelmasse zu erhalten, was – wie wir in den vorherigen Kapiteln gesehen haben – ein wesentlicher Faktor sowohl für die Gesamt- wie auch für die gesunde Lebenszeit ist. Das heißt, jede diätetische Intervention, die die Muskulatur oder fettfreie Körpermasse beeinträchtigt, ist ein Rohrkrepierer – sowohl für unter- wie auch für überernährte Patienten.
Früher dachte ich, Diät und Ernährung seien der einzig wahre Weg zu perfekter Gesundheit. Jahrelange Erfahrungen, mit mir selbst und meinen Patienten, brachten mich dazu, meine Erwartungen etwas herunterzuschrauben. Veränderungen in der Ernährung können mächtige Werkzeuge sein, mit denen sich das Stoffwechselgleichgewicht wiederherstellen und das Risiko für chronische Krankheiten reduzieren lässt. Aber können sie auch Gesamtlebenszeit und gesunde Lebenszeit fast wie von Zauberhand verlängern und verbessern, so wie das sportliche Betätigung kann? Ich bin nicht mehr davon überzeugt.
Ich glaube immer noch, dass die meisten Menschen etwas an ihrem Essverhalten ändern müssen, um ihre Stoffwechselgesundheit in den Griff zu bekommen oder um wenigstens Schlimmeres zu verhindern. Aber ich glaube auch, dass wir unterscheiden müssen zwischen einem Verhalten, das gute Gesundheit erhält, und einer Strategie, die schlechte Gesundheit und Krankheit korrigiert. Bei einem gebrochenen Arm hilft der Gipsverband dem Knochen zu heilen. Bei einem gesunden Arm führt ein Gipsverband zur Atrophie (zu Muskelschwund). Dieses Beispiel ist absolut einleuchtend, und trotzdem haben erstaunlich viele Menschen Schwierigkeiten, es auf Ernährung zu übertragen. Dabei liegt es doch auf der Hand, dass eine diätetische Intervention, die ein ernsthaftes Problem korrigieren soll (wie Diäten mit extremer Beschränkung der Kalorienzahl oder Fasten, um Adipositas, nichtalkoholische Fettleber und Diabetes Typ 2 zu behandeln), anders aussieht als ein Ernährungsplan, der aufgestellt wurde, um einen guten Gesundheitszustand zu erhalten (z. B. balancierte Diäten bei stoffwechselgesunden Menschen).
Ernährung ist etwas ganz Einfaches, eigentlich. Es gibt nur einige wenige Regeln: Iss weder zu viele noch zu wenige Kalorien; nimm genügend Eiweiß und essenzielle Fette zu dir; sorge für ausreichend Vitamine und Mineralstoffe; meide Krankheitserreger wie E. coli und Gifte wie Quecksilber oder Blei. Darüber hinaus wissen wir nur relativ wenig mit absoluter Sicherheit. Bitte lesen Sie diesen Satz noch einmal.
Viele alte Sprüche gehen vermutlich im Großen und Ganzen in die richtige Richtung: Wenn deine Urgroßmutter es nicht als essbar erkannt hätte, lass vielleicht besser die Finger davon. Was du am Rand des Supermarktes in den Einkaufswagen legst, ist wahrscheinlich besser als das, was du in der Mitte des Marktes einpackst. Pflanzen sind ausgezeichnete Nahrung. Tierisches Protein ist »sichere«, also unbedenkliche Nahrung. Die Evolution hat uns zu Omnivoren (Allesfressern) gemacht, das heißt, die meisten Menschen können alles essen und dabei völlig gesund sein.
Bitte missverstehen Sie mich nicht, ich habe noch eine Menge zu sagen – darum sind die Ernährungskapitel auch nicht kurz. Es gibt zu diesem Thema so viel ideologischen Hickhack und absoluten Blödsinn in der Welt, dass ich hoffe, wenigstens ein bisschen Klarheit in die Diskussion bringen zu können. Der größte Teil dieses und des nächsten Kapitels zielt darauf ab, die Art und Weise zu verändern, wie Sie über Diät und Ernährung denken, nicht darauf, Ihnen zu sagen, was Sie essen sollen und was nicht. Ich will Ihnen die Mittel an die Hand geben, die richtige Ernährungsweise für sich selbst herauszufinden, eine, die Ihr Leben besser machen soll, indem sie Ihre Gesundheit schützt und erhält.
Das Wenige, was wir über die Biochemie der Ernährung wissen (und wie wir dazu kamen)
Was mich im Bereich der Ernährung – Entschuldigung, der Biochemie der Ernährung – mit am meisten frustriert, ist das geringe gesicherte Wissen darüber. Die Wurzel des Problems liegt in der schlechten Qualität eines großen Teils der ernährungswissenschaftlichen Forschung, die zu schlechten Berichten in den Medien, ausufernden Diskussionen in den sozialen Netzen und großer Verwirrung der Öffentlichkeit führt. Was sollte man essen (oder auch nicht)? Was ist die richtige Ernährung für Sie?
Wenn wir nichts anderes tun können, als die Presseberichte über die neueste große Harvard-Studie oder die Weisheiten irgendeines selbst ernannten Diätexperten zu lesen, dann haben wir keine Chance, je diesem Zustand der hoffnungslosen Verwirrung zu entkommen. Bevor wir in die Details eintauchen, lohnt es sich, einen Schritt zurückzugehen und zu verstehen versuchen, was wir über Ernährung wissen und was nicht – welche Studien wirklich lesenswert sind und welche wir getrost ignorieren können. Den Unterschied zwischen einem Signal und einem Geräusch zu erkennen, das ist der erste wichtige Schritt, wenn wir einen eigenen Plan entwickeln wollen.
Unser Wissen über Ernährung stammt im Wesentlichen aus zwei Arten von Studien: epidemiologischen und klinischen Studien. In der Epidemiologie sammeln Wissenschaftler Daten über die Gewohnheiten großer Gruppen von Menschen und suchen darin nach sinnvollen Assoziationen und Korrelationen mit Endpunkten wie einer Krebsdiagnose, einer Herz-Kreislauf-Erkrankung oder der Sterblichkeit. Vieles, was als »neueste Nachricht« zur Ernährung in Ihrem täglichen Internet-Feed aufploppt – ob Kaffee gut für Sie ist und Schinkenspeck schlecht, oder umgekehrt –, wird aus diesen epidemiologischen Studien herausgelesen.
Die Epidemiologie war ein nützliches Mittel, um den Ursachen von Epidemien auf die Spur zu kommen – bekanntes Beispiel: Im 19. Jahrhundert konnte so der Cholera-Ausbruch in London gestoppt werden. Ein weniger bekanntes Beispiel: Sie bewahrte die Jungs, die als Schornsteinfeger arbeiteten, vor einer Epidemie von Skrotalkarzinomen, die, wie sich zeigte, mit ihrer Tätigkeit in Zusammenhang standen.[311] Sie konnte einige echte Triumphe für das öffentliche Gesundheitswesen verbuchen, wie etwa Rauchverbote oder die Trinkwasseraufbereitung. Aber für die Ernährung vermochte sie nichts Vergleichbares beizusteuern. Selbst wenn man sie für bare Münze nimmt, sind die »Assoziationen«, mit denen Ernährungsepidemiologen um die Ecke kommen, oft absurd: Wird der tägliche Verzehr von zwölf Haselnüssen meine Lebensspanne tatsächlich um zwei Jahre verlängern, wie eine Studie behauptet?[312] Schön wär’s ja.
Das Problem ist, dass die Epidemiologie nicht zwischen Korrelation und Ursache unterscheiden kann. Daher rührt, unterstützt und begünstigt von schlechtem Journalismus, die Konfusion. Beispielsweise haben viele Studien einen starken Zusammenhang (Assoziation) zwischen dem Konsum von Light-Getränken und Bauchfett, Hyperinsulinämie und Herz-Kreislauf-Risiko gefunden[313] Klingt, als seien Diätlimonaden übles Zeug, das Fettleibigkeit verursacht, nicht wahr? Aber das zeigen diese Studien nicht wirklich, weil sie eine wichtige Frage nicht stellen: Wer trinkt diese Light-Produkte?
Es sind Menschen, die wegen ihres Gewichtes oder ihres Diabetesrisikos besorgt sind! Sie trinken die Light-Limos, weil sie übergewichtig sind oder Angst haben, übergewichtig zu werden. Die Epidemiologie verfügt nicht über die Mittel, die Richtung der Kausalität zwischen einem bestimmten Verhalten (wie dem Konsum von Light-Produkten) und einem bestimmten Ergebnis (zum Beispiel Adipositas) festzustellen – ganz so, wie keines meiner Hühner über die Mittel verfügt, das Ei, das es gerade für mich gelegt hat, zu Rührei zu schlagen.
Um zu verstehen, warum das so ist, müssen wir wieder Sir Austin Bradford Hill konsultieren, den britischen Wissenschaftler, den wir bereits in Kapitel 11 kennengelernt haben.[314] Hill hatte in den frühen 1950er-Jahren dazu beigetragen, die Verbindung zwischen Rauchen und Lungenkrebs aufzuklären, und er entwickelte neun Kriterien, um die Stärke epidemiologischer Befunde zu evaluieren und die wahrscheinliche Richtung der Kausalität zu ermitteln; im Zusammenhang mit der sportlichen Betätigung haben wir darauf Bezug genommen.[315] Das wichtigste Kriterium, das auch am besten Korrelation von Ursache zu trennen vermag, ist im Bereich Ernährung am schwierigsten anzuwenden: das Experiment. Versuchen Sie doch mal, eine Studie vorzuschlagen, mit der Sie testen wollen, wie sich der lebenslange Verzehr von Fast Food auf die Gesundheit auswirkt, und für die Sie Mädchen und Jungen nach dem Zufallsprinzip entweder einer Gruppe zuweisen, die sich mit den Produkten einer bestimmten Burger-Kette ernähren muss, oder die ganz ohne Fast Food verpflegt wird. Selbst wenn Sie auf irgendeine Art und Weise die Genehmigung der Ethikkommission für diese gruselige Idee erhalten würden, kann das Experiment auf ganz unterschiedliche Weise scheitern. Ein paar der Burger-Kinder könnten heimlich zu Vegetariern werden, während sich vielleicht einige der Kontrollkinder zum Besuch von Fast Food-Tempeln entschließen. Fakt ist, dass Menschen denkbar schlechte Studienobjekte für Ernährung (oder was auch immer) abgeben, weil wir ungehorsame, undisziplinierte, chaotische, vergessliche, schlampige, hungrige und komplexe Wesen sind.
Darum setzen wir auf eine Epidemiologie, die ihre Daten aus Beobachtungen bezieht und oft auch direkt von den Subjekten. Wie wir weiter vorn gesehen haben, besteht die Epidemiologie rund um den Sport die Bradford-Hill-Kriterien mit Bravour, doch wenn man sie auf Ernährung anwendet, fällt sie häufig glatt durch; das beginnt meist schon mit der Größe des Effekts, der Stärke der Assoziation, die gern in Prozenten angegeben wird. Während die Epidemiologie des Rauchens (wie die des Sports) den Bradford-Hill-Tests locker besteht, weil die Effektgröße so gewaltig ist, sind die Effektgrößen im Bereich der Ernährung typischerweise so klein, dass sie auch von anderen Faktoren – sogenannten Störfaktoren oder Confoundern – hervorgerufen worden sein könnten.
Typisches Beispiel: die Behauptung, der Verzehr von rotem Fleisch und verarbeiteten Fleischprodukten »verursache« Darmkrebs. Einer viel beachteten Studie der Harvard School of Public Health und der WHO aus dem Jahr 2017 zufolge erhöht der Konsum dieser Nahrungsmittel das Darmkrebsrisiko um 17 Prozent (HR = 1,17).[316] Das klingt beängstigend, aber besteht es den Bradford-Hill-Test? Eher nicht, denn die Assoziation ist so schwach. Nur zum Vergleich: Jemand, der Zigaretten raucht, hat ein um 1000 bis 2500 Prozent erhöhtes Risiko (10- bis 25-mal höher), an Lungenkrebs zu erkranken, je nachdem, welche Bevölkerungsgruppe untersucht wurde.[317] Dieses Ergebnis lässt vermuten, dass tatsächlich eine Ursache-Wirkungs-Beziehung im Spiel sein könnte. Aber nur sehr wenige epidemiologische Studien zeigen einen Risikoanstieg von auch nur 50 Prozent (HR = 1,50) für irgendein Nahrungsmittel.
Zweitens und noch weit schlimmer ist, dass die Rohdaten, auf denen diese Schlussfolgerungen typischerweise beruhen, bestenfalls auf wackeligen Beinen stehen. Viele epidemiologische Ernährungsstudien sammeln Informationen über ihre Teilnehmer mit Fragenbögen zur Verzehrhäufigkeit ein, eine ellenlange Checkliste, in die man sehr detailliert alles eintragen soll, was man im letzten Monat oder gar im letzten Jahr gegessen hat. Ich habe versucht, solche Fragebögen auszufüllen, und ich schaffe es schon nicht, mich daran zu erinnern, was ich vor zwei Tagen gegessen habe, geschweige denn vor drei Wochen.[318] Wie verlässlich können Studien sein, die auf solchen Daten beruhen? Wie sehr können wir also der Studie zu rotem Fleisch und Darmkrebs vertrauen?
Verursachen rotes Fleisch und verarbeitete Fleischprodukte nun tatsächlich Darmkrebs oder nicht? Wir wissen es nicht, und wahrscheinlich werden wir auch nie eine definitive Antwort erhalten, weil es unwahrscheinlich ist, dass je eine klinische Studie zu dieser Fragestellung durchgeführt wird. Die Verwirrung bleibt. Trotzdem werde ich mich jetzt aus dem Fenster lehnen und behaupten, dass ein relatives Risiko von 1,17 so gering ist, dass es vermutlich keine Rolle spielt, ob Sie rotes/verarbeitetes Fleisch oder Eiweiß aus einer anderen Quelle zu sich nehmen, zum Beispiel Hühnchen. Diese spezielle Studie kann natürlich mitnichten eine definitive Antwort auf die Frage liefern, ob der Verzehr von rotem Fleisch »sicher« ist. Und trotzdem streiten sich die Leute seit Jahren deswegen.
Das bringt uns zu einem anderen Problem in der Welt der Ernährung: Zu viele Menschen widmen den kleinen Fragen zu große Aufmerksamkeit, während sie den großen Themen keine Beachtung schenken. Kleine Unterschiede in dem, was wir essen, spielen wahrscheinlich eine viel geringere Rolle, als die meisten Menschen annehmen. Aber schlecht gemachte Epidemiologie, unterstützt und gefördert von schlechtem Journalismus, macht aus solchen Mücken gerne Elefanten.
Schlechte Epidemiologie beherrscht den öffentlichen Diskurs über Ernährung in einem Maß, dass es Skeptiker wie John Ioannidis vom Stanford Prevention Research Center, der gegen alle Arten von schlechter Wissenschaft zu Felde zieht, zu einem Gegenschlag veranlasst hat. Sein Hauptargument: Nahrung ist so komplex, aus Tausenden chemischer Komponenten in Millionen möglicher Kombinationen zusammengesetzt, und sie kann mit dem menschlichen Stoffwechsel in so vielfältiger Weise interagieren, dass die Epidemiologie mit ihren Mitteln schlicht nicht in der Lage ist, die Wirkung jedes einzelnen Nahrungsmittels herauszufiltern.[319] In einem Interview mit CBC News wurde der normalerweise ausgesprochen verbindliche Ioannidis brutal direkt: »Epidemiologie auf Ernährung anzuwenden ist ein Skandal«, sagte er. »Das sollte man unbesehen in die Tonne treten.«[320]
Der große Schwachpunkt der Epidemiologie, zumindest als Mittel, um verlässliche Information zu Ursache-Wirkungs-Beziehungen in der Ernährung von Menschen zu erhalten, ist, dass es in derartigen Studien fast immer von Störfaktoren wimmelt. Die Faktoren, die unsere Nahrungs(mittel)auswahl und unsere Essgewohnheiten bestimmen, sind unvorstellbar komplex. Genetik und soziale Einflüsse zählen ebenso dazu wie ökonomische Faktoren, Bildung, Stoffwechselgesundheit, Marketing, Religion und alles, was dazwischenliegt – und sie lassen sich so gut wie nicht von den biochemischen Wirkungen der Nahrungsmittel selbst trennen.
Vor einigen Jahren führte David Allison, ein Wissenschaftler und Statistiker, ein elegantes Experiment durch, das eindrücklich zeigt, wie uns epidemiologische Methoden in die Irre führen können, selbst wenn man Studienteilnehmer wählt, die man voll unter Kontrolle hat: Labormäuse, die genetisch identisch sind und unter identischen Bedingungen gehalten werden.[321]
Allison legte sein Mäuse-Experiment ähnlich den Experimenten zur Kalorienrestriktion an, über die wir in Kapitel 5 gesprochen haben. Er teilte die Versuchstiere nach dem Zufallsprinzip auf drei Gruppen auf. Die Gruppen unterschieden sich lediglich in der Menge Futter, die sie erhielten: Es gab eine niederkalorische Gruppe, eine mittelkalorische und eine hochkalorische Ad-libitum-Gruppe, in der die Tiere so viel fressen konnten, wie sie wollten. Die Mäuse, die mit dem Futter am wenigsten Kalorien erhielten, lebten am längsten, danach kamen die Mäuse, deren Futter einen mittleren Kaloriengehalt hatte, die Lebenszeit der Mäuse mit dem hohen Kalorienkonsum war – im Durchschnitt – am kürzesten. Dieses Ergebnis entsprach den Erwartungen, die man nach vielen vorausgegangenen Studien hatte.
Dann aber machte Allison etwas sehr Schlaues. Er sah sich die hochkalorische Gruppe etwas genauer an, also die Mäuse, die ohne Einschränkung Futter zu sich nehmen durften, und analysierte sie noch einmal separat als eigene nicht randomisierte epidemiologische Kohorte. Allison stellte fest, dass einige Mäuse in dieser Gruppe mehr fraßen als andere – und diese hungrigeren Mäuse lebten länger als die anderen aus der hochkalorischen Gruppe, die von sich aus weniger fraßen. Es war das genaue Gegenteil dessen, was er in der größeren, zuverlässigeren und viel öfter wiederholten randomisierten Studie gefunden hatte.
Für das Ergebnis gab es eine einfache Erklärung: Die kräftigsten und gesündesten Mäuse hatten den größten Appetit, darum fraßen sie mehr. Und weil sie schon zu Beginn am gesündesten waren, lebten sie auch am längsten. Doch wenn wir nur Allisons Analyse dieser speziellen Untergruppe hätten und nicht noch die größere und besser angelegte klinische Studie, dann könnten wir den Schluss ziehen, dass der Konsum von mehr Kalorien dazu führt, dass alle Mäuse länger leben, was ganz sicher nicht der Fall ist.
Dieses Experiment zeigt, wie leicht einen die Epidemiologie in die Irre führen kann. Der allgemeine Gesundheitszustand ist einer der großen Störfaktoren in dieser Art von Studien. Man spricht vom healthy user bias (wörtlich: Verzerrung durch gesunde Teilnehmer), und es bedeutet, dass die Studienergebnisse manchmal mehr den allgemeinen Gesundheitszustand der Teilnehmer widerspiegeln als den Einfluss des Faktors, der in dieser Studie untersucht werden sollte; genau das war bei den »hungrigen« Mäusen in Allisons Studie der Fall.[322]
Ein klassisches Beispiel dafür ist vermutlich auch die umfangreiche und viel beachtete Literatur zum »moderaten Alkoholkonsum«, der angeblich der Gesundheit förderlich sein soll. Diese Behauptung ist fast schon zu einem Credo in den Massenmedien geworden, doch auch diese Studien kranken fast ausnahmslos am healthy user bias:[323] Das heißt, Personen, die selbst im höheren Alter noch trinken, tun das, weil sie gesund sind, und nicht umgekehrt. Und Menschen, die keinen Alkohol trinken, haben oft einen Grund, ihn zu meiden, zum Beispiel wegen gesundheitlicher Probleme oder einer Suchtproblematik. Außerdem schließen solche Studien natürlich diejenigen aus, die bereits an den Folgen des Alkoholismus gestorben sind.
Die Epidemiologie sieht lediglich einen Haufen offenbar gesunder älterer Menschen, die alle Alkohol trinken, und schließt daraus, dass der Alkohol der Grund für ihre gute Gesundheit ist. Doch eine neuere Studie, die in JAMA veröffentlicht wurde und die sich der mendelschen Randomisierung bedient, über die wir in Kapitel 3 gesprochen haben, kommt zu dem Ergebnis, dass das wohl nicht stimmt.[324] Aus dieser Studie geht hervor, dass jeglicher beobachtete Nutzen des Alkoholkonsums vollständig verschwindet, sobald man die Effekte anderer Faktoren, die mit moderatem Alkoholkonsum einhergehen könnten – wie niedriger BMI, Wohlstand und Nichtrauchen –, herausrechnet. Die Studienautoren kommen zu dem Schluss, dass es keine Alkoholmenge gibt, die man als gesund bezeichnen kann.
Klinische Studien scheinen ein wesentlich besseres Mittel zu sein, um eine Ernährungsweise gegen eine andere zu testen: Eine Teilnehmergruppe nimmt Diät X zu sich, die andere Diät Y, und man vergleicht die Ergebnisse. (Oder, um das Alkohol-Beispiel aufzugreifen, eine Gruppe trinkt moderat, eine Gruppe trinkt stark und eine dritte bleibt komplett trocken.)
Dieser Ansatz ist rigoroser als die Epidemiologie, und er bietet eine gewisse Chance, etwas über die Kausalität herauszufinden, weil die Teilnehmer randomisiert, also nach dem Zufallsprinzip auf die Gruppen verteilt werden; trotzdem sind auch klinische Studien häufig fehlerhaft. Man muss immer Kompromisse eingehen zwischen der Größe der Stichprobe, der Studiendauer und der Kontrolle. Wenn Sie eine Langzeitstudie mit einer großen Teilnehmerzahl durchführen wollen, müssen Sie sich unbedingt darauf verlassen können, dass sich alle an die verordnete Ernährungsweise halten, sei es nun die Burger-Diät aus unserem hypothetischen Beispiel von weiter oben oder eine einfache Low-Fat-Diät. Wenn Sie sicherstellen wollen, dass sich Ihre Teilnehmer tatsächlich an die Diät halten, müssen Sie jeden einzelnen mit Essen versorgen, ihn beim Verzehr beobachten und ihn in der Stoffwechsel-Abteilung der Klinik einsperren (damit er ja nichts anderes isst). Das ist vielleicht im Prinzip machbar, aber nur für eine Handvoll Teilnehmer und für wenige Wochen, aber dann ist weder die Stichprobengröße groß genug noch die Studiendauer lang genug, um irgendetwas daraus abzuleiten, was über ein paar mechanistische Erkenntnisse zu Nährstoffen und Gesundheit hinausgeht.
Medikamentenstudien scheinen im Vergleich dazu einfach zu sein. Um herauszufinden, ob Pille X den Blutdruck stark genug absenkt, um Herzinfarkte zu verhindern, müssen sich Studienteilnehmer nur daran erinnern, für ein paar Monate oder Jahre jeden Tag ihre Tabletten einzunehmen, und selbst diese einfache Mitmachregel erweist sich als Herausforderung. Jetzt stellen Sie sich vor, wie Sie sicherstellen wollen, dass Studienteilnehmer den Fettanteil in ihrer Nahrung auf maximal 20 Prozent der Gesamtmenge an Kalorien senken und mindestens fünf Portionen Obst und Gemüse am Tag zu sich nehmen, und das ein Jahr lang.[325]
Ich bin fest davon überzeugt, dass die Compliance, die Befolgung der Regeln, der Schlüsselfaktor in der Ernährungsforschung und bei Diäten im Allgemeinen ist: Werden Sie es schaffen, sich daran zu halten? Die Antwort fällt für fast jeden anders aus. Aus diesem Grund können Experimente die zentralen Fragen zu Ernährungsweise und Krankheiten nur schwer beantworten, unabhängig davon, wie groß und ambitioniert die Untersuchungen angelegt werden.
Ein klassisches Beispiel für eine gut gemeinte Ernährungsstudie, die für mehr Verwirrung als Klarheit gesorgt hat, ist die Women’s Health Initiative (WHI), eine gewaltige randomisierte und kontrollierte Studie, die eine Ernährung mit wenig Fett und vielen Ballaststoffen an fast 50 000 Frauen testen sollte. Sie begann im Jahr 1993, dauerte acht Jahre und kostete fast 750 Millionen US-Dollar (falls Ihnen das bekannt vorkommt, das liegt am anderen Studienarm, über den wir bereits gesprochen haben und der die Effekte einer Hormonersatztherapie bei älteren Frauen untersucht hat). Trotz aller Bemühungen fand die WHI-Studie schlussendlich keine statistisch signifikanten Unterschiede zwischen der Low-Fat- und der Kontrollgruppe,[326] was die Häufigkeit von Neuerkrankungen (Inzidenz) an Brustkrebs, Darmkrebs, Herz-Kreislauf-Erkrankungen und die Gesamtsterblichkeit anging.[327]
Viele Leute, ich selbst eingeschlossen, sagten damals, die Ergebnisse dieser Studie belegten die Unwirksamkeit von Low-Fat-Diäten. In Wahrheit jedoch verriet sie uns vermutlich nur wenig über fettarme Ernährung, weil die Low-Fat-Gruppe etwa 28 Prozent ihrer Gesamtkalorien als Fett zu sich nahm, während die Kontrollgruppe etwa 37 Prozent ihrer Gesamtkalorien aus Fett bezog. (Dabei können wir nur annehmen, dass die Forscher in der Lage waren, annähernd genau zu ermitteln, was ihre Studienobjekte in all den Jahren tatsächlich aßen, eine Annahme, die mit einem dicken Fragezeichen zu versehen ist.) Das heißt, diese Studie verglich zwei Diäten, die sich nur wenig unterschieden, und fand, dass sich die Ergebnisse nur wenig unterschieden. Welche Überraschung. Und obwohl die WHI-Studie so fehlerhaft war, wurde sie viele Jahre lang von Verfechtern verschiedener Ernährungsweisen aufs Heftigste bekämpft.
Nur nebenbei: Die WHI-Studie kann auch als schönes Beispiel dafür dienen, wie wichtig es ist, jede Intervention – sei es eine Ernährungsänderung oder eine andere Behandlungsmaßnahme – im Hinblick darauf zu überprüfen, ob sie nicht nur wirksam, sondern ob sie auch wirklich effektiv ist. Tests zur Wirksamkeit (efficacy) zeigen, wie gut eine Maßnahme bei perfekten Bedingungen und Adhärenz (wenn man alles genauso macht wie vorgeschrieben) funktioniert. Tests zur Effektivität (effectiveness) zeigen, wie gut die Maßnahme unter Alltagsbedingungen mit echten Menschen funktioniert. Die meisten Leute sind sich des Unterschieds nicht bewusst und können dieses wichtige Detail bei klinischen Studien nicht einschätzen. Die WHI-Studie war kein Wirksamkeitstest für eine Low-Fat-Diät, schlicht deshalb nicht, weil (a) keine Low-Fat-Diät getestet wurde und weil (b) die Studienteilnehmer die Diät-Vorschriften nicht perfekt einhielten. Darum kann man aus der WHI-Studie nicht ableiten, dass Low-Fat-Diäten die Gesundheit nicht verbessern, sondern nur, dass die Verordnung einer Low-Fat-Diät bei dieser Patientengruppe keine gesundheitliche Verbesserung gebracht hat. Sehen Sie den Unterschied?
Und doch haben uns einige klinische Studien einige kleinere Erkenntnisgewinne gebracht. Eine der besten (oder am wenigsten schlechten) jemals durchgeführten klinischen Studien schien einen klaren Vorteil für die mediterrane Ernährung zu zeigen – oder wenigstens für die Verwendung von Nüssen und Olivenöl. Außerdem legte diese Studie ein Augenmerk auf die Rolle von Nahrungsfetten.
Die große spanische Studie mit dem Namen PREDIMED (PREvencíon con DIeta Mediterránea) war elegant konzipiert: Statt den annähernd 7500 Teilnehmern genau vorzuschreiben, was sie essen sollten, »schenkten« die Wissenschaftler einer Gruppe wöchentlich einen Liter Olivenöl, mit dem Hintergedanken, sie zu anderen erwünschten Änderungen in der Ernährung zu animieren (zum Beispiel genau die Dinge zu essen, die typischerweise mit Olivenöl zubereitet werden). Die zweite Gruppe erhielt jede Woche eine bestimmte Menge Nüsse und wurde angehalten, jeden Tag 30 Gramm davon zu essen. Der Kontrollgruppe dagegen sagte man nur, sie solle ihre Ernährung fettärmer gestalten, ohne Nüsse, ohne weiteres Fett auf dem Fleisch, das sie konsumierten, ohne Sofrito (eine spanische Tomatensoße mit viel Knoblauch, Zwiebeln und Paprika, was sich köstlich anhört) und merkwürdigerweise ohne Fisch.
Die Studie sollte eigentlich sechs Jahre dauern, aber im Jahr 2013 verkündeten die Forscher, dass sie sie vorzeitig beendet hätten, nach gerade einmal eineinhalb Jahren, weil die Ergebnisse so dramatisch waren. In der Olivenöl-Gruppe lag die Inzidenz für Schlaganfall, Herzinfarkt und Tod um 31 Prozent niedriger als in der Fettarm-Gruppe, und auch in der Nuss-Gruppe war das Risiko ähnlich stark vermindert (28 Prozent). Es wäre daher unethisch gewesen, den fettarmen Teil der Studie fortzusetzen. Von den Zahlen her, ausgedrückt in number needed to treat (siehe Kapitel 7), schien die Olivenöl-oder-Nüsse-»Mittelmeerdiät« für die Primärprävention[328] von Herz-Kreislauf-Krankheiten ebenso gut zu funktionieren wie Statine.[329]
Es sah nach einem Volltreffer aus, denn es kommt selten vor, dass Forscher mit so harten Endpunkten aufwarten können wie Tod oder Herzinfarkt statt lediglich mit Gewichtsverlust in einer einfachen Ernährungsstudie. Dass die Teilnehmer bereits mindestens drei ernsthafte Risikofaktoren aufwiesen, wie zum Beispiel Diabetes Typ 2, Rauchen, Bluthochdruck, erhöhte LDL-C, niedrige HDL-C, Übergewicht oder Fettleibigkeit oder eine Familiengeschichte mit früh auftretenden Herz-Kreislauf-Erkrankungen, trug ebenfalls dazu bei. Trotz ihres erhöhten Risikos hatte die Olivenöl- bzw. Nuss-Diät den Studienteilnehmern eindeutig geholfen, Krankheit und Tod aufzuschieben. Eine spätere Analyse der PREDIMED-Daten fand außerdem bei denjenigen, die den Mittelmeerdiät-Gruppen zugeordnet waren, kognitive Verbesserungen, während bei den Teilnehmern mit der fettarmen Ernährung die kognitiven Fähigkeiten vermindert waren.[330]
Aber heißt das, dass eine mediterrane Ernährung für jeden die richtige ist oder dass natives Olivenöl extra das gesündeste Fett ist? Schon möglich, aber nicht notwendigerweise.
An Studien zu Diät und Ernährung ärgert mich am meisten, dass das Ausmaß der Variation zwischen Individuen zwar festgestellt, oft jedoch verschleiert wird, besonders häufig zu beobachten bei Studien, die allein oder fast ausschließlich auf den Gewichtsverlust als Endpunkt schauen. Die in den veröffentlichten Studien berichteten Ergebnisse sind fast immer ziemlich enttäuschend, im Schnitt verlieren die Teilnehmer nur ein paar Pfund. In Wirklichkeit jedoch haben manche Individuen mit der Diät vielleicht sogar ziemlich viel Gewicht verloren, während andere kaum abgenommen oder sogar zugenommen haben.
Zwei Dinge spielen hier eine Rolle. Das erste ist die Compliance, also das Befolgen der Regeln oder Anordnungen: Wie gut gelingt es, sich an die Diät zu halten? Das ist für jeden Menschen anders; wir alle unterscheiden uns in unseren Gewohnheiten und Ernährungsmustern. Das zweite betrifft die Art und Weise, wie eine Diät den jeweiligen individuellen Stoffwechsel oder andere Risikofaktoren beeinflusst. Beides wird nur allzu oft ignoriert, und dann landen wir bei Verallgemeinerungen wie »Diäten funktionieren nicht«. Eigentlich heißt es nur, dass Diät X oder Diät Y nicht für jeden funktioniert.
Im nächsten Kapitel wollen wir Ihnen helfen, den bestmöglichen Essensplan für sich als Individuum herauszufinden. Dafür müssen wir von Etikettierungen Abstand nehmen und in die Biochemie der Ernährung eintauchen.
Kapitel 15
Die Biochemie der Ernährung in die Praxis umsetzen
Wie Sie für sich die richtige Ernährungsweise finden
Mein Arzt rät mir, auf Abendessen für vier zu verzichten.
Es sei denn, zusammen mit drei anderen Personen.
Orson Welles (1915–1985)
Die meisten meiner Patienten halten bereits irgendeine Form von Diät, wenn sie zu mir kommen. Doch fast alle sind mit dem Ergebnis unzufrieden.
Das kann ich gut verstehen. Während meiner Assistenzarztzeit, als ich noch etwas fülliger war als der vollschlanke Peter, habe ich es eine Zeit lang mit veganer Ernährung probiert. Rein theoretisch sollten die Pfunde purzeln, wenn man auf vegan umstellt, allein schon wegen der Salatberge, die man kauen muss, um auf den Kaloriengehalt eines Ribeye-Steaks zu kommen. In Wahrheit nahm ich die meisten Mahlzeiten im Krankenhaus ein, das bedeutete jede Menge Chips und andere Snacks und jeden Tag zu Mittag ein Brötchen mit Veggie-Belag. Ich habe in sechs Monaten kein verdammtes Pfund abgenommen. Rückblickend lag das Problem auf der Hand. Während ich formal brav meine »vegane« Diät einhielt, aß ich im Prinzip jede Menge Junkfood, das rein zufällig keine tierischen Produkte enthielt. Mit anderen Worten, ich verpflegte mich mit der veganen Version der »amerikanischen Standardernährung« (Standard American Diät, abgekürzt SAD).
Nicht einmal der Umstieg auf vegan befreit einen also aus den Fängen der »traurigen« Durchschnittsernährung. Das liegt an der Nahrungsmittelumwelt, wie sie sich üblicherweise in der Mitte eines Supermarktes vor uns aufbaut: der ganze tiefgefrorene, in Schachteln oder Beutel verpackte Überfluss eines Agrarsystems, das megatonnenweise subventionierte Landwirtschaftsprodukte wie Mais, Mehl, Zucker und Sojabohnen auswirft. Eigentlich ist das System genial, die Lösung für vier Probleme, die die Menschheit seit ihren Anfängen plagen: (1) Wie kann man genügend Nahrung für (fast) alle produzieren? (2) Wie lässt sich das kostengünstig bewerkstelligen? (3) Wie können wir Nahrungsmittel haltbar machen, sodass sie sich sicher lagern und transportieren lassen? (4) Wie können wir sie sehr schmackhaft machen? Wenn es gelingt, alle vier Kriterien zu optimieren, landen wir mit ziemlicher Sicherheit bei der amerikanischen Standardernährung SAD, bei der es sich weniger um eine Ernährungsweise als vielmehr um ein Geschäftsmodell handelt, wie sich die Welt effizient ernähren lässt. Ein zweifaches Hoch auf die moderne industrielle Nahrungsmittelerzeugung.
Aber Achtung, ein fünftes Kriterium fehlt noch: Wie schaffen wir es, dass sie nicht schadet? Natürlich wollte niemand, dass die SAD jemandem schadet. Der Umstand, dass sie den meisten von uns nicht guttut, wenn sie im Übermaß genossen wird, ergibt sich zwangsläufig daraus, dass die vier oben genannten Punkte mit Millionen Jahren der Evolution kollidieren, die uns zu hocheffizienten Fettspeicher-Apparaten gemacht haben. Es handelt sich um eine bedauerliche Begleiterscheinung dieses Geschäftsmodells, ähnlich wie bei Zigaretten. Die Tabakproduzenten beabsichtigten, mit einem reichlich vorhandenen Agrarrohstoff viel Geld zu verdienen, aber ihre geniale Idee, die Zigarette, hatte eine bedauerliche Nebenwirkung: Sie brachte die Kunden langsam um.
Die Bestandteile der amerikanischen Standardernährung sind für die meisten Menschen ebenso schädlich wie Tabak, wenn man sie – wie beabsichtigt – in großen Mengen konsumiert: zugesetzter Zucker, hoch raffinierte Kohlenhydrate mit geringem Ballaststoffanteil, verarbeitete Öle und andere Nahrungsmittel mit sehr hoher Kaloriendichte. Ich sollte dazusagen, dass das nicht heißt, dass alle »verarbeiteten« Nahrungsmittel schlecht sind. Abgesehen von frischem Gemüse ist fast alles, was wir zu uns nehmen, in irgendeiner Weise verarbeitet. Käse zum Beispiel ist ein verarbeitetes Nahrungsmittel, er wurde erfunden, um Milch haltbar zu machen, die sonst ohne Kühlung schnell verderben würde. Worüber wir wirklich sprechen, wenn wir von amerikanischer Standardernährung reden, ist Junkfood.
Das grundlegende Problem, vor dem wir stehen, vielleicht erstmals in der Geschichte der Menschheit, ist die massenhafte Verfügbarkeit von Kalorien für viele, wenn nicht sogar die meisten Bewohner dieses Planeten. Aber darauf hat uns die Evolution nicht vorbereitet. Mutter Natur ist glücklich, wenn wir schön Fett ansetzen, und es stört sie überhaupt nicht, wenn wir Diabetes bekommen. Daher konterkariert SAD unsere wichtigsten Ernährungsziele: Sie verleitet uns, mehr zu essen, als wir brauchen, sodass wir überernährt werden, und weil die qualitativ minderwertigen, hoch verarbeiteten Bestandteile einen so großen Anteil an der Ernährung ausmachen, verdrängen sie andere Nährstoffe, die wir brauchen, um gesund zu bleiben, wie zum Beispiel Proteine.
Die amerikanische Standardernährung bringt unseren Stoffwechsel aus dem Gleichgewicht. Unser Körper verwendet große Mühe darauf, unseren Blutzuckerspiegel zu kontrollieren, was dazu führt, dass wir Fett einlagern, obwohl wir es besser verbrauchen sollten. Dem US Department of Agriculture zufolge ist die Hauptkalorienquelle der Amerikaner eine Produktkategorie, die als »grain-based desserts« (etwa: Süßspeisen auf Getreidebasis) bezeichnet wird: Kuchen, süße Teilchen, Kekse. Das ist unsere Nahrungsmittelgruppe Nummer 1. Wenn wir uns in einer Käsekuchenfabrik mit Unmengen von Süßspeisen auf Getreidebasis den Bauch vollschlagen, dann wird unser Blutzuckerspiegel in die Höhe schießen. Und wenn wir das wieder und wieder tun, ist unser Körper – wie wir in den vorherigen Kapiteln gesehen haben – irgendwann nicht mehr in der Lage, all diese Kalorien so weiterzuverarbeiten, dass sie keinen Schaden anrichten. Die SAD führt quasi Krieg gegen unsere Stoffwechselgesundheit, und wenn der lange genug dauert, verlieren ihn die meisten von uns.
Je weiter wir uns von der amerikanischen Standardernährung entfernen, desto besser wird es uns gehen. Dieses Ziel haben die meisten Diäten gemeinsam – sie wollen uns aus der verhängnisvollen Anziehungskraft der SAD herausziehen, damit wir weniger und hoffentlich auch besser essen können. Das vordringliche Ziel ist es jedoch, weniger zu essen. Wenn man sämtliche Etiketten und Ideologien beiseitelässt, beruhen fast alle Diäten mit diesem Ziel auf mindestens einer der folgenden drei Strategien:
Beschränkung der Kalorienmenge (caloric restriction, abgekürzt CR): insgesamt weniger essen, jedoch ohne darauf zu achten, was gegessen bzw. wann gegessen wird
Beschränkung der Nahrungsmittelauswahl (dietary restriction, abgekürzt DR): verringerter Konsum eines bestimmten Teils der Ernährung, wie zum Beispiel Fleisch, Zucker, Fett
Zeitliche Beschränkung (time restriction, abgekürzt TR): Beschränkung der Nahrungsaufnahme auf bestimmte Zeiten, bis hin zu mehrtägigem Fasten
Mit anderen Worten, wenn Sie überernährt sind, und laut Statistik trifft das auf zwei Drittel der US-Amerikaner[331] zu, kommen Sie nicht umhin, wenigstens einen dieser Wege zur Kalorienrestriktion zu beschreiten: genau darauf achten, was Sie essen, und die Menge reduzieren, bestimmte Nahrungsmittel weglassen und/oder die Zeiten, zu denen Sie essen, beschränken. Das war’s. Wenn wir unsere Herangehensweise an Ernährung auf diese drei Strategien konzentrieren, können wir objektiver über Änderungen des Essverhaltens sprechen als durch die Verwendung von Etiketten wie »Low-Fat« oder »Mittelmeer«, die nicht viel aussagen. Falls wir jedoch keine dieser drei Variablen verändern – und weiter essen, was immer wir wollen, wann immer wir wollen und so viel wir wollen –, landen wir prompt wieder bei der amerikanischen Standardernährung.
Jede der drei Herangehensweisen hat ihre Vor- und Nachteile, wie ich in meiner jahrelangen Arbeit mit unzähligen Patienten gesehen habe. Weiter unten gehe ich im Detail darauf ein, hier erst einmal die Kurzfassung:
Was die Effektivität angeht, ist die Beschränkung der Kalorienmenge (caloric restriction, CR) am besten, ohne Wenn und Aber. So bauen beispielsweise Bodybuilder Gewicht ab, ohne Muskelmasse zu verlieren, und die Flexibilität bei der Auswahl der Nahrungsmittel ist am höchsten. Der Haken ist, dass man sehr diszipliniert sein muss – man muss sehr genau darauf achten, was man isst, und darf sich nicht verleiten lassen zu naschen –, sonst funktioniert es nicht. Vielen Menschen fällt es schwer, das länger durchzuhalten.
Der Verzicht auf einen bestimmten Bestandteil der Ernährung (dietary restriction, DR) ist vermutlich eine der beliebtesten Methoden zur Beschränkung der Energieaufnahme. Der Gedanke dahinter ist einfach: Sie wählen einen Nahrungsmitteltyp aus und essen diese Nahrungsmittel dann nicht mehr. Das funktioniert natürlich nur, wenn diese Nahrungsmittel in der Ernährung so häufig und in so großer Menge vorkommen, dass der Verzicht darauf zu einem Kaloriendefizit führt. Wenn Sie beschließen, keinen Salat mehr zu essen, wird das nicht den gewünschten Erfolg haben. Außerdem können Sie sich trotzdem noch überessen, obwohl Sie Ihre selbst gewählte Beschränkung perfekt einhalten, wie auch ich erfahren musste, als ich versuchte, mich vegan zu ernähren.
Die Beschränkung der Essenszeiten (time restriction, TR), die auch als »Intervallfasten« bezeichnet wird, steht gerade hoch im Kurs, wenn es ums Kalorieneinsparen geht. In gewisser Weise ist das am einfachsten, denke ich. Als ich noch Radrennen gefahren bin und versuchte, die letzten sechs Pfund von meinem (für meine Verhältnisse) bereits sehr geringen Wettkampfgewicht loszuwerden, war das meine bevorzugte Methode. Ich nahm nur eine Mahlzeit am Tag zu mir, obwohl ich etwa drei Stunden am Tag trainierte. Doch der Schuss kann nach hinten losgehen, wenn man (bei der einen Mahlzeit) zu viel isst. Ich habe – zu meinem großen Vergnügen – Patienten erlebt, die mit der Eine-Mahlzeit-am-Tag-Strategie Gewicht zugelegt haben, weil sie diese eine Mahlzeit in einen Wettbewerb à la »Wer schafft am meisten Pizza und Eiscreme?« umgemünzt haben. Der größte Nachteil dieses Ansatzes ist allerdings, dass die meisten Menschen, die es damit versuchen, am Ende ein starkes Proteindefizit aufweisen (über den Eiweißbedarf sprechen wir später in diesem Kapitel). Außerdem kann man bei der Beschränkung häufig beobachten, dass die betreffende Person so viel Gewicht verliert, dass sich die Zusammensetzung der Körpermasse zum Schlechteren verändert: Sie verliert fettfreie Körpermasse (Muskulatur), während die Masse an Körperfett gleich bleibt oder sogar zunimmt.
Mit diesen drei Herangehensweisen werden wir uns nun beschäftigen und gleich mit der wichtigsten Frage beginnen: wie viel wir essen.
CR: Kalorien zählen
Auch auf die Gefahr hin, dass ich mich langsam anhöre wie eine Schallplatte mit Sprung, aber es sollte inzwischen auf der Hand liegen, dass viele der Probleme, die wir angehen oder vermeiden wollen, daher rühren, dass wir mehr Kalorien verzehren, als wir gefahrlos speichern können. Wenn wir uns mehr Energie zuführen, als wir benötigen, landet der Überschuss auf die eine oder die andere Art in unserem Fettgewebe. Wenn dieses Ungleichgewicht länger anhält, überschreiten wir die Grenzen der »sicheren« Fetteinlagerung im Unterhautfettgewebe, und das überschüssige Fett wandert weiter in unsere Leber, unsere Eingeweide und unsere Muskeln (siehe Kapitel 6).
Wie viele Kalorien jemand zu sich nimmt, hat eine enorme Bedeutung für alles, worüber wir in diesem Buch sprechen. Wenn Sie jeden Tag tausend Kalorien mehr als nötig verzehren, egal wovon, dann werden Sie irgendwann Probleme bekommen. In den vorangegangenen Kapiteln haben wir gesehen, wie überzählige Kalorien zu vielen chronischen Krankheiten beitragen, nicht nur zu Stoffwechselstörungen, sondern auch zu Herz-Kreislauf-Erkrankungen, Krebs und Alzheimer. Aus über Jahrzehnte gesammelten experimentellen Daten (Kapitel 5) wissen wir, dass es das Leben verlängert, weniger Kalorien zu sich zu nehmen – zumindest bei Versuchstieren wie Ratten und Mäusen, obwohl es eine Diskussion darüber gibt, ob es sich dabei wirklich um eine Verlängerung der Lebenszeit handelt oder lediglich um eine Beseitigung der Gefahren, die durch Überfütterung drohen, was für die Kontrolltiere in den meisten dieser Experimente der Normalfall ist. (Und auch für viele Menschen.)
Bei Menschen läuft die Kalorienrestriktion in der Regel unter einem anderen Namen als bei Versuchstieren: Kalorienzählen. Viele Forschungsergebnisse zeigen, dass Menschen, die ihre Kalorien zählen und beschränken, tatsächlich Gewicht verlieren können, was für die meisten dieser Studien der Endpunkt ist. So funktionieren auch die Weight Watchers. Die größten Hindernisse für einen Erfolg sind in erster Linie der Hunger und zum Zweiten die Erfordernis, alles, was man isst, genau im Auge zu behalten. Das funktioniert heute mit Apps besser als noch vor zehn Jahren, aber es ist immer noch schwer. Für Leute, denen das liegt, funktioniert der Ansatz hervorragend – viele Bodybuilder und Sportler arbeiten damit –, doch für viele Menschen ist die ständige Überwachung der Kalorienaufnahme nicht umsetzbar.
Ein kleiner Vorteil des Kalorienzählens ist, dass man im Prinzip auf nichts verzichten muss. Sie können essen, was Sie wollen, solange Sie sich innerhalb Ihres täglichen »Kalorienbudgets« bewegen. Wenn Sie aber zu viele schlechte Entscheidungen treffen, werden Sie sehr hungrig sein, also seien Sie auf der Hut. Sie können auch mit einer kalorienbeschränkten Schokoriegel-Diät Gewicht verlieren, doch Sie werden sich sehr viel besser fühlen, wenn Sie sich stattdessen für gedünsteten Brokkoli und Hühnchen entscheiden.
Die Diskussion darüber, ob man Kalorienrestriktion bei Menschen als Mittel zur Lebensverlängerung einsetzen kann oder soll, wird schon sehr lange geführt. Bei Luigi Cornaro, dem Diät haltenden Edelmann aus dem 16. Jahrhundert, scheint es geklappt zu haben: Er behauptete, hundert Jahre alt geworden zu sein, obwohl er in Wahrheit wohl in seinen Achtzigern war, als er starb. Die angeblich lebensverlängernde Wirkung ist aus verschiedenen Gründen, von denen ich einige bereits erläutert habe, eine am Menschen wissenschaftlich schwer zu überprüfende Hypothese. Darum wurde sie an Affen getestet, in zwei Langzeitstudien. Die Ergebnisse waren so überraschend, dass man noch heute darüber diskutiert.
Im Juli 2009 wurde in der Fachzeitschrift Science eine Studie veröffentlicht, die festgestellt hatte, dass Rhesusaffen, die mehr als 20 Jahre lang eine kalorienreduzierte Ernährung erhalten hatten, deutlich länger lebten als Artgenossen, die fressen konnten, so viel sie wollten.[332] »Dieting Monkeys Offer Hope for Living Longer« (»Diät haltende Affen machen Hoffnung auf ein längeres Leben«), verkündete die Schlagzeile auf der Titelseite der New York Times.[333] Die beigefügten Fotos sagten alles: Links war ein Affe namens Canto zu sehen, der für sein fortgeschrittenes Alter von siebenundzwanzig Jahren erstaunlich frisch und munter aussah, während rechts Owen hockte, der nur zwei Jahre älter war und wie Cantos schlaffer, verlebter Onkel wirkte. Canto hatte fast sein ganzes Leben lang eine kalorienreduzierte Ernährung bekommen, während Owen ganz nach Belieben fressen konnte.
Owen und Canto waren zwei der 76 Affen dieser Studie, die zwei Jahrzehnte zuvor an der University of Wisconsin-Madison begonnen worden war. Die Hälfte der Affen, die Kontrollgruppe, wurde ad libitum ernährt, das heißt, sie konnten so viel fressen, wie sie wollten. Die andere Hälfte dagegen wurde auf eine »Diät« gesetzt, die den Tieren etwa 25 Prozent weniger Kalorien zugestand als der Kontrollgruppe. Und so lebten sie dann ihr Leben, während ihnen die Forscher dabei zusahen, wie sie älter wurden.
Altersstudien können so spannend sein, wie Wandfarbe beim Trocknen zuzusehen, aber die Endergebnisse waren dann doch ganz aufregend. Es zeigte sich, dass die Affen mit der kalorienbeschränkten Ernährung statistisch signifikant länger lebten und wesentlich seltener an altersbedingten Erkrankungen starben als die Affen aus der Kontrollgruppe, die nach Belieben fressen konnten. Sie waren in vielerlei Hinsicht gesünder, etwa auch, was die Insulinresistenz angeht. Selbst ihre Gehirne waren besser in Form als die der Kontrolltiere, sie behielten während des Alterungsprozesses mehr von ihrer grauen Substanz. »Diese Daten zeigen, dass Kalorienbeschränkung bei einer Primaten-Spezies die Alterung verlangsamen kann«, schlussfolgerten die Autoren der Studie.
Damit war der Fall abgeschlossen. So schien es jedenfalls.
Drei Jahre später, im August 2012, schaffte es eine weitere Affenstudie[334] auf die Titelseite der Times, dieses Mal mit einer völlig anderen Schlagzeile: »Severe Diet Doesn’t Prolong Life«, verkündete die Zeitung düster, mit dem Nachsatz »At Least in Monkeys« (»Strenge Diät nicht lebensverlängernd – zumindest nicht bei Affen«)[335]. Diese Studie, die ebenfalls in den 1980er-Jahren begonnen worden war, fand unter der Federführung des National Institute of Aging statt, das zu den National Institutes of Health gehört, und war vom Studiendesign her fast identisch mit der Studie aus Wisconsin: Eine Affengruppe erhielt 25 bis 30 Prozent weniger Futter als die andere. Und doch stellten die Forscher des NIH fest, dass ihre kalorienbeschränkt ernährten Affen nicht länger lebten als die Kontrolltiere. Zwischen den Lebensspannen der beiden Gruppen gab es keinen statistisch signifikanten Unterschied. Aus der Sicht eines Schlagzeilentexters hatte die Kalorienbeschränkung »nichts gebracht«.
Journalisten mögen es, wenn die Ergebnisse einer Studie im Widerspruch zu denen einer früheren viel beachteten Studie stehen. In der kleinen Gemeinschaft der Alternsforscher jedoch löste die NIH-Studie Bestürzung aus. Alle hatten erwartet, dass diese Studie die Ergebnisse der Affenstudie aus Wisconsin bestätigen würde. Nun sah es so aus, als hätten zwei Forscherteams zig Millionen Dollar staatlicher Gelder dafür ausgegeben, um zu zeigen, dass eine kalorienbeschränkte Ernährung die Lebensdauer von Affen in Wisconsin verlängert, in Maryland, wo die NIH-Affen gehalten wurden, aber nicht.
Doch manchmal lernen wir aus »fehlgeschlagenen« wissenschaftlichen Experimenten mehr als aus solchen, die die erwarteten Ergebnisse liefern, so war das auch in diesem Fall. Als man die beiden Affenstudien Punkt für Punkt verglich, kamen ein paar kleinere Unterschiede zum Vorschein, die sich als äußerst bedeutsam erwiesen – auch im Hinblick auf unsere Strategie. Zusammen stellen die beiden konkurrierenden Affenstudien eines der am strengsten kontrollierten Experimente dar, die jemals zu der komplexen Beziehung von Ernährung und langfristiger Gesundheit durchgeführt wurden. Und wie bei so vielen herausragenden wissenschaftlichen Experimenten spielte auch bei diesem der Zufall zumindest teilweise eine Rolle.
Der größte Unterschied zwischen den beiden Studien war auch der – für eine Ernährungsstudie – bedeutsamste: das Futter, das die Affen bekamen. Die Tiere der Wisconsin-Studie erhielten handelsübliches Affenfutter, das »halb gereinigt« war, das heißt, die Zutaten waren stark verarbeitet und die Mengen (der Bestandteile) immer genau gleich. Das Futter der NIH-Affen hatte zwar eine ähnliche Zusammensetzung, was die wichtigsten Makronährstoffe angeht, aber es war »natürlich« und weniger stark verfeinert; ein Fachmann für Primatenernährung am NIH hatte es speziell für diesen Versuch aus ganzen Zutaten maßgeschneidert. Der frappierendste Unterschied: Während das NIH-Affenfutter etwa 4 Prozent Zucker enthielt, waren es bei dem Futter für die Wisconsin-Affen sage und schreibe 28,5 Gewichtsprozent. Damit war der Zuckeranteil höher als der von Eiscreme aus dem Supermarkt.
Könnte das als alleiniger Grund ausreichen, um den Unterschied in den beobachteten Lebensspannen zu erklären? Möglicherweise ja: Über 40 Prozent der Affen aus der Wisconsin-Kontrollgruppe, also diejenigen, die ohne Einschränkung fressen konnten, entwickelten Insulinresistenz und Prädiabetes, während nur einer von sieben aus der NIH-Kontrollgruppe Diabetes entwickelte.[336] Außerdem war die Wahrscheinlichkeit, an Krebs oder einer Herz-Kreislauf-Erkrankung zu sterben, in der Kontrollgruppe von Wisconsin sehr viel höher als die aller anderen Affengruppen. Daraus könnte man den Schluss ziehen, dass die Kalorienrestriktion wohl eher den frühzeitigen Tod aufgrund der schlechten Ernährung in Wisconsin verhinderte, als dass sie das Altern wirklich verhinderte – dennoch eine wertvolle Information, da das Verhindern von Diabetes und anderen Stoffwechselstörungen für unsere Strategie wichtig ist.
Die Wisconsin-Forscher verteidigten das von ihnen verwendete Affenfutter mit dem Hinweis, es ähnele mehr dem, was Amerikaner tatsächlich essen, was allerdings ein Argument ist. Der Vergleich mag vielleicht hie und da ein wenig hinken, aber im Prinzip ernährten sich die Wisconsin-Affen von Fast Food, während den NIH-Affen ein Salatbuffet zur Verfügung stand. Die Kontrollgruppe aus Wisconsin verzehrte die meisten Kalorien aus dem schlechtesten Futter, und ihre Gesundheit wurde geschädigt. Das passt: Wenn Ihre Ernährung vor allem aus Cheeseburgern und Milchshakes besteht, dann wird es Ihnen besser gehen, wenn Sie weniger Cheeseburger und Milchshakes konsumieren.
Das Futter für die NIH-Affen war von wesentlich besserer Qualität. Statt hoch verarbeiteter Zutaten wie Maisöl und Maisstärke (an die 30 Prozent des Wisconsin-Futters) enthielt es Vollkornweizen und Mais in gemahlener Form und damit auch mehr sekundäre Pflanzenstoffe und andere vermutlich vorteilhafte Mikronährstoffe, die man typischerweise in frischen Nahrungsmitteln findet. Wenn dieses Futter auch nicht genau dem entsprach, was Rhesusaffen in freier Wildbahn üblicherweise fressen, kam es dem doch zumindest nahe. Ob die NIH-Affen von diesem Futter nun mehr oder weniger zu fressen erhielten, machte keinen großen Unterschied, weil die Ausgangssituation als solche nicht so schädlich war.
Was lehren uns diese beiden Affenstudien nun über die Biochemie der Ernährung?
Für die Langlebigkeit ist es sehr wichtig, Diabetes und andere Stoffwechselstörungen zu vermeiden – insbesondere durch den Verzicht auf Junkfood oder zumindest durch eine Einschränkung von dessen Konsum.
Zwischen Kalorien und Krebs scheint es eine starke Beziehung zu geben; Krebs war in beiden Studien die Haupttodesursache für die Affen aus der Kontrollgruppe. Die Tiere mit der kalorienreduzierten Ernährung hatten ein um 50 Prozent niedrigeres Risiko, Krebs zu bekommen.
Die Qualität Ihrer Nahrung kann unter Umständen ebenso wichtig sein wie die Quantität. Wenn Sie der amerikanischen Standardernährung frönen, sollten Sie besser sehr viel weniger davon zu sich nehmen.
Wenn Sie sich umgekehrt bereits qualitativ hochwertig ernähren und einen gesunden Stoffwechsel haben, dann können Sie sich mit einer leichten Kalorienrestriktion – oder einfach durch maßvolles Essen – einen weiteren Vorteil verschaffen.
Den letzten Punkt halte ich für besonders wichtig. Die beiden Studien legen nahe, dass es unter Umständen gar nicht nötig ist, sich eine starke Kalorienbeschränkung aufzuerlegen, wenn man sich qualitativ hochwertig ernährt und noch metabolisch gesund ist. Die Kontrollgruppe der NIH-Affen konnte von ihrem hochwertigen Futter fressen, so viel sie wollte, und sie lebte trotzdem fast ebenso lang wie die Tiere aus den beiden Gruppen mit der kalorienreduzierten Ernährung. Nachträgliche Analysen ergaben interessanterweise, dass die Affen aus der NIH-Kontrollgruppe von sich aus etwa 10 Prozent weniger Kalorien zu sich nahmen als die aus der Wisconsin-Kontrollgruppe, vermutlich, weil sie sich dank ihres qualitativ besseren Futters weniger hungrig fühlten. Die Forscher spekulierten, dass selbst diese sehr geringe Kalorienreduktion möglicherweise statistisch signifikant war – in jedem Fall stützt das unsere These, dass man Überernährung nach Möglichkeit vermeiden sollte.
Bitte beachten: Diese Studienergebnisse besagen nicht, dass wir alle unsere Kalorienzufuhr drastisch einschränken sollten. Eine Kalorienrestriktion kann für Menschen sinnvoll sein, die einen gestörten Stoffwechsel haben und/oder überernährt sind. Aber ich bin nicht überzeugt, dass eine wie auch immer geartete Lebensverlängerung einige der Nachteile einer langfristigen, starken Beschränkung der Kalorienzufuhr aufwiegen kann, unter anderem ein möglicherweise geschwächtes Immunsystem und eine Anfälligkeit für Kachexie und Sarkopenie (Auszehrung und Muskelschwund), ganz zu schweigen vom ständigen Hunger. Diese unerwünschten Nebenwirkungen könnten einige der negativen Prozesse beschleunigen, die eh schon mit dem Altern einhergehen, und von daher könnte eine Kalorienrestriktion bei älteren Menschen womöglich mehr schaden als nutzen.
Von den Rhesusaffen lernen wir, dass jemand, der stoffwechselgesund und nicht überernährt ist, so wie die NIH-Tiere, nichts weiter tun muss, als qualitativ schlechte Ernährung zu meiden. Einige Exemplare aus der NIH-Gruppe mit der kalorienreduzierten Ernährung brachten es auf die längsten Lebensspannen, die jemals für Rhesusaffen registriert wurden. Es scheint ziemlich klar, dass die Beschränkung der Kalorienaufnahme und die Verbesserung der Nahrungsqualität selbst für Affen »etwas bringt« – das Schwierige ist die Umsetzung. Wie wir im nächsten Abschnitt sehen werden, gibt es noch viele andere Strategien, um die Kalorienaufnahme zu beschränken und unseren Nahrungsmittelkonsum an unseren Stoffwechsel und unsere Lebensweise anzupassen.
DR: Diät à la Biochemie der Ernährung
Der Verzicht auf einen bestimmten Bestandteil der Ernährung, also die Beschränkung der Nahrungsmittelauswahl, ist der Klassiker unter den konventionellen Diäten, auf den sich 90 Prozent der Aufmerksamkeit konzentrieren – ebenso die Forschungsgelder, die Energie, die Wut und natürlich die Debatten über die Biochemie der Ernährung. Dabei ist es genau genommen ganz einfach: Finden Sie heraus, welches in Ihrer Ernährungswelt der oder die Bösewichte sind, beispielsweise Gluten, und streichen Sie sie vom Speiseplan. Je allgegenwärtiger der Bösewicht ist, desto restriktiver fällt »die Diät« aus und desto höher die Wahrscheinlichkeit, dass damit Ihre Gesamtkalorienaufnahme sinkt. Selbst wenn Sie beschließen würden, nur noch Kartoffeln zu essen, würden Sie Gewicht verlieren, weil ein Mensch nur eine bestimmte Menge Kartoffeln pro Tag verdrücken kann. Ich habe es erlebt, dass Leute das tun, und es funktioniert. Der schwierige Teil ist herauszufinden, welche Lebensmittel man streichen oder beschränken sollte.
Diese Frage stellte sich unseren Vorfahren nicht. Nach allem, was wir heute wissen, waren sie opportunistische Omnivoren, aus purer Notwendigkeit. Sie aßen einfach alles, was ihnen in die Hände fiel: viele Pflanzen, viele stärkehaltige Wurzeln und Knollen, tierisches Protein, wann immer sie es bekommen konnten, Honig und Früchte, wann immer sie sie fanden.[337] Metabolisch scheinen sie ziemlich gesund gewesen zu sein, zumindest wenn man die Ergebnisse von Untersuchungen der wenigen noch existierenden Jäger-Sammler-Gesellschaften zugrunde legt.[338]
Sollen wir dasselbe tun? Sollen wir als opportunistische Omnivoren einfach alles essen, dessen wir habhaft werden können? Unsere evolutionäre Entwicklung hat uns so werden lassen, doch unsere moderne Umwelt macht es ein bisschen zu einfach, Nahrung zu finden. Darum sind Überernährung und Stoffwechselprobleme heute an der Tagesordnung. Wir haben zu viele Wahlmöglichkeiten und zu viele köstliche Mittel und Wege, uns Kalorien zuzuführen. Darum ist es notwendig, die Nahrungsmittelauswahl zu beschränken. Wir müssen das, was wir essen können, und das, was wir nicht essen können (oder sollen), klar eingrenzen.
Der Vorteil bei der Beschränkung der Nahrungsmittelauswahl: Sie lässt sich absolut individuell gestalten, und Sie können das Maß der Restriktion variieren, je nach Ihren Bedürfnissen. Zum Beispiel könnten Sie beschließen, alle mit Zucker gesüßten Getränke wegzulassen, das wäre ein großartiger erster Schritt (und noch dazu ein sehr leichter). Sie könnten noch einen Schritt weiter gehen und auch keine süßen Fruchtsäfte mehr trinken. Sie könnten aufhören, mit Zucker gesüßte Lebensmittel zu essen. Sie könnten aber auch so weit gehen, Kohlenhydrate ganz allgemein zu streichen oder ihren Konsum stark einzuschränken.
Ein Grund, warum die Beschränkung des Kohlenhydratverzehrs bei vielen Menschen gut funktioniert, ist, dass dadurch sowohl der Appetit als auch die Auswahl der möglichen Nahrungsmittel verringert wird.[339] Aber nicht allen Menschen gelingt es gleich gut, das durchzuhalten. (Selbst ich bin mir ziemlich sicher, dass ich nie wieder eine ketogene Diät machen könnte, die länger als ein paar Tage dauert.) Die Beschränkung des Fettkonsums verkleinert ebenfalls die Auswahl der möglichen Nahrungsmittel, der Appetit wird jedoch weniger effektiv verringert, wenn Sie sich die falschen Low-Fat-Produkte zum Essen aussuchen (etwa kohlenhydratreiches Junkfood). Wenn Sie beispielsweise die meisten Kohlenhydrate in Form von Cornflakes oder Ähnlichem zu sich nehmen, werden Sie ständig großen Hunger haben.
Ein größeres Risiko bei der Beschränkung der Nahrungsmittelauswahl ist, dass man am Ende doch mit Überernährung dasteht, wenn man es nicht gut durchdacht hat. Viele Leute glauben (irrtümlicherweise), dass man nicht zu viel essen kann, wenn man einfach nur auf _Zutreffendes bitte einfügen_ (zum Beispiel Kohlenhydrate) verzichtet. Das ist falsch. Selbst wenn man sich penibel daran hält, kann eine Beschränkung der Nahrungsmittelauswahl zur Überernährung führen. Wenn Sie Kohlenhydrate komplett streichen, bei Wagyu-Steak und Frühstücksspeck jedoch übermäßig zuschlagen, dann werden Sie sich ganz schnell in einem Zustand des Kalorienüberschusses wiederfinden. Es ist wichtig, eine Strategie zu wählen, bei der Sie langfristig bleiben können, die Ihnen aber auch beim Erreichen Ihrer Ziele hilft. Das erfordert Geduld, etwas Willenskraft und die Bereitschaft, ein wenig zu experimentieren.
Außerdem wollen wir sichergehen, Ihre anderen Ziele auf diesem Weg nicht zu beeinträchtigen. Jede Beschränkung der Nahrungsmittelauswahl, bei der etwa die Proteinaufnahme verringert wird, ist für die meisten Leute nicht ratsam, weil dadurch wahrscheinlich auch der Muskelaufbau bzw. die vorhandene Muskelmasse beeinträchtigt wird. In ähnlicher Weise kann der Schuss nach hinten losgehen, wenn man Kohlenhydrate durch große Mengen gesättigter Fette ersetzt, denn dadurch steigt die ApoB-Konzentration enorm an (und mit ihr das Risiko für kardiovaskuläre Erkrankungen).
Eine wesentlich wichtigere Rolle im Zusammenhang mit einer Beschränkung der Nahrungsmittelauswahl spielt die individuell unterschiedliche Stoffwechselausstattung. Manche Menschen verlieren mit Low-Carb oder mit einer ketogenen Diät sehr viel Gewicht und verbessern ihre Stoffwechselmarker, während andere – bei exakt derselben Ernährungsweise – sogar zunehmen und erleben, dass ihre Fettmarker durch die Decke gehen. Umgekehrt kommt es vor, dass Leute mit einer Low-Fat-Diät Gewicht verlieren, während andere dabei zunehmen. Ich habe das in meiner Praxis immer wieder erlebt, dass ähnliche Diäten – individuell verschieden – zu völlig unterschiedlichen Ergebnissen geführt haben.
Als Eduardo vor einigen Jahren als Patient zu mir kam, stellte sich heraus, dass er bereits einen ausgeprägten Diabetes Typ 2 hatte, von daher war es keine Frage, dass Kohlenhydrate von seinem Speiseplan gestrichen werden mussten. Bei Diabetes Typ 2 ist schließlich der Kohlenhydratstoffwechsel gestört. Auf den ersten Blick machte Eduardo eigentlich einen ziemlich gesunden Eindruck, er hatte eine athletische Figur und einen körperlich anstrengenden Job auf dem Bau. Er entsprach überhaupt nicht dem (falschen) Stereotyp des faulen, gefräßigen Diabetikers. Doch die Tests ergaben, dass sein Körper kaum in der Lage war, überschüssigen Zucker, den er aufnahm, zu speichern.
Sein HbA1c-Wert (Langzeit-Blutzucker) lag bei 9,7 Prozent, also weit im roten diabetischen Bereich. Als Latino hatte er – aufgrund seiner genetischen Veranlagung – ein höheres Risiko für Diabetes und eine nichtalkoholische Fettleber.[340] Er war noch keine vierzig, doch wenn wir nicht schnell drastische Maßnahmen ergriffen, würde er höchstwahrscheinlich früh sterben.
Als Allererstes mussten wir Eduardo natürlich auf weitgehenden Kohlenhydratentzug setzen. Keine Tortillas mehr, keinen Reis, keine stärkehaltigen Bohnen – und auch keine isotonischen Getränke. Da er im Freien in der Hitze arbeitete, schüttete er täglich drei oder vier Liter dieses »Sportgetränks« in sich hinein. Ich habe diese Diät nie als »ketogen« bezeichnet, und Eduardo erzählte seinen Kollegen vom Bau gewiss nichts von seiner neuen trendigen Diät. Er trank einfach keine isotonischen Getränke mehr. (Ich verordnete ihm außerdem Metformin, ein Diabetes-Medikament, das ebenso preisgünstig wie effektiv ist.) Innerhalb von fünf Monaten hatten sich bei Eduardo alle Marker normalisiert, sein Diabetes schien verschwunden zu sein, sein Langzeit-Blutzuckerwert lag bei absolut normalen 5,3 Prozent, und das nur mit der Umstellung der Ernährung und dem Metformin. Außerdem hatte er fast 25 Pfund abgenommen. Ich behaupte nicht, dass diese Diät der einzig mögliche Weg zu diesem Ergebnis war, aber die relativ einfache und machbare Form der Beschränkung der Nahrungsmittelauswahl führte zu einer Verringerung der Energiezufuhr, die ihn Gewicht abbauen ließ, und parallel dazu verbesserte sich alles andere.
In der Vergangenheit war ich ein überzeugter Verfechter von ketogenen Diäten, weil ich sie für besonders nützlich hielt, um Diabetes bei Patienten wie Eduardo zu verhindern oder in den Griff zu bekommen. Ich mag sie auch, weil sie klar definiert sind, im Gegensatz zu »Low-Carb« oder »Low-Fat«. Ketogen heißt, dass die Menge an Kohlenhydraten so stark eingeschränkt wird, bis der Körper beginnt, Fett in sogenannte Ketonkörper zu verwandeln, die von Muskeln und Gehirn als Brennstoff verwendet werden können. Mit einer ketogenen Diät hat sich der vollschlanke Peter wieder in die Reihe gebracht, und vermutlich hat sie auch Eduardo das Leben gerettet. Ich dachte, das sei die Medizin, die jeder Mensch mit einem kranken Stoffwechsel braucht.
Wie so oft brachten mich meine Patienten auf den Boden der Tatsachen zurück. Als Arzt erhält man Rückmeldungen oft auf sehr direkte, persönliche Art. Wenn ich jemandem ein Medikament verschreibe oder eine Maßnahme vorschlage, merke ich ziemlich schnell, ob es wirkt bzw. funktioniert. Das sind keine »Daten« im engeren Sinn, aber es kann ebenso aussagekräftig sein. Ich hatte mehr als einen Patienten, bei dem eine ketogene Diät rein gar nichts brachte. Sie nahmen nicht ab, und ihre Leberenzyme und andere Biomarker verbesserten sich nicht. Oder sie schafften es nicht, die Diät einzuhalten. Dann hatte ich Patienten, denen das zwar gelang, aber ihre Blutfettwerte (insbesondere das ApoB) gingen durch die Decke, wahrscheinlich weil sie so viele gesättigte Fette zu sich nahmen.
Damals verwirrte mich das. Was stimmte nicht mit ihnen? Warum konnten sie die Diät nicht richtig einhalten? Bis mir wieder einfiel, was Steve Rosenberg zu sagen pflegte, wenn die Krebserkrankung bei einem Patienten trotz Behandlung fortschritt: Nicht der Patient hat bei der Behandlung versagt, die Behandlung hat beim Patienten versagt.
Diese Patienten brauchten eine andere Behandlung.
Die wahre Kunst in der Beschränkung der Nahrungsmittelauswahl à la Ernährung 3.0 besteht nicht darin, die Bösewichte herauszupicken, die wir eliminieren wollen. Es geht vielmehr darum, die beste Zusammensetzung der Makronährstoffe für jeden einzelnen Patienten zu finden – dazu einen Essensplan, der ihnen hilft, ihre Ziele zu erreichen, und den sie langfristig einhalten können. Das ist ein schwieriger Balanceakt, und es kommt (wieder einmal) darauf an, alte Vorurteile und Ansichten zu ignorieren und sich ganz auf die Biochemie der Ernährung zu konzentrieren. Wir tun dies, indem wir mit unseren vier Makronährstoffen »spielen«: Kohlenhydrate, Protein, Fett – und Alkohol. Wie gut vertragen Sie Kohlenhydrate? Wie viel Protein benötigen Sie? Welche Art von Fett bekommt Ihnen am besten? Wie viele Kalorien brauchen Sie pro Tag? Welche Kombination wäre für Sie ideal?
Jetzt wollen wir uns die vier Makronährstoffe etwas genauer anschauen.
Alkohol
Es wird meist übersehen, aber eigentlich sollte Alkohol eine eigene Kategorie in der Gruppe der Makronährstoffe erhalten, weil er so häufig konsumiert wird, denn er hat enorme Auswirkungen auf den Stoffwechsel und mit 7 Kilokalorien pro Gramm eine hohe Kaloriendichte (die näher an den 9 Kilokalorien pro Gramm für Fette liegt als an den 4 Kilokalorien pro Gramm für Proteine oder Kohlenhydrate).
Alkohol dient weder der Ernährung noch der Gesundheit, sein Konsum ist ein rein hedonistisches Vergnügen, das geregelt werden muss. Für überernährte Menschen ist er besonders heikel, und zwar aus drei Gründen: Es handelt sich um »leere« Kalorien ohne irgendeinen Wert für die Ernährung; durch die Oxidation des Alkohols verzögert sich die Fettoxidation, das genaue Gegenteil von dem, was wir wollen, wenn es um Fettabau geht; der Alkoholkonsum führt sehr oft zu unüberlegtem Essen.
Natürlich trinke auch ich gelegentlich gern ein Glas meines belgischen Lieblingsbiers, einen spanischen Rotwein oder einen mexikanischen Tequila (nicht alles am selben Abend, versteht sich), aber dennoch glaube ich, dass sich der Alkoholkonsum insgesamt negativ auf die Langlebigkeit auswirkt. Ethanol ist ein starkes Karzinogen, und zwischen chronischem Alkoholkonsum und Alzheimer gibt es einen starken Zusammenhang,[341] vor allem über den negativen Effekt auf den Schlaf,[342] möglicherweise aber auch über andere Mechanismen. Wie Fructose wird auch Alkohol vor allem in der Leber verstoffwechselt, mit den bekannten Langzeitfolgen bei denen, die übermäßig trinken. Schließlich senkt er auch die Hemmschwellen für andere Arten des Nahrungsmittelkonsums: Nach ein paar Drinks finde ich mich unversehens mit der Hand in der Chipstüte wieder und auf dem Weg zum Vorratsschrank, wo ich nach dem nächsten Snack Ausschau halte.
Eine ganze Reihe viel beachteter Studien scheint nahezulegen, dass mäßiger Alkoholkonsum positive Wirkungen haben kann,[343] etwa indem sich die Endothelfunktion verbessert oder die Gefahr der Gerinnselbildung im Blut herabgesetzt wird, was beides das kardiovaskuläre Risiko senkt. Aber stärkerer Alkoholkonsum hebt diese Effekte in der Regel auf und kehrt sie um. Und wie die im vorherigen Kapitel erwähnte JAMA-Studie (die mit der mendelschen Randomisierung) gezeigt hat,[344] liegt in der Kategorie »mäßiges Trinken« eine derartige Verzerrung durch gesunde Teilnehmer (healthy user bias) vor, dass man den Studien, die einen gesundheitlichen Nutzen für die Gesundheit behaupten, unmöglich großen Glauben schenken kann.
Nichtsdestoweniger bedeutet ein Lebensstil mit maßvollem Alkoholkonsum (etwa das schöne Glas Wein während eines guten Abendessens) für viele meiner Patienten auch Stressabbau. Mein persönliches Fazit: Wenn du trinkst, trinke mit Verstand. Dann hast du mehr Genuss und weniger negative Konsequenzen. Trinke nie, nur weil man es dir anbietet, zum Beispiel im Flugzeug. Ich halte meine Patienten dazu an, den Alkoholkonsum nach Möglichkeit auf weniger als sieben Portionen pro Woche zu beschränken, idealerweise nicht mehr als zwei pro Tag. Ich selbst schaffe es ganz gut, mich an diese Regel zu halten.
Kohlenhydrate
Der nichtalkoholische Teil unserer Ernährung besteht aus Kohlenhydraten, Proteinen und Fetten, und es ist gar nicht so leicht, für jedes einzelne Individuum die richtige Mischung herauszufinden. In der Zeit der »Etiketten-Diäten« haben wir uns die versammelten Makronährstoffe angeschaut und dann verschiedene Nahrungsmitteltypen aussortiert, nach bestimmten Regeln und mit willkürlich festgelegten Grenzen – das können Sie essen und das nicht, das hier schon, aber bloß nicht das da. Seinerzeit haben wir die richtige Kombination mehr oder weniger geraten. Und dann haben wir abgewartet, um zu sehen, ob es »funktioniert«, typischerweise mit der Gewichtsabnahme als Kriterium. Heute verfügen wir über feinere Methoden zur Betrachtung der Makronährstoffe. Beginnen wir mit den mengenmäßig häufigsten, den Kohlenhydraten.
Was Kohlenhydrate angeht, herrscht vermutlich noch größere Verwirrung als bei den anderen Makronährstoffen. Sie sind weder »gut« noch »schlecht« – obwohl einige Typen besser sind als andere. Insgesamt ist es eher die Frage, wie man sie so dosiert, dass Bedarf und Verträglichkeit zusammenpassen, und das gestaltet sich weniger schwierig als früher. Dank technischer Fortschritte müssen wir heute nicht mehr raten, heute haben wir Daten.
Kohlenhydrate sind unsere Hauptenergiequelle. In unserem Verdauungssystem werden die meisten Kohlenhydrate in Glucose zerlegt, die von allen Zellen dafür verwendet wird, Energie in Form von ATP herzustellen. Überschüssige Glucose, also das, was wir nicht sofort benötigen, kann für den baldigen Verbrauch als Glycogen in der Leber oder in den Muskeln zwischengelagert oder als Fett im Fettgewebe (oder anderswo) deponiert werden. Die Entscheidung darüber wird mithilfe des Hormons Insulin getroffen, dessen Konzentration als Reaktion auf den erhöhten Blutzuckerspiegel ansteigt.
Wir wissen bereits, dass es nicht gut ist, Kalorien im Übermaß zu konsumieren. In Form von Kohlenhydraten verursachen diese Extrakalorien, wie wir in Kapitel 6 gesehen haben, eine Vielzahl von Problemen, von der nichtalkoholischen Fettleber über die Insulinresistenz bis hin zum Diabetes Typ 2. Wir wissen, dass ein erhöhter Blutzuckerspiegel, wenn er lange genug erhöht bleibt, das Risiko für alle Alterskrankheiten erhöht. Doch es gibt auch Hinweise, dass häufige Blutzuckerspitzen und die damit verbundenen Insulinanstiege bereits für sich genommen negative Folgen haben können.[345]
Die Reaktion auf einströmende Glucose ist von Mensch zu Mensch individuell verschieden. Was für den einen zu viel Glucose (oder Kohlenhydrate) ist, ist für den anderen möglicherweise gar nicht genug. Ein Athlet, der trainiert oder der an einem Wettbewerb im Hochleistungssport teilnimmt, kann problemlos 600 oder 800 Gramm Kohlenhydrate pro Tag aufnehmen und verbrennen. Wenn ich das jeden Tag täte, hätte ich wahrscheinlich binnen Jahresfrist Diabetes. Wie viel ist also zu viel? Und wie sieht es mit der Qualität aus? Offensichtlich wirkt sich ein Stück Kuchen auf einen Ausdauersportler anders aus als auf einen Bewegungsmuffel. Aber der Kuchen hat auch andere Auswirkungen als Ofenkartoffeln oder Pommes frites.
Heute verfügen wir über ein Mittel, das uns hilft zu verstehen, wie viele Kohlenhydrate wir vertragen und wie wir auf bestimmte Nahrungsmittel reagieren. Die Methode nennt sich kontinuierliche Glucosemessung (continuos glucose monitoring, abgekürzt CGM), und sie hat sich in den letzten Jahren für mich zu einem sehr wichtigen Werkzeug in meinem ärztlichen Instrumentenkasten entwickelt.[346]
Das Messgerät besteht aus einem mikroskopisch kleinen fadenförmigen Sensor, der in den Oberarm eingesetzt wird.[347] An ihm ist ein Transmitter befestigt, nicht größer als die Fläche eines Fingerabdrucks, der in Echtzeit Daten an das Smartphone des Patienten schickt. Wie sein Name verrät, liefert das CGM kontinuierlich und in Echtzeit die Information über den Blutzuckergehalt, was schon außergewöhnlich ist: Der Patient kann so jederzeit sehen, wie sein Blutzuckerspiegel auf das reagiert, was er gerade isst, sei es nun ein Donut, ein Steak oder eine Handvoll schokolierte Rosinen. Wichtiger noch, registriert CGM den Verlauf des Blutzuckerspiegels über die Zeit, es kann frühere Durchschnittswerte und Abweichungen ermitteln und alle Blutzuckerspitzen nach oben oder auch Abstürze nach unten festhalten.
Die kontinuierliche Glucosemessung stellte eine gewaltige Verbesserung gegenüber dem standardmäßigen Nüchternblutzuckertest einmal pro Jahr dar, der meiner Meinung nach so gut wie nichts von Bedeutung aussagt. Denken Sie an meinen Vergleich mit selbst fahrenden Autos aus dem ersten Teil des Buches: Nüchternblutzuckertests einmal im Jahr sagen vielleicht etwas aus, aber sie sind fast so sinnvoll, wie einen Ziegelstein aufs Gaspedal zu legen. Mit kontinuierlicher Glucosemessung nähern wir uns – um in diesem Bild zu bleiben – den Sensoren, die es seit Neuestem in Autos mit Assistenzsystemen für den Fahrer gibt.
Der große Vorzug der kontinuierlichen Glucosemessung ist, dass wir die Reaktion eines Menschen auf den Verzehr von Kohlenhydraten in Echtzeit sehen und schnell Maßnahmen ergreifen können, um die Kurve abzuflachen und den Durchschnittswert zu senken. Der Echtzeit-Glucosewert dient als grobe Annäherung an die Insulinantwort, die wir ja ebenfalls möglichst niedrig halten wollen. Und schließlich finde ich diesen Wert genauer und praktikabler als den HbA1c-Wert aus dem traditionellen Bluttest, mit dem der durchschnittliche Blutzuckerwert über die Zeit (Langzeit-Blutzucker) geschätzt wird.
Geräte zur CGM sind im Augenblick nur auf Rezept erhältlich und werden meist von Patienten mit diagnostiziertem Diabetes Typ 1 oder Typ 2 getragen, die ihren Blutzuckerspiegel ständig im Blick haben müssen. Für diese Menschen ist die CGM ein wichtiges Mittel, das sie vor lebensbedrohlichen Schwankungen des Blutzuckerspiegels bewahren kann. Doch ich bin der Auffassung, dass fast jeder Erwachsene davon profitieren könnte, wenn er sie zumindest für ein paar Wochen nutzen würde. Wahrscheinlich werden entsprechende Geräte in nicht allzu ferner Zukunft rezeptfrei für alle erhältlich sein.[348] Aber es ist ganz einfach, auch für Nichtdiabetiker, bei Internet-Start-ups für »Metabolic Health« ein solches CGM-Gerät zu bestellen.
Manche Experten und einige Vertreter der evidenzbasierten Medizin kritisieren den wachsenden Gebrauch von CGM-Geräten durch Menschen, die nicht an Diabetes leiden. Und wie diese Art Leute es immer tut, argumentieren sie mit den zu hohen Kosten. Die kontinuierliche Glucosemessung kostet etwa 120 US-Dollar im Monat, was nicht wenig ist – aber ich behaupte, es ist immer noch sehr viel billiger, als jemanden in eine metabolische Dysfunktion und vielleicht Diabetes Typ 2 hineinschlittern zu lassen. Allein die Behandlung mit Insulin kostet Hunderte von US-Dollar pro Monat. Außerdem würden die Kosten für CGM-Geräte sicher sinken, wenn sie weiter verbreitet und leichter rezeptfrei erhältlich wären. Meine Patienten nutzen die Geräte typischerweise einen oder zwei Monate lang, bis sie gelernt haben, welche Nahrungsmittel ihren Blutzuckerspiegel (und ihr Insulin) in die Höhe treiben und wie sie ihr Essverhalten ändern müssen, um eine stabilere Blutzuckerkurve zu erreichen. Sobald sie das wissen, brauchen viele von ihnen keine kontinuierliche Glucosemessung mehr. Es ist eine lohnende Investition.
Das zweite Argument gegen die Verwendung von CGM-Geräten bei Gesunden ist genauso typisch: Es gibt keine randomisierten klinischen Studien, die den Nutzen der Methode nachweisen. Das stimmt zwar, ist in meinen Augen aber ebenfalls ein schwaches Argument. Zum einen verbreitet sich die Nutzung der kontinuierlichen Glucosemessung so schnell und die Technik entwickelt sich so rasch weiter, dass es sehr gut sein kann, dass dann, wenn Sie diese Zeilen lesen, solche Studien vorliegen (vorausgesetzt, eine Studie kann so konzipiert werden, dass sie die wichtigsten Messgrößen über einen ausreichend langen Zeitraum prüft).
Ich bin zuversichtlich, dass derartige Studien, richtig durchgeführt, einen Nutzen ergeben werden, weil wir bereits über umfangreiche Daten verfügen, die zeigen, wie wichtig es ist, den Blutzuckerspiegel niedrig und stabil zu halten. Eine Studie aus dem Jahr 2011 mit 20 000 Teilnehmern, die zum größten Teil keinen Diabetes Typ 2 hatten, stellte fest, dass deren Sterberisiko gleichförmig mit ihrem Langzeit-Blutzucker (gemessen als HbA1c) anstieg.[349] Je höher der Blutzuckerwert, desto höher das Sterberisiko – selbst in dem Bereich, der noch nicht als diabetisch definiert war. Eine andere Studie aus dem Jahr 2019 betrachtete das Ausmaß der Variation der Blutzuckerspiegel bei den einzelnen Teilnehmern und fand, dass Personen, deren Variabilität in der obersten Quartile lag, ein 2,67-mal höheres Sterberisiko hatten als Personen aus der untersten (stabileren) Quartile.[350] Nach diesen Studien scheint es relativ klar zu sein, dass wir den Langzeit-Blutzucker senken und das Ausmaß der Variabilität von Tag zu Tag, von Stunde zu Stunde verringern möchten. Die kontinuierliche Glucosemessung ist das Mittel, mit dem wir das erreichen können. Wir verwenden es bei gesunden Menschen, um ihnen zu helfen, gesund zu bleiben. Darüber sollte man sich nicht streiten müssen.
Wenn ich meinen Patienten die kontinuierliche Glucosemessung verordne, beobachte ich einen Prozess, der in zwei Phasen verläuft. Die erste ist die Aha-Phase, wo sie in Echtzeit erleben, wie unterschiedliche Nahrungsmittel, Sport, Schlaf (vor allem Schlafmangel) und Stress ihre Glucosewerte beeinflussen. Der Nutzen dieser Information kann überhaupt nicht überschätzt werden. Fast immer sind die Patienten fassungslos, wenn sie sehen, wie manche ihrer Lieblingsspeisen den Blutzuckerspiegel erst nach oben schießen und dann in den Keller rasseln lassen. Das führt zur zweiten, der Änderungs-Phase. Die Patienten wissen jetzt, wie ihr Blutzucker auf eine Tüte Kartoffelchips reagiert, und dieses Wissen hält sie davon ab, die nächste gedankenlos zu verdrücken. Nach meiner Beobachtung aktiviert die CGM höchst wirkungsvoll den Hawthorne-Effekt, ein altbekanntes Phänomen, wonach Menschen ihr Verhalten ändern, sobald sie beobachtet werden. (Derselbe Effekt macht Studien, die beobachten wollen, was Menschen tatsächlich essen, so schwierig.)
In den ersten ein, zwei Monaten der CGM-Nutzung überwiegt das Lernen und Verstehen. Danach spielt die Verhaltensänderung die größte Rolle. Beide Phasen sind sehr wirkungsvoll, und selbst wenn meine Patienten aufhören, CGM zu nutzen, stelle ich fest, dass der Hawthorne-Effekt weiter anhält, weil sie nun wissen, was die Tüte Kartoffelchips mit ihrem Blutzuckerspiegel macht. (Diejenigen, die mehr »Training« brauchen, um von ihrem Snackverhalten loszukommen, nutzen die CGM in der Regel länger.) Als ganz besonders nützlich hat sich die kontinuierliche Glucosemessung für Patienten mit ApoE-ε4 erwiesen; bei ihnen sehen wir oft große Blutzuckerspitzen, sogar bei relativ jungen Leuten. Für diese Patienten stellen die Verhaltensänderungen, die die CGM bewirkt, einen wichtigen Teil der Alzheimer-Präventionsstrategie dar.
Das Beste an der kontinuierlichen Glucosemessung ist jedoch, dass sie es mir erlaubt, die Ernährung eines Patienten genau einzustellen und dabei immer noch flexibel zu bleiben. Wir müssen nicht länger versuchen, eine willkürlich festgesetzte Zielvorgabe für die Kohlenhydrat- oder die Fettzufuhr zu erreichen, und dann hoffen, dass es etwas bringt. Stattdessen können wir in Echtzeit zusehen, wie der Körper mit den Nahrungsmitteln umgeht, die er aufgenommen hat. Ist der Blutzucker im Schnitt etwas zu hoch? Gibt es Spitzen über 160 Milligramm pro Deziliter öfter, als mir lieb ist? Vielleicht könnte er doch etwas mehr Kohlenhydrate vertragen? Nicht jeder muss sich bei Kohlenhydraten einschränken, manche vertragen mehr als andere, und einigen Menschen fällt es ausgesprochen schwer, eine Diät mit sehr wenigen Kohlenhydraten durchzuhalten. In der Regel versuche ich, den Langzeit-Blutzuckerwert bei oder unter 100 Milligramm pro Deziliter zu halten, mit einer Standardabweichung von weniger als 15 Milligramm pro Deziliter.[351] Das ist ein sehr ambitioniertes Ziel: 100 Milligramm pro Deziliter entsprechen einem HbA1c von 5,1 Prozent, was schon ziemlich wenig ist. Angesichts des zu erwartenden Lohns, ein verringertes Risiko für Krankheit und Tod, und der zahlreichen Belege bei Diabetikern und Nichtdiabetikern finde ich jedoch, dass es das wert ist.
Das Ganze erfordert Experimentierfreude und schrittweise Annäherung, die Beschränkung der Nahrungsmittelauswahl muss flexibel sein, je nach Lebensweise, Alter, sportlicher Betätigung und so fort. Es ist immer interessant zu sehen, welche Lebensmittel bei manchen Patienten die CGM-Messwerte steigen lassen, bei anderen aber nicht. Die amerikanische Standardernährung treibt sie bei den meisten in die Höhe, da der ganze Zucker und all die stark verarbeiteten Kohlenhydrate gleichzeitig in die Blutbahn gelangen und damit eine heftige Insulinantwort provozieren – genau das, was wir nicht wollen. Selbst scheinbar gesundes Essen, wie zum Beispiel bestimmte vegetarische Tacos, können bei einigen Menschen zu einem kräftigen Anstieg des Blutzuckerspiegels führen. Wann die Kohlenhydrate gegessen werden, kann ebenfalls eine Rolle spielen. Wenn Sie 150 Gramm Kohlenhydrate in Form von Reis und Bohnen in einer Mahlzeit zu sich nehmen, hat das eine andere Wirkung, als wenn Sie die gleiche Menge Reis und Bohnen über den Tag verteilt essen (und noch einmal anders ist die Wirkung, versteht sich, wenn die 150 Gramm Kohlenhydrate als Frühstückscerealien mit Zuckerglasur verzehrt werden). Außerdem ist die Insulinempfindlichkeit generell morgens höher als am Abend, sodass es durchaus sinnvoll sein kann, seinen Kohlenhydratkonsum zeitlich vorzuverlagern.
Was man mithilfe der kontinuierlichen Glucosemessung relativ schnell lernt, ist, dass die individuelle Kohlenhydratverträglichkeit stark von anderen Faktoren abhängt, vor allem vom persönlichen Aktivitätslevel und vom Schlaf. Ausdauersportler, die für einen Marathon oder einen Triathlon trainieren, können sehr viel mehr Kohlenhydrate zu sich nehmen, weil die bei jedem Training sofort verbrannt werden, außerdem verbessert sich die Fähigkeit, Glucose in der Muskulatur und ihren effizienteren Mitochondrien zu verwerten, dadurch erheblich.[352] Schlafmangel oder häufig unterbrochener Schlaf beeinträchtigt die Glucose-Homöostase ebenfalls im Laufe der Zeit. Trotz meiner jahrelangen Erfahrung mit der kontinuierlichen Glucosemessung bei mir selbst und bei meinen Patienten erstaunt es mich immer noch, in welchem Umfang eine Nacht mit schlechtem Schlaf unsere Fähigkeit zur Glucoseverwertung am nächsten Tag zunichtemacht.
Und noch etwas Überraschendes habe ich dank CGM über die nächtlichen Blutzuckerspiegel von Patienten gelernt. Wenn jemand mit, sagen wir, 80 Milligramm pro Deziliter zu Bett geht und der Spiegel dann auf 110 ansteigt und für den Rest der Nacht mehr oder weniger dort bleibt, dann heißt das, dass dieser Mensch wahrscheinlich unter psychischem Stress leidet. Stress bewirkt eine Erhöhung des Cortisolspiegels, was wiederum dazu führt, dass die Leber angeregt wird, mehr Glucose in Umlauf zu bringen. Ich lerne daraus, dass wir uns um das Stressniveau des Patienten und wahrscheinlich auch um seine Schlafqualität kümmern müssen.
Bei alldem handelt es sich nicht um Übungen in Entbehrung. Einer meiner Patienten beichtete mir freudestrahlend, dass ihm seine CGM – die er nur sehr zögerlich akzeptiert hatte – fantastische Möglichkeiten zum Schummeln eröffnet habe. Indem er bestimmte »verbotene« Kohlenhydrattypen nur zu bestimmten Zeiten aß, entweder zusammen mit anderen Nahrungsmitteln oder nach dem Sport, hatte er einen Weg gefunden, seine Langzeitzucker-Ziele zu erreichen, ohne auf den Genuss seiner Lieblingsspeisen verzichten zu müssen. Er spielte mit seiner CGM, und dabei war er aus Versehen auf eine andere Ernährungsregel gestoßen, dass nämlich auch das Timing eine Rolle spielt. Wenn Sie vor dem Work-out eine große Ofenkartoffel verdrücken, wird sie einen viel kleineren Fußabdruck in Ihrem täglichen Glucoseprofil hinterlassen, als wenn Sie sie direkt vor dem Zubettgehen verspeisen.
Es ist wichtig, sich die Grenzen der kontinuierlichen Glucosemessung in Erinnerung zu rufen, hauptsächlich, dass sie lediglich eine einzige Variable misst. Diese Variable ist zufälligerweise von großer Bedeutung, aber sie ist nicht die einzige. Das heißt, dass die CGM-Daten allein nicht ausreichen, um die ideale Ernährungsweise zu finden. Schinkenspeck zum Frühstück, zu Mittag und zum Abendessen bringt Ihnen vielleicht großartige Glucosewerte, doch stellt das ganz sicher keine optimale Ernährung dar. Das ist so, als würde Ihnen Ihre Badezimmerwaage sagen, Rauchen sei gut für Sie, weil Sie dadurch abgenommen haben. Darum überwache ich auch die anderen Biomarker meiner Patienten engmaschig, um sicherzustellen, dass ihre CGM-geleiteten Essensentscheidungen nicht etwa das Risiko für etwas anderes erhöhen, zum Beispiel Herz-Kreislauf-Erkrankungen. Wir behalten auch andere Variablen im Auge, die für die Ernährung wichtig sind, angefangen (natürlich) beim Gewicht, aber auch die Körperzusammensetzung, das Verhältnis von fettfreier Körpermasse zu Körperfett und wie es sich verändert. Wir achten außerdem auf Biomarker wie Lipide, Harnsäure, Insulin und Leberenzyme. Alle Werte zusammen ermöglichen uns eine bessere Abschätzung der erzielten Fortschritte als einer allein.
Lehren aus der kontinuierlichen Glucosemessung
In den Jahren, in denen ich die CGM angewendet habe, habe ich folgende Einsichten gewonnen; einige davon mögen vielleicht auf der Hand liegen, aber die Bestätigungen sind beeindruckend und können nicht ignoriert werden:
Nicht alle Kohlenhydrate sind gleich. Je stärker sie raffiniert sind (Weißbrot, Kartoffelchips), desto schneller und höher der Glucoseanstieg. Weniger stark verarbeitete Kohlenhydrate und solche mit einem höheren Ballaststoffanteil dagegen schwächen die Glucosewirkung ab. Ich versuche, etwa 50 Gramm Ballaststoffe pro Tag zu mir zu nehmen.
Reis und Haferflocken haben einen überraschend deutlichen glykämischen Effekt (das heißt, sie verursachen einen steilen Glucoseanstieg), obwohl sie nicht besonders stark verarbeitet sind. Noch überraschender: Bei braunem (»Vollkorn«-)Reis fällt die glykämische Reaktion nur wenig niedriger aus als bei weißem Langkornreis.
Fructose wird mit der kontinuierlichen Glucosemessung nicht erfasst, weil sie aber fast immer zusammen mit Glucose verzehrt wird, verursachen Lebensmittel mit hohem Fructosegehalt ebenfalls Blutzuckerspitzen.
Zeit, Dauer und Intensität von sportlicher Betätigung spielen eine große Rolle. Generell scheint aerobes Training Glucose am wirkungsvollsten aus dem Blutkreislauf zu holen, während intensives Ausdauer- und Krafttraining den Blutzuckerspiegel vorübergehend ansteigen lassen können, weil die Leber dann mehr Glucose in die Blutbahn abgibt, um die Muskeln zu versorgen. Also bekommen Sie keinen Schreck, wenn Ihr Blutzuckerspiegel bei intensivem Training Spitzen aufweist.
Eine Nacht mit schlechtem Schlaf oder eine mit gutem, in Bezug auf die Glucoseregulation ist das ein himmelweiter Unterschied. Wenn die sonstigen Umstände gleich sind, führt eine Schlafdauer von nur fünf bis sechs Stunden (verglichen mit acht Stunden) dazu, dass Glucosespitzen um etwa 10 bis 20 Milligramm pro Deziliter (das ist viel!) höher ausfallen und der Blutzuckerspiegel insgesamt um 5 bis 10 Milligramm pro Deziliter ansteigt.
Stress hat – vermutlich über Cortisol und andere Stresshormone – einen überraschenden Einfluss auf den Blutzuckerspiegel, selbst wenn die betreffende Person fastet oder nur wenige Kohlenhydrate zu sich nimmt. Der Effekt ist schwer zu quantifizieren, aber er ist am deutlichsten während des Schlafs zu erkennen oder zu Zeiten, wenn die letzte Mahlzeit lange zurückliegt.
Gemüse, die keine Stärke enthalten, wie Spinat oder Brokkoli, haben so gut wie keinen Effekt auf den Blutzucker. Greifen Sie zu.
Lebensmittel mit einem hohen Protein- und Fettgehalt (wie zum Beispiel Eier oder Querrippe vom Rind) haben praktisch keine Auswirkungen auf den Blutzuckerspiegel (vorausgesetzt, die gegrillte Querrippe wird nicht mit dicker Soße übergossen),[353] große Mengen von fettarmem Fleisch (zum Beispiel Hähnchenbrust) treiben ihn leicht in die Höhe. Proteinshakes, insbesondere solche mit geringem Fettgehalt, haben einen deutlichen Effekt (vor allem natürlich, wenn sie auch Zucker enthalten).
Mit diesen Einsichten – positive wie negative zusammengenommen – können wir schon sehr viel erreichen. Wenn Sie völlig gestresst sind, schlecht schlafen und keine Zeit für Sport finden, dann sollten Sie, was das Essen angeht, sehr vorsichtig sein.
Die wichtigste Erkenntnis von allen? Allein dass ich den Verlauf meiner Blutzuckerkurve immer mitverfolgen konnte, hat mein Essverhalten positiv verändert. Mittlerweile schätze ich den Umstand, dass die kontinuierliche Glucosemessung den Hawthorne-Effekt hervorruft, das Phänomen, dass Studienteilnehmer ihr Verhalten ändern, weil sie wissen, dass sie beobachtet werden. So kommt es, dass ich zweimal nachdenke, wenn ich die Tüte mit den schokolierten Rosinen (oder irgendetwas anderes, das meinen Blutzuckerspiegel in die Höhe treiben könnte) im Vorratsschrank liegen sehe.
Proteine
Warum sind Proteine so wichtig? Einen Hinweis liefert ihr Name, der sich aus dem griechischen Wort protos herleitet, das »zuerst« bedeutet. Proteine und Aminosäuren zählen zu den wichtigsten Bausteinen des Lebens. Ohne sie können wir die Muskelmasse, die wir brauchen, weder aufbauen noch aufrechterhalten. Wie wir in Kapitel 11 gesehen haben, sind sie auch für unsere Strategie von zentraler Bedeutung, denn je älter wir werden, desto leichter verlieren wir Muskelmasse und umso schwieriger wird es, sie wieder aufzubauen.
Erinnern Sie sich an die Studie, um die es in Kapitel 12 ging? Sie untersuchte, welche Wirkung Krafttraining auf 62 gebrechliche Senioren hatte. Die Personen, die sechs Monate lang nur Krafttraining machten und sonst nichts, legten keine Muskelmasse zu. Was ich dort nicht erwähnt habe: Es gab noch eine andere Teilnehmergruppe, die zusätzlich Proteine (in Form von Proteinshakes) erhielt; diese Personen legten im Schnitt drei Pfund fettfreie Masse zu. Das Extraprotein machte vermutlich den Unterschied.[354]
Anders als Kohlenhydrate und Fette sind Proteine keine primäre Energiequelle. Weder hängt unsere ATP-Versorgung von ihnen ab,[355] noch speichern wir sie in einer ähnlichen Weise wie Fett (in den Fettzellen) oder Glucose (als Glykogen). Wenn Sie mehr Protein aufnehmen, als Sie fettfreie Masse bilden können, dann scheiden Sie den Überschuss mit dem Urin als Harnsäure aus. Proteine sind reines Baumaterial. Die zwanzig Aminosäuren, aus denen Proteine bestehen, sind die Bausteine für unsere Muskeln, unsere Enzyme und für einige der wichtigsten Hormone in unserem Körper. Sie mischen praktisch überall mit, angefangen bei der Bildung von Haaren, Haut und Nägeln bis hin zur Herstellung von Antikörpern in unserem Immunsystem. Überdies müssen wir neun der zwanzig Aminosäuren, die wir brauchen, mit der Nahrung aufnehmen, da unser Körper sie nicht selbst produzieren kann.
Das Erste, was Sie zu Protein (als Makronährstoff) wissen müssen: Die übliche Empfehlung für die tägliche Aufnahme mit der Nahrung ist ein Witz. Die in den USA verwendete Recommended Daily Allowance (RDA) für Protein ist 0,8 Gramm pro Kilogramm Körpergewicht.[356] Vielleicht gibt dieser Wert an, wie viel Protein wir brauchen, um am Leben zu bleiben, von der Menge, die wir brauchen, damit es uns wirklich gut geht, ist er jedoch meilenweit entfernt. Uns liegen jede Menge Hinweise vor, die belegen, dass wir mehr benötigen als das und dass eine Aufnahme, die darunterliegt, üble Folgen hat. Mehr als eine Studie hat festgestellt,[357] dass ältere Menschen, die gemäß der RDA-Empfehlung 0,8 Gramm Protein pro Tag und Kilogramm Körpergewicht zu sich nahmen, Muskelmasse verloren,[358] und zwar bereits innerhalb von zwei Wochen, also einem sehr kurzen Zeitraum. Es ist einfach nicht genug.
Noch eine Anmerkung in diesem Zusammenhang: Möglicherweise hat der ein oder andere von Ihnen den Eindruck, eine eiweißarme Diät könnte der Langlebigkeit dienlich sein. Gewiss, eine ganze Reihe von Studien an Mäusen legen nahe, dass eine Beschränkung der Proteinaufnahme die Lebenszeit von Mäusen verlängern könnte. Aber ich bin trotzdem nicht überzeugt, dass sich diese Ergebnisse auf den Menschen übertragen lassen. Menschen und Mäuse reagieren sehr unterschiedlich auf niedrige Proteinzufuhr, und andere Studien legen nahe, dass dies bei älteren Menschen zu einem Verlust von Muskelmasse führt, wodurch sich die Lebensqualität verschlechtert und die Sterblichkeit zunimmt. Ich finde diese an Menschen gewonnenen Daten überzeugender als die Studien mit Mäusen, diese Tiere sind einfach anders als wir.
Wie viel Protein brauchen wir nun wirklich? Das ist individuell verschieden. Für meine Patienten setze ich normalerweise 1,6 Gramm pro Tag und Kilogramm Körpergewicht als Minimum an, das Doppelte der offiziellen Empfehlungen. Die ideale Menge kann von Person zu Person variieren, doch die Daten legen nahe, dass 2,2 Gramm pro Tag und Kilogramm Körpergewicht – also fast das Dreifache des RDA-Wertes – für aktive Menschen mit normaler Nierenfunktion ein guter Ausgangspunkt sind.[359]
Jemand mit einem Gewicht von 82 Kilogramm benötigt demnach mindestens 130 Gramm Protein pro Tag, besser noch 180 Gramm, vor allem, wenn diese Person Muskelmasse aufbauen will. Das ist eine ziemlich große Menge, und die nächste Herausforderung besteht darin, sie nicht in einer Mahlzeit zu konsumieren, sondern über den Tag verteilt, damit möglichst wenige Proteine durch Oxidation verloren gehen (damit sie nicht etwa für die Energiegewinnung eingesetzt werden, obwohl wir sie für die Produktion von Muskelprotein haben wollen). Der Fachliteratur zufolge erreicht man das idealerweise mit vier Proteinmahlzeiten am Tag, von denen jede etwa 0,55 Gramm pro Kilogramm Körpergewicht enthält.[360] Eine Portion Huhn, Fisch, Rind- oder Schweinefleisch von etwa 200 Gramm liefert zwischen 40 und 45 Gramm Protein, das heißt, unsere Beispielperson mit 82 Kilogramm sollte jeden Tag vier solche Portionen verzehren.
Die meisten Menschen müssen keine Angst haben, dass sie zu viel Protein zu sich nehmen. Man müsste sich schon gewaltig anstrengen, um mehr als 3,7 Gramm pro Tag und Kilogramm Körpergewicht zu konsumieren, was als sichere Obergrenze für den Proteinkonsum gilt (sonst ist die Belastung für die Nieren zu hoch). Für unsere Beispielperson läge diese Obergrenze bei 300 Gramm Protein oder 1,3 Kilogramm (!) Fleisch am Tag.
Wie viel Protein Sie brauchen, hängt von Ihrem Geschlecht, Ihrem Körpergewicht, Ihrer fettfreien Masse, Ihrem Aktivitätslevel, Ihrem Alter und weiteren Faktoren ab. Es gibt einige Hinweise dafür, dass ältere Menschen mehr Protein benötigen, weil sich mit dem Alter eine »anabole Resistenz« (anabolic resistance) entwickelt, wodurch es schwieriger wird, neue Muskelmasse aufzubauen.[361] Leider gibt es für Proteine nichts, was der kontinuierlichen Glucosemessung für Kohlenhydrate vergleichbar wäre, darum bleibt nichts anderes übrig, als sich mit Versuch und Irrtum vorzutasten. Ich versuche, so viel Protein aufzunehmen, dass meine Muskelmasse konstant bleibt, wenn ich trainiere. Stelle ich fest, dass sich meine Muskelmasse verringert, bemühe ich mich, mehr Proteine zu mir zu nehmen. Vor allem ältere Menschen sollten ihre fettfreie Masse im Auge behalten, zum Beispiel über eine Waage, die auch die Körperzusammensetzung anzeigt (oder besser noch über einen DEXA-Scan), und ihren Proteinkonsum erhöhen, wenn ihre fettfreie Masse abnimmt. Für mich und meine Patienten funktioniert das gut mit vier Proteineinheiten am Tag, von denen mindestens eine aus einem Molkedrink besteht. (Mir fällt es wirklich schwer, vier Mahlzeiten am Tag einzunehmen; meist komme ich auf einen Proteinshake, einen proteinreichen Snack und zwei Proteinmahlzeiten.)
Und was ist mit pflanzlichen Proteinen? Muss man Fleisch, Fisch und Milchprodukte verzehren, um genügend Proteine zu bekommen? Nein. Doch wenn Sie beschließen, alles Protein aus Pflanzen zu beziehen, müssen Sie zwei Dinge wissen. Erstens, die Pflanzenproteine sind so aufgebaut, dass sie den Pflanzen nutzen, das heißt, sie bilden lange und zum Teil miteinander vernetzte Komplexe, die nicht oder nur schwer verdaulich sind; das mindert ihre Bioverfügbarkeit für die Person, die sie essen will. Weil ein großer Teil des Pflanzenproteins in dieser Form in Wurzeln, Blättern und anderen Strukturen vorliegt, kann Ihr Körper nur etwa 60 bis 70 Prozent des Pflanzenproteins, das Sie essen, auch für sich nutzen. Das sagt Don Layman, emeritierter Professor für Lebensmittelwissenschaften und menschliche Ernährung an der University of Illinois Urbana-Champaign und Proteinexperte.
Dieses Problem lässt sich teilweise durch Kochen lösen, ein zweites aber bleibt: Die Aminosäurezusammensetzung von pflanzlichem Protein ist nicht die gleiche wie die von tierischem. Insbesondere die essenziellen Aminosäuren Methionin, Lysin und Tryptophan kommen in Pflanzenprotein nur in geringerer Menge vor, was sich negativ auf die Proteinsynthese auswirken kann. Beides zusammen bedeutet, dass die Qualität von aus Pflanzen gewonnenem Protein insgesamt deutlich geringer ist als die von tierischen Produkten.
Das Gleiche gilt für Protein-Supplemente. Aus Molke, einem Milchprodukt, hergestellte Nahrungsergänzungsmittel enthalten mehr verfügbare Aminosäuren als solche auf Basis von Sojaprotein. Das heißt, wenn Sie auf tierisches Protein verzichten wollen, müssen Sie genau rechnen, damit die Proteinqualität am Ende stimmt. In der Praxis kann das ganz schnell ziemlich kompliziert werden, weil Sie sich dann mit solchen Dingen beschäftigen müssen wie dem Protein Digestibility Corrected Amino Acid Score (PDCAAS, deutsch etwa »um die Proteinverdaulichkeit korrigierter Aminosäureindex«) oder dem Digestible Indispensable Amino Acid Score (DIAAS, deutsch etwa »Index verdaulicher, unentbehrlicher Aminosäuren«). Die beiden Indexe sind hervorragend, wenn Sie Zeit haben, den ganzen Tag in Datenbanken zu stöbern, für diejenigen, die arbeiten müssen, empfiehlt Layman, sich auf eine Handvoll wichtiger Aminosäuren wie Leucin, Lysin und Methionin zu konzentrieren. Achten Sie auf die absolute Menge dieser Aminosäuren in jeder Mahlzeit; zur Aufrechterhaltung der fettfreien Masse sollten Sie jeden Tag drei bis vier Gramm Leucin und Lysin aufnehmen, Methionin mindestens ein Gramm pro Tag. Wenn Sie versuchen, Muskelmasse aufzubauen, brauchen Sie sogar noch mehr Leucin, eher zwei bis drei Gramm pro Mahlzeit, viermal am Tag.
Im Allgemeinen gilt, je höher der Proteinverzehr, desto besser – das lässt sich aus zahlreichen Studien ablesen. Eine große prospektive Studie, die Healthy Aging and Body Composition Study, mit über 2000 älteren Teilnehmern stellte fest, dass diejenigen, die die meisten Proteine konsumierten (etwa 18 Prozent der Gesamtkalorienmenge), im Lauf von drei Jahren mehr ihrer fettfreien Masse behielten als die mit dem niedrigsten Proteinkonsum (unterste Quintile, 10 Prozent der Gesamtkalorienmenge).[362] Dieser Unterschied war statistisch signifikant, die Gruppe mit dem niedrigen Proteinverzehr verlor 40 Prozent mehr Muskelmasse als die Gruppe mit dem hohen.
Andere Studien ergaben, dass selbst eine Proteinaufnahme, die nur wenig über den offiziellen RDA-Empfehlungen liegt, den fortschreitenden Verlust von Muskelmasse bei alten Menschen verlangsamen konnte, sogar bei Patienten, die an Herzschwäche und Auszehrung litten.[363] Als Argument könnte man noch anführen, dass Protein ein leistungssteigernder Makronährstoff ist. Nachdem die Kost von gebrechlichen alten Menschen mit 30 Gramm Milchprotein supplementiert worden war, verbesserte sich deren körperliche Leistungsfähigkeit statistisch signifikant.[364]
Über seine Rolle für den Muskelaufbau hinaus hat Protein auch noch positive Auswirkungen auf den Stoffwechsel. In einer Studie, für die ältere Menschen Supplemente mit essenziellen Aminosäuren erhalten hatten (wodurch ähnliche Effekte erzielt werden sollten wie durch eine Erhöhung der Proteinzufuhr über die Ernährung), verminderten sich die Fettmenge in der Leber und die Triglycerid-Konzentration in der Blutbahn.[365] Eine andere Studie untersuchte Männer mit Diabetes Typ 2 und stellte fest, dass sich deren Empfindlichkeit für Insulin sowie die Glucoseregulation verbesserte, wenn sie ihren Proteinkonsum von 15 auf 30 Prozent der Gesamtkalorienmenge verdoppelten und gleichzeitig die aufgenommene Kohlenhydratmenge halbierten.[366] Wenn wir Proteine essen, fühlen wir uns eher gesättigt, da sie das Freisetzen des Hunger auslösenden Hormons Ghrelin hemmen; dadurch nehmen wir auch insgesamt weniger Kalorien auf.
Nur für den Fall, dass ich mich nicht klar genug ausgedrückt habe, wiederhole ich meinen Standpunkt: Achten Sie auf die Proteine. Dieser Makronährstoff ist absolut unverzichtbar für das Erreichen unserer Ziele. Für Kohlenhydrate und Fette gibt es praktisch keine Mindestaufnahmemenge, doch wenn Sie beim Protein nicht aufpassen, erhalten Sie ziemlich sicher irgendwann die Rechnung, vor allem, wenn Sie älter werden.
Fette
Ein weiterer wesentlicher Bestandteil unserer Ernährung ist Fett oder, besser gesagt, sind Fette. Zu viel davon kann jedoch problematisch werden, sowohl was die Gesamtkalorienmenge angeht als auch vom Stoffwechsel her. Eigentlich könnte es ganz einfach sein, aber das Nahrungsfett hat eine üble Vergangenheit, die immer noch für einige Verwirrung sorgt.
Für den lange Zeit schlechten Ruf der Fette gibt es zwei Gründe: ihren hohen Kaloriengehalt (9 Kilokalorien pro Gramm) und ihre Rolle beim Anstieg des LDL-Cholesterins und für die Erhöhung des Herz-Kreislauf-Risikos. Ähnlich wie Kohlenhydrate werden Fette oft – je nach ernährungsideologischer oder politischer Couleur – als »gut« oder »schlecht« bezeichnet. In Wirklichkeit sind sie, natürlich, weder das eine noch das andere. Fette spielen für jede Art der Ernährung eine bedeutende Rolle, darum ist es wichtig, sie zu verstehen.
Während Kohlenhydrate vor allem Brennstofflieferanten und Proteine vor allem Baumaterial sind, erfüllen Fette beide Funktionen. Sie sind hocheffiziente Brennstoffe für die Oxidation (denken Sie an langsam brennende Holzscheite), aber auch Bausteine für viele Hormone (in Form von Cholesterin zum Beispiel) und Zellmembranen. Die richtige Fettkombination in der Ernährung hilft, den Stoffwechsel im Gleichgewicht und das Gehirn gesund zu halten, das zu einem großen Teil aus Fetten und fettähnlichen Substanzen besteht. Auf der eher praktischen Seite steht, dass der Verzehr von Fett oft schneller zur Sättigung führt als der von vielen Kohlenhydratarten, insbesondere in Kombination mit Protein.[367]
Ganz grob lassen sich die Fette in drei Typen einteilen: solche mit gesättigten (saturated fatty acids, abgekürzt SFA), mit einfach ungesättigten (monounsaturated fatty acids, MUFA) oder mit mehrfach ungesättigten Fettsäuren (polyunsaturated fatty acids, PUFA).[368] Die unterscheiden sich in ihrer chemischen Struktur, »gesättigte« Fettsäuren haben schlicht mehr Wasserstoffatome an ihren Kohlenstoffketten.[369] Bei den mehrfach ungesättigten Fettsäuren machen wir noch eine weitere wichtige Unterscheidung: Je nach Lage der ersten Doppelbindung in der Kohlenstoffkette sprechen wir von Omega-6- oder Omega-3-Fettsäuren.
Und die Omega-3-Fettsäuren kann man noch weiter unterteilen: EPA (Eicosapentaensäure) und DHA (Docosahexaensäure) stammen aus Quellen aus dem Meer, zum Beispiel von Lachs, Hering oder Fischöl, ALA (Alpha-Linolensäure) (in Nüssen und Leinsamen) dagegen nicht.
An eins sollte man sich immer erinnern – und trotzdem wird es leider fast immer vergessen –, es gibt so gut wie kein Nahrungsmittel, das nur einen Fettsäuretyp enthält. Olivenöl und Distelöl kommen einem reinen einfach ungesättigten Öl sehr nahe, während Palmöl und Kokosöl beinahe als reine gesättigte Fette gehandelt werden können; nichtsdestoweniger enthalten alle fetthaltigen Nahrungsmittel normalerweise Fettsäuren aller drei Kategorien: gesättigte ebenso wie einfach und mehrfach ungesättigte. Selbst ein saftiges Ribeye-Steak enthält eine ganze Menge ungesättigter Fettsäuren.
Von daher ist es nicht wirklich möglich oder machbar, bestimmte Kategorien von Fettsäuren ganz aus der Ernährung streichen zu wollen; deshalb versuchen wir, ein bisschen an den Mengenverhältnissen zu drehen. Wenn sie zu mir kommen, sieht die Ausgangslage bei den meisten meiner Patienten so aus: Ihr Fettkonsum besteht zu je 30 bis 40 Prozent aus gesättigten und einfach ungesättigten und zu 20 bis 30 Prozent aus mehrfach ungesättigten Fetten; von Letzteren verzehren sie normalerweise sechs- bis zehnmal mehr Omega-6- als Omega-3-Fettsäuren, die Anteile von EPA und DHA sind meist sehr gering.
Aufgrund meiner empirischen Beobachtungen und der von mir als relevant erachteten Literatur – was alles andere als perfekt, aber besser als nichts ist – versuchen wir, den Anteil einfach ungesättigter Fette auf 50 bis 55 Prozent zu erhöhen, die gesättigten auf 15 bis 20 Prozent zu drücken und die mehrfach ungesättigten so weit nachzuregeln, dass die Lücke gefüllt wird. Wir pushen auch EPA und DHA, die Fettsäuren, die wahrscheinlich für das Gehirn und die kardiovaskuläre Gesundheit von Bedeutung sind, mit fettem Seefisch und/oder mit Supplementen (Fischöl). Die Mengen von EPA und DHA in der Ernährung meiner Patienten regulieren wir danach, wie viel von beiden in den Membranen ihrer roten Blutkörperchen nachweisbar ist; das geschieht über einen speziellen, aber leicht verfügbaren Bluttest.[370] Welchen Wert wir anpeilen, hängt vom ApoE-Genotyp des Patienten und anderen Risikofaktoren für neurodegenerative und kardiovaskuläre Erkrankungen ab. Für die meisten Patienten streben wir einen Bereich von 8 bis 12 Prozent EPA und DHA in der Membran der roten Blutkörperchen an.
In die Praxis umgesetzt bedeuten die geschilderten Veränderungen, dass Sie mehr Olivenöl, Avocados und Nüsse und deutlich weniger Butter und Speck essen sollten (Sie müssen aber nicht ganz darauf verzichten). Außerdem sollten Sie den Konsum von Mais-, Soja- und Sonnenblumenöl zurückfahren, die alle reich an Omega-6-Fettsäuren sind, und dafür nach Wegen suchen, mehr Omega-3-haltige Fettsäuren zu sich zu nehmen, etwa über Lachs oder Sardellen.[371]
Hier kommt wieder die amerikanische Standardernährung ins Spiel, unsere moderne Ernährungsumwelt, und macht die Dinge kompliziert. Noch vor hundert Jahren haben unsere Urgroßeltern all ihre Fette in Form von Butter, Speck und Talg von Tieren bezogen oder aus Früchten wie Oliven, Kokosnüssen und Avocados. Diese Nahrungsmittel konnten sie in einem relativ naturbelassenen Zustand verzehren und so ohne größere Probleme eine ziemlich ausgewogene Mischung von Fettsäuren aufnehmen. Im Lauf des 20. Jahrhunderts ermöglichten es die Fortschritte der Lebensmitteltechnologie, nicht mehr nur mechanisch, sondern auch chemisch Öle aus Samen und Früchten zu extrahieren, bei denen es sonst nicht möglich gewesen wäre. Dank dieser neuen Technologien gelangten plötzlich enorme Mengen von Ölen mit mehrfach ungesättigten Fettsäuren, wie zum Beispiel Maisöl oder Baumwollsamenöl (die Alpha-Linolensäure enthalten), auf den Lebensmittelmarkt. In den USA hat sich der Pro-Kopf-Verbrauch von Sojaöl seit 1909 mehr als vertausendfacht;[372] es gibt inzwischen sogar Studien, die zeigen, dass die Konzentration von Alpha-Linolensäure, einer mehrfach ungesättigten Fettsäure, im menschlichen Fettgewebe ebenfalls gestiegen ist: über 136 Prozent im Laufe der letzten fünfzig Jahre.
Diese industrielle Fettrevolution führte auch zur Entstehung von Transfetten, auf den Inhaltsangaben als »teilweise gehärtete Pflanzenöle« aufgeführt (denken Sie »Margarine«), die die Ausbreitung der amerikanischen Standardernährung zumindest förderten, auch weil die Nahrungsmittel dadurch länger lagerfähig wurden. Doch Transfette trugen unter anderem zur Atherosklerose bei (weil sie ApoB erhöhten) und wurden deshalb von der amerikanischen Lebensmittelbehörde FDA verboten.[373] Die Versuchung ist groß, der massiven Zunahme der Verbreitung von Sojaöl und anderen aus Samen gewonnenen Ölen die Schuld an unserer Fettleibigkeitsepidemie und dem grassierenden metabolischen Syndrom zuzuweisen. Etwas, was sich in der gleichen Zeitspanne von wenigen Jahrzehnten, in der unsere Gesundheit vor die Hunde ging, vertausendfacht, kann nicht gut sein, oder? Noch vor ein paar Jahren, dachte ich, dass das zutrifft. Aber je genauer ich mir die Daten ansehe, desto unsicherer bin ich, ob sie wirklich viel darüber aussagen.
Der umfassendste Überblick zum Thema wurde 2018 von der Cochrane Collaboration veröffentlicht.[374] Diese Übersichtsarbeit mit dem Titel »Polyunsaturated Fatty Acids for the Primary and Secondary Prevention of Cardiovascular Disease« (»Mehrfach ungesättigte Fettsäuren für die Primär- und Sekundärprävention von kardiovaskulären Erkrankungen«) fasst auf 422 Seiten sämtliche relevante Literatur aus 49 Studien mit 24 000 randomisierten Patienten zusammen und kommt zu folgendem Schluss: »Eine Erhöhung der Zufuhr von mehrfach ungesättigten Fettsäuren macht vermutlich keinen oder nur einen geringen Unterschied (weder Nutzen noch Schaden) hinsichtlich des Mortalitätsrisikos, und sie macht wahrscheinlich nur einen geringen oder keinen Unterschied hinsichtlich des Risikos, an einer Herz-Kreislauf-Erkrankung zu sterben. Nichtsdestoweniger reduziert die Erhöhung der Zufuhr von mehrfach ungesättigten Fettsäuren wahrscheinlich in geringem Umfang das Risiko für kardiovaskuläre Ereignisse sowie für kardio- und zerebrovaskuläre Ereignisse zusammengenommen (Evidenz mäßiger Qualität).«
Okay, das Erhöhen der Zufuhr von mehrfach ungesättigten Fettsäuren bringt also einen leichten Nutzen. Eine neuere Veröffentlichung der Cochrane Collaboration stammt aus dem Jahr 2020.[375] Die 287-seitige Abhandlung mit dem Titel »Reduction in Saturated Fat Intake for Cardiovascular Disease« (»Verringerung der Aufnahme gesättigter Fette für kardiovaskuläre Erkrankungen«) betrachtete 15 randomisierte klinische Studien mit über 56 000 Patienten; sie stellte unter anderem fest, dass »die Verringerung der Aufnahme gesättigter Fette das Risiko für alle kardiovaskulären Ereignisse zusammengenommen um 17 Prozent verringert«. Interessant. Doch in derselben Übersichtsarbeit heißt es auch, die Verringerung der Aufnahme von gesättigtem Fett habe »keine oder nur eine geringe Auswirkung auf die Gesamtmortalität oder die kardiovaskuläre Mortalität«. Und weiter: »Es gab nur eine geringe oder keine Auswirkung auf Krebsmortalität, Krebsdiagnosen, Diabetesdiagnosen, HDL-Cholesterin, Blutfette oder Blutdruck und nur kleine Verringerungen bei Gewicht, Gesamtcholesterin, LDL-Cholesterin und BMI.«
Gesättigte Fette also leicht im Nachteil, aber keine Auswirkungen auf die Sterblichkeit beobachtet. Und jetzt zum Schluss noch eine andere Übersichtsarbeit aus dem Jahr 2021 mit dem Titel »Total Dietary Fat Intake, Fat Quality, and Health Outcomes: A Scoping Review of Systematic Reviews of Prospective Studies« (»Gesamtfettzufuhr, Fettqualität und Folgen für die Gesundheit: eine orientierende Übersicht über systematische Reviews zu prospektiven Studien«).[376] Sie untersuchte 59 systematische Reviews von randomisierten klinischen und prospektiven Kohorten-Studien und fand »im Wesentlichen keinen Zusammenhang zwischen der Gesamtfettaufnahme, dem Verzehr von einfach ungesättigten Fettsäuren (MUFA), mehrfach ungesättigten Fettsäuren (PUFA) und gesättigten (SFA) und dem Risiko für chronische Krankheiten«.
Ich könnte noch mehr Beispiele bringen, aber ich denke, Sie verstehen, worauf ich hinauswill. Die Daten zu dieser Fragestellung sind ziemlich weich, zumindest auf Populationsebene. Wie wir bereits in der Einführung zu Medizin 3.0 und in Kapitel 14 diskutiert haben, sind die Hoffnungen auf die Anwendung der Erkenntnisse der evidenzbasierten Medizin zum Scheitern verurteilt, sobald es um Ernährung geht, da auf Populationsebene gewonnene Daten auf der individuellen Ebene nicht viel Aussagewert haben, wenn die Effekte so klein sind, wie es ganz offenkundig hier der Fall ist. Das Einzige, was Medizin 2.0 anbieten kann, ist der große Rahmen: Einfach ungesättigte Fette scheinen von den drei Fett-Typen noch am »besten« zu sein (auf der Grundlage von PREDIMED und der Lyon Heart Study), dann kommen den Metaanalysen zufolge die mehrfach ungesättigten knapp vor den gesättigten Fetten. Das war’s, für alles Weitere sind wir auf uns selbst gestellt.
Medizin 3.0 fragt, welches der beste Fettmix für welchen Patienten ist. Um zu sehen, wie die Veränderungen im Fettsäurekonsum bei meinen Patienten Cholesterin-Synthese und -Absorption sowie ihre Lipide und Entzündungswerte beeinflussen, behalte ich eine ganze Reihe von Lipiden im Auge. Selbst minimale Veränderungen im Fettverzehr, vor allem von gesättigten Fetten, können bei manchen Patienten die Lipidspiegel merklich beeinflussen, das habe ich immer wieder festgestellt. Einige Menschen können (so wie ich)[377] nahezu folgenlos gesättigte Fette konsumieren, während andere ein Stück Frühstücksspeck nur von der Seite ansehen, und die Zahl ihrer ApoB-Moleküle springt schon in die 90. Perzentile. Medizin 2.0 sagt, das beweist, dass niemand gesättigte Fette konsumieren sollte, Punkt. Medizin 3.0 nimmt die Daten und sagt: »Dass die ApoB-Werte des Patienten so in die Höhe geschossen sind, ist natürlich schlecht. Das stellt uns vor die Wahl: Sollen wir ihm eine Medikation verschreiben, die die ApoB-Werte senkt, oder sollen wir ihm eine Beschränkung des Verzehrs gesättigter Fette verordnen? Oder beides?« Es gibt keine klare und eindeutige Antwort, und da diese Situation alles andere als selten ist, läuft es auf eine Ermessensentscheidung hinaus.
Schlussendlich rate ich meinen Patienten auf Grundlage der am wenigsten schlechten und am wenigsten unklaren verfügbaren Daten, dass die einfach ungesättigten Fettsäuren wohl den Löwenanteil ihres Fettmix ausmachen sollten, das heißt, natives Olivenöl extra und andere pflanzliche Öle mit hohem MUFA-Gehalt. Am Ende ist es eine Art Lotterie, und was das Mengenverhältnis von gesättigten zu mehrfach ungesättigten Fettsäuren angeht, hängt viel von individuellen Faktoren ab, etwa wie die Lipidspiegel und die gemessenen Entzündungsmarker darauf reagieren. Und wenn sie nicht gerade viel fetten Fisch essen, um ihre Vorräte mit mehrfach ungesättigten Omega-3-Fettsäuren aus dem Meer zu füllen, kommen sie um EPA- und DHA-Supplemente in Kapsel- oder Ölform fast nicht herum.
TR: Argumente für (und gegen) Fasten
Fasten oder zeitlich beschränktes Essen (das regelt, wann Sie essen), bringt uns in eine taktische Zwickmühle. Einerseits ist es ein ausgezeichnetes Mittel, um einige unserer großen und kleinen Ziele zu erreichen. Andererseits hat Fasten ein paar nicht zu unterschätzende unerwünschte Nebenwirkungen, die seinen Nutzen einschränken. Während das sogenannte Intervallfasten in seinen verschiedenen Varianten in den letzten Jahren immer populärer, um nicht zu sagen trendy geworden ist, hat bei mir die Skepsis mehr und mehr zugenommen, was seine Effektivität angeht. Häufigeres längerfristiges Fasten bringt so viele negative Nebeneffekte mit sich, dass ich es kaum mehr anwende, höchstens noch bei metabolisch schwer kranken Patienten. Über den Nutzen von gelegentlichem längerem Fasten (zum Beispiel einmal im Jahr) ist das abschließende Urteil noch nicht gesprochen. Insgesamt, so meine Erfahrung, müssen Interventionen, die auf Fasten beruhen, vorsichtig und punktgenau gehandhabt werden.
Unbestritten kommt es zu einigen positiven Effekten, wenn wir nichts essen. Der Insulinspiegel fällt, weil es keine Kalorien gibt, die eine Insulinantwort auslösen. Der Glykogenspeicher in der Leber leert sich in relativ kurzer Zeit. Nach etwa drei Tagen geht der Körper in einen »Hungerstoffwechsel« über, dann werden die Fettdepots mobilisiert, um die Energieversorgung zu sichern. Etwa zu dieser Zeit verschwindet auch das Hungergefühl, wie ich selbst oft erlebt habe, als ich regelmäßig längere Fastenperioden einlegte. Dieses paradoxe Phänomen hat wahrscheinlich mit den extrem hohen Ketonkörperspiegeln zu tun, die in diesem Zustand entstehen und die das Hungergefühl dämpfen.
Längere Fastenzeiten regeln zudem den Wachstum und Altern fördernden mTor-Stoffwechselweg herunter,[378] den wir in Kapitel 5 diskutiert haben. Das könnte wünschenswert sein, möchte man meinen, zumindest für einige Gewebe. Gleichzeitig führt der Nährstoffmangel zu einer Beschleunigung der Autophagie,[379] dem zellulären »Recyclingprozess«, der unsere Zellen widerstandsfähiger werden lässt, und zur Aktivierung von FOXO,[380] den Zellreparaturgenen, die Hundertjährigen helfen, so lange zu leben. Kurz gesagt, Fasten setzt viele der physiologischen und zellulären Mechanismen in Gang, die wir gerne sehen. Also warum empfehle ich es nicht allen meinen Patienten?
Die Frage ist heikel, weil die wissenschaftliche Literatur zum Fasten immer noch relativ dünn ist, unabhängig von der Vielzahl populärwissenschaftlicher Bücher, die zu den verschiedensten Varianten des Fastens geschrieben wurden. Ich empfehle (und praktiziere selbst) verschiedene Formen des Fastens, vom zeitlich beschränkten Essen (Essen gibt es jeden Tag nur innerhalb eines bestimmten Zeitfensters) bis zum Wasserfasten über bis zu zehn Tage. Weil ich mich selbst so intensiv mit dem Fasten beschäftigt habe, hatte ich das Gefühl, es auch hier, in diesem Zusammenhang, ansprechen zu müssen. Ich bin immer noch der Meinung, dass es manchmal bei einigen Patienten von Nutzen ist – vor allem bei Patienten mit sehr schweren Stoffwechselstörungen –, aber ich glaube nicht, dass es sich um ein Allheilmittel handelt, wie manche Leute glauben.
Genau genommen gibt es drei verschiedene Kategorien zeitlich beschränkten Essens, und wir werden sie uns der Reihe nach anschauen. Als Erstes haben wir das kurzfristig beschränkte Essen, das oben erwähnte Zeitfenster für Essen, hier beschränkt man die Nahrungsaufnahme auf einen bestimmten zeitlichen Rahmen, der sechs oder acht Stunden betragen kann. In der Praxis kann das heißen, das Frühstück wegzulassen und um 11 Uhr die erste Mahlzeit einzunehmen, die letzte Mahlzeit findet dann abends um 19 Uhr statt. Oder man frühstückt um 8 Uhr morgens, isst um 14 Uhr zu Mittag und danach nichts mehr.
Für dieses Konzept sind unzählige Varianten vorstellbar, es funktioniert aber nur dann richtig, wenn das Fenster zum Essen klein genug ist. Der Standard ist 16/8 (16 Stunden Fasten, 8 Stunden, in denen gegessen werden kann), was für die meisten Menschen nicht ausreicht, aber es kann funktionieren. In der Regel braucht man ein kleineres Fenster, zum Beispiel 18/6 oder 20/4, um ein größeres Kaloriendefizit zu erzielen. Eine Zeit lang habe ich mit einem 2-Stunden-Fenster experimentiert, was im Grunde genommen hieß, dass ich eine einzige große Mahlzeit pro Tag einnahm. Über den Gesichtsausdruck des Kellners, wenn ich mehrere Vorspeisen bestellte, habe ich mich immer amüsiert.
Nach meiner Erfahrung fällt den meisten Menschen diese Art der Kalorienreduktion am leichtesten; sie finden es einfacher, sich darauf zu konzentrieren, wann sie essen, statt darauf, wie viel oder was sie zu sich nehmen. Aber ich bin nicht überzeugt, dass die kurzzeitige beschränkte Nahrungsaufnahme darüber hinaus Vorteile bringt.
Die ursprüngliche 16/8-Version geht auf eine Studie mit Mäusen zurück. Diese Studie ergab, dass Mäuse, die nur in einem Zeitfenster von 8 Stunden fressen konnten und während der übrigen 16 Stunden des Tages »fasten« mussten, gesünder waren als Mäuse, die ständig Zugang zu Futter hatten. Die zeitbeschränkten Mäuse nahmen weniger zu als die Mäuse, die fressen konnten, wann immer sie wollten, selbst wenn beide Gruppen die gleiche Kalorienmenge verzehrten.[381] Das war die Geburtsstunde der 8-Stunden-Diät-Mode, aber irgendwie ist dabei der Umstand aus dem Blick geraten, dass es sich um eine große Extrapolation der Ergebnisse einer Mäuse-Studie handelt. Mäuse leben gerade einmal zwei oder drei Jahre – und sterben bereits nach 48 Stunden ohne Futter. Wenn eine Maus 16 Stunden nichts zu fressen erhält, entspricht das einem mehrtägigen Fasten bei Menschen.[382] Man kann das einfach nicht vergleichen.
Studien, die dieses zeitliche Essensmuster an Menschen untersuchten, konnten kaum einen Nutzen feststellen. Ethan Weiss und Kollegen führten 2020 mit 116 Freiwilligen eine klinische Studie zum 16/8-Modell durch und fanden weder Gewichtsverlust noch einen kardiovaskulären Nutzen.[383] Zwei weitere Studien stellten ebenfalls nur einen minimalen Nutzen fest.[384] Eine andere Studie ergab, dass ein Vorverlegen des Essensfensters auf die Zeit zwischen 8 Uhr und 14 Uhr – verglichen mit der Kontrollgruppe – tatsächlich zu einer Absenkung der 24-Stunden-Blutzuckerwerte, der Blutzuckerspitzen und der Insulinspiegel führte. Das heißt, ein frühes Essensfenster könnte eventuell etwas bewirken, doch meiner Meinung nach sind 16 Stunden ohne Essen einfach nicht genug, um Autophagie zu aktivieren oder zu verhindern, dass mTOR dauerhaft aktiv ist, oder um einen der anderen langfristigen Vorteile des Fastens zu bewirken, die wir gerne erzielen würden.
Ein anderer Nachteil: Sie würden auf diese Weise mit fast hundertprozentiger Sicherheit Ihr Proteinziel verfehlen (siehe oben). Das heißt, jemand, der Muskelmasse aufbauen will (weil er unterernährt oder seine Muskulatur zu schwach ausgeprägt ist), sollte die Fastenidee entweder komplett aufgeben oder außerhalb des gewählten Essensfensters noch eine reine Proteinquelle konsumieren (was den Zweck des Intervallfastens mehr oder weniger konterkariert). Außerdem kann es sehr leicht passieren, dass man während der erlaubten Essenszeit in die Appetitfalle tappt, gedankenlos vor sich hin futtert und beispielsweise eine Literpackung Eiscreme auf einen Schlag verdrückt. Mit dieser Kombination von zu wenig Protein und zu vielen Kalorien erreichen wir das genaue Gegenteil von dem, was wir wollen: Wir setzen Fett an und verlieren Muskelmasse. Aus meiner Praxis kann ich sagen, dass dieser Effekt relativ häufig eintritt.
Wie schon gesagt, empfehle ich bestimmten Patienten manchmal ein Intervallfasten, weil ich festgestellt habe, dass es ihnen hilft, ihre Gesamtkalorienzahl mit minimalem Hungern zu verringern. Aber es handelt sich eher um eine disziplinarische Maßnahme als um eine Diät. Die Nahrungsaufnahme zeitlich einzugrenzen hilft, ein Schlüsselelement der amerikanischen Standardernährung zu unterbinden, dass es nämlich so schwierig ist, nicht zu essen. Die zeitliche Beschränkung der Essenszeit ist eine Möglichkeit, das Naschen und das nächtliche Kühlschrank-Ge(h)n auszubremsen – diese Formen des gedankenlosen Essens, nur um etwas zu essen, das die Japaner als kuchisabishii (»einsamer Mund«) bezeichnen. Darüber hinaus halte ich es nicht für besonders hilfreich.
Das Nächste wäre die Variante »Einen-über-den-anderen-Tag«-Fasten (alternate-day fasting, kurz ADF), das sich ebenfalls einiger Beliebtheit erfreut. Hier isst man an einem Tag normal oder sogar etwas mehr als gewöhnlich und am nächsten sehr wenig oder gar nichts. Zu diesem Essensmuster gibt es umfangreichere Forschung mit menschlichen Studienobjekten – und natürlich wurden darüber auch schon Bücher geschrieben –, aber die Ergebnisse sind nicht besonders erfreulich. Einige Studien ergaben, dass die Teilnehmer unter abwechselnden Ess- und Fastentagen tatsächlich Gewicht verlieren können,[385] doch bei genauerem Nachforschen offenbaren sich ein paar bedeutsame Nachteile. Eine kleine, aber aufschlussreiche Studie stellte fest, dass die Teilnehmer bei dieser Form des Fastens zwar abnahmen, aber sie verloren auch mehr Muskelmasse als Studienteilnehmer, die einfach nur 25 Prozent weniger Kalorien pro Tag zu sich nahmen.[386]
Diese Studie hatte die Einschränkung einer kleinen Teilnehmerzahl und einer relativ kurzen Beobachtungszeit, doch sie legt nahe, dass Fasten bei manchen Menschen, insbesondere eher schlanken Zeitgenossen, zu einem zu hohen Verlust an Muskelmasse führen könnte.[387] Obendrein hatten die Teilnehmer der Wechselfasten-Gruppe während der Studie viel niedrigere körperliche Aktivitätslevel, woraus man schließen kann, dass sie sich an den Tagen, an denen sie nichts aßen, nicht wohl fühlten. Je länger die Fastenzeit dauerte, desto ausgeprägter wurden diese Effekte, insbesondere der Verlust von Muskelmasse. Aus diesem Grund bin ich geneigt, mich der Aussage von James Betts anzuschließen, dem verantwortlichen Leiter dieser Studie: »Wenn Sie fasten, sollten Sie daran denken, dass längere Fastenperioden es erschweren, Muskelmasse und Aktivitätslevel aufrechtzuerhalten, und beide sind bekanntermaßen von sehr großer Bedeutung für die langfristige Gesundheit.«
Aufgrund dieser und weiterer Forschungsergebnisse bin ich zu der Überzeugung gelangt, dass häufiges längeres Fasten für die meisten Patienten weder notwendig noch sinnvoll ist. Der mögliche Nutzen, welcher Art auch immer, rechtfertigt die Kosten – in Form eines Verlusts von fettfreier Masse (Muskeln) und sinkender Aktivitätsniveaus – schlicht und einfach nicht. Meine Faustregel für Essensmuster jeglicher Art lautet: Man muss genug essen, um fettfreie Masse (Muskeln) und Aktivitätsniveau langfristig aufrechtzuerhalten. Nur dann ist eine Diät nachhaltig. Wenn wir ein so mächtiges Werkzeug einsetzen wie das Fasten, müssen wir das überlegt und mit Vorsicht tun.
Nichtsdestoweniger kann Fasten manchmal bei manchen Patienten hilfreich sein, vor allem bei solchen, bei denen keine andere Ernährungsintervention etwas gebracht hat. Typisches Beispiel: mein Freund Tom Dayspring, der Lipid-Experte, den wir in Kapitel 7 kennengelernt haben. Vor einigen Jahren wurde Tom zu meinem Patienten, weil ich mir große Sorgen um seine Stoffwechselgesundheit machte. Damals war er Mitte sechzig, bei einer Körpergröße von 1,73 Meter trug er 109 Kilogramm mit sich herum, das heißt, sein BMI lag bei 36,4, also deutlich im adipösen Bereich. Seine Blutwerte zeigten an, dass er auf eine ausgeprägte nichtalkoholische Fettleber, wenn nicht sogar auf eine nichtalkoholische Fettleberhepatitis zusteuerte. Jahrelang hatte ich ihm schon in den Ohren gelegen, bis er sich endlich entschloss, etwas dagegen zu tun. Angesichts seiner Ausgangssituation kam für den Anfang eigentlich gar nichts anderes infrage als eine ketogene Diät. Wenn wir seine Kohlenhydratzufuhr beschränkten, so meine Vorstellung, würde er abnehmen, seine nichtalkoholische Fettleber hätte hoffentlich eine Chance, sich zurückzubilden, und wir würden seine Biomarker und sein Gewicht in den Griff bekommen.
Aber nichts davon geschah. Nach sechs Monaten, in denen sich Tom abmühte, die Diät einzuhalten, hatte sich weder bei seinen Leberwerten noch bei seinem Gewicht etwas getan. Dasselbe nach einem Jahr. Nach zwei Jahren, nach drei Jahren immer noch keine Veränderung. In der Zwischenzeit verschlechterte sich sein Gesundheitszustand so weit, dass er Probleme hatte, zu Fuß einmal um den Block zu gehen. Am Ende brauchte er eine neue Hüfte und musste seine Wirbelsäule versteifen lassen. Das Problem war, dass Tom es einfach nicht schaffte, die ketogene Diät für längere Zeit einzuhalten. Das ging ein oder zwei Wochen gut, aber dann knickte er ein und aß ein Sandwich oder einen Teller Pasta. Keto war für ihn einfach nicht machbar.
Tom brauchte eindeutig eine stärkere Medizin, und ich beschloss, dass er es mit Fasten probieren sollte. Leider mochte Tom – wie viele auf die amerikanische Standardernährung »geeichte« Nordamerikaner – nicht einmal an Hunger denken. Das war auch der Grund, warum er die ketogene Diät nicht lange durchhalten konnte, er hatte Hunger und großes Verlangen nach seinen gewohnten kohlenhydratreichen Lebensmitteln. Deshalb gelang es ihm nie, seinen Stoffwechsel in die Ketose zu bringen und seinen Hunger zu dämpfen. Weil sein Insulinspiegel ständig hoch war, weigerten sich seine Fettzellen, die gespeicherte Energie freizusetzen. Er war ständig hungrig und wurde sein Fett nicht los. Es war klar, dass er irgendwie aus diesem Teufelskreis ausbrechen musste.
Allein die Vorstellung zu fasten war für Tom zunächst der Horror. Aber er ist auch Wissenschaftler, und nachdem er sich näher mit der Forschung zu Nährstoffentzug beschäftigt hatte und das Gelesene mit seinem bereits vorhandenen Wissen über Lipide, Stoffwechsel und Krankheitsrisiken zusammenbrachte, war er bereit, es zu versuchen. Sein wissenschaftlicher Verstand war überzeugt, doch ich denke, irgendwann wurde ihm auch klar, dass er in absehbarer Zeit sein Testament machen konnte, wenn er nicht bald drastische Veränderungen herbeiführte. Der Plan, den wir aufstellten, war mehr als ehrgeizig, hart an der Grenze dessen, was er zu schaffen glaubte: Eine Woche pro Monat, von Montag bis Freitag, würde Tom eine Radikaldiät von etwa 700 Kalorien täglich halten; sie sollte vor allem aus Fett bestehen, dazu ein paar Proteine und so gut wie keine Kohlenhydrate.
Diese Art des Fastens nennt sich »hypokalorisch«, weil man ja nicht wie sonst fastet, ohne irgendeine Nahrung zu sich zu nehmen. Man isst gerade genug, um die übelsten Heißhungerattacken zu unterdrücken, aber nicht so viel, dass der Körper glaubt, man sei satt. Und so aß Tom an 25 Tagen im Monat »normal« (wenn auch in seinem Fall mit möglichst wenig Stärke und Zucker), und auch das nur zwischen 12 Uhr und 20 Uhr. Während seiner Fastenwoche bestand das Tagesmenü aus einem Salat mit einem leichten Dressing, einer Avocado und ein paar Macadamianüssen oder Oliven. Er war überrascht, wie gut er sich fühlte. »Es war nicht so schrecklich, wie ich befürchtet hatte«, erzählte er mir später. »Nach Tag drei verschwindet der Hunger.«
Schon nach kurzer Zeit verbesserten sich seine Blutwerte dramatisch: Waren sie vorher in der Aufstellung aus dem Labor immer rot oder gelb unterlegt – was anzeigte, dass sie grenzwertig bis schlecht waren –, waren sie jetzt fast alle im grünen Bereich. Seine Lipide sind nun in Ordnung, seine Leberwerte bewegen sich wieder im normalen, sicheren Rahmen. Nach mehreren dieser Fastenzyklen konnte Tom wieder Treppen steigen oder mehrere Blocks zu Fuß umrunden, ohne dass ihm die Puste ausging. Sein Blutdruck sank, und er konnte einige von den unzähligen Medikamenten absetzen, die er bislang eingenommen hatte. Und schlussendlich wiegt er jetzt 30 Kilogramm weniger als vorher, ein Zeichen, dass sein Stoffwechsel wirklich auf einem guten, gesunden Weg ist, und ein Anreiz für ihn dranzubleiben. »Die Pfunde sind nur so weggeschmolzen«, erzählte er mir.
Das Fasten hatte auf seinen schwer gestörten Stoffwechsel gewirkt wie die Betätigung des Resetknopfs am Computer und ihn sozusagen neu hochgefahren; das wäre mit keiner anderen Ernährungsintervention möglich gewesen. Weil sich diese Maßnahme so nachteilig auf die Muskelmasse auswirkt, wende ich sie auch nur bei Patienten wie Tom an, wenn gar nichts anderes greift. Tom war am Anfang so stark übergewichtig, dass der Verlust an Muskelmasse zu verkraften war, weil er gleichzeitig auch so viel Fett abbaute. Doch die meisten Menschen können nicht problemlos Muskelmasse verlieren, deshalb setzen wir Fasten nur in Extremfällen ein, wenn es keine anderen gangbaren Optionen gibt.
Schlussfolgerung
In den letzten beiden Kapiteln haben wir uns angesehen, wie sich das, was wir essen (und manchmal auch das, was wir nicht essen), auf unsere Gesundheit auswirkt und wie wichtig es ist, unser Denken in Richtung Ernährung 3.0 zu verändern, die auf Feedback und Daten beruht und nicht auf Etiketten, Ideologien oder Modetrends.
Auch ich habe einmal geglaubt, mit Diäten und Ernährungsweisen ließen sich fast alle Krankheiten heilen, doch heute bin ich davon nicht mehr so überzeugt. Die Biochemie der Ernährung ist ein wichtiger Bestandteil unserer Taktik, aber sie ist nicht der einzige Weg zur Langlebigkeit, ja noch nicht einmal der wirkungsvollste. Ich betrachte sie eher als eine Rettungsmaßnahme, vor allem für Patienten wie Eduardo und Tom, die mit schweren Stoffwechselproblemen wie nichtalkoholischer Fettleber und Diabetes Typ 2 zu kämpfen haben. Für ältere Menschen, die ihre Muskelmasse aufrechterhalten wollen, ist sie ebenfalls sehr wichtig. Doch ihre Fähigkeit, die Gesamtlebenszeit und die gesunde Lebenszeit zu verlängern, ist eher begrenzt. Schlechte Ernährung vermag uns mehr zu schaden, als uns gute Ernährung helfen kann. Wenn Sie bereits metabolisch gesund sind, bringen Ernährungsinterventionen nicht unbedingt viel.
Ich weiß, dass es schwerfällt, das zu glauben, nachdem wir alle konditioniert wurden, so zu denken, und angesichts des großen Tamtams, das immer veranstaltet wird, um eine neue Diät und ihre Vorzüge gegenüber einer anderen zu propagieren. Doch in Wirklichkeit laufen die Probleme erster, zweiter oder dritter Ordnung am Ende auf die Energiebilanz hinaus. Die Beschränkungen der Kalorienaufnahme, der Nahrungsmittelauswahl oder der Essenszeiten sind nichts weiter als Mittel zur Beschränkung der Energieaufnahme, Maßnahmen, um den Zustand der Überernährung oder eine schlechte Stoffwechselgesundheit zu korrigieren.
Die schlechte Nachricht ist: Die meisten Amerikaner haben keinen gesunden Stoffwechsel, sie sollten also auf ihre Ernährung achten. Wenn man dagegen etwas tun möchte, bedeutet das in den meisten Fällen, die Gesamtenergieaufnahme zu verringern (weniger Kalorien), aber auf eine Art und Weise, die für die jeweilige Person machbar und verträglich ist. Wir sollten außerdem darauf achten, die Nahrungsmitteltypen von unserem Speiseplan zu streichen, die den Blutzuckerspiegel zu stark ansteigen lassen, aber so, dass weder die Proteinaufnahme noch die fettfreie Körpermasse darunter leiden.
An dieser Stelle kann es knifflig werden. Denn Protein ist der wichtigste Makronährstoff, derjenige, den man am wenigsten beschneiden sollte. Sie erinnern sich: Die meisten Menschen sind überernährt, gleichzeitig jedoch zu schwach bemuskelt. Für sie ist es kontraproduktiv, auf Kosten von Protein und damit Muskelmasse Kalorien zu sparen.
Hier kommen dann noch andere Taktiken ins Spiel. Wie wir in Kapitel 12 gesehen haben, kann aerobes Training der Zone 2 unsere Fähigkeit zur sicheren Glucoseverwertung enorm beeinflussen, ebenso die Fähigkeit, auf Energie zurückzugreifen, die wir als Fett gespeichert haben. Und über je mehr Muskelmasse wir verfügen, desto größer ist unsere Kapazität, überschüssige Glucose zu nutzen und zu speichern sowie gespeichertes Fett nutzbar zu machen. Im nächsten Kapitel werden wir sehen, wie wichtig guter Schlaf ist, um die metabolische Balance aufrechtzuerhalten.
Wenn Ihre Probleme eher im Bereich Blutfette und dem Herz-Kreislauf-Risiko liegen, ist es sinnvoll, die Fette in die Überlegungen mit einzubeziehen – hier vor allem die gesättigten Fette, die bei manchen Menschen ApoB in die Höhe treiben, obwohl sich das auch recht gut mit Medikamenten in den Griff bekommen lässt. Übermäßiger Kohlenhydratkonsum kann sich – in Form von erhöhten Triglycerid-Werten – ebenfalls auf die ApoB-Menge auswirken. (Wenn es einen Nahrungsmitteltyp gibt, den ich am liebsten bei allen Leuten vom Speiseplan streichen würde, dann sind das mit Fructose gesüßte Getränke, inklusive Limonaden und Fruchtsäfte, die beide zu schnell zu viel Fructose an Darm und Leber liefern, während diese Fructose lieber langsam verarbeiten. Essen Sie einfach mehr Obst, und lassen Sie die Natur die richtige Menge von Wasser und Ballaststoffen bereitstellen.)
Schlussendlich ist der beste Ernährungsplan der, den wir auf Dauer beibehalten können. Es liegt bei Ihnen, wie und wie weit Sie die drei Diätansätze – Beschränkung der Kalorienaufnahme, Beschränkung der Nahrungsmittelauswahl, Beschränkung der Essenszeit – für sich nutzen. Im Idealfall verbessern oder erhalten Sie mit Ihrem Plan alle Parameter, um die wir uns kümmern wollen – nicht nur Blutzucker und Insulin, sondern auch Muskelmasse und Lipidspiegel, eventuell auch das Gewicht –, während sich die Risiken für einen oder mehrere der apokalyptischen Reiter des Alterns verringern. Ihre Ernährungsziele hängen von Ihrem individuellen Risikoprofil ab: Haben Sie ein höheres Risiko für eine Stoffwechselstörung oder eine Herz-Kreislauf-Erkrankung? Die eine Antwort, die für jeden stimmt, gibt es nicht. Jeder Patient muss seine eigene Balance finden, seine beste Herangehensweise. Ich hoffe, ich konnte Ihnen mit diesem Kapitel ein paar Werkzeuge an die Hand geben, mit denen es Ihnen gelingt, für sich selbst einen Plan zu entwickeln, der funktioniert.
Noch ein Letztes: Falls Sie sich bei der Lektüre dieses Kapitels geärgert haben sollten, weil Sie mit dem ein oder anderen Detail meiner Ausführungen nicht einverstanden waren – seien es nun die Mengenverhältnisse der verschiedenen Fettsäuren, die exakte Bioverfügbarkeit von Sojaprotein, die Rolle von aus Samen gewonnenen Ölen oder der ideale Zielwert für den Langzeit-Blutzucker – oder weil ich Sie gekränkt habe, indem ich die von Ihnen bevorzugte Diät nicht als die beste dargestellt habe, habe ich noch einen letzten Rat für Sie. Hören Sie auf, zu viel über Ernährung nachzudenken. Legen Sie das Buch in die Ecke. Gehen Sie raus und treiben Sie Sport.
Kapitel 16
Das Erwachen
Den Schlaf lieben lernen – die beste Medizin für das Gehirn
Jeden Abend, wenn ich schlafen gehe, sterbe ich. Und wenn ich am nächsten Morgen aufwache, werde ich wiedergeboren.
Mahatma Gandhi
Es hat einen guten Grund, warum die Facharztausbildung im Englischen als residency (eigentlich »Wohnsitz«) bezeichnet wird: In dieser Zeit verbringt man sein Leben im Grunde in der Klinik, Tag und Nacht. Irgendwann arbeitete ich durchschnittlich fast 120 Stunden pro Woche, oft über 30 Stunden am Stück. Das heißt, es blieben rund 48 Stunden pro Woche für Essen, Schlafen, Work-outs, Dates (meist zum ersten und letzten Mal) und alles andere. Ein Freund, der mir im Medizinstudium um ein Jahr voraus war, gab mir den weisen Rat: »Selbst wenn du in allen diesen freien Stunden schlafen würdest, wärst du trotzdem noch müde – und wenn du nur arbeitest und schläfst, fühlst du dich mies. Also hab ein bisschen was vom Leben. Aufs Schlafen kannst du verzichten.«
An einem Sommerabend während meiner Facharztausbildung bekam ich nach einem ungewöhnlich langen Arbeitspensum einen Vorgeschmack davon, welche Folgen akuter Schlafentzug haben kann. Weil einer meiner Kollegen krank war, hatte ich mich bereit erklärt, in der Nacht vor meinem eigenen Bereitschaftsdienst auch noch seinen zu übernehmen. Das bedeutete, dass ich von fünf Uhr dreißig am Montag bis achtzehn Uhr am Mittwoch arbeitete. Als ich aus der Klinik kam, stieg ich in mein Auto und machte mich Richtung Autobahn auf den Heimweg. Als ich vor einer roten Ampel wartete, ruckte mein Kopf plötzlich hoch. Shit, dachte ich, ich bin gerade am Steuer eingeschlafen. Bei der nächsten Ampel passierte es wieder. Dieses Mal rutschte mein Fuß von der Kupplung, und der Motor wurde abgewürgt.
Bis heute bin ich dem Himmel dankbar, dass ich, obwohl ich seit über 60 Stunden auf den Beinen war, noch gerade genug Verstand beisammenhatte, um mein Leben zu retten. Ich hielt am Straßenrand der Eastern Avenue und stieg aus dem Auto, um ein bisschen frische Luft zu schöpfen. Es ging ein angenehm warmer Wind, und die tief stehende Sonne schien mir wohltuend ins Gesicht. Direkt an der Straße war ein Park, und ich beschloss, meinen Pager (jawohl, meinen Pager) auf 30 Minuten zu stellen und mich ins Gras zu legen, um »kurz die Augen zu schließen«.
Sechs Stunden später wurde ich wach, mitten im Patterson Park von Baltimore, der damals ein Freiluftmarkt für Heroin und ein lebhaftes Zentrum der Prostitution war. Wir hatten schon öfter Ortsansässige bei uns in der Notaufnahme wieder zusammengeflickt. Jetzt war es mitten in der Nacht, und ich lag da auf dem Rücken, alle viere von mir gestreckt in meinem hellgrünen Arztkittel, mit einem Sabberpfützchen im Nacken. An den Unterarmen hatte ich mysteriöse Bissspuren, und um mich herum lagen ein paar Spritzen, aber sonst war alles okay. Offensichtlich hatte niemand gewagt, sich mit dem verrückten Typen anzulegen, der da in Arztklamotten auf dem Boden lag.
Ich würde gerne sagen können, dass mir dieser gruselige Vorfall eine Lehre war und ich sofort begriff, wie wichtig Schlafen ist. Doch das war nicht der Fall. Ehrlich gesagt, dauerte es fast noch ein weiteres Jahrzehnt, bis die Botschaft in mein Hirn gedrungen war – zum Teil, weil man solche Extremfälle von akutem Schlafmangel leicht als Besonderheiten der Facharztausbildung beiseiteschieben konnte. Das gehörte nun mal dazu. Es war übrigens nicht das einzige Mal, dass mir so was passierte. Einmal schlief ich auf dem Parkplatz eines Fitnessstudios bei laufendem Radio in meinem Auto ein, und Jill musste um zwei Uhr morgens anrücken und mir Starthilfe geben, nachdem wir erst ein paar Monate zusammen waren. (Ich bin ein Glückspilz.)
Zu der Zeit, als ich mein ungeplantes Nickerchen im Park hielt, gab es große Diskussionen über die Arbeitszeiten von Assistenzärzten, und ich schäme mich zuzugeben, dass ich mich vehement gegen eine Reduzierung aussprach. Der Vorschlag lautete, die maximale Stundenzahl von über 110 auf 80 zu begrenzen. Ich fand, das würde uns verweichlichen, und viele meiner älteren Kollegen stimmten dem zu.
Rückblickend ist es schockierend, dass in einem medizinischen Umfeld eine solch leichtfertige Missachtung des Schlafbedürfnisses hingenommen, ja, sogar kultiviert wurde. Fast so, als hätte man uns ermuntert, bei der Arbeit zu rauchen oder sich zu betrinken. Der Vergleich hinkt nicht einmal – mittlerweile wissen wir, dass schon eine einzige schlaflose Nacht einen Zustand hervorrufen kann, der dem mit 0,8 Promille Alkohol im Blut ähnelt.[388] Laut Studien begeht insbesondere unter Schlafentzug leidendes medizinisches Personal viel mehr Fehler und verursacht viel mehr Todesfälle als ausgeschlafenes.[389] Ich nehme mich da nicht aus: Einen meiner schlimmsten Momente als Assistenzarzt unter Schlafentzug erlebte ich während einer weiteren absurd langen Schicht (von über 48 Stunden), als ich mit der Nase voran auf die Abdecktücher eines Patienten plumpste, bei dem ich gerade eine »lap. Galle«, eine laparoskopische Gallenblasenentfernung, vornehmen wollte. Glücklicherweise fügte ich dem Patienten keinen Schaden zu, aber die Erinnerung daran treibt mir immer noch die Schamröte ins Gesicht.
Obwohl dies nicht einmal zwanzig Jahre her ist, wussten wir damals ziemlich wenig darüber, warum wir schlafen, was passiert, während wir schlafen, und wie wichtig Schlaf sowohl für unsere kurzfristige Leistungsfähigkeit als auch für unsere langfristige Gesundheit ist. Heute wissen wir, dass chronischer Schlafmangel ein noch viel tückischerer Killer ist als ein akuter Schlafentzug, der dazu führt, dass wir vor Stoppschildern einschlafen. In zahlreichen Studien hat sich gezeigt, dass zu wenig Schlaf (von durchschnittlich unter sieben Stunden pro Nacht) gesundheitsschädigende Auswirkungen hat, von einer erhöhten Anfälligkeit für Erkältungen bis zum Tod durch Herzinfarkt. Schlechter Schlaf erhöht die Neigung zu Stoffwechselstörungen drastisch,[390] bis hin zu Typ-2-Diabetes,[391] und kann verheerende Folgen für den Hormonhaushalt haben.[392] Rückblickend vermute ich, dass zumindest einige meiner gesundheitlichen Probleme, die ich in den Dreißigern hatte, dem leichtfertigen Umgang mit meinem Schlafbedürfnis zu verdanken waren.
So wichtig der Schlaf für den gesamten Körper ist – für das Gehirn ist er von ganz besonderer Bedeutung. Guter Schlaf, nicht nur in quantitativer, sondern auch qualitativer Hinsicht, ist entscheidend für unsere kognitiven Funktionen, unser Gedächtnis und sogar für unser seelisches Gleichgewicht.[393] Nach einer Nacht mit gutem Schlaf fühlen wir uns rundum besser. Selbst wenn die bewusste Wahrnehmung im Schlaf ausgeschaltet ist, arbeitet das Gehirn weiter – es produziert Gedanken, Erinnerungen und Gefühle (und infolgedessen Träume). Es führt sogar eine Selbstreinigung durch.[394] Entsprechend weist immer mehr darauf hin, dass guter Schlaf entscheidend dazu beiträgt, unsere geistigen Fähigkeiten im Alter zu bewahren und die Alzheimerkrankheit abzuwehren.[395]
Diese Schlussfolgerungen beruhen großenteils auf Beobachtungsstudien, die ich in Kapitel 14 im Hinblick auf Ernährung infrage gestellt habe. Zudem enthalten sie die gleichen Fehler – vor allem, dass sich Versuchspersonen wohl nicht sehr genau daran erinnern können, wie viel sie schlafen. (Wissen Sie genau, wie lange und wie gut Sie letzte Nacht geschlafen haben? Vermutlich nicht.) Allerdings unterscheiden sich diese Studien insofern von Ernährungsepidemiologie, als sie Daten zu nur einem Untersuchungsgegenstand berücksichtigen – dem Schlaf. Einige ihrer zentralen Ergebnisse wurden in eingehenderen klinischen Studien bestätigt, und die Daten sind einheitlicher und weisen konsistent in die gleiche Richtung.
Kurz gesagt, kann schlechter Schlaf zerstörerische Auswirkungen auf Ihre langfristige Gesundheit sowie auf Ihre Tagesform haben. Wenn man die Welleneffekte auf eine Gesellschaft bedenkt, die dem Schlaf so wenig Bedeutung beimisst, wie ich es einst getan habe, zeichnet sich ein katastrophales Bild ab.
»Die Dezimierung des Schlafes in Industrienationen hat […] katastrophale Folgen für unsere Gesundheit, unsere Lebenserwartung, unsere Sicherheit, unsere Produktivität und die Ausbildung unserer Kinder«, erläutert Matthew Walker, Direktor des Center for Human Sleep Science an der University of California in Berkeley, in seinem Buch Why We Sleep, dt. Das große Buch vom Schlaf.[396] Wie ich festgestellt habe, sind auch die Gesundheitsprobleme meiner Patienten häufig auf schlechten Schlaf zurückzuführen – und ihre Schlafstörungen zu beheben, erhöht die Wirksamkeit der Behandlung.
Zum Glück brauchte es nicht noch eine Beinahe-Katastrophe, um mir die Wichtigkeit des Schlafs vor Augen zu führen. Es war vielmehr eine gezielte Frage von meinem Freund Kirk Parsley. Kirk war ein ehemaliger Angehöriger der Navy SEALs, einer Spezialeinheit der US-Marine, der sich später als Marinearzt um SEALs kümmerte. Bei einem Abendessen im Jahr 2012 hatte ich Kirk dargelegt, dass fünf bis sechs Stunden Schlaf pro Nacht mehr als genug seien, und wenn ich nicht müde wäre, bräuchte ich auch nicht mehr Schlaf. Tatsächlich ging ich so weit zu behaupten, es sei ein Jammer, dass wir überhaupt unsere Zeit im Bett vergeuden müssten. Man stelle sich vor, wie viel mehr wir auf die Beine stellen könnten, wenn wir ganz aufs Schlafen verzichteten!
Wieder einmal präsentierte ich mich dumm wie Bohnenstroh. Aber Kirk holte mich mit einer simplen sokratischen Frage auf den Boden der Tatsachen zurück. »Wenn Schlaf so unwichtig wäre, warum hat ihn die Evolution dann nicht längst abgeschafft?«, fragte er mich.
Seine Logik war derart stichhaltig, dass ich ihr nichts entgegensetzen konnte. Wenn wir schlafen, bringen wir nichts Nützliches zustande – wir pflanzen uns nicht fort, sammeln keine Nahrung, beschützen unsere Familie nicht. Noch schlimmer ist, dass wir Beutegreifern und Feinden im Schlaf wehrlos ausgeliefert sind, so wie ich seinerzeit im Patterson Park. Gerade das zeige, so argumentierte Kirk, dass Schlaf so wichtig sei. Warum erlaube uns die Evolution, bis zu einem Drittel unseres Lebens in einem Zustand der »Unbewusstheit« zu verbringen, in dem wir mit Leichtigkeit getötet oder gefressen werden könnten? Er wurde noch deutlicher: »Glaubst du nicht, dass die natürliche Selektion die Notwendigkeit zu schlafen schon vor Hunderten Millionen Jahren abgeschafft hätte – wenn sie nicht absolut notwendig wäre?«
Das war so überzeugend, dass ich das Gefühl hatte, in meinem Gehirn sei paradoxerweise ein Weckruf ertönt. Jedes Tier schläft auf irgendeine Weise; bislang hat die Wissenschaft noch keine Gegenbeispiele entdeckt.[397] Pferde schlafen im Stehen, Delfine schlafen mit nur einer Hirnhälfte, und selbst Weiße Haie, die immer in Bewegung sind, befinden sich zuweilen in einem schlafähnlichen, erholsamen Zustand. Elefanten schlafen nur vier Stunden pro Tag, Breitflügelfledermäuse dagegen neunzehn Stunden, was mir ein bisschen viel vorkommt. Der Punkt ist jedoch, dass keines von den Tieren, die bisher sorgfältig untersucht wurden, ohne Schlaf auskommt. Kirk hatte recht: Aus evolutionärer Sicht ist Schlaf nicht verhandelbar.
Ich war nicht der Einzige, der die Bedeutung des Schlafs ignorierte oder missachtete. Die Wissenschaft wie auch die westlichen Industriegesellschaften hatten ihn lange mit Verachtung gestraft. Vor einigen Jahrzehnten galt Schlaf lediglich als ein nichtssagender Zustand, eine Periode des ausgeschalteten Bewusstseins, in der nichts Relevantes passierte. Heutzutage scheint unsere Hochleistungskultur Schlafen immer noch als Zeitverschwendung zu betrachten, als etwas, was nur Babys, Hunde und Faulpelze nötig haben. In den letzten dreißig Jahren hat die Schlafforschung jedoch an Fahrt gewonnen, und neuere Erkenntnisse legen nahe, dass diese Einstellung grundfalsch ist. Wir wissen jetzt, dass Schlaf für unsere Gesundheit genauso unverzichtbar ist wie Stabilität für Kraft.
Da ich dem Schlafen in meinem Leben mittlerweile einen hohen Stellenwert einräume, genieße ich jeden Tag die Vorteile, die das mit sich bringt. Wenn ich nach einem richtig guten Schlaf aufwache, bin ich voller Power. Mein Gehirn sprudelt über von neuen Ideen, mein Work-out mache ich gefühlt mit links, und im Umgang mit anderen bin ich ein ganz anderer, besserer Mensch. Aber wann haben Sie sich zum letzten Mal beim Aufwachen so gefühlt? Heute Morgen? Letzte Woche? Vor einem Monat? Sie können sich nicht erinnern?
Sollten Sie sich jetzt angesprochen fühlen, ist es an der Zeit, Ihre Schlafmuster und Schlafqualität auf den Prüfstand zu stellen und etwas zu unternehmen, um sie zu verbessern – genauso, wie Sie sich um Ihre Lipoproteine, Ihre Stoffwechselgesundheit oder Ihre körperliche Fitness kümmern sollten. Es ist wirklich wichtig!
Wie lange sollten wir schlafen? Das ist eine schwierige Frage, weil unser Schlafzyklus starken äußeren Einflüssen unterliegt, wie Sonnenlicht, Lärm und künstlichem Licht, von unserer eigenen seelischen Verfassung und Stress ganz zu schweigen. Außerdem gelingt es uns recht gut, uns zumindest für eine Weile an nicht ausreichenden Schlaf anzupassen. Zahllose Studien haben jedoch bekräftigt, was Ihnen schon Ihre Mutter gesagt hat: Wir brauchen etwa siebeneinhalb bis achteinhalb Stunden Schlaf pro Nacht. Untersuchungen in dunklen Höhlen lassen sogar vermuten, dass unser 8-Stunden-Schlaf-Rhythmus mehr oder weniger vorprogrammiert ist, was darauf hindeutet, dass er nicht mit sich reden lässt.[398] Signifikant weniger oder mehr zu schlafen, schafft auf längere Sicht nahezu unausweichlich Probleme.
Schon eine einzige Nacht mit schlechtem Schlaf wirkt sich erwiesenermaßen schädlich auf unsere körperliche und geistige Leistungsfähigkeit aus.[399] Sportler, die in der Nacht vor einem Rennen oder Spiel schlecht schlafen, zeigen deutlich schwächere Leistungen als in ausgeruhtem Zustand. Die Ausdauer lässt nach, ebenso VO2max (die maximale Sauerstoffaufnahme) und das One-Rep-Max (das maximale Gewicht, das man für eine einzelne Wiederholung bei einer bestimmten Übung heben oder drücken kann). Selbst unsere Fähigkeit zu schwitzen wird beeinträchtigt.[400] Außerdem steigt die Verletzungsgefahr: Laut einer Beobachtungsstudie von 2014 war bei jungen Sportlern, die pro Nacht weniger als sechs Stunden schliefen, die Wahrscheinlichkeit, sich zu verletzen, zweieinhalbmal höher als bei gleichaltrigen Sportlern, die acht Stunden oder länger schliefen.[401]
Guter Schlaf wirkt wie ein leistungsförderndes Mittel. In einer Studie wurden Basketballspieler ermuntert, pro Nacht möglichst zehn Stunden – mit oder ohne zusätzliche Nickerchen – zu schlafen und weder Alkohol noch Koffein zu sich zu nehmen.[402] Fünf Wochen später hatte sich ihre Treffsicherheit um 9 Prozent gesteigert, und sie sprinteten schneller.[403] Für LeBron James ist Schlafen ein zentraler Bestandteil seiner Regenerationsroutine.[404] Er versucht immer, jede Nacht neun, manchmal auch zehn Stunden zu schlafen und am Tag zusätzlich ein Nickerchen zu machen. »Wenn du gut geschlafen hast, fühlst du dich nach dem Aufwachen einfach erfrischt«, sagt er. »Du brauchst keinen Wecker. Du hast einfach das Gefühl: Okay, an diesem Tag kann ich mein Bestes geben.«
Für diejenigen von uns, die keine Profisportler sind, ist Schlaf nichtsdestoweniger von entscheidender Bedeutung, um alltäglichere – und auch gefährlichere – Aufgaben wie Autofahren zu meistern. Bei einer Studie wurden in einer Gruppe von Berufskraftfahrern nach einer Nacht mit Schlafmangel deutlich schlechtere Reaktionszeiten in Situationen registriert, in denen man beispielsweise bremsen musste, um einen Unfall zu verhindern.[405] Weil leider kein Pendant zu einem Alkoholmessgerät existiert, das misst, ob man zu müde zum Fahren ist, gibt es keine genauen Statistiken. Bei einer Umfrage der American Automobile Association gab jedoch fast einer von drei Fahrern (32 Prozent) zu Protokoll, in den letzten 30 Tagen auch mal am Steuer gesessen zu haben, obwohl er so müde gewesen sei, dass er kaum die Augen offenhalten konnte.[406]
Trotzdem sind wir uns oft gar nicht bewusst, welch schädliche Folgen schlechter Schlaf für unseren Energiepegel und unser Leistungsvermögen hat. Forscher haben herausgefunden, dass Personen mit Schlafmangel diese Folgen fast immer unterschätzen, weil sie sich daran anpassen.[407] Wie jeder weiß, der schon mal einen Säugling zu versorgen hatte, empfinden wir den sich dann einstellenden Dauerzustand von leichter Erschöpfung und geistigem Nebel irgendwann als normal. Das nennt man baseline resetting, zu übersetzen etwa als »Neujustierung des Normalzustands«. Bei mir war es so, das weiß ich. Als Assistenzarzt und später als Facharzt ging ich davon aus, genug zu schlafen, weil ich keine Vergleichsmöglichkeiten hatte. Nun, da ich besser schlafe, bin ich erstaunt, dass ich so lange in jenem Zustand überlebt habe. Das ist wie beim Fernsehen. Wenn man immer nur einen normalen Fernseher hatte, findet man das okay. Aber sobald man einmal einen 4K-Bildschirm gesehen hat, wird einem klar, dass das Bild auf dem alten Röhrenmonitor alles andere als gestochen scharf war. Genauso drastisch ist der Unterschied beim Schlafen.
Das Blut eines alten Mannes
Auch wenn die kurzfristigen Folgen von einer oder drei Nächten mit schlechtem Schlaf in gewissen Situationen beängstigend sein können, ist das nichts gegen den Schaden, den wir uns selber zufügen, wenn diese Situation andauert. Das beobachtete Kirk Parsley, als er Arzt bei den SEALs war. Nach außen hin schienen die Männer dank dem Schliff ihrer rigorosen Ausbildung in allerbester Verfassung zu sein. Doch als Parsley sich ihre Blutbilder ansah, war er schockiert: Viele dieser jungen Kerle hatten Hormonspiegel und Entzündungsmarker wie Männer, die Jahrzehnte älter waren als sie. »Das Blut eines alten Mannes«, sagte Parsley. Weil ihre Trainingseinheiten und Missionen häufig mitten in der Nacht begannen und sie 24 Stunden am Stück oder noch länger auf den Beinen waren, litten sie unter chronischem Schlafmangel, und ihr natürlicher Schlaf-wach-Rhythmus war völlig aus den Fugen geraten.
Als Kirk mir davon erzählte, hatte ich ein Déjà-vu-Gefühl – auch ich hatte in meiner Phase als vollschlanker Peter das »Blut eines alten Mannes« gehabt, mit erhöhtem Insulinspiegel, hohen Triglyceridwerten und einem Testosteronspiegel, der für die Männer in den Vereinigten Staaten den niedrigsten 5 Prozent entsprach. Bis dahin hatte ich meine schlechte Gesundheit und das hormonelle Ungleichgewicht meiner miserablen Ernährung zugeschrieben – und nur ihr. Allerdings hatte ich während der Facharztausbildung und danach mindestens ein Jahrzehnt in einem Zustand gravierenden Schlafmangels verbracht. Im Nachhinein erkannte ich, dass der Schlafentzug ebenfalls seinen Tribut gefordert hatte. Vermutlich sah man mir das sogar am Gesicht an: Laut Studien haben Menschen, die chronisch zu wenig schlafen, häufig eine älter wirkende, schlaffere Haut als Altersgenossen, die mehr Schlaf bekommen.[408]
Heute ist mir klar, dass zwischen Schlaf, Ernährung und dem Risiko langfristiger Erkrankungen ein enger Zusammenhang besteht. Nach dem, was ich jetzt weiß, würde ich wetten, dass ein paar Monate mit perfektem Schlaf 80 Prozent meiner damaligen Probleme hätten beheben können – miese Ernährung hin oder her.
Vielleicht überrascht es Sie genauso, wie es mich überrascht hat, aber schlechter Schlaf wirkt sich verheerend auf unseren Stoffwechsel aus. Selbst kurzfristig kann Schlafmangel eine schwere Insulinresistenz hervorrufen. Die Schlafforscherin Eve Van Cauter von der University of Chicago ließ gesunde junge Menschen nachts nur noch viereinhalb Stunden schlafen und stellte fest, dass sie nach vier Tagen den erhöhten Insulinspiegel fettleibiger Diabetiker mittleren Alters aufwiesen und, noch schlimmer, eine um etwa 50 Prozent verminderte Kapazität zum Glucoseabbau.[409] Das scheint eines der durchgängigsten Ergebnisse der Schlafforschung zu sein. Nicht weniger als neun unterschiedliche Studien haben erbracht, dass Schlafmangel die Insulinresistenz um bis zu einem Drittel erhöht.[410] Solche übereinstimmenden experimentellen Belege kommen in der Medizin sehr selten vor, und darum sollte man sie beachten. Es scheint auf der Hand zu liegen, dass schlechter oder zu wenig Schlaf Stoffwechselstörungen hervorrufen kann.
Leider fehlen momentan noch entsprechende Langzeitstudien, doch Beobachtungsstudien sprechen für einen deutlichen Zusammenhang zwischen zu kurzem Schlaf und langfristigen Stoffwechselproblemen. Mehrere große Metaanalysen von Schlafuntersuchungen haben eine enge Relation zwischen Schlafdauer und dem Risiko von Typ-2-Diabetes sowie dem metabolischen Syndrom offenbart.[411] Doch auch umgekehrt gilt: Zu viel Schlaf ist ebenfalls problematisch. Bei Menschen, die pro Nacht elf Stunden oder länger schlafen, ist die Gesamtmortalität um 50 Prozent erhöht. Das kann damit zusammenhängen, dass langes Schlafen qualitativ minderwertiges Schlafen ist, kann aber auch von einer zugrunde liegenden Krankheit herrühren. Ähnliche Zusammenhänge bestehen offenbar zwischen schlechtem oder zu wenig Schlaf und Bluthochdruck (17 Prozent), Herz-Kreislauf-Erkrankungen (16 Prozent), koronaren Herzerkrankungen (26 Prozent) und Fettleibigkeit (38 Prozent).[412] Insgesamt legen diese Ergebnisse nahe, dass die langfristigen Folgen von schlechtem Schlaf dem entsprechen, was die Kurzzeitstudien erwarten lassen: erhöhte Insulinresistenz und weitere Krankheiten, die damit einhergehen, von NASH über Typ-2-Diabetes bis zu Herz-Kreislauf-Erkrankungen. Wenn unser Schlaf chronisch gestört wird, kann das für unseren Stoffwechsel ebenfalls gelten.
Die Verbindung zwischen Schlaf und Stoffwechselgesundheit ist zunächst vielleicht verblüffend, aber ich denke, das fehlende Bindeglied könnte Stress sein. Höhere Stresslevel können bewirken, dass wir schlecht schlafen, wie wir alle wissen, aber schlechter Schlaf bewirkt auch, dass wir uns noch gestresster fühlen. Es ist ein Teufelskreis. Schlechter Schlaf wie auch starker Stress aktivieren das sympathische Nervensystem, das – trotz seines Namens – alles andere als einen beruhigenden Einfluss hat. Es ist eine Komponente unserer Kampf-oder-Flucht-Reaktion und triggert die Ausschüttung von Hormonen namens Glucocorticoiden, einschließlich des Stresshormons Cortison. Cortison erhöht den Blutdruck; es kann auch bewirken, dass die Leber Glucose ausschüttet, während es zugleich die Aufnahme und Nutzung von Glucose im Muskel- und Fettgewebe hemmt.[413] Das hat womöglich den Sinn, in erster Linie das Gehirn mit Glucose zu versorgen. Im Körper manifestiert sich dies in einem erhöhten Blutzuckerspiegel aufgrund stressbedingter Insulinresistenz. Das beobachte ich häufig – bei mir selbst und bei einigen meiner Patienten: Wenn eine kontinuierliche Glucosemessung (CGM) ergibt, dass der Blutzuckerspiegel nachts erhöht ist, deutet dies fast immer auf einen übermäßig hohen Cortisonspiegel hin, was manchmal dadurch verschärft wird, dass wir spät am Abend noch essen und trinken. Langfristig kann dieser erhöhte Blutzuckerspiegel in Typ-2-Diabetes münden.
Das Problem wird noch dadurch verschlimmert, dass schlechter Schlaf auch unser Essverhalten beeinflusst. Eve Van Cauters Team hat herausgefunden, dass bei Versuchspersonen, deren Nachtschlaf auf vier bis fünf Stunden begrenzt wurde, der Leptinspiegel sank.[414] Leptin ist das Hormon, das uns signalisiert, wann wir genug gegessen haben. Zugleich stieg der Spiegel des »Hungerhormons« Ghrelin. Wenn wir schlecht schlafen, kann das bewirken, dass wir am nächsten Tag eigentlich ohne Grund furchtbar hungrig sind und eher mal nach kalorienreichen und zuckerhaltigen Lebensmitteln als nach gesunden greifen. Laut Studien nehmen Menschen mit Schlafmangel häufiger abends noch eine vierte Mahlzeit zu sich. Folgestudien von Van Cauters Team haben erbracht, dass Probanden mit wenig Schlaf am darauffolgenden Tag etwa 300 Kalorien mehr zu sich nahmen als ausgeschlafene.[415] Insgesamt ergibt dies die besten Voraussetzungen, um NAFLD und eine Insulinresistenz zu entwickeln.
Schlaf und Herz-Kreislauf-Erkrankungen
Das sympathische Nervensystem kann uns verraten, warum schlechter Schlaf so eng mit Herz-Kreislauf-Erkrankungen und Herzinfarkt in Verbindung gebracht wird. Werden wir bedroht, übernimmt es das Kommando und mobilisiert Stresshormone wie Cortison und Adrenalin, die Puls und Blutdruck ansteigen lassen. Unglücklicherweise hat schlechter Schlaf im Grunde die gleichen Auswirkungen, weil er das sympathische Nervensystem in einen permanenten Alarmzustand versetzt. Wir stecken im Kampf-oder-Flucht-Modus fest, und Blutdruck und Puls bleiben erhöht. Das wiederum verstärkt die Belastung für das Gefäßsystem. Ich habe das an mir selbst beobachtet, weil ich ein Faible für Selftracking-Geräte habe: In einer Nacht, in der ich nicht gut schlafe, ist mein Ruhepuls höher (schlecht) und meine Herzfrequenzvariabilität niedriger (ebenfalls schlecht).
Das erklärt vielleicht, warum ein über lange Zeiträume unzureichender Schlaf mit einem erhöhten Risiko von kardiovaskulären Ereignissen einhergeht. Das lässt sich nicht eindeutig mit Untersuchungen, etwa mit einer randomisierten kontrollierten Studie, belegen. Gemäß zwei großen Metaanalysen geht verkürzter Schlaf (laut Definition weniger als sechs Stunden pro Nacht) mit einem um 6 bis 26 Prozent erhöhten Auftreten von Herz-Kreislauf-Erkrankungen einher.[416] Das sagt jedoch nichts über Ursache und Wirkung aus. Bestimmt tragen einige Gründe für schlechten Schlaf, wie übermäßiges Arbeitspensum, geringes Einkommen oder Stress, auch zu einem höheren Risiko solcher Krankheiten bei. Eine besonders interessante Studie verglich jedoch Beobachtungsdaten mit Daten aus Mendelscher Randomisierung bei Personen mit zuvor festgestellten Genvarianten, welche ihre Veranlagung zu einer längeren oder kürzeren Schlafdauer verstärken oder verringern.[417] Die MR-Daten bestätigten die Beobachtungsergebnisse, dass eine Schlafdauer von unter sechs Stunden pro Nacht mit einer Erhöhung des Herzinfarktrisikos um etwa 20 Prozent einherging.[418] Noch bemerkenswerter ist das Ergebnis der Studie, dass eine nächtliche Schlafdauer von sechs bis neun Stunden (was die Forscher als adäquat definierten) das Herzinfarktrisiko senkte – selbst bei Personen, die eine hohe genetische Prädisposition für Erkrankungen der Herzkranzgefäße aufwiesen.
Kurz gesagt: Guter Schlaf kann helfen, das genetische Risiko von Herz-Kreislauf-Erkrankungen, mit dem Leute wie ich leben, zu verringern. All die oben genannten Erkenntnisse haben mich davon überzeugt, dem Schlaf in meinem Leben eine hohe Priorität einzuräumen und ein Auge auf die Schlafgewohnheiten meiner Patienten zu haben.
Schlaf und das Gehirn
Dass der Schlaf für die metabolische und kardiovaskuläre Gesundheit von entscheidender Bedeutung ist, haben wir nun erfahren. Bemerkenswert ist, dass die Beziehung zwischen Schlaf und Gehirn hierbei ebenfalls eine große Rolle spielt. Schlaf ist, besonders im fortgeschrittenen Alter, für die Hirngesundheit zentral – nicht nur, was gelegentliche geistige »Aussetzer« betrifft, sondern auch langfristig.
Wir haben uns alle nach einer ruhelosen Nacht schon mal schlapp und schwerfällig gefühlt – dann ist unser Gehirn schlicht nicht in gleichem Maß auf Zack wie gewöhnlich. Wenn wir die Nacht danach durchschlafen oder auch nur ein ausgiebiges Nickerchen machen, geht es uns meist wieder besser. Schlafforscher zeigen jedoch unzählige Gründe auf, warum guter Schlaf von zentraler Bedeutung für die langfristige Hirngesundheit ist – und inwiefern schlechter Schlaf beträchtlichen Schaden anrichtet. Lange ging man davon aus, dass schlechter Schlaf eines der ersten Symptome einer beginnenden Alzheimerkrankheit ist. Nachfolgende Untersuchungen lieferten aber Hinweise darauf, dass chronisch schlechter Schlaf eine gravierende mögliche Ursache für Alzheimer und Demenz ist.[419] Wie sich herausgestellt hat, ist der Schlaf ebenso entscheidend für die Erhaltung der Hirngesundheit wie für die Hirnfunktionen.
Wenn wir ins Bett gehen und die Augen schließen, wird eine Reihe physiologischer Veränderungen in Gang gesetzt. Während wir in den Schlaf sinken, verlangsamt sich der Puls, die Kerntemperatur sinkt, und der Atem wird regelmäßig. Und unser Gehirn macht sich auf seine eigene spezielle Reise.
Wie die Forschung mittlerweile weiß, durchlaufen wir im Schlaf mehrere fest umrissene Stadien, die jeweils eine ganz bestimmte Funktion und eine spezifische Gehirnwellen-»Signatur« aufweisen, an der man die verschiedenen Schlafstadien ursprünglich identifiziert hat.[420] Zur Veranschaulichung dieser Stadien stellen wir uns nun Folgendes vor: Wenn wir uns zum Schlafen ins Bett legen, erwartet uns eine Tiefsee-Expedition in einem Unterseeboot. Während sich der Körper entspannt, schlafen wir hoffentlich in wenigen Minuten ein – unser U-Boot sinkt unter die Meeresoberfläche und entführt uns in die Tiefe.
Zunächst geht alles recht schnell. Der Weg nach unten führt uns durch ein Stadium mit leichtem Schlaf, bevor wir im Tiefschlaf versinken. Dies ist das sogenannte Non-REM- oder NREM-Stadium, das wiederum in Stadien mit leichterem NREM-Schlaf und tiefem NREM-Schlaf unterteilt ist. Letzterer ist, insbesondere für unsere neurologische Gesundheit, von größerer Bedeutung. In unserer Unterwasser-Metapher ist dies das Stadium, in dem wir in die lichtlosen Tiefen des Meeres hinabgleiten, wo unser Gehirn für äußere Reize unempfänglich ist. Das heißt aber keineswegs, dass weiter nichts passiert. Beim Übergang in den Tiefschlaf verlangsamen sich die Gehirnwellen, bis sie eine extrem niedrige Frequenz erreichen, einen rhythmischen Sprechgesang von einer bis vier Zyklen pro Sekunde. Dieser Tiefschlaf dominiert die erste Nachthälfte, obwohl wir typischerweise zwischen tiefem und leichterem NREM-Schlaf hin und her wechseln.
Im späteren Verlauf der Nacht steigt unser Unterseeboot im Normalfall wieder weiter nach oben in eine REM-Schlaf-Zone (von Rapid Eye Movement). In diesem Stadium bewegen sich die Augäpfel schnell unter den geschlossenen Lidern. Wir »sehen« etwas, aber nur innerlich. In diesem Stadium treten die meisten Träume auf – unser Gehirn produziert Bilder und Vorgänge, die vertraut erscheinen, aber doch ungewöhnlich oder losgelöst von ihrem üblichen Kontext sind. Interessanterweise ähnelt die Gehirnwellen-Signatur des REM-Schlafs den Gehirnwellen im wachen Zustand; der wichtigste Unterschied besteht darin, dass unser Körper gelähmt ist, was uns vermutlich daran hindern soll, unsere bizarren Traumerlebnisse auszuagieren. Es wäre nicht so gut, wenn wir im REM-Schlaf einfach so aufstehen und herumrennen könnten. (Das erklärt vermutlich auch Träume, in denen wir versuchen, vor etwas davonzulaufen, und unser Körper nicht funktionieren will.)
Normalerweise treten die genannten Schlafstadien in Zyklen auf, die jeweils etwa neunzig Minuten andauern. Es kann sogar vorkommen, dass wir zwischen ihnen kurz aufwachen. Das hat die Evolution wahrscheinlich so eingerichtet, damit wir nachts nicht von einem Löwen verspeist oder von Feinden überrascht werden, wie der in Stanford ausgebildete Schlafmediziner Dr. Vikas Jain erklärt, der die Schlafprobleme meiner Patienten behandelt.
Sowohl REM- als auch NREM-Schlaf (den ich hier der Einfachheit halber als »Tiefschlaf« bezeichne) sind zentral für Lernen und Gedächtnis, jedoch auf verschiedene Weisen. Im Tiefschlaf leert das Gehirn seinen Speicher für Kurzzeiterinnerungen im Hippocampus und wählt die wichtigen für die Langzeitspeicherung in der Hirnrinde aus, wo sie sich verfestigen oder »konsolidieren«.[421] Wissenschaftler haben eine direkte Beziehung zwischen der Länge des Tiefschlafs und der Gedächtnisleistung am folgenden Tag festgestellt.[422]
Wenn wir jung sind, unterstützt der REM-Schlaf Wachstum und Entwicklung des Gehirns.[423] Selbst im Schlaf bildet es neue Verbindungen und erweitert die neuronalen Netze. Aus diesem Grund sind die REM-Stadien bei jungen Menschen länger. Das relativiert sich im Erwachsenenalter, aber vor allem für Kreativität und das Lösen von Problemen bleibt der REM-Schlaf relevant. Indem das Gehirn scheinbar zufällige Assoziationen zwischen Fakten und Erinnerungen herstellt und vielversprechende Verbindungen von bedeutungsloseren trennt, kann es häufig mit Lösungen für Probleme aufwarten, die uns am Tag zuvor noch Kopfzerbrechen bereitet haben. Zudem haben Forschungen erbracht, dass REM-Schlaf besondere Bedeutung für das sogenannte prozedurale Gedächtnis hat, das für das Erlernen neuer Bewegungsabläufe, etwa beim Sport oder Musizieren, zuständig ist.[424]
Eine weitere ausgesprochen wichtige Funktion des REM-Schlafs betrifft die Verarbeitung unserer emotionalen Erinnerungen, indem er dazu beiträgt, unsere Gefühle von der Erinnerung an das negative (oder positive) Erlebnis, das diese Gefühle ausgelöst hat, zu trennen.[425] So erklärt sich, dass Dinge, die uns beim Zubettgehen stark belasten, am nächsten Morgen fast immer ihren größten Schrecken verloren haben. Wir erinnern uns noch an das Ereignis, aber vergessen (letztlich) die negativen Gefühle, die es begleitet haben. Ohne diese Pause, die der emotionalen Heilung dient, würden wir in einem permanenten Zustand der Angst leben, denn jede Erinnerung an das Erlebte würde erneut eine Welle jener Gefühle auslösen. Wenn sich das nach einer posttraumatischen Belastungsstörung anhört, haben Sie nicht ganz unrecht – laut Studien mit Kriegsveteranen sind diese weniger gut in der Lage, Erinnerungen von Gefühlen zu trennen, eben weil sie zu oft ohne REM-Schlaf auskommen mussten.[426] Es zeigte sich, dass die Veteranen große Mengen an Noradrenalin ausschütteten, das Kampf-oder-Flucht-Hormon, das sie wirksam vor dem REM-Schlaf und damit vor Entspannung bewahrte.[427], [428]
Am faszinierendsten ist vielleicht, dass der REM-Schlaf wichtig für die Erhaltung unserer emotionalen Intelligenz ist.[429] Wenn wir an zu wenig REM-Schlaf leiden, fällt es uns laut Untersuchungen schwerer, den Gesichtsausdruck anderer Menschen richtig zu deuten. Versuchspersonen mit REM-Schlafmangel interpretierten selbst freundliche oder neutrale Gesichtsausdrücke als bedrohlich. Das ist keineswegs trivial – unsere Fähigkeit, als soziale Tiere zu funktionieren,[430] hängt von unserer Fähigkeit ab, die Gefühle anderer Menschen zu verstehen und adäquat damit umzugehen.[431] Der REM-Schlaf scheint, kurz gesagt, unser emotionales Gleichgewicht zu schützen, während er bei der Verarbeitung von Erinnerungen und Informationen hilft.
Tiefschlaf wiederum scheint für die Gesundheit unseres Gehirns als Organ an sich von zentraler Bedeutung zu sein. Vor einigen Jahren entdeckten Forscher in Rochester, dass das Gehirn im Schlaf eine Art inneres Abfallentsorgungssystem aktiviert, bei dem Rückenmarksflüssigkeit zwischen die Neuronen geleitet wird, um interzellulären Müll wegzuschwemmen[432]. Die Reinigungsaktion beseitigt Abfälle wie Beta-Amyloid und Tau, die beiden mit Neurodegeneration in Verbindung gebrachten Proteine.[433] Verbringen wir jedoch zu wenig Zeit im Tiefschlaf, kann das System seine Wirksamkeit nicht voll entfalten, und zwischen den Nervenzellen können sich Beta-Amyloid und Tau-Proteine ansammeln. Breiter angelegte Studien haben gezeigt, dass das Gehirn von Menschen, die jahrzehntelang meist weniger als sieben Stunden pro Nacht geschlafen haben, gemeinhin viel größere Beta-Amyloid- und Tau-Ablagerungen aufweist als das von Personen, die sieben Stunden oder mehr schlafen.[434] Tau, das Protein, das in befallenen Neuronen »Faserbündel« bildet, korreliert mit Schlafstörungen bei geistig normalen Personen sowie bei denjenigen mit MCI, einem frühen Stadium der Demenz.
Daraus kann ein Teufelskreis entstehen.[435] Alzheimer-Patienten leiden oft an Schlafstörungen; bei ihnen werden die Tiefschlaf- und REM-Schlafphasen immer kürzer, und auch der zirkadiane Rhythmus, ihr Schlaf-wach-Zyklus, kann sich drastisch verändern. Zudem entwickeln bis zur Hälfte der Menschen mit Alzheimer eine Schlafapnoe.[436]
Allerdings können Schlafstörungen ihrerseits auch Bedingungen schaffen, die ein Fortschreiten der Alzheimerkrankheit begünstigen. Von Schlaflosigkeit sind 30 bis 50 Prozent der älteren Erwachsenen betroffen, und viele Forschungsergebnisse belegen, dass Schlafstörungen einer Demenzdiagnose häufig um mehrere Jahre vorausgehen.[437] Sie können sogar auftreten, bevor es Anzeichen von geistigem Verfall gibt. Eine Studie erkannte einen Zusammenhang zwischen schlechtem Schlaf bei geistig normalen Personen und dem Einsetzen kognitiver Beeinträchtigungen nur ein Jahr später.[438]
Zugleich wird eine gute Schlafqualität bei älteren Erwachsenen mit einem niedrigeren Risiko für MCI und Alzheimer sowie mit der Bewahrung der kognitiven Funktionen auf einem höheren Niveau in Verbindung gebracht.[439] Die erfolgreiche Behandlung von Schlafstörungen kann das erstmalige Auftreten von MCI hinauszögern – laut einer Studie um rund elf Jahre – und die kognitiven Funktionen von Patienten verbessern, bei denen bereits eine Alzheimer-Erkrankung diagnostiziert wurde.[440]
Schlaf und geistige Gesundheit sind eindeutig eng miteinander verbunden. Darum ist eine Säule der Alzheimer-Prävention, insbesondere für Hochrisikopatienten, die Verbesserung ihres Schlafs. Es reicht nicht aus, einfach mehr Zeit im Bett zu verbringen – qualitativ hochwertiger Schlaf ist für die langfristige Hirngesundheit entscheidend. Diese Differenzierung ist sehr wichtig. Schlaf, der oft unterbrochen wird oder nicht tief genug ist, kann dem Gehirn die genannten Vorzüge nicht liefern.
Leider nimmt unsere Fähigkeit zum Tiefschlaf mit zunehmendem Alter, bereits mit Ende zwanzig oder Anfang dreißig, ab. Diese Tendenz verschärft sich im mittleren Alter aber noch. Es ist nicht ganz klar, in welchem Maß dieser Rückgang der Schlafqualität auf das Älterwerden an sich zurückzuführen ist, oder ob er sich dadurch erklärt, dass mit zunehmendem Alter die Wahrscheinlichkeit für einen Gesundheitszustand zunimmt, der zu schlechtem Schlaf führt. Laut einer Analyse erfolgen die allermeisten Veränderungen im Schlafmuster von Erwachsenen im Alter von neunzehn bis sechzig, und danach tut sich kaum noch etwas, falls man gesund bleibt. (FALLS!)
Dass die Tiefschlafstadien im Alter kürzer werden, liegt möglicherweise auch daran, dass sich die Ausschüttung des Wachstumshormons (Somatropin) verändert. Die pulsatile Sekretion des Hormons erfolgt typischerweise etwa eine Stunde nachdem wir eingeschlafen sind, ungefähr dann, wenn das Stadium des Tiefschlafs beginnt. Wird die Ausschüttung des Wachstumshormons gehemmt, beeinträchtigt dies auch den Tiefschlaf. Was hier Ursache und was Wirkung ist, ist noch unklar. Das Maximum der Sekretion wird im jugendlichen Alter erreicht; vom jungen Erwachsenenalter an bis zum mittleren Alter nimmt sie rasch ab, danach langsamer. Dieses Muster verläuft parallel zu den Veränderungen, die im Lauf der Jahre beim Tiefschlaf zu beobachten sind.
Weitere Untersuchungen haben darauf hingewiesen, dass der Tiefschlaf in den Lebensjahrzehnten zwischen dem vierzigsten und siebzigsten Geburtstag besonders wichtig ist, um der Alzheimerkrankheit vorzubeugen.[441] Es sieht so aus, als seien Personen, die in dieser Zeit weniger schlafen, später stärker gefährdet, an Demenz zu erkranken. Demnach scheint guter Schlaf in mittleren Jahren von besonderer Bedeutung für die Bewahrung der geistigen Gesundheit zu sein.
Wie mir heute klar ist, bin ich in all den Jahren, in denen ich pro Nacht nur fünf oder sechs Stunden geschlafen und geglaubt habe, in Bestform zu sein, in Wirklichkeit dank dem chronischen Schlafmangel weit unter meinen Möglichkeiten geblieben. Zugleich habe ich vermutlich mein Risiko erhöht, eine langfristige Erkrankung des Stoffwechsels, des Herz-Kreislauf-Systems oder meiner kognitiven Funktionen zu erleiden. Mein großspuriges Mantra lautete: »Ich schlafe, wenn ich tot bin.«
Ich hatte keine Ahnung, dass ich mit dem Verzicht auf Schlaf einiges dafür getan habe, diesen Tag früher zu erleben.
Wie können wir unseren Schlaf bewerten?
Es wäre schön, wenn die Forschung so etwas wie einen »Schlafschalter« im Gehirn aufspüren würde, der sich so erregen oder hemmen ließe, dass man auf Wunsch umgehend einschlafen und mühelos den Zyklus von Tiefschlaf und REM-Schlaf durchwandern könnte, bis man erfrischt aufwacht. Das ist aber bislang noch nicht geschehen.
Was nicht heißt, dass die Pharmariesen es noch nicht versucht hätten. So viele Menschen haben Schlafprobleme, dass mittlerweile etwa ein Dutzend von der FDA zugelassene schlaffördernde Mittel auf dem Markt sind. Der erste sehr erfolgreiche Wirkstoff dieser Art war Zolpidem, der nach der Zulassung in den 1990er-Jahren in den USA innerhalb von zwei Jahren Einnahmen in Höhe von 4 Milliarden Dollar erzielte.[442] Die Nachfrage war riesig, aber die Suche nach entsprechenden Medikamenten hatte schon lange vorher eingesetzt. Das Schmerzmittel Morphin (Morphium), das erstmals um 1804 aus Schlafmohn gewonnen wurde, wurde wegen seiner einschläfernden Wirkung nach Morpheus, dem Gott des Schlafes, benannt. Das passte gut, weil Schlafen und Träumen uns von körperlichen und seelischen Schmerzen befreien können. Wegen seines hohen Suchtpotenzials eignet sich Morphin jedoch nicht wirklich als Schlafmittel.
Derzeit bemisst sich der Marktwert von Schlafmitteln in den USA auf rund 28 Milliarden Dollar im Jahr.[443] Die Zahl der Verschreibungen ist allerdings in jüngerer Zeit rückläufig, weil den Verbrauchern möglicherweise klar wird, dass diese Arzneimittel im Großen und Ganzen eigentlich gar nicht so gut wirken. Sie eignen sich zwar dafür, einen Menschen kurzzeitig zu betäuben, doch das konnte man von Muhammad Alis rechtem Cross auch behaupten. Schlaffördernde Arzneistoffe wie Zolpidem und Eszopiclon fördern keinen gesunden, lang andauernden Schlaf, sondern eher einen schlafähnlichen Zustand der Bewusstlosigkeit, der es in seiner Wirkung kaum oder gar nicht mit den heilenden Kräften des REM- oder Tiefschlafs aufnehmen kann. Laut einer Studie reduzierte Zolpidem den Tiefschlaf, ohne den REM-Schlaf zu befördern, was bedeutet, dass Personen, die das Mittel einnehmen, im Grunde qualitativ hochwertigen Schlaf gegen qualitativ minderwertigen eintauschen.[444] Zudem hat Zolpidem die gut dokumentierte Nebenwirkung, dass es manche Menschen schlafwandeln lässt, was alle möglichen Probleme zur Folge hat.
Danach entwickelte die Pharmaindustrie eine neue Klasse von Medikamenten, die das Schlafwandelproblem vorgeblich lösten, indem sie den im Gehirn wirkenden wach machenden Botenstoff Orexin blockierten.[445] Interessanterweise hielt man die appetitanregende Wirkung von Orexin ursprünglich für relevanter. Dann wurden aber sogenannte Orexin-Rezeptorantagonisten wie Lemborexant und Daridorexant zur Behandlung von Schlafstörungen zugelassen, die Erfolg versprechend zu sein scheinen – nicht zuletzt, weil man trotz ihrer Einnahme noch auf akustische Reize reagieren kann (zum Beispiel möchten Eltern schlafen können, ohne ein weinendes Kind zu überhören).[446] Sie sind allerdings sehr teuer.
Dann gibt es noch die älteren Benzodiazepine wie Diazepam und Alprazolam, die in unserer Gesellschaft nach wie vor fast allgegenwärtig und sehr beliebt sind und manchmal gegen Schlaflosigkeit verordnet werden.[447] Diese Mittel wirken normalerweise betäubend, ohne die Schlafqualität zu verbessern. Es ist etwas besorgniserregend, dass man sie auch mit geistigem Verfall in Verbindung gebracht hat, und gemeinhin empfiehlt man ihre Anwendung bei älteren Erwachsenen nur für sehr kurze Zeit (das Gleiche gilt übrigens auch für Zolpidem).
Wenn neue Patienten in unsere Praxis kommen, nehmen sie nicht selten bereits eines dieser Schlafmittel. Wenn sie Zolpidem oder Alprazolam einmal im Monat oder nur auf Reisen einnehmen oder um in einer Zeit mit emotionalem Stress Schlaf zu finden, ist das nicht beunruhigend. Nehmen sie solche Mittel jedoch regelmäßig, setzen wir alles daran, um sie von diesen Schlafmitteln zu entwöhnen und ihnen zu helfen, ohne die Medikamente gut schlafen zu lernen.
Ein Arzneimittel, das wir zur Förderung des Schlafs tatsächlich als hilfreich erachten, ist Trazodon, ein bereits ziemlich altes Antidepressivum, das 1981 zugelassen wurde und auf dem Markt nie so recht Fuß fassen konnte. Die Dosierung von täglich 200 bis 300 mg pro Tag, die zur Behandlung von Depressionen verordnet wurde, hatte die unerwünschte Nebenwirkung, dass die Patienten einschliefen. Doch des einen Leid ist des anderen Freud. Genau diese Nebenwirkung wünschen wir uns bei der Behandlung von Schlafstörungen, vor allem, wenn der Wirkstoff zugleich die Schlafarchitektur verbessert.[448] Genau das tut Trazodon – im Gegensatz zu den meisten anderen Schlafmitteln.[449] Wir verordnen meist viel geringere Dosierungen von 100 bis 50 mg oder noch weniger. Die optimale Dosis ist vom Patienten abhängig; wir versuchen immer, diejenige Menge zu finden, die die Schlafqualität verbessert, ohne ein Gefühl von Benommenheit am nächsten Tag hervorzurufen. (Zur ergänzenden Behandlung verwenden wir auch Ashwagandha, die Schlafbeere, mit der wir ebenfalls gute Erfahrungen gemacht haben.)
Zur Behebung von Schlafstörungen gibt es nach wie vor kein pharmazeutisches Wundermittel, aber Sie können einige wirksame Dinge tun, um besser ein- und durchzuschlafen – und hoffentlich gut genug zu schlafen, um all den furchterregenden Dingen zu entgehen, über die wir in diesem Kapitel gesprochen haben. Sie sollten jedoch beherzigen, dass diese Tipps und Strategien nichts gegen eine echte Schlaferkrankung wie eine Insomnie oder eine Schlafapnoe ausrichten können (siehe die Fragebogen weiter unten).[450]
Der erste Schritt in diesem Prozess ähnelt dem ersten Schritt in einem Drogenentwöhnungsprogramm: Wir müssen uns von unserer »Abhängigkeit« vom chronischen Schlafmangel lossagen und eingestehen, dass wir mehr Schlaf in ausreichender Qualität und Quantität benötigen. Wir erteilen uns die Erlaubnis zu schlafen. Für mich war das zuerst wirklich schwierig, weil ich jahrzehntelang das Gegenteil praktiziert hatte. Ich hoffe, dass ich Sie von der großen Relevanz des Schlafs für alle möglichen gesundheitlichen Aspekte überzeugen konnte.
Der nächste Schritt besteht in der Analyse Ihrer Schlafgewohnheiten. Mittlerweile sind zahlreiche Schlaftracker erhältlich, die Ihnen einen recht guten Einblick in die Qualität Ihres Schlafs vermitteln können. Sie messen Variablen wie Puls, Herzfrequenzvariabilität, Bewegung oder Atemfrequenz. Mithilfe dieser Inputs werden Schlafdauer und Schlafstadien recht genau (wenn auch nicht perfekt) geschätzt. Ich für meinen Teil fand diese Daten ganz hilfreich, um meinen Schlaf zu optimieren, aber es gibt auch Menschen, denen schlechte Schlafwerte Stress bereiten – was ihren Schlaf noch mehr beeinträchtigen kann. Wenn das der Fall ist, bestehe ich darauf, dass meine Patienten einige Monate auf den Tracker verzichten. Ich sollte auch noch einmal darauf hinweisen, dass langes Schlafen oft nicht nur auf eine schlechte Schlafqualität, sondern auch auf andere gesundheitliche Probleme hindeutet.
Parallel dazu sollten Sie eine längerfristige Einschätzung Ihrer Schlafqualität im vergangenen Monat vornehmen. Der wahrscheinlich am besten validierte Schlaf-Fragebogen ist der Pittsburgh Sleep Quality Index, ein vierseitiges Dokument, das Schlafmuster aus dem jeweils letzten Monat erfragt – zum Beispiel, wie oft Sie Probleme hatten, innerhalb von dreißig Minuten einzuschlafen, wie oft Sie in der Nacht wach geworden sind, wie oft Sie Schwierigkeiten beim Atmen hatten (Schnarchen), wie oft es Ihnen tagsüber schwergefallen ist, wach zu bleiben (etwa beim Autofahren), oder wie oft Ihnen »der Antrieb, Dinge zu erledigen, gefehlt hat«.
Fragebogen und Auswertungsschlüssel sind online einfach zu finden.[451] Wie ich häufig feststelle, verhilft er meinen Patienten zu der Einsicht, dass es an der Zeit ist, den Schlaf ernst zu nehmen und ihm in ihrem Leben Priorität einzuräumen. Es gibt eine weitere, noch simplere Frageliste namens Epworth Sleepiness Scale. Dort soll man mittels einer Skala von 0 (unwahrscheinlich) bis 3 (sehr wahrscheinlich) einschätzen, ob man in bestimmten Situationen einschläft:
beim Lesen im Sitzen
beim Fernsehen
beim Sitzen in einer Besprechung oder an einem anderen öffentlichen Ort
als Mitfahrer bei einer einstündigen Autofahrt
beim Ausruhen im Liegen
beim Zusammensitzen und Reden mit jemandem
im Sitzen nach dem Mittagessen (ohne Alkohol)
als Autofahrer bei minutenlang ruhendem Verkehr
Eine Gesamtpunktzahl von 10 oder mehr spricht für übermäßige Schläfrigkeit und deutet auf ein wahrscheinliches Problem mit der Schlafqualität hin.[452]
Ein hilfreiches Screening-Instrument ist auch der Insomnia Severity Index. Er bietet die Möglichkeit, sich Schlafprobleme und ihre Folgen für Funktionen und Wohlbefinden bewusst zu machen und festzuhalten.[453]
Ein wichtiger, aber oft ignorierter Faktor beim Einschätzen der Schlafqualität ist, dass Menschen völlig unterschiedlichen »Chronotypen« angehören, womit gemeint ist, dass es »Morgenmenschen« (»Lerchen«) und »Abendmenschen« (»Eulen«) gibt. Die innere Uhr ist zu einem großen Teil genetischen Einflüssen unterworfen – Lerchen und Eulen haben verschiedene zirkadiane Gene.[454] Laut Untersuchungen gibt es Personen, die genetisch so veranlagt sind, dass sie morgens gleich aus dem Bett springen, während andere von Natur aus eher später aufwachen (und später schlafen gehen) und erst am Nachmittag so richtig in die Gänge kommen.[455] Letztere sind keine »Faulpelze«, wie man lange angenommen hat – sie haben vermutlich nur einen anderen Chronotyp.
Wie auch für so vieles andere in der Biologie gibt es dafür möglicherweise eine evolutionsgeschichtliche Erklärung: Wenn alle Mitglieder einer Sippe oder eines Stammes das gleiche Schlafmuster aufweisen, ist die gesamte Gruppe jede Nacht für mehrere Stunden Beutegreifern und Feinden wehrlos ausgeliefert. Das ist nicht gerade günstig. Doch wenn die Schlafmuster gestaffelt sind und einige Individuen früh schlafen gehen, während andere lieber noch aufbleiben und das Feuer in Gang halten, ist die Gruppe als Ganzes deutlich weniger angreifbar. Das erklärt vielleicht auch, warum Teenager zuerst spät ins Bett wollen und dann nicht aus den Federn kommen: In der Pubertät verschiebt sich der Chronotyp offensichtlich zu spätem Einschlafen und späterem Aufwachen. Zum Nachteil von Teenagern und ihren Eltern halten die Schulen stur an einem sehr frühen Unterrichtsbeginn fest – doch landesweit formiert sich eine wachsende Bewegung für einen späteren Beginn, um den Schlafmustern von Jugendlichen Rechnung zu tragen.
Bleibt noch zu erwähnen, dass man das mögliche Vorliegen einer obstruktiven Schlafapnoe abchecken sollte, die verblüffend häufig ist, aber sehr oft nicht diagnostiziert wird. Das kann man in einem Schlaflabor oder zu Hause mit einem formalen Test überprüfen. Es gibt aber auch dafür einen Fragebogen, den STOP-BANG, der zu ganz ähnlichen Ergebnissen wie der formale Apnoetest gelangt.[456] Wenn Sie schnarchen, einen hohen Blutdruck haben und meistens müde sind oder wenn Ihrem Partner aufgefallen ist, dass es bei Ihnen nachts zu gelegentlichen, auch ganz kurzen, Atemaussetzern kommt, sollten Sie sich bei einem Arzt einem weiteren Schlafapnoetest unterziehen. (Weitere Risikofaktoren sind ein BMI über dreißig und männlich zu sein.) Schlafapnoe ist ein ernstes medizinisches Problem, dass sich nachteilig auf die kardiovaskuläre Gesundheit und das Demenzrisiko auswirken kann.
Besser schlafen
Sobald Sie gravierende Probleme wie eine Schlafapnoe ausgeschlossen haben (oder angegangen sind), können Sie konkrete Schritte unternehmen, um Ihren Schlaf zu verbessern – oder wenigstens Ihre Chancen, gut zu schlafen.
Am wichtigsten ist, dass Sie sich ein Umfeld schaffen, das gutes Schlafen fördert. Die erste Voraussetzung für einen guten Schlaf ist Dunkelheit. Licht ist der Feind des Schlafs. Punkt. Das heißt, Sie sollten Ihr Schlafzimmer so stark verdunkeln wie möglich, mit Rollläden oder dichten Vorhängen, falls es draußen hell ist, und indem Sie sämtliche Lichtquellen im Zimmer ausschalten oder entfernen, selbst die an elektronischen Geräten wie Fernsehern oder Receivern. Ihre stecknadelkopfgroßen LED-Anzeigen reichen völlig aus, um Ihren Schlaf zu beeinträchtigen. Besonders Digitaluhren sind tödlich – nicht nur wegen der hellen Zahlen. Wenn Sie nachts wach werden und sehen, dass es 03:31 Uhr ist, fangen Sie vielleicht an, sich Sorgen um Ihren Flug um 07:00 Uhr zu machen, und können nicht mehr einschlafen.
Diese Maßnahmen sind leichter gesagt als getan, weil es im Grunde bedeutet, das 21. Jahrhundert aus Ihrem Schlafzimmer zu verbannen. Das moderne Leben ruiniert fast systematisch unsere Fähigkeit, gut zu schlafen. Das beginnt schon mit der Allgegenwart von elektrischem Licht. Künstliches Licht bringt nicht nur unsere natürliche innere Uhr aus dem Takt, sondern hemmt auch die Ausschüttung von Melatonin, dem durch Dunkelheit aktivierten Hormon, das unserem Gehirn sagt, dass es Zeit zum Schlafengehen ist.[457] Das ist so ähnlich wie bei der amerikanischen Standardernährung, die störend auf Sättigungshormone einwirkt, welche uns normalerweise signalisieren, dass wir satt sind und aufhören können zu essen.
Noch schlimmer ist die seit jüngerer Zeit verbreitete Wohnungsbeleuchtung mit LED-Lampen, die überwiegend am blauen Ende des Lichtspektrums angesiedelt sind und damit dem Tageslicht ähneln. Registriert unser Gehirn dieses blaue Licht, denkt es, es sei Tag und wir sollten wach sein, und hindert uns demzufolge am Einschlafen. Darum sollten Sie sich am Abend möglichst wenig hellem LED-Licht aussetzen. Sorgen Sie aus diesem Grund dafür, dass unnötiges Licht im Haus ein paar Stunden bevor Sie zu Bett gehen nach und nach ausgeschaltet wird. Außerdem ist es sinnvoll, LED-Lampen mit hohem Blauanteil durch wärmeres Licht zu ersetzen.
Die Geräte, auf die wir vor dem Schlafengehen starren – Handys, Laptops, Videospiele – wirken sich auf unseren Schlaf ganz besonders nachteilig aus. Sie bombardieren uns nicht nur mit noch mehr blauem Licht, sondern aktivieren auch unseren Geist auf eine Weise, die ihn vom Schlafen abhält. Laut einer groß angelegten Studie hatten Versuchspersonen umso größere Probleme, ein- und durchzuschlafen, je mehr sie sich in der Stunde vorher mit interaktiven Geräten beschäftigt hatten.[458] Dagegen hatten Geräte, die eher passiv genutzt wurden, wie Fernseher oder MP3-Player, und vor allem Bücher eine weniger nachteilige Wirkung auf den Schlaf. Wie Michael Gradisar, Schlafforscher und Professor für Psychologie an der Flinders University in Australien, behauptet, könnte das zum Teil erklären, warum Fernsehen vor dem Schlafengehen den Schlaf weniger zu beeinträchtigen scheint als Videospiele oder durch Social Media zu scrollen.[459]
Ich bin immer mehr davon überzeugt, dass unsere Rund-um-die-Uhr-Abhängigkeit von Bildschirmen und Social Media unsere schädlichste Angewohnheit ist – nicht nur, was unseren Schlaf betrifft, sondern ganz allgemein unsere geistige Gesundheit. Darum halte ich mich abends von ihnen fern (oder versuche es zumindest). Wenigstens eine Stunde bevor Sie zu Bett gehen, sollten Sie den Computer ausschalten und das Handy beiseitelegen. Und nehmen Sie NICHT den Laptop oder das Handy mit ins Bett.
Ein weiterer äußerst bedeutsamer Umweltfaktor ist die Temperatur. Viele Leute verbinden Schlaf mit Wärme, aber in Wahrheit ist es genau umgekehrt. Dass wir einschlafen, signalisiert der Körper unter anderem dadurch, dass die Körpertemperatur um etwa 1 Grad Celsius sinkt.[460] Um ihn dabei zu unterstützen, sollten Sie Ihr Schlafzimmer möglichst kühl halten – etwa 18 Grad sind optimal. Ein warmes Bad vorm Zubettgehen ist hilfreich, und zwar nicht nur, weil uns das Bad entspannt. Wenn wir uns danach ins kühle Bett legen, sinkt die Körpertemperatur, und das signalisiert dem Gehirn, dass es Zeit zum Einschlafen ist. (Es gibt übrigens eine große Auswahl an kühlenden Matratzen und Matratzenauflagen zu kaufen.)
Unsere innere »Umwelt« ist für guten Schlaf genauso wichtig. Als Erstes rate ich meinen Patienten, weniger Alkohol zu trinken – oder, noch besser, gar keinen. Das klingt erst mal wenig plausibel, weil Alkohol zunächst sedierend wirkt und wir deshalb schneller einschlafen.[461] Doch im Laufe der Nacht wandelt sich der Alkohol vom Freund des Schlafs zum Feind, weil er beim Abbau in Stoffe aufgespalten wird, die das Schlafen beeinträchtigen. Je nach Menge des konsumierten Alkohols wird es in der zweiten Nachthälfte schwieriger, in den REM-Schlaf zu finden; wir werden häufiger wach und schlafen nur noch leicht.
Selbst bei mäßigem Alkoholgenuss zeigen sich deutliche Auswirkungen auf Gedächtnis und Kognition. In Studien hat sich herausgestellt, dass junge Leute, die viel Alkohol getrunken haben, mit größerer Wahrscheinlichkeit auch einfache Aufgaben wie das Abschließen der Haustür oder das Abschicken eines Briefes vergessen. Studierende, die pro Woche durchschnittlich neun Drinks konsumierten (was nach Hochschulstandard nicht viel ist), schnitten bei einem verbalen Gedächtnistest schlechter ab. Und was niemanden überraschen wird: Studierende, die mehr tranken, schliefen später ein, waren tagsüber müder und erzielten schlechtere Testergebnisse. Alarmierender ist, dass sich Studierende, die sich zwei Tage nach intensivem Lernen oder Studium betranken, an das meiste von dem, was sie gelernt hatten, nicht mehr erinnern konnten.[462]
Bedenken Sie, dass all diese Resultate junge Menschen betrafen, Studierende, die sich vermutlich auf der Höhe ihrer geistigen Leistungsfähigkeit befinden. Wenn wir die Ergebnisse auf Personen in mittleren Jahren oder im Alter hochrechnen, die Alkohol möglicherweise weniger gut vertragen und eher mal etwas vergessen, sind die Folgen besorgniserregend. Meine persönliche Schwelle liegt bei zwei Drinks am Abend; wird es mehr, kann ich einen erholsamen Schlaf vergessen und bin am nächsten Tag bei der Arbeit weniger fit – egal, wie viel Kaffee ich trinke.
Kaffee ist keine Lösung für Schlafprobleme, insbesondere, wenn man davon zu viel oder (vor allem) zur falschen Zeit trinkt. Die meisten Menschen halten Koffein für ein Aufputschmittel, das uns auf irgendeine Weise Energie verleiht, aber eigentlich ist es eher ein Schlafverhinderer.[463] Es hemmt den Rezeptor für Adenosin, eine chemische Verbindung, die uns normalerweise beim Einschlafen hilft. Im Lauf des Tages reichert es sich im Gehirn an und erzeugt einen »Schlafdruck«, wie Wissenschaftler sagen, also den Drang zu schlafen. Wir werden zwar müde und brauchen Schlaf, aber wenn wir Kaffee trinken, legen wir den Hörer gewissermaßen neben das Telefon, und das Gehirn erhält die Botschaft nicht.
Besonders morgens um sechs Uhr, wenn unser Chronotyp uns mitteilt, dass wir jetzt eigentlich noch schlafen sollten, kann Kaffee offenkundig hilfreich sein. Die Halbwertszeit von Koffein in unserem Körper beträgt jedoch bis zu sechs Stunden; wenn wir also mittags eine Tasse Kaffee trinken, zirkuliert abends um sechs immer noch das Koffein einer halben Tasse im Körper.[464] Das bedeutet: Wenn Sie Ihren letzten doppelten Espresso des Tages nachmittags um drei trinken, haben Sie abends um neun immer noch eine volle Ladung Koffein im Blut. Aber höchstwahrscheinlich nicht den Drang, sich bald schlafen zu legen.
Die Koffeintoleranz ist, abhängig von den Genen und anderen Faktoren, von Mensch zu Mensch verschieden (das Biotechnologie-Unternehmen 23andMe führt Tests auf ein verbreitetes »Koffein-Gen« durch). Da ich ein sehr schneller Verstoffwechsler bin, kann ich mir den nachmittäglichen Espresso leisten, ohne dass mein Schlaf allzu sehr darunter leidet; sogar wenn ich noch nach dem Abendessen Kaffee trinke, bleibt das folgenlos (anders als bei Alkohol). Wer Koffein langsam verstoffwechselt, sollte es vermutlich bei einer bis zwei Tassen vor dem Mittagessen bewenden lassen.
In unserer Taktik zur Behebung von Schlafproblemen ist das Konzept des Schlafdrucks, also unser Bedürfnis oder Verlangen nach Schlaf, von großer Bedeutung. Wir wollen einen Schlafdruck entwickeln, aber im richtigen Ausmaß und zur richtigen Zeit – nicht zu viel, nicht zu wenig und nicht zu bald. Aus diesem Grund arbeiten Ärzte bei der Behandlung von Schlafproblemen tatsächlich oft mit Schlafentzug, indem sie ihren Patienten maximal sechs Stunden Schlaf »erlauben«.[465] Das macht sie im Allgemeinen so müde, dass sie abends leichter einschlafen und ihr normaler Schlafzyklus (hoffentlich) wiederhergestellt wird. Ihr Schlafdruck wird letztlich stärker als die Ursachen der Schlafstörung. Ein Nickerchen tagsüber ist dann zwar manchmal verlockend, kann allerdings kontraproduktiv sein, weil es den Schlafdruck wieder verringert und so das Einschlafen am Abend erschwert.
Schlafdruck lässt sich auch durch sportliche Betätigung entwickeln, vor allem durch konstantes Ausdauertraining (zum Beispiel in Zone 2), im Idealfall nicht in den zwei oder drei Stunden, bevor man ins Bett geht.[466] Meine Patienten stellen häufig fest, dass ein 30-Minuten-Training in Zone 2 Wunder wirkt, was das Einschlafen betrifft. Noch besser sind Übungen, in denen man dem Sonnenlicht ausgesetzt ist, also im Freien. Während blaues Licht spät am Abend den Schlaf beeinträchtigen kann, hilft eine halbstündige Dosis an hellem Tageslicht dem Schlaf-wach-Rhythmus, wieder auf Spur zu kommen und die Weichen für einen guten Nachtschlaf zu stellen.
Wichtig ist auch, sich mental aufs Schlafen vorzubereiten. Für mich bedeutet das, alles zu vermeiden, was Stress oder Sorgen verursachen kann, wie das Lesen beruflicher E-Mails oder die Nachrichten zu verfolgen. Das aktiviert das sympathische Nervensystem (dasjenige für Kampf oder Flucht) zu einer Zeit, in der wir entspannen und allgemein zur Ruhe kommen möchten. Ich muss mich selber zwingen, am Abend dem Computer fernzubleiben – die neu reingekommenen E-Mails sind am nächsten Morgen auch noch da. Liegt mir ein Problem besonders auf der Seele, mache ich mir ein paar Notizen, wie ich am nächsten Tag damit umgehen will. Auch Meditation kann helfen, um das sympathische Nervensystem herunterzufahren und das Gehirn aufs Schlafen einzustimmen.[467] Es gibt sehr gute Apps mit Anleitungen zum Meditieren, darunter auch einige, die speziell den Schlaf betreffen.
Über alldem steht der Gedanke, dass ein guter Nachtschlaf auf einem guten, wachen Tag beruht – mit sportlicher Betätigung, Zeit an der frischen Luft, vernünftiger Ernährung (keine Snacks am späten Abend), wenig bis gar keinem Alkohol, einem guten Stressmanagement und dem Wissen, wo man der Arbeit und anderen Stressfaktoren Grenzen setzen muss.
Wie Sie Ihren Schlaf verbessern
Die folgenden Regeln oder Anregungen versuche ich zu beherzigen, um besser zu schlafen. Es sind keine Wundermittel – meist geht es darum, bessere Voraussetzungen fürs Schlafen zu schaffen und alles Übrige Gehirn und Körper zu überlassen. Natürlich müssen Sie nicht alles tun, was ich vorschlage – generell ist es am besten, wenn Sie sich nicht zu viele Gedanken übers Schlafen machen. Doch je mehr von den Bedingungen Sie erfüllen können, desto höher steigen Ihre Chancen auf einen guten Nachtschlaf.
Trinken Sie keinen Alkohol, basta. Und wenn Sie unbedingt müssen, beschränken Sie sich auf nur einen Drink, den Sie vor sechs Uhr abends zu sich nehmen. Wahrscheinlich beeinträchtigt Alkohol die Schlafqualität mehr als jeder andere Faktor, den wir kontrollieren können. Verwechseln Sie den benebelten Zustand, den er hervorruft, nicht mit qualitativ hochwertigem Schlaf.
Essen Sie in den drei Stunden, bevor Sie zu Bett gehen, nichts mehr – im Idealfall dehnen Sie diesen Zeitraum sogar noch aus. Am besten geht man mit einem leichten Hungergefühl schlafen (wenn der Magen zu sehr knurrt, kann dies das Einschlafen allerdings behindern).
Halten Sie sich zwei Stunden, bevor Sie schlafen gehen, von stimulierenden elektronischen Geräten fern. Wenn Sie Schwierigkeiten haben einzuschlafen, versuchen Sie jeder Art von Bildschirm aus dem Wege zu gehen. Wenn es sich nicht vermeiden lässt, reduzieren Sie möglichst das vom Bildschirm ausgehende blaue Licht.
Vermeiden Sie mindestens eine Stunde vorm Schlafengehen alles, was Besorgnis auslöst oder stimulierend wirkt, wie das Lesen beruflicher E-Mails oder – um Himmels willen – das Checken von Social Media. Denn damit bringen Sie die für Grübelei und Beunruhigung zuständigen Hirnareale so richtig in Fahrt, und das wollen Sie nicht.
Wer die Möglichkeit hat, sollte kurz vor der Nachtruhe in eine Sauna oder einen Whirlpool gehen. Wenn Sie sich danach ins kühle Bett legen, signalisiert Ihre sinkende Körpertemperatur dem Gehirn, dass es Zeit zu schlafen ist. (Ein heißes Bad oder eine heiße Dusche wirken auch.)
Das Schlafzimmer sollte kühl sein, idealerweise um 18 Grad. Auch das Bett sollte kühl sein. Zu diesem Zweck sind viele verschiedene kühlende Matratzen und Matratzenauflagen erhältlich.
Verdunkeln Sie das Zimmer vollständig. Es sollte so dunkel sein, dass Sie buchstäblich die Hand vor den Augen nicht mehr sehen können. Ist das nicht möglich, verwenden Sie eine Schlafmaske. Ich benutze eine aus Seide, die etwa 8 Dollar kostet und besser funktioniert als teurere Modelle, die ich ausprobiert habe.
Geben Sie sich genug Zeit zum Schlafen – Schlafforscher sprechen von sleep opportunity, der Gelegenheit zum Schlafen. Das heißt, Sie sollten mindestens acht, vorzugsweise neun Stunden bevor Sie aufstehen müssen, ins Bett gehen. Wenn Sie sich gar nicht erst die Chance geben, genug zu schlafen, nützt Ihnen auch der Rest dieses Kapitels nichts.
Legen Sie eine bestimmte Weckzeit fest, und weichen Sie nicht davon ab, auch nicht am Wochenende. Wenn Sie flexibel sein müssen, können Sie auch Ihre Zubettgehzeit variieren, aber achten Sie darauf, dass Sie sich jede Nacht wenigstens acht Stunden zum Schlafen einräumen.
Machen Sie sich nicht verrückt, vor allem, wenn Sie Schlafstörungen haben. Wenn Sie einen Wecker brauchen, drehen Sie ihn so, dass Sie die Zeitangabe nicht sehen können. Auf die Uhr zu sehen erschwert das Einschlafen. Und falls Ihnen Ihre schlechten Schlafwerte Sorgen machen, verbannen Sie Ihren Schlaftracker für eine Weile.
Aber was ist, wenn wir trotz allem immer noch nicht schlafen können? Das bringt uns zum letzten und verzwicktesten Schlafproblem, einer echten Insomnie. Uns allen ist es vermutlich schon einmal so gegangen, dass wir nicht schlafen konnten, aber viele Menschen leiden an einer chronischen Schlafstörung. Also sollten Sie zunächst klären, ob es sich tatsächlich um eine Insomnie handelt. Oder haben Sie einfach nicht die richtigen Voraussetzungen für guten Schlaf geschaffen?
Wenn Sie nachts wach liegen und einfach nicht wieder einschlafen können, lautet mein Rat: Gehen Sie nicht dagegen an. Am besten stehen Sie auf, gehen in ein anderes Zimmer und tun etwas, was Sie entspannt. Machen Sie sich eine Tasse Tee (natürlich ohne Koffein), und lesen Sie ein (möglichst langweiliges) Buch, bis Sie wieder müde werden. Entscheidend ist laut Vikas Jain, etwas zu finden, was entspannend ist und Ihnen gefällt, ohne eine bestimmte Funktion zu haben. Ihre Insomnie soll keinen Zweck erfüllen, etwa zu arbeiten oder Rechnungen zu bezahlen, denn sonst wird Ihr Gehirn dafür sorgen, dass Sie regelmäßig wach werden. Und denken Sie daran, dass Sie möglicherweise gar nicht an einer Insomnie leiden, sondern schlicht eine Eule sind und glauben, Sie »müssten« schon ins Bett gehen, während Ihr Gehirn oder Körper noch längst nicht dafür bereit ist. Wenn möglich, passen Sie Ihre Zubettgeh- und Aufstehzeit also daran an.
Hält die Schlaflosigkeit trotz all der genannten Maßnahmen an, besteht die wirksamste Behandlung in einer Form der Psychotherapie, der kognitiven Verhaltenstherapie der Insomnie (KVT-I; im Englischen Cognitive Behavioral Therapy for Insomnia, CBT-I). Ziel der KVT-I ist, das Vertrauen in die eigene Schlaffähigkeit zu stärken, schlechte Schlafgewohnheiten durchbrechen zu helfen und Ängste zu zerstreuen, die einen vom Schlafen abhalten können. Bei dieser Therapie wird ebenfalls mit Schlafentzug gearbeitet, um den Schlafdruck zu erhöhen. Das wiederum hilft, das Vertrauen in die Fähigkeit zu schlafen wiederzugewinnen. Studien über Verfahren der KVT-I haben erbracht, dass sie wirksamer als Schlafmedikamente sind.
Nachdem ich den Schlaf jahrzehntelang ignoriert habe, bin ich nun sein Fan. Ich betrachte ihn als ein leistungsförderndes Mittel, und zwar nicht nur in körperlicher, sondern auch geistiger Hinsicht. Langfristig wirkt sich Schlaf ausgesprochen positiv auf unsere gesunde Lebenszeit aus. Genau wie körperliche Betätigung ist Schlafen eine ganz eigene Art von Wunderdroge, mit generellen wie auch speziellen Vorteilen für unser Gehirn, unser Herz und insbesondere für unseren Stoffwechsel.
Fazit: Wenn die Evolution den Schlaf unverzichtbar gemacht hat, werde ich nicht länger gegen ihn argumentieren. Ich heiße ihn vielmehr mit offenen Armen willkommen.
Kapitel 17
In Arbeit
Wer die seelische Gesundheit ignoriert, bezahlt einen hohen Preis
Jeder Mann ist eine Brücke, und so umspannt seine Lebenszeit die Bilder und Traditionen der Männlichkeit, die er von vergangenen Generationen ererbt hat, und reicht seine eigene Version an die weiter, die nach ihm kommen.
Terrence Real
Montags kommen immer die neuen Patienten, und ich war als Erster da. In wenigen Wochen war Weihnachten, und ich war von San Diego nach Nashville geflogen und in ein klappriges Minivan-Taxi geklettert, in dem es nach abgestandenem Zigarettenrauch stank. Vor mir lag eine zweistündige Fahrt zu einer Stadt, von der ich noch nie gehört hatte – Bowling Green, Kentucky. Der Morgen war kalt, und während der Fahrt starrte der Fahrer pausenlos auf sein Handy. Merkwürdigerweise störte mich das nicht. Ich wollte, dass wir einen Unfall hatten. Dann würde mir wenigstens erspart, was vor mir lag.
Am späten Vormittag saß ich dann im Gemeinschaftsbereich einer Einrichtung namens The Bridge to Recovery (»Die Brücke zur Genesung«), einem abgelegenen Fleckchen tief im Wald. Es roch muffig. Während ich auf die anderen wartete, wanderte ich durch die Küche, wo ich ein Schild mit der Aufschrift entdeckte: »Religion ist für Menschen, die Angst vor der Hölle haben. Spiritualität ist für Menschen, die schon dort waren.«
Wo, verdammt noch mal, bin ich hier gelandet?, fragte ich mich.
Die Erste der anderen Neuankömmlinge war eine Frau um die fünfzig. Wir starrten uns wortlos an. Sie sah so traurig aus, als hätte sie ein Jahr lang nur geweint. Ob ich auf sie wohl denselben Eindruck machte? Als es Abend wurde, waren alle »Neuen« da. Sie wirkten erschöpft, blass, völlig ausgelaugt. Einige waren süchtig – nach Drogen, Alkohol, Sex oder irgendeiner Mischung davon. Ich betrachtete sie voller Entsetzen und glaubte, nicht so zu sein wie sie.
Nach ein paar einführenden Worten ging es zum sogenannten Check-in, bei dem wir der Reihe nach unseren Gefühlszustand beschrieben. Wie genau wir uns in diesem Moment fühlten. Ich wusste nicht, was ich sagen sollte. Ich war unsagbar wütend. In mir brodelte es. Ich konnte einfach nicht – ich war nicht einmal in der Lage, meine eigenen Gefühle zu verstehen, und schon gar nicht, sie in Worte zu kleiden. Ich war wütend darüber, dass ich an diesen Ort hatte kommen müssen. Ich war wütend, weil ich gescheitert war. Ich glaubte, nicht dorthin zu gehören, zu diesen gebrochenen Menschen. Jede Zelle meines Körpers wollte auf der Stelle bei Taxi Todeskommando anrufen und schleunigst wieder verschwinden.
Einer Frau in meinem Alter, die Sarah hieß und schon seit mehr als zwei Wochen da war (und immer die richtigen Worte fand, wie ich noch feststellen sollte), war vermutlich mein Gesichtsausdruck aufgefallen. Obwohl sie nicht einmal meinen Namen kannte, wandte sie sich mir zu und sagte: »Hey, schon okay – keiner kommt hierher, weil er gerade eine Glückssträhne hat.«
Vielleicht hatte ich noch nicht das Gefühl, ganz unten angelangt zu sein, aber ich war kurz davor. Vor einigen Wochen hätte ich mich um ein Haar auf einem Parkplatz mit irgendeinem Kerl geprügelt. Wir standen uns Auge in Auge gegenüber, und ich forderte ihn auf zuzuschlagen, damit ich ihm den Kehlkopf rausreißen könne. Ich beschrieb ihm mit chirurgischer Präzision, was ihm blühte, und garnierte das Ganze noch mit einigen erlesenen Kraftausdrücken. Ziemlich sicher wäre ich aus dem Kampf siegreich hervorgegangen, aber im Gegenzug hätte ich damit alles andere aufs Spiel gesetzt – mein Haus, meine Approbation, meine Freiheit und wahrscheinlich auch das, was von meiner Ehe noch übrig geblieben war. Nach außen hin war ich ein scheinbar erfolgreicher Typ mit einer gut laufenden Praxis, einer schönen Frau und Kindern, wunderbaren Freunden, robuster Gesundheit und einem Autorenvertrag für dieses Buch. Aber in Wahrheit hatte ich völlig die Kontrolle verloren.
Ich war auch nicht bloß irgendein herumtobender Feld-Wald-und-Wiesen-Irrer. Es war noch viel schlimmer. Einige Monate zuvor – genauer gesagt, am 11. Juli 2017, abends um Viertel vor sechs – hatte mich meine Frau Jill angerufen, aus einem Krankenwagen, in dem sie mit unserem kleinen Säugling Ayrton saß, um in die Klinik zu fahren. Aus irgendeinem Grund hatte er plötzlich aufgehört zu atmen und das Bewusstsein verloren. Er hatte die Augen verdreht, war blau angelaufen und leblos, ohne Puls. Nur die schnelle Reaktion unserer Nanny hatte ihn gerettet. Sie rannte mit ihm zu Jill, die Krankenschwester ist. Instinktiv legte sie ihn auf den Boden und begann mit der Wiederbelebung, indem sie mit den Fingern rhythmisch auf sein winziges Brustbein drückte, während die Nanny panisch den Notruf wählte. Er war noch nicht einmal einen Monat alt.
Als die Feuerwehrleute etwa fünf Minuten später ins Haus stürmten, atmete Ayrton schon wieder; seine Haut verlor den bläulichen Farbton und wurde wieder rosig, als der Sauerstoff durch seinen Körper strömte. Die Feuerwehrleute waren sprachlos – sie hätten noch nie gesehen, dass ein Kind das überlebt habe, sagten sie zu Jill. Wir wissen bis heute nicht, wie und warum es passiert ist, aber wahrscheinlich hätte es sich um einen Fall von plötzlichem Kindstod gehandelt, bei dem Babys unerwartet im Schlaf sterben. Sie verschlucken sich an ihrem Speichel oder werden aus irgendeinem anderen Grund bewusstlos, und dann gelingt es ihrem noch sehr unreifen Nervensystem nicht, die Atmung wieder in Gang zu bringen.
Als mich Jills Anruf erreichte, fuhr ich gerade auf dem Weg zum Abendessen mit einem Taxi durch New Yorks 54th Street. Als sie mir alles erzählt hatte, sagte ich nur völlig emotionslos: »Okay, ruf mich an, wenn du in der Klinik bist, dann kann ich mit den Ärzten auf der Intensivstation sprechen.«
Sie legte ziemlich schnell auf, und natürlich hatte sie allen Grund, aufgebracht zu sein. Unser Sohn war beinahe gestorben, und ich hätte nur eines sagen müssen – und zwar unbedingt: dass ich mit dem nächsten Flugzeug heimkommen würde.
Jill blieb vier Tage lang allein mit Ayrton im Krankenhaus und bat mich inständig, nach Hause zu kommen. Ich rief jeden Tag an, um mit den Ärzten über die Testergebnisse zu sprechen, aber ich blieb in New York, weil ich »wichtige« berufliche Dinge zu erledigen hatte. Am Dienstag hatte Ayrton den Herzstillstand erlitten, aber ich kehrte erst am Freitag der darauffolgenden Woche nach San Diego zurück. Zehn Tage später.
Selbst heute wird mir noch schlecht, wenn ich über mein Verhalten von damals nachdenke. Ich kann nicht fassen, dass ich meiner Familie so etwas angetan habe. Ich kann nicht fassen, was für ein blinder, egoistischer, ignoranter Ehemann und Vater ich war. Und ich weiß, dass ich mir das, solange ich lebe, niemals wirklich verzeihen kann.
Ich muss zu jener Zeit ausgesprochen gestört gewirkt haben, denn irgendwann begann mein guter Freund Paul Conti, ein Kommilitone aus dem Medizinstudium, der heute ein brillanter und sehr einfühlsamer Psychiater ist, auf mich einzureden, ich müsse diese Einrichtung in Kentucky aufsuchen. Ich machte mich schlau und hatte den Eindruck, dass es sich um einen Ort für Suchtkranke handelte. »Das hat doch keinen Sinn«, sagte ich zu ihm. »Ich bin doch nicht süchtig.«
Über Monate versuchte er mir geduldig zu erklären, dass Sucht viele Formen annehmen kann und nicht nur mit Drogen oder Alkohol zu tun hat. Oft, so erläuterte er, handele es sich um die Folgen eines Traumas, das man irgendwann in der Vergangenheit durchlebt habe. Paul ist Traumaexperte und erkannte, dass ich alle einschlägigen Verhaltensmerkmale aufwies: Wut, Distanziertheit, Besessenheit, ein Bedürfnis, mich zu beweisen, das aus Unsicherheit erwuchs. »Ich weiß nicht, was dir da passiert ist, aber du musst mir vertrauen«, sagte er. Er ließ nicht locker.
Ich willigte ein, nach Kentucky zu fahren, suchte aber immer noch nach Entschuldigungen, nicht hinzumüssen. Anfang November rief eine Frau von The Bridge für ein Aufnahmegespräch an. Es war eine lange, zähe Unterhaltung, und mit meiner Geduld war es zu Ende, als sie fragte: »Haben Sie irgendwann eine Form von Misshandlung erlitten?«
Ich wurde dermaßen wütend, dass ich »Fuck you!« brüllte und auflegte. Dann beschloss ich, den Klinikaufenthalt abzusagen. Was stimmte nicht mit diesen Leuten, dass sie mir so bescheuerte Fragen stellten?
An das Thanksgiving-Wochenende habe ich nur noch verschwommene Erinnerungen. Zum ersten Mal in unserem gemeinsamen Leben besuchten wir weder Freunde noch Verwandte, um bei ihnen zu essen, und luden auch niemanden zu uns nach Hause ein. Wir blieben einfach für uns allein. Sonntag abend redete Jill wieder flehentlich auf mich ein, ich solle nach Kentucky fahren. Ich sagte, ich könne einfach nicht so lange von der Bildfläche verschwinden. Meine Patienten würden mich brauchen, und Jill brauche auch meine Hilfe wegen der Kinder. Das war totaler Quatsch, und das wussten wir beide. Jill sagte geradeheraus: »Du bist mir keine Hilfe. Im Gegenteil – du tust mir sehr weh und deinen Kindern ebenfalls.«
Mit der brutalen Wahrheit konfrontiert, wusste ich, dass ich gehen musste.
Zweifellos haben Sie inzwischen bemerkt, dass dieses Kapitel anders ist als der Rest des Buches, denn in ihm bin ich nicht der Arzt – ich bin der Patient. Und ich bin ein Patient, der sich glücklich schätzt, noch am Leben zu sein. Bisher habe ich mich fast ausschließlich auf die körperlichen Aspekte von gesunder Lebenszeit und Langlebigkeit konzentriert, aber nun möchte ich ihre seelischen und mentalen Seiten untersuchen, die in gewisser Hinsicht wichtiger sind als alles andere, was ich hier bereits behandelt habe.
Meine Reise hat nicht nur mein eigenes Leben und das meiner Familie umgekrempelt, sondern auch, wie ich über Langlebigkeit denke. Dieser Prozess ist noch nicht abgeschlossen, er verlangt mir täglich Arbeit ab – fast so viel Zeit und Mühe, wie ich dem Sport widme (und das ist eine Menge, wie Sie mittlerweile wissen). Genau so sollte es sein, das habe ich mit der Zeit gelernt. Seelische und körperliche Gesundheit sind miteinander verflochten, auf eine Weise, die Medizin 2.0 erst allmählich erfasst. Ein schlagendes Beispiel war mein Wutanfall auf dem Parkplatz. Es wäre durchaus möglich gewesen, dass die Konfrontation, insbesondere angesichts meiner genetischen Prädisposition für einen Herzinfarkt, ein böses Ende für mich genommen hätte. Ich hätte auf der Stelle tot umfallen können.
Die geistige Gesundheit beeinflusst die Gesamtlebenszeit auf eine noch andere Weise sehr direkt, wenn Menschen Selbstmord begehen.[468] Unter den Todesursachen bei allen Altersgruppen, von Teenagern bis zu Achtzigjährigen, rangiert er unter den Top Ten. Wenn ich über Selbstmord nachdenke, fällt mir immer Ken Baldwin ein, der 1985 mit achtundzwanzig Jahren von der Golden Gate Bridge sprang.[469] Anders als 99 Prozent der Menschen, die von dieser Brücke springen, überlebte er. Später erzählte er dem Autor Tad Friend, was er im Fallen gedacht hatte: »Ich erkannte sofort, dass sich alles in meinem Leben, von dem ich geglaubt hatte, es sei nicht mehr in Ordnung zu bringen, sehr wohl wieder in Ordnung bringen ließ – nur nicht, dass ich gerade gesprungen war.«
Nicht alle Selbstmörder springen von einer Brücke. Noch viel mehr Menschen rutschen gewissermaßen über gewundene Pfade nach und nach ins Elend und in einen frühen Tod. Sie lassen zu, dass Stress und Ärger ihre Gesundheit ruinieren, oder verfallen in eine selbst verordnete Sucht nach Medikamenten, Drogen und Alkohol oder gehen anderen waghalsigen, lebensgefährlichen Aktivitäten nach, die Psychotherapeuten als Parasuizid bezeichnen. Es überrascht nicht, dass Todesfälle in Verbindung mit Alkohol und generell Substanzmissbrauch in den letzten zwei Jahrzehnten, vor allem in der Altersgruppe zwischen dreißig und fünfundsechzig Jahren, stark zugenommen haben.[470] Nach Schätzungen der Seuchenschutzbehörde sind von April 2020 bis April 2021 über hunderttausend US-Amerikaner an einer Überdosis Drogen gestorben – etwa so viele wie an Diabetes.[471]
Diese »versehentlichen« Überdosen sind für nahezu 40 Prozent aller tödlichen Unfälle verantwortlich.[472] In diese Kategorie gehören auch Verkehrsunfälle und tödliche Stürze. Einige dieser Überdosierungen waren zweifellos nicht beabsichtigt, aber ich wette, dass die große Mehrheit auf die eine oder andere Weise letztlich auf seelische Probleme der Todesopfer zurückzuführen war. Es handelte sich um Selbstmord auf Raten, Tod aus Verzweiflung – eine qualvolle, aber häufig unsichtbare Form des »langsamen Sterbens«, über das wir bereits gesprochen haben.[473]
Diese Art des Sterbens hat, befördert durch die Allgegenwart suchtfördernder Schmerzmittel in unserer Gesellschaft, etwa in den beiden letzten Jahrzehnten so stark zugenommen, dass sie die Lebenserwartung in einigen Teilen der amerikanischen Bevölkerung gesenkt hat – zum ersten Mal in über hundert Jahren.[474] Vor allem weiße Männer und Frauen in mittleren Jahren sterben in nie dagewesener Zahl an Überdosen von Drogen und Alkohol, Lebererkrankungen und Selbstmord, wie Anne Case und Angus Deaton erstmals 2015 festgestellt haben.[475] Die Krise des Drogenmissbrauchs hat zu einer Krise der Langlebigkeit geführt, denn eigentlich handelt es sich um eine verkappte Krise der seelischen Gesundheit.
Diese Form des Leidens ist viel verbreiteter, als die Selbstmordraten vermuten lassen. Sie raubt dir die Freude, die dir ermöglicht, dich auf deine Gesundheit, dein Leben und deine Beziehungen zu anderen Menschen zu konzentrieren – statt zu leben, wartet man nur noch auf den Tod. Das hat mich zu der Erkenntnis geführt, dass die seelische Gesundheit vielleicht die wichtigste Komponente der gesunden Lebenszeit ist. Lange zu leben ist im Grunde nichts wert, ohne ein gewisses Maß an Glück, Erfüllung und Verbundenheit mit anderen Menschen. Zudem können Elend und Unglücklichsein auch unsere körperliche Gesundheit zerstören, ebenso sicher wie Krebs, Herz-Kreislauf-Erkrankungen, neurodegenerative Erkrankungen und Unfälle.
Sogar allein zu leben oder sich einsam zu fühlen geht mit einem sehr viel höheren Sterberisiko einher. Während die meisten Probleme mit seelischer Gesundheit altersunabhängig sind, ist dies der eine emotionale »Risikofaktor«, der mit zunehmendem Alter an Brisanz zunimmt. Laut Erhebungen sind ältere Amerikaner Tag für Tag länger allein – bei Fünfundsiebzigjährigen sind es im Durchschnitt täglich etwa sieben Stunden –, und die Wahrscheinlichkeit, dass sie allein leben, ist sehr viel höher als bei Personen mittleren Alters oder Jüngeren.[476] Und so, wie die Dinge für mich standen, sah auch ich einem traurigen, einsamen, elenden Leben im Alter entgegen.
Ich brauchte eine Weile, um das zu erkennen, aber sich mit anderen Menschen verbunden zu fühlen und eine gesunde Beziehung zu anderen und zu sich selbst zu pflegen ist so unverzichtbar wie ein effizienter Glucosestoffwechsel oder ein optimales Lipoproteinprofil. Den emotionalen Haushalt in Ordnung zu halten ist genauso wichtig, wie eine Darmspiegelung oder einen Lp(a)-Test vornehmen zu lassen, wenn nicht noch wichtiger. Allerdings ist es sehr viel komplizierter.
Zwischen seelischer und körperlicher Gesundheit besteht eine Wechselbeziehung. In meiner Praxis erlebe ich jeden Tag aus erster Hand, dass viele körperliche und altersbedingte Probleme meiner Patienten ihren Ursprung in der seelischen Gesundheit haben oder von ihr verschärft werden. Wenn ein Patient mit Depressionen kämpft, ist es schwieriger, ihn zu einem Sportprogramm zu motivieren; wer beruflich überlastet ist und sich privat elend fühlt, hat vielleicht keine Lust, zur Krebsfrüherkennung zu gehen oder den Blutzuckerspiegel kontrollieren zu lassen. Und so lassen sie sich treiben, und die seelischen Qualen ziehen die körperliche Gesundheit mit in den Abgrund.
Ich selber erlebte allerdings im Grunde das Gegenteil: Ich tat alles dafür, um länger zu leben – nur mein Seelenleben war komplett aus den Fugen geraten. Etwa 2017 war ich körperlich so fit wie eh und je, aber was hatte ich davon? Mit mir ging es steil bergab – sowohl emotional als auch beziehungsmäßig. Praktisch jeden Tag klangen mir die Worte meiner Therapeutin Esther Perel in den Ohren: »Warum wollen Sie länger leben, wenn Sie so unglücklich sind?«
Eines hatte ich mit manchen meiner Patienten gemeinsam: Wir fanden es einfacher, uns gar nicht erst mit solch komplexen und erdrückenden Problemen zu beschäftigen. Ich wusste nicht einmal, wo ich anfangen sollte – nein, falsch –, ich habe nicht einmal gemerkt, dass ich Hilfe brauchte, obwohl es allen in meinem Umfeld längst klar war. Ich musste wirklich erst fast am Ende sein, um der Wahrheit ins Gesicht sehen zu können und zu The Bridge zu gehen, jenem gottverlassenen, problembeladenen, letztlich wunderbaren Ort in den Wäldern von Kentucky, und meine längst überfällige Arbeit aufzunehmen. Und so begann ich, das Handwerkszeug zu erwerben, das ich brauchte, um seelisch besser zu funktionieren.
Meine ersten Tage in The Bridge kamen mir wie Wochen oder Monate vor. Die Zeit dehnte sich endlos. Ich hatte kein Telefon, und meine Bücher hatten sie mir weggenommen. Das war Teil des Plans – man ließ uns in unserem Elend schmoren. Man konnte buchstäblich nichts anderes tun. Ich geisterte wie ein Zombie durch die täglichen Aktivitäten, von der einen Tasse Kaffee am Morgen über die Arbeit mit dem sogenannten inneren Kind bis zur Pferdetherapie. Mein einziger Trost war mein Work-out um halb fünf am Morgen, was zugleich auch die einzige Sucht war, der ich nach wie vor frönen durfte. Davon abgesehen gab es keine Gnade und keine Einsamkeit.
Vor meiner Ankunft hatte ich meine Sprechstundenhilfe beauftragt, in The Bridge anzurufen und um ein Einzelzimmer zu bitten. Man hatte sie mehr oder weniger ausgelacht. »Teilen Sie Ihrer very important person bitte mit, dass es das bei uns nicht gibt. Wir haben nur Zweibettzimmer.« Also bekam ich einen Zimmergenossen, der eigentlich ganz nett zu sein schien und auch ein paar coole Tattoos hatte, aber in meinem Eifer, über ihn (und alle anderen) sofort ein Urteil zu fällen, stachen mir nur die Unterschiede zu mir ins Auge. Er hatte keine Hochschulbildung. Er arbeitete in einer Maschinenwerkstatt. Er mochte Stripteasetänzerinnen und Kokain. Seine Frau hasste ihn – wobei das wohl doch etwas war, was wir damals gemeinsam hatten. Zuerst machte ich komplett dicht. Den größten Horror hatte ich vor den zweimal täglich stattfindenden Check-ins, wo wir genau beschreiben sollten, wie wir uns gerade fühlten. Das brachte ich einfach nicht fertig. Ich saß nur da und kochte vor Wut. Als es Mittwoch oder Donnerstag wurde, machten sich die anderen schon fast über mich lustig. Von allen anderen hatten wir zumindest ein paar Einzelheiten aus ihrer Lebensgeschichte erfahren, aber über mich wusste keiner auch nur das Geringste. Irgendwann sagte jemand: »Na komm, Dude, bist du so was wie ’n Serienmörder, oder was? Was ist los?«
Ich sagte nichts. Ich glaube, in dieser Nacht schlief mein Zimmergenosse nicht sehr gut.
Nach vier oder fünf Tagen musste ich dann aber mein Schweigen brechen. Fast ein ganzer Tag war dafür reserviert, dass alle ihre Lebensgeschichte von Anfang bis Ende erzählten. Jeder hatte eine Stunde Zeit dafür, und wir sollten uns darauf vorbereiten. Und so kam es, dass ich schließlich zum ersten Mal dieser Gruppe von wildfremden Leuten meine Lebensgeschichte offenbarte – nicht einmal Jill hatte ich alles erzählt. Aber ich blieb ganz sachlich: Das passierte, als ich fünf war, das passierte, als ich sieben war, und so weiter. Manches war sexueller Art, manches körperlicher. Aber es hatte nicht nur schlimme Seiten, und zumindest hatte mir niemand aus meiner Familie das angetan, erklärte ich. So schrecklich diese Erlebnisse auch gewesen seien, hätten sie mich dazu bewogen, mit dreizehn Jahren Boxen und Kampfsport aufzunehmen. Ich durfte Sandsäcke und Leute verprügeln und damit meine Wut abreagieren. Ich lernte, mich zu schützen, aber ich erwarb auch Disziplin und die Fähigkeit, mich zu fokussieren, was sich als unschätzbar erwies, als ich mit etwa neunzehn die Boxhandschuhe an den Nagel hängte und mich der Mathematik zuwandte.
So schlimm meine Vergangenheit auch gewesen sei, so fuhr ich etwas defensiver fort, habe sie mir doch den Weg gewiesen, Arzt zu werden. Während meiner Collegezeit als Mathematikstudent arbeitete ich ehrenamtlich in einer Anlaufstelle für Teenager, die sexuellen Missbrauch erfahren hatten, und baute innerhalb von vier Jahren zu zahlreichen von ihnen eine enge Beziehung auf. Eine davon war eine junge Frau, die von ihrem Vater missbraucht worden war. Obwohl dies nicht meiner Situation entsprach, konnte ich mich damit identifizieren. Als sie nach einem Selbstmordversuch – einem von vielen – im Krankenhaus lag, ging ich sie besuchen. Inzwischen hatte ich das Grundstudium abgeschlossen und mich bereits für Promotionsstudiengänge in Raumfahrttechnik beworben. Trotzdem war ich nicht ganz sicher, ob das meine wahre Bestimmung war. Die etlichen Stunden, die ich bei der jungen Frau im Krankenhaus verbrachte, führten mich schließlich zu der Erkenntnis, dass meine eigentliche Berufung nicht darin bestand, Gleichungen zu lösen, sondern Menschen zu helfen.
Man sähe also, so beschloss ich meinen Bericht, dass mein früheres Leben zum Teil zwar schlimm gewesen sei, aber mir gewissermaßen auch den Weg zu einem besseren Leben aufgezeigt habe. Einige Jungs, mit denen ich aufgewachsen sei und geboxt habe, säßen mittlerweile wegen bewaffneten Raubüberfalls im Knast und hätten auf der Highschool Mädchen geschwängert und auch sonst alles Mögliche angestellt. So hätte es mir auch ergehen können. In gewisser Hinsicht, sagte ich, habe mir der Missbrauch, den ich erfahren hätte, vielleicht sogar das Leben gerettet – eigentlich müsse ich jetzt gar nicht hier sein!
An dieser Stelle unterbrach mich Julie Vincent, eine der Therapeutinnen. In The Bridge gibt es viele Regeln, und eine der wichtigsten lautet, nicht zu bagatellisieren. Das gilt für alles, was eine andere Person sagt, und vor allem für die eigenen Erfahrungen. Sie ermahnte mich jedoch nicht, sondern fragte schlicht: »Sie waren fünf Jahre alt, als Ihnen das zum ersten Mal passiert ist, richtig?«
»Das stimmt«, antwortete ich.
»Und jetzt ist Ihr Sohn Reese fast fünf, richtig?«
Ich nickte.
»Sie behaupten also, es sei okay, dass Ihnen das passiert ist, als Sie so alt waren wie er – aber fänden Sie es okay, wenn irgendwer das Gleiche jetzt mit Reese machen würde?«
Eine andere Regel in The Bridge lautet, dass man jemandem, der weint, kein Taschentuch anbietet. Man soll selber aufstehen und sich eins holen. Nun war ich an der Reihe, aufzustehen und zur Kleenex-Box zu gehen. Es brach alles aus mir heraus, und endlich verstand ich, warum ich dort war und mich der harten Arbeit stellen musste, die letzten vierzig Jahre meines Lebens unter die Lupe zu nehmen.
Ein Instrument, mit dem die Therapeuten von The Bridge arbeiten und das ich hilfreich finde, ist der Trauma-Baum. Er gründet sich auf die Idee, dass bestimmte unerwünschte Verhaltensweisen, die wir im Erwachsenenalter zeigen, wie etwa Sucht und unkontrollierbare Wut, eigentlich Anpassungen an die verschiedenen Arten von Traumata sind, die wir in der Kindheit erlitten haben. Weil wir vom Baum nur das sehen, was sich über dem Erdboden befindet, also den Stamm und die Äste, müssen wir unter die Erdoberfläche schauen und die Wurzeln betrachten, um den Baum in seiner Gänze zu verstehen. Oft sind die Wurzeln aber tief verborgen, wie es bei mir der Fall war.
Im Wesentlichen gibt es fünf Arten von Traumata: (1) Missbrauch oder Misshandlung (körperlich oder sexuell, aber auch seelisch oder geistlich); (2) Vernachlässigung; (3) Verlassenheit; (4) Verstrickung (das Verschwimmen der Grenze zwischen Erwachsenen und Kindern); (5) Zuschauertrauma (durch Beobachten tragischer Ereignisse). Die meisten traumatischen Erlebnisse, die Kinder erleiden, fallen in diese fünf Kategorien.
»Trauma« ist ein bedeutungsschwerer Begriff. Wie uns die Bridge-Therapeuten erläuterten, gibt es Typ-I-Traumata und Typ-II-Traumata. Opfer einer Vergewaltigung erleiden ein Typ-I-Trauma, während Kinder mit einem alkoholabhängigen Elternteil womöglich zahlreichen Typ-II-Traumata ausgesetzt sind. In starker Dosierung über einen längeren Zeitraum können Typ-II-Traumata das Leben eines Menschen jedoch ebenso stark prägen wie ein einziges schwerwiegendes Ereignis.
Beide Arten können gravierende Schäden anrichten, doch Traumata vom Typ II sind schwerer zu behandeln – zum Teil, wie ich vermute, weil wir eher dazu neigen, sie herunterzuspielen. Jeff English, ein Therapeut, mit dem ich zusammengearbeitet habe, fasste es folgendermaßen zusammen: Ein Trauma, gleich ob Typ I oder II, bedeutet, dass man Momente wahrgenommener Hilflosigkeit erlebt hat. Wie er erklärte, muss es sich nicht unbedingt um eine Situation handeln, in der es um Leben und Tod geht, »aber für ein Kind mit einem noch unreifen Gehirn fühlt es sich möglicherweise so an«.
Das beschrieb perfekt, was ich in meiner Kindheit zuweilen gefühlt hatte. Mein Schmerz (und später im Leben meine Wut) war in großen Teilen auf das Empfinden von Machtlosigkeit zurückzuführen. Ich möchte aber auch auf den wichtigen Unterschied zwischen Trauma und Unglücklichsein hinweisen. Das ist nicht dasselbe. Ich will hier nämlich nicht darauf hinaus, dass Kinder idealerweise so aufwachsen, dass sie niemals irgendeine Art von Unglück erfahren, obwohl das in der modernen Kindererziehung mitunter ein Hauptziel zu sein scheint. Viele Stressfaktoren können auch nutzbringend sein; auf andere trifft das nicht zu. Zwischen Trauma und Unglücklichsein verläuft keine klare Linie. So schrecklich meine Erfahrungen waren, haben sie mich auf gewisse Weise doch stärker gemacht. Julies Frage ist ein guter Gradmesser: Würde ich wollen, dass mein Kind ebenfalls so etwas erlebt? Wenn beispielsweise meine Tochter beim Crosslauf als Allerletzte ins Ziel käme und ohne Medaille bliebe, wäre das okay. Klar, zunächst wäre sie natürlich schwer enttäuscht, aber das könnte sie auch motivieren, mehr zu trainieren, und falls sie irgendwann tatsächlich unter den ersten drei landen würde, könnte sie sich noch viel mehr darüber freuen. Nicht okay wäre, wenn ich sie vor versammelter Mannschaft runtergeputzt hätte, weil sie sich sogar von der Kleinsten aus der Mannschaft habe schlagen lassen.
Nebenbei bemerkt kam auch eine kluge Studie von 2019 zu dem Ergebnis, dass Rückschläge unter dem Strich positiv sein können. Das Forscherteam hatte junge Wissenschaftler ins Visier genommen, die sich um NIH-Stipendien beworben hatten, und sie in zwei Gruppen aufgeteilt: Die eine Gruppe hatte knapp die erforderliche Punktzahl für ein Stipendium erreicht, die andere war knapp darunter geblieben, sodass sie kein Stipendium erhielt. Während die Angehörigen der ersten Gruppe mit größerer Wahrscheinlichkeit kurz darauf der Wissenschaft wieder den Rücken kehrten, überflügelten diejenigen der zweiten Gruppe schließlich ihre Altersgenossen, die gleich beim ersten Versuch ein Stipendium erhalten hatten. Der frühe Rückschlag hatte ihrer Karriere nicht geschadet, sondern vielleicht den gegenteiligen Effekt gehabt.
Bei einem Kindheitstrauma ist das Wichtigste nicht das Ereignis an sich, sondern die Art und Weise, wie das Kind es bewältigt. Kinder sind erstaunlich belastbar, und verwundete Kinder werden zu Kindern, die sich gut anpassen können. Problematisch wird es, wenn diese anpassungsfähigen Kinder zu unangepassten, dysfunktionalen Erwachsenen werden. Die möglichen Formen dieser Dysfunktion werden durch die vier Äste des Trauma-Baums illustriert: (1) Sucht, nicht nur nach Lastern wie Drogen, Alkohol und Glücksspiel, sondern auch nach gesellschaftlich anerkannten Dingen wie Arbeit, Sport und Perfektionismus (passt!); (2) Co-Abhängigkeit oder übermäßige psychische Bindung an eine andere Person; (3) habitualisierte Überlebensstrategien, wie die Neigung zu Ärger und Wutanfällen (passt!); (4) Bindungsstörungen, also die Schwierigkeit, Kontakte zu knüpfen oder enge Beziehungen zu anderen Personen herzustellen (passt!). Diese Äste sind häufig kaum zu übersehen; kompliziert wird es, wenn man zu den darunterliegenden Wurzeln vordringt und versucht, sie zu entwirren. Dies alles hängt stark vom jeweiligen Menschen ab – jeder reagiert anders auf ein Trauma und hat ganz eigene Strategien, damit umzugehen. Und keineswegs gibt es so etwas wie eine Pille, die ein Trauma oder die betreffenden Bewältigungsstrategien mit einem Mal verschwinden lässt. Das erfordert harte Arbeit – und es kann, wie ich irgendwann begriffen habe, sehr viel Zeit in Anspruch nehmen.
Hier greift Medizin 2.0 häufig zu kurz: Die meisten Therapeuten orientieren sich bei ihrer Diagnose an der Bibel der geistigen Gesundheit, dem Diagnostic and Statistical Manual of Mental Disorders, 5. Auflage (DSM-5), einem 991-Seiten-Kompendium aller denkbaren psychischen Erkrankungen (in Deutschland orientiert man sich eher an der ICD-10, der internationalen statistischen Klassifikation der Krankheiten und verwandter Gesundheitsprobleme der WHO). Das DSM ist der kühne Versuch, die unzähligen Formen von psychischen Störungen zu strukturieren und zu kodifizieren – sie im Grunde in einen wissenschaftlichen Kontext zu betten und damit auch die Rückerstattung der Kosten durch die Krankenversicherung zu gewährleisten. Wie Paul Conti bemerkt, hat in der Realität jeder Patient jedoch seine ganz eigene, einzigartige Leidensgeschichte und Krankheit. Nicht alle fallen in übersichtlich sortierte diagnostische Kategorien. Jeder Mensch ist anders, jede Lebensgeschichte auch. Niemand ist ein »Code«. Darum, so Conti, ist eine solch rigorose Kodifizierung »ein Hindernis für das wirkliche Verstehen der Person«.
Aus diesem Grund ist es auch schwierig, zu diesem Thema allen Leuten allgemeingültige Ratschläge zu geben. Sie alle haben ihre ganz persönliche seelische Verfassung, ihre persönliche Geschichte und ihre persönlichen Probleme. Für uns alle aber gilt das Problem, dass Medizin 2.0 die geistige und seelische Gesundheit im Großen und Ganzen genauso behandelt wie alles andere auch: mit Diagnose, Rezept und, natürlich, Rechnung. Antidepressiva und andere Psychopharmaka haben zwar schon vielen Menschen, mich eingeschlossen, geholfen, aber damit eine vollumfängliche Lösung zu finden ist selten einfach. Zum einen handelt es sich in erster Linie um ein krankheitsbasiertes Modell, mit dem Medizin 2.0 auch andere Probleme, wie Infektionen und akute Erkrankungen, angeht und löst: Man behandelt die Symptome und schickt den Patienten wieder nach Hause. Oder wenn die Situation ernster ist, wie es bei mir der Fall war, überweist man den Patienten für ein paar Wochen an einen Ort wie The Bridge und schickt ihn dann wieder nach Hause – voilà, Problem gelöst.
Dieser Ansatz hat sich auf dem Feld der psychischen Erkrankungen als weniger wirksam erwiesen, weil geistige Gesundheit und seelische Gesundheit nicht dasselbe sind. Die geistige Gesundheit umfasst Zustände, die Krankheiten ähneln, wie klinische Depression und Schizophrenie, die komplex und schwer zu behandeln sind, aber tatsächlich mit erkennbaren Symptomen einhergehen. Hier interessieren wir uns jedoch mehr für seelische Gesundheit, die geistige Gesundheit zwar mit einschließt, aber noch weit darüber hinausgeht – und nicht so leicht zu kodifizieren und kategorisieren ist. Seelische Gesundheit hat mehr damit zu tun, wie wir mit unseren Gefühlen umgehen und unsere zwischenmenschlichen Beziehungen gestalten. Ich habe nicht an einer Geisteskrankheit im engeren Sinne gelitten, aber meine seelische Gesundheit war schwer angeschlagen, was mir im Grunde verwehrte, ein glückliches, ausgeglichenes Leben zu führen – und mein Leben möglicherweise sogar in Gefahr brachte. Solche Situationen zeigen Medizin 2.0 in gewisser Hinsicht ihre Grenzen auf.
Die Pflege unserer seelischen Gesundheit erfordert einen ähnlichen Paradigmenwechsel wie den von Medizin 2.0 zu Medizin 3.0. Gefragt ist langfristige Prävention, wie bei unserem Ansatz zur Prävention von Herz-Kreislauf-Erkrankungen. Wir müssen potenzielle Probleme frühzeitig erkennen und bereit sein, sie über einen langen Zeitraum hinweg sehr engagiert anzugehen. Zudem muss unser Ansatz auf jede einzelne Person mit ihrer ganz eigenen Geschichte und Problematik passgerecht zugeschnitten sein.
Unsere Medizin-3.0-These lautet: Wenn wir uns rechtzeitig um unsere seelische Gesundheit kümmern, haben wir bessere Chancen, klinischen psychischen Erkrankungen wie Depressionen und einer chronischen Angststörung aus dem Wege zu gehen – und auch unsere allgemeine Gesundheit wird davon profitieren. Es gibt jedoch nur selten eine rasche Heilung oder Behebung der Probleme, so wie sich auch Krebs oder Stoffwechselerkrankungen nicht im Handumdrehen beheben lassen.
Zur Pflege unserer seelischen Gesundheit sind dauerhafte Anstrengungen und tägliche Übung gefragt, so wie auch andere Aspekte unserer körperlichen Gesundheit von uns verlangen, dass wir regelmäßig Sport treiben, unsere Ernährung umstellen oder Schlafrituale einhalten. Entscheidend ist, möglichst proaktiv zu handeln, um unsere gesunde Lebenszeit in jeder Hinsicht auch auf die späteren Jahrzehnte des Lebens auszudehnen.
Ich denke, im Vergleich zur körperlichen Gesundheit stellt uns die seelische vor die Herausforderung, dass wir häufig nicht gleichermaßen deutlich erkennen, etwas ändern zu müssen. Wer übergewichtig und nicht in Form ist, weiß in den meisten Fällen, dass es angebracht wäre, etwas dagegen zu unternehmen. Ob man es tatsächlich schafft, steht auf einem anderen Blatt. Was hingegen die seelische Gesundheit betrifft, brauchen zahllose Menschen ganz dringend Hilfe, erkennen aber die Anzeichen und Symptome ihres Leidens nicht. Ich war ein Paradebeispiel dafür.
Nach zwei Wochen verließ ich The Bridge. Meinen Therapeuten war es nicht recht, dass ich so früh wieder ging. Sie hätten mich gern noch einen Monat länger dabehalten, aber ich hatte das Gefühl, in dieser relativ kurzen Zeit bereits einen Riesenschritt nach vorn getan zu haben. Mir meine Vergangenheit einzugestehen war eine große Sache für mich. Ich war voller Hoffnung, und schließlich willigten sie ein, mich zu entlassen. Und so flog ich einen Tag vor Weihnachten nach Hause.
Das war wahrscheinlich ein Fehler.
Ich würde gerne berichten, dass dies das Ende der Geschichte war, der Punkt, an dem sich der alte Peter mit seinem Egoismus und seiner Wut verabschiedete und der neue Peter seinen Platz einnahm und wir alle fortan glücklich und zufrieden miteinander lebten. Doch das war leider nicht der Fall. Es war bestenfalls das Ende vom Anfang.
Nach meiner Rückkehr hatte ich eine Menge zu tun – ich musste verarbeiten, was in The Bridge ans Tageslicht gekommen war, und versuchen, die Beziehung zu meiner Frau und meinen Kindern wieder in Ordnung zu bringen. Mit der Unterstützung von zwei wunderbaren Therapeutinnen, Esther Perel (Einzeltherapie) und Lorie Teagno (Paartherapie), machte ich in den darauffolgenden Wochen und Monaten langsame Fortschritte. Lorie und Esther fanden beide, dass mir ein männlicher Therapeut guttun würde, der mit mir ein Modell für ein gesundes männliches Gefühlsleben erarbeitete. Ich probierte mehrere gute Therapeuten aus, aber zu keinem hatte ich einen so guten Draht wie zu Jeff English, meinem wichtigsten Therapeuten in The Bridge.
Ich wollte schon aufgeben, als Esther mir Terrence Real’s Buch I Don’t Want to Talk About It (dt. »Mir geht’s doch gut«) empfahl, ein bahnbrechendes Werk über die Ursachen der männlichen Depression.[477] Sobald ich zu lesen begonnen hatte, konnte ich es nicht mehr aus der Hand legen. Es war fast gespenstisch, dass dieser Typ von mir zu schreiben schien, obwohl er mich nie gesehen hatte. Seine Hauptthese lautet, dass es für Außenstehende gemeinhin besser erkennbar ist, wenn Frauen an Depressionen leiden, während die Sozialisation bei Männern dafür sorgt, dass sie ihre Depressionen verbergen und in sich verschließen oder in Wut umwandeln und nie darüber reden wollen (worauf sich der englische Buchtitel bezieht). Mit den Geschichten von seinen Patienten konnte ich mich identifizieren. Und so begann ich, auch mit Terry an meinen Problemen zu arbeiten. Nachdem ich viel zu lange auf jegliche Therapie verzichtet hatte, ging ich nun gleich zu drei Therapeuten.
Terry war als Kind einer Arbeiterfamilie in Camden, New Jersey, aufgewachsen. Seinen Vater beschreibt er als »zärtlich«, »klug« und »brutal wie eine Naturgewalt«. Wie sich herausstellte, waren der Grund dafür die verborgenen Depressionen des Vaters, die er geschickt auf Terry übertrug. »Mein Vater prügelte mir seine Depressionen mit einem Gürtel ein«, erzählte er mir. Die Auseinandersetzung mit der Wut und Gewalttätigkeit des Vaters bewog ihn schließlich dazu, Psychotherapie zu studieren. »Ich musste mir einen Reim auf meinen Vater und seine Gewaltausbrüche machen, um nicht in das gleiche Muster zu verfallen«, sagte er.
Terry half mir, die Verbindungen zwischen meiner Kindheit und den Formen der Dysfunktion, die meine Jugend und mein Erwachsenenleben geprägt hatten, noch besser zu erkennen. Wenn ich heute auf mich als Teenager und Collegestudent zurückblicke, wird mir klar, dass ich ernsthaft depressiv war – im klinischen Sinne durch und durch depressiv. Damals wusste ich es nur nicht. Ich hatte die klassischen Symptome einer versteckten männlichen Depression: die Tendenz, mich zu isolieren, und vor allem die Neigung zu Wutanfällen, meine vielleicht mächtigste Sucht. Einer der ersten Sätze, die ich nach einem frühen Gespräch mit Terry in mein Tagebuch schrieb, klingt noch heute in mir nach: »Wutausbrüche von Männern sind zu 90 Prozent ein Zeichen von Hilflosigkeit, die sich als Frustration maskiert.«
Terry half mir, die Hilflosigkeit zu erklären, die ich nach wie vor spürte. Nach und nach verstand ich, dass der für mich entscheidende Faktor die Scham war, zum Opfer gemacht worden zu sein. Wie es bei vielen Männern der Fall ist, hatte ich diese Scham in ein Gefühl der Grandiosität verkehrt. »Scham fühlt sich schlecht an, Grandiosität fühlt sich gut an«, sagte er. »Diese Umkehrung vom unterlegenen Opfer zum überlegenen Rächer ist von zentraler Bedeutung für maskulines Auftreten und traditionelle Männlichkeit. Das Teuflische an dieser Umwandlung von Scham in Grandiosität ist, dass sie funktioniert. Kurzfristig bewirkt sie, dass man sich besser fühlt, aber langfristig sorgt sie für Chaos in deinem Leben.«
Noch schlimmer war die Erkenntnis, was ich meiner Familie, vor allem meinen Kindern, mit meinem Verhalten angetan hatte. Ich bildete mir damals nicht gerade ein, ein besonders guter Vater zu sein, aber ich war schon ein wenig stolz darauf, dass ich meine Kinder vor dem Trauma, das ich erlitten hatte, bewahren konnte. Ich war ein großartiger »Ernährer« und »Beschützer«. Sie würden nie die Art von Scham erdulden, die meine Kindheit geprägt hatte. Aber ich wusste, dass sie meine überschäumende Wut wahrnahmen, auch wenn sie sich nur selten gegen sie oder Jill richtete.
In The Bridge lernte ich, dass Kinder nicht logisch auf die Wut eines Elternteils reagieren. Wenn sie erleben, dass ich einen Autofahrer anbrülle, der mich gerade geschnitten hat, nehmen sie diesen Wutausbruch so auf, als habe er sich gegen sie gerichtet. Außerdem wird ein Trauma von einer Generation zur nächsten weitergegeben, auch wenn es sich nicht zwangsläufig manifestiert. Kinder von Alkoholikern sind nicht dazu verdammt, selber Alkoholiker zu werden, aber auf die eine oder andere Weise pflanzt sich das Trauma fort.
So schrieb Terry: »Durch den Mechanismus der übernommenen Scham und der übernommenen Gefühle wirkt der unerledigte Schmerz früherer Generationen in manchen Familien weiter wie eine emotionale Verschuldung. … Ein Mann, der die verinnerlichte Stimme der Verachtung verwandelt, stellt sich gegen die Gewalt … Ein solcher Mann dient sozusagen als Wellenbrecher. Die Wogen des Schmerzes, die viele Generationen zerstört haben, branden über ihn hinweg, verlieren ihre bösartige Kraft – und verschonen seine Kinder.«[478]
Dieser Mann wollte ich sein.
Mit der Unterstützung von Terry wie auch von Esther und Lorie entdeckte ich Stück für Stück einige Werkzeuge, die mir beim Umgang mit meiner Vergangenheit halfen und mein Verhalten von einem Tag zum anderen in bessere Bahnen lenkten. Terry verdankte ich ein nützliches Denkmodell: Ich sollte mir meine Beziehungen als empfindliches Ökosystem vorstellen. Warum sollte ich die Umwelt vergiften, in der ich leben musste?
Das klingt so einfach, aber es in die Tat umzusetzen verlangte mir einiges an Überlegung, ja sogar an strategischem Denken ab. Es bedeutete, mich jeden Tag aufs Neue oder gar stündlich von den Kleinigkeiten zu distanzieren, die mich an Leuten um mich herum üblicherweise rasend machten. Wie ich nun begriff, hatte dies das Trinkwasser in unserem Ökosystem vergiftet. Ich musste lernen, mit den Problemen und Frustrationen des Alltags anders umzugehen. In Terrys Therapiekonzept hat dieses Stadium des Lehrens und Lernens einen wichtigen Stellenwert: »So machst du es richtig. So musst du zuhören, wenn sich dein Partner beklagt, und einfühlsam sein.«
Terry erklärte es mir: »Dies alles sind Fertigkeiten. Und wie sämtliche Fertigkeiten, die du dir in deinem Leben angeeignet hast, kannst du die auch lernen.«
Manches, was ich änderte, klingt total banal. Ich achtete darauf, jeden Tag, an dem ich zu Hause war, Zeit mit meinen Kindern zu verbringen – mit jedem einzelnen, und ohne aufs Handy zu sehen. Ich fragte Jill jeden Tag, wie es ihr ergangen war (nicht danach, was sie »erlebt« hatte). Ich setzte mir ein striktes Zeitfenster für die Nutzung des Handys und meine Arbeitsstunden. An einem Tag in der Woche, meistens Samstag oder Sonntag, arbeitete ich überhaupt nicht – womit ich gegen eine jahrzehntelange tief verwurzelte Angewohnheit anging. Noch erstaunlicher war, dass Jill und ich tatsächlich zum ersten Mal seit Jahren richtig Urlaub machten, nur wir beide, ohne Kinder.
Eine etwas kompliziertere Fertigkeit, an der ich mich abmühte, nennt sich »Reframing«. Damit ist im Wesentlichen die Fähigkeit gemeint, eine bestimmte Situation aus dem Blickwinkel einer anderen Person zu betrachten – sie buchstäblich in einen anderen Rahmen zu stellen. Den meisten Menschen fällt das unsagbar schwer, wie David Foster Wallace es 2005 in seiner mittlerweile berühmten Rede »This Is Water« (dt. »Das hier ist Wasser«) den Absolventen des Kenyon College erläutert hat:[479]
Meine unmittelbare Erfahrung stützt meine tief sitzende Überzeugung, dass ich der absolute Mittelpunkt des Universums bin, der echteste, lebendigste und bedeutendste existierende Mensch. Wir denken selten über diese natürliche, grundlegende Selbstzentriertheit nach, weil sie sozial so abstoßend ist, aber im Grunde ist sie bei uns allen so ziemlich gleich. Sie ist unsere Standardeinstellung, die mit der Geburt in unseren psychischen Festplatten verdrahtet wird. Überlegen Sie mal: Sie haben nie eine Erfahrung gemacht, bei der Sie nicht im absoluten Mittelpunkt standen. Die Welt, die Sie erfahren, liegt vor Ihnen oder hinter Ihnen, links oder rechts von Ihnen, auf Ihrem Fernseher, Ihrem Monitor oder sonst wo. Die Gedanken und Gefühle anderer Leute müssen Ihnen irgendwie kommuniziert werden, aber Ihre eigenen sind unmittelbar, zwingend und wirklich.
Darin erkannte ich mich wieder. Das war, solange ich denken konnte, immer meine Standardhaltung gewesen. Es ist verlockend, meine traumatische Geschichte dafür verantwortlich zu machen und die Notwendigkeit, mich zu schützen, aber offensichtlich war der Schuss irgendwann nach hinten losgegangen. Leichter gesagt als getan verlangt Reframing, einen Schritt von der jeweiligen Situation zurückzutreten und sich dann zu fragen: Wie nimmt eine andere Person diese Situation wahr? Wie geht es ihr damit? Und warum sollte deine Zeit, deine Bequemlichkeit, dein Vorhaben wichtiger sein als ihre?
Das erweist sich praktisch jeden Tag als hilfreich. Wenn beispielsweise meine Frau nach Hause kommt und sauer ist, weil ich nicht geholfen habe, die Einkäufe wegzuräumen, würde ich normalerweise gleich denken: Hey, ich hab verdammt viel zu tun und kann nicht immer sofort parat stehen! Und dann würde das Gefühl in mir aufwallen, dass ich alles Recht der Welt habe, so zu denken, weil ich nun mal verdammt viel zu tun habe und jemand anders die Einkäufe wegräumen kann.
Aber dann frage ich mich: Moment mal, wie hat denn Jills Tag ausgesehen?
Sie musste unsere Jungs von der Schule abholen und mit ihnen zum Supermarkt fahren, wo sich die beiden vermutlich wie die Kesselflicker gestritten haben, sodass jeder im Laden dachte, Jill sei ja wohl die mieseste Mutter der Welt, weil sie nicht in der Lage sei, diese verzogenen kleinen Bälger zu bändigen, während sie an der Feinkosttheke anstand, um für mich das in perfekte Scheiben geschnittene köstliche Fleisch zu kaufen, das man abgepackt so nicht bekommt, und auf der Heimfahrt quälte sie sich von einer roten Ampel zur nächsten, während sich die Jungs mit Legosteinen bewarfen.
Und wissen Sie was? Sobald ich mich in sie hineinversetze, kann ich mich selbst zurücknehmen und erkenne, dass ich derjenige bin, der egoistisch ist und es beim nächsten Mal besser machen sollte. Das bewirkt Reframing. Man begreift, dass man von einer Situation ein wenig Abstand gewinnen muss, reflexartige Reaktionen zügeln und versuchen zu erkennen, was eigentlich vor sich geht.
Irgendwann, als ich über längere Zeit beruflich unterweges war, fiel mir in einem Flughafen David Brooks’ Buch The Road to Character (dt. »Charakter – Die Kunst, Haltung zu zeigen«) in die Hände.[480] Im Flugzeug las ich den Abschnitt über die zentrale Unterscheidung zwischen »Lebenslauf-Tugenden«, womit die Leistungen gemeint sind, die wir bei einer Bewerbung auflisten, wie Studienabschlüsse, Stipendien und bisherige Jobs, und »Trauerreden-Tugenden«, also das, was unsere Familie und Freunde über uns sagen, wenn wir gestorben sind. Und das erschütterte mich zutiefst.
In meinem ganzen Leben hatte ich fast ausschließlich Lebenslauf-Tugenden gesammelt. Davon konnte ich eine Menge vorweisen. Kürzlich war ich aber auch auf der Beerdigung einer Frau in meinem Alter gewesen, die an Krebs gestorben war, und es hatte mich sehr berührt, wie liebevoll und bewegend ihre Familie von ihr gesprochen hatte – und ihre beeindruckenden Erfolge im Beruf und in der Ausbildung kaum erwähnte. Was für sie zählte, war der Mensch, der sie gewesen war, und was sie für andere, vor allem für ihre Kinder, getan hatte.
Würde irgendwer auch so über mich sprechen, wenn ich zur letzten Ruhe gebettet wurde?
Das bezweifelte ich. Und ich beschloss, dass sich das ändern musste.
Ich fing an, all diese Werkzeuge und Strategien täglich anzuwenden, und entwickelte eine Art Seelische-Gesundheits-Routine. Ich legte den Fokus nicht mehr auf Lebenslauf-, sondern auf Trauerreden-Tugenden. Ich bemühte mich, mehr für meine Familie da zu sein und verwandtschaftliche Beziehungen zu pflegen. Ich übte mich in Reframing. Aber irgendetwas fühlte sich immer noch falsch an. Selbst als ich an der Beziehung zu den Menschen arbeitete, die mir am nächsten standen, gab es da nach wie vor einen großen blinden Fleck: meine Beziehung zu mir selbst. Ich war ein viel besserer Ehemann und Vater geworden, aber innerlich ging ich mit mir so unerbittlich wie eh und je zu Gericht. Der tief verwurzelte Selbsthass und die Verachtung, die ich mir gegenüber empfand, vergifteten nach wie vor fast alle meine Gedanken und Gefühle, und ich bemerkte es nicht einmal und verstand nicht, was da vor sich ging.
Ich weiß, dass ich mit diesem Gefühl nicht allein war. Einmal sprach ich mit einem meiner Patienten, einer ausgesprochen erfolgreichen und bekannten Person, und er sagte etwas Schockierendes: »Ich muss großartig sein, damit ich mich nicht wertlos fühle.«
Ich war sprachlos. Selbst er fühlte sich so?
Doch meine Unsicherheit und der Selbsthass nagten weiter an mir. Ich konnte zwar einige Fortschritte vorweisen, was meinen Umgang mit anderen Menschen betraf, aber zu mir selbst blieb ich so hart, wie ich es immer gewesen war. Die Wut gewann stets die Oberhand, auch wenn ich scheinbar Spaß hatte. Schon nach einem Fehlschuss beim Bogenschießen oder wenn ich in meinem Fahrsimulator aus der Kurve flog, stieg eine brodelnde Wut über mich selbst in mir hoch. Ich verlor ständig die Geduld mit mir und flippte aus, brüllte los und zerbrach sogar Pfeile über meinem Oberschenkel, wenn ich danebenschoss. Das war zwar schmerzhaft, aber ich hörte nicht damit auf.
Es war, als hause in meinem Hirn mein persönlicher Bobby Knight, der Basketballtrainer der Indiana University, der für seine cholerischen Ausraster an der Seitenlinie berüchtigt war (und deswegen schließlich seinen Job verlor). Sobald ich einen Fehler beging oder das Gefühl hatte, eine schlechte Leistung abzuliefern, auch wenn es um Kleinigkeiten ging, sprang mein innerer Coach von der Bank und brüllte mich nieder. Ein Lapsus beim Kochen? »Du bist ja nicht mal in der Lage, ein beschissenes Steak zu braten!« Die Aufnahme von einem Podcast-Intro vermasselt? »Du bist ein wertloser Sack Scheiße, der nicht verdient zu leben, und erst recht nicht, einen Podcast zu haben!«
Das Verrückte daran ist, dass ich tatsächlich glaubte, diese innere Stimme tue mir etwas Gutes. Ich sagte mir, diese Wut und der Selbstzweifel hätten mich zu vielen schönen Erfolgen getrieben. Sie seien halt der Preis dafür. Aber in Wirklichkeit hatte ich einfach nur weitere Lebenslauf-Tugenden gesammelt. Und darauf war ich nicht einmal stolz. Es würde niemals gut genug sein.
Zum ersten Mal in meinem Leben kam mir ein radikaler Gedanke: Wen kümmert es, wie gut du performst, wenn du solch ein Kümmerling bist?
Damals witterte Paul Conti, der den Niedergang meiner seelischen Gesundheit als mein Freund nach wie vor im Auge hatte, dass sich wieder ein Sturm zusammenbraute. Er schlug einen weiteren längeren Aufenthalt in einer anderen Klinik vor. The Bridge war mir eine große Hilfe gewesen – ohne sie hätte ich meine Familie verloren. Aber Paul meinte, ich hätte mich nach zwei Wochen zu früh entlassen und sei darum noch nicht zum Kern der Dinge vorgedrungen, was meine Beziehung zu mir selbst betraf. Doch ich blieb stur. »Es wird schon alles gut werden.«
Etwas musste in Bewegung geraten, und bald darauf war es so weit.
Wäre 2020 ein Jahr wie jedes andere gewesen, hätte ich meine Misere wahrscheinlich noch ein paar Jahre länger aussitzen können und wäre irgendwie damit durchgekommen. Nichts bringt unter dem Deckel gehaltene Probleme jedoch so zuverlässig zum Überkochen wie eine Krisensituation.
Als Covid zuschlug, waren die Kapazitäten unserer Praxis bereits erschöpft. Wir nehmen die meisten neuen Patienten in den ersten beiden Quartalen des Jahres auf, und so quoll meine mentale Festplatte mit den individuellen Besonderheiten all dieser Fälle bereits über. Covid verdoppelte oder verdreifachte unsere Arbeitsbelastung mit einem Schlag. Täglich gab es Telefonkonferenzen mit dem Wissenschaftlerteam, um alles zu besprechen, was wir über die Krankheit herausfinden konnten. Frühmorgens ging es los, und dazu gab es noch eine brandaktuelle und beängstigende Welle von Podcasts zu Covid. Ich gab meine morgendliche Meditation auf, um die zahllosen Anrufe von Patienten zu beantworten, die verständlicherweise in Panik waren und beruhigt werden wollten.
Als der März in den April überging, wurde klar, dass kein Ende in Sicht war. Eines Tages Ende April 2020, beim routinemäßigen morgendlichen Telefongespräch mit meiner Praxismanagerin, hielt ich es plötzlich nicht mehr aus und explodierte. »Ich hab den Überblick verloren«, erklärte ich ihr. »Ich kriege die Krankengeschichten unserer Patienten nicht mehr auf die Reihe. War das Patient X oder Patient Y, der mir erst letzte Woche erzählt hat, dass seine Tochter Schwierigkeiten in der Schule hat? War es Patientin A oder Patientin B, bei der ich mich heute Abend melden sollte?« Sie versuchte mich zu beruhigen und sagte, unter den gegebenen Umständen würde ich mein Bestes tun, und unsere Patienten seien dankbar. Doch je länger sie redete, desto wütender wurde ich.
Und von einem Moment zum anderen steigerte ich mich in einen drastischen, selbstzerstörerischen Anfall, wie ich ihn vorher und auch danach nie erlebt habe. Selbst heute ist die Erinnerung daran immer noch furchterregend. Ich warf einen Tisch quer durch unser Wohnzimmer. Ich riss mein T-Shirt in Fetzen. Ich schrie vor Wut und Schmerz. Meine Frau bettelte mich an, das Haus zu verlassen, weil sie Angst hatte, ich würde ihr oder den Kindern etwas antun. Ich dachte daran, gegen einen Brückenpfeiler oder sonst was zu fahren, um mich umzubringen. Ich war mir sicher, komplett zerstört zu sein, eine Fehlkonstruktion. Wenn eine Autopsie von meinem Gehirn gemacht würde, würden sie sehen, wie verkorkst ich war. Da gab’s rein gar nichts mehr zu reparieren. Nichts konnte das wieder in Ordnung bringen.
Schließlich verkroch ich mich in einem Motel und telefonierte mit Paul, Esther und Terry. Sie bestanden darauf, dass ich in eine Einrichtung wie The Bridge fahren sollte. Sofort. Erwartungsgemäß weigerte ich mich hartnäckig und behauptete, ich käme klar, wenn ich nur noch etwas mehr Zeit und Unterstützung hätte, ich müsste bloß nach Hause fahren und mich ausruhen. Nach achtundvierzig Stunden mit inständigen Bitten und Ermahnungen lenkte ich endlich ein. Mitten in der Nacht fuhr ich nach Phoenix, Arizona, und wurde von einem Beratungszentrum namens Psychological Counseling Services (PCS) aufgenommen.
Terry hatte mir fast ein Jahr lang vom PCS erzählt. Wie er sagte, war dies ein Ort, der Wunder bewirkte und Wunden heilte, die unheilbar schienen. Ich fragte ihn, warum er da so sicher sei. Er sagte, ich solle ihm einfach vertrauen.
Genau wie bei meinem Aufenthalt in The Bridge vor zweieinhalb Jahren brauchte ich ein paar Tage, um mich zurechtzufinden. Weil die Pandemie erst vor Kurzem ausgebrochen war, war ich allein. Per Zoom stand ich täglich zwölf Stunden in Kontakt mit meinen Therapeuten, während ich in einer kleinen Airbnb-Wohnung saß, die ein paar Kilometer von der Einrichtung entfernt war.
Erst in der zweiten Woche zeigten sich erste Fortschritte. Langsam akzeptierte ich, dass ich ein Gebäude aus Perfektionismus und Arbeitssucht errichtet hatte, das von Säulen aus leistungsbasierter Wertschätzung getragen wurde. Die ganze Konstruktion ruhte auf einem Fundament aus Scham, die teilweise von meinem Trauma herrührte und teilweise ein Erbteil war, weil sich die Scham nahestehender Personen auf die Kinder überträgt. All das wurde jedoch noch verschärft durch den Teufelskreis aus Selbsthass und Schuldgefühlen über mein Verhalten. Es ist kein Zufall, dass ich immer zu Sportarten tendiert habe, die Perfektion verlangen, wie Bogenschießen und Autorennen.
Schließlich verbrachte ich drei Wochen beim PCS – einundzwanzig quälende Tage ohne Unterbrechung –, in denen ich die Arbeit, die ich in The Bridge begonnen hatte, zu Ende brachte und dabei viel weiter kam, als ich mir jemals hätte vorstellen können. Wir beackerten ein riesiges Terrain, aber eine Aufgabe überforderte mich völlig. An meinem zweiten Tag sollte ich, meinen Lebensjahren entsprechend, siebenundvierzig positive Aussagen über mich aufschreiben. Ich brachte circa fünf oder sechs zustande, aber dann ging nichts mehr. Tag für Tag fiel mir absolut nichts Gutes ein, was ich über mich sagen konnte. Mein Perfektionismus und meine Scham verboten mir, irgendetwas Nettes über mich zu denken. Es ging einfach nicht.
Und dann, am neunzehnten Tag – einem glühend heißen Mittwochmorgen – geschah es. Ich hatte Marcus, einem von meinen Therapeuten, bereits vorher etwas erzählt, und nun versuchte er, mehr darüber aus mir herauszulocken. Mit etwa sieben Jahren wollte ich plötzlich meine Geburtstage nicht mehr feiern. Wie ich ihm verriet, hielt ich meinen Geburtstag tatsächlich immer noch »geheim«, als ich schon weit über zwanzig war. Seine Fragen führten mir vor Augen, dass sich ein gesundes Kind nicht so verhalten würde und dahinter vermutlich etwas noch Schlimmeres verborgen war. Er bohrte immer weiter nach und ließ nicht locker.
Die daraufhin plötzlich einsetzende Erkenntnis stürzte meine Gefühle in einen freien Fall. Zweieinhalb Jahre hatte sie in mir gegärt, und nun war ich endlich so weit, loszulassen und die Wahrheit über meine Vergangenheit und die Art und Weise, wie sie mich geformt hatte, zu akzeptieren, ohne jede Entschuldigung oder Rationalisierung. Alles, was ich geworden war – im Guten und im Schlechten –, war eine Reaktion auf das, was ich erlebt hatte. Es war auch nicht einfach ein Typ-I-Trauma; aus versteckten Winkeln holten wir unzählige weitere Typ-II-Traumata ans Tageslicht, die mich noch tiefer getroffen hatten. Ich war nicht beschützt worden. Ich hatte mich nicht sicher gefühlt. Mein Vertrauen war von Menschen missbraucht worden, die mir nahestanden. Ich fühlte mich allein und verlassen. All dies hatte sich in mir, als ich erwachsen wurde, in Selbsthass verwandelt – ich war zu meinem ärgsten Feind geworden. Und nichts davon hatte ich verdient. Das war die wichtigste Erkenntnis. Jener kleine, liebe Junge hatte nichts davon verdient. Und er war immer noch da.
Sobald ich dies alles akzeptiert hatte, fiel es mir leicht, die siebenundvierzig Aussagen aufzuschreiben:
Ich bin unvollkommen, aber nicht wertlos.
Ich bin ein guter Ehemann und Vater.
Ich bin ein guter Koch.
Ich muss mich nicht für mich schämen.
Ich werde einen Weg finden, mich zu lieben.
Die Sätze strömten nur so aus mir heraus. Ich fühlte mich an eine Beobachtung von Jacob Riis, dem großen dänisch-amerikanischen Journalisten und Sozialreformer, erinnert:
»Wenn nichts zu helfen schien, ging ich zu einem Steinmetz, um zuzuschauen, wie er wohl hundertmal auf seinen Felsblock einhämmerte, ohne dass sich auch nur der kleinste Riss zeigte. Doch beim hundertsten Schlag zersprang er in zwei Teile, und ich wusste, dass das nicht dieser Schlag bewirkt hatte, sondern alle vorigen zusammen.«[481]
Wie mir in der Rückschau auf all dies klar geworden ist, lautet eine der wichtigsten Lektionen, die ich gelernt habe, dass der in diesem Kapitel beschriebene innere Wandel nur möglich ist, wenn wir mit einem Satz wirksamer Werkzeuge und Sensoren ausgestattet sind, mit denen wir unser seelisches Gleichgewicht überwachen, aufrechterhalten und wiederherstellen können. Diese Werkzeuge und Sensoren sind nicht angeboren. Wir müssen sie meist erst erlernen, verfeinern und täglich erproben. Und sie eignen sich nicht für schnelle Reparaturen.
Es stimmt, dass Medikamente wie Antidepressiva und Stimmungsstabilisierer helfen können. Und es stimmt, dass regelmäßige Achtsamkeitsmeditation vieles erleichtern kann. Zudem können chemische Verbindungen wie MDMA (früher synonym mit »Ecstasy«) und Psilocybin, wenn sie unter professioneller Anleitung und in einem geeigneten Umfeld eingenommen werden, äußerst wirksam sein. Ich habe beide in kritischen Phasen meiner Genesung mit bemerkenswertem Erfolg verwendet. Doch zu häufig beobachte ich, dass Menschen all ihre Hoffnungen auf Veränderung einzig und allein auf einen Ketamintrip setzen oder eine Reise in den peruanischen Dschungel mit einem Schamanen, der sie durch das bewusstseinserweiternde Erleben einer Ayahuasca-Trance geleitet, oder auf irgendeine andere singuläre Erfahrung (oder auch, dass sie sich, wie ich damals, einbilden, zwei Wochen in einer Einrichtung wie The Bridge seien ausreichend und danach könne man einfach weitermachen, als habe sich nichts Grundlegendes verändert).
All diese Möglichkeiten sind wirkungsvoll und theoretisch hilfreich, aber sie sind lediglich Ergänzungen der tief greifenden und oft sehr unangenehmen, unbequemen, zuweilen quälend langsamen – oder auch zu rasanten – Selbsterkundung, die eine echte Psychotherapie erfordert. Wahre Genesung verlangt, die Abgründe zu sondieren, die uns geformt haben, zu verstehen, wie wir uns daran angepasst haben und wie diese Anpassungen uns nun helfen (oder auch nicht, wie in meinem Fall). Auch das braucht Zeit, wie ich schmerzhaft lernen musste. Der größte Fehler ist, sich für »geheilt« zu halten, wenn man ein paar Monate ein Medikament genommen oder eine Handvoll Therapiesitzungen hinter sich gebracht hat, obwohl in Wahrheit nicht einmal die Hälfte der Strecke zurückgelegt ist.
Meine Fortschritte nach der Rückkehr vom PCS gründeten sich auf tägliche Übung, was großenteils unangenehm war. Die drängendste Herausforderung lautete schlicht, einen weiteren Ausraster wie denjenigen zu vermeiden, der mir den Weg zum PCS gewiesen hatte. Davor hatte ich schon andere, weniger heftige Wutausbrüche gehabt, aber dieser hatte sich wie eine Explosion angefühlt. Ich musste an die Raumfähre Challenger denken, die 1986 kurz nach dem Start über dem Atlantik auseinanderbrach.
Diese Katastrophe schien damals völlig unerwartet geschehen zu sein, doch eine langwierige Untersuchung offenbarte, dass das keineswegs der Fall war. Schon über Jahre hatte es im Shuttle-Programm zunehmend Warnzeichen und Systemausfälle gegeben. Die Ingenieure hatten diese Probleme dokumentiert, aber das Management ignorierte oder verheimlichte sie, weil das »einfacher« schien, als den Start zu verschieben. Das Ergebnis war eine Katastrophe, die hätte verhindert werden können. Mein Ziel war es, die Warnzeichen und Systemausfälle, die in meinem Leben zu einer Katastrophe führen konnten, erkennen zu lernen, damit sich so etwas wie damals nie mehr wiederholte. Im Grunde steht dahinter dieselbe Idee, die wir im Hinblick auf Medizin 3.0 bereits erörtert haben, nur dass es jetzt um die seelische Gesundheit geht: Man muss mögliche Probleme früh erkennen und so bald wie möglich präventive Maßnahmen ergreifen.
Mein Vorgehen dabei und das von mir verwendete Instrumentarium stützen sich auf eine Psychotherapieform namens Dialektisch-Behaviorale Therapie (DBT) oder dialektische Verhaltenstherapie, die in den 1980er-Jahren von Marsha Linehan entwickelt wurde. Sie geht auf die Prinzipien der kognitiven Verhaltenstherapie zurück, die den Patienten neue Wege aufzeigen möchte, über ihre Probleme nachzudenken und auf sie einzuwirken. Die DBT sollte Menschen mit schwerwiegenderen und potenziell gefährlichen Störungen helfen, wie der Unfähigkeit, Emotionen zu regulieren, und der Tendenz, sich zu verletzen oder sogar Selbstmordversuche zu begehen. Diese Probleme werden unter dem Oberbegriff der Borderline-Persönlichkeitsstörung zusammengefasst, einer Art Sammeldiagnose. Die DBT hat sich jedoch auch bei weniger dramatischen und gefährlichen seelischen Gesundheitsproblemen als hilfreich erwiesen, die sehr viel mehr Menschen betreffen. Ich ziehe da, natürlich, gerne die Formel 1 zum Vergleich heran: Die Rennstrecke ist ein Labor mit hohem Einsatz und hohem Risiko, in dem Autohersteller Technologien entwickeln und testen, die nach und nach zu unseren alltäglichen Gebrauchsfahrzeugen durchsickern.
An der DBT gefällt mir, dass für die Therapie Fakten sprechen: Laut klinischen Studien trägt sie dazu bei, suizidale und sich selbst verletzende Patienten von ihren gefahrvollen Handlungen abzuhalten.[482] Darüber hinaus vermittelt sie nicht nur theoretisches Wissen, sondern ist kompetenzorientiert. Bei einer DBT macht man jeden Tag mit einem Therapeuten Übungen aus einem Arbeitsbuch. Manchmal liegt mir praktisches Handeln besser als Denken. In der DBT lernt man in Wiederholungen unter Stress konkrete Fertigkeiten, mit dem Ziel, die Kettenreaktion negativer Reiz -> negative Emotion -> negatives Denken -> negatives Handeln zu durchbrechen.
Die DBT besteht aus vier Säulen, die ein übergreifendes Motiv miteinander verbindet. Dieses übergreifende Motiv ist Achtsamkeit, die die Auseinandersetzung mit den vier anderen Themen ermöglicht: Emotionsregulation (Kontrolle über unsere Gefühle gewinnen), Frustrationstoleranz (die Fähigkeit, mit psychischer Belastung umzugehen), zwischenmenschliche Fertigkeiten (die Fähigkeit, anderen Personen unsere Bedürfnisse und Gefühle mitzuteilen) und Selbstmanagement (Verantwortung für sich selbst zu übernehmen, beginnend mit grundlegenden Aufgaben wie rechtzeitigem Aufstehen, um zur Arbeit oder in die Schule zu gehen). Da ich insbesondere an den beiden ersten – Emotionsregulation und Frustrationstoleranz – arbeiten muss, habe ich mich mit meinem Therapeuten Andy White darauf konzentriert.
Ich stelle mir meine Frustrationstoleranz als Schiebefenster vor, das sich vertikal öffnen und schließen lässt. Je enger die Fensteröffnung wird, desto mehr droht eine Dysregulation. Mein Ziel ist, das Fenster möglichst weit offen zu halten und sehr sorgsam auf alles zu achten, was die Öffnung verkleinert – auch Faktoren, die außerhalb meiner Kontrolle liegen (siehe Abbildung 15).
Es gibt viele Verhaltensweisen, die das Fenster weiter öffnen: Sport, gesunder Schlaf, gute Ernährung, Zeit mit meiner Familie, Medikamente wie Antidepressiva oder Stimmungsstabilisierer, enge soziale Beziehungen, Aufenthalt in der Natur und Freizeitaktivitäten ohne Selbstbewertung. Diese Dinge kann ich kontrollieren. Weniger Kontrolle habe ich über Dinge, die die Fensteröffnung verkleinern, aber einige kann ich trotzdem beeinflussen – zum Beispiel das übertriebene Engagement für Projekte und zu häufiges Ja-Sagen. Fast täglich bemühe ich mich gedanklich und praktisch, dieses Fenster so weit wie möglich offen zu halten (indem ich etwa lerne, Nein zu sagen).
Die Fertigkeiten sind miteinander verknüpft – um meine Emotionen unter Kontrolle zu halten, musste ich meine Frustrationstoleranz stärken. Und je besser ich meine Emotionen reguliere, desto weniger bin ich auf die Öffnung des Toleranzfensters angewiesen. Als ich an diesen beiden Fertigkeiten arbeitete, merkte ich, dass sich meine zwischenmenschliche Kompetenz, die offenkundig alles andere als perfekt war, ganz von selbst verbesserte. Mit Selbstmanagement hatte ich nie große Schwierigkeiten, aber anderen geht es vielleicht nicht so – die DBT ist da sehr anpassungsfähig.
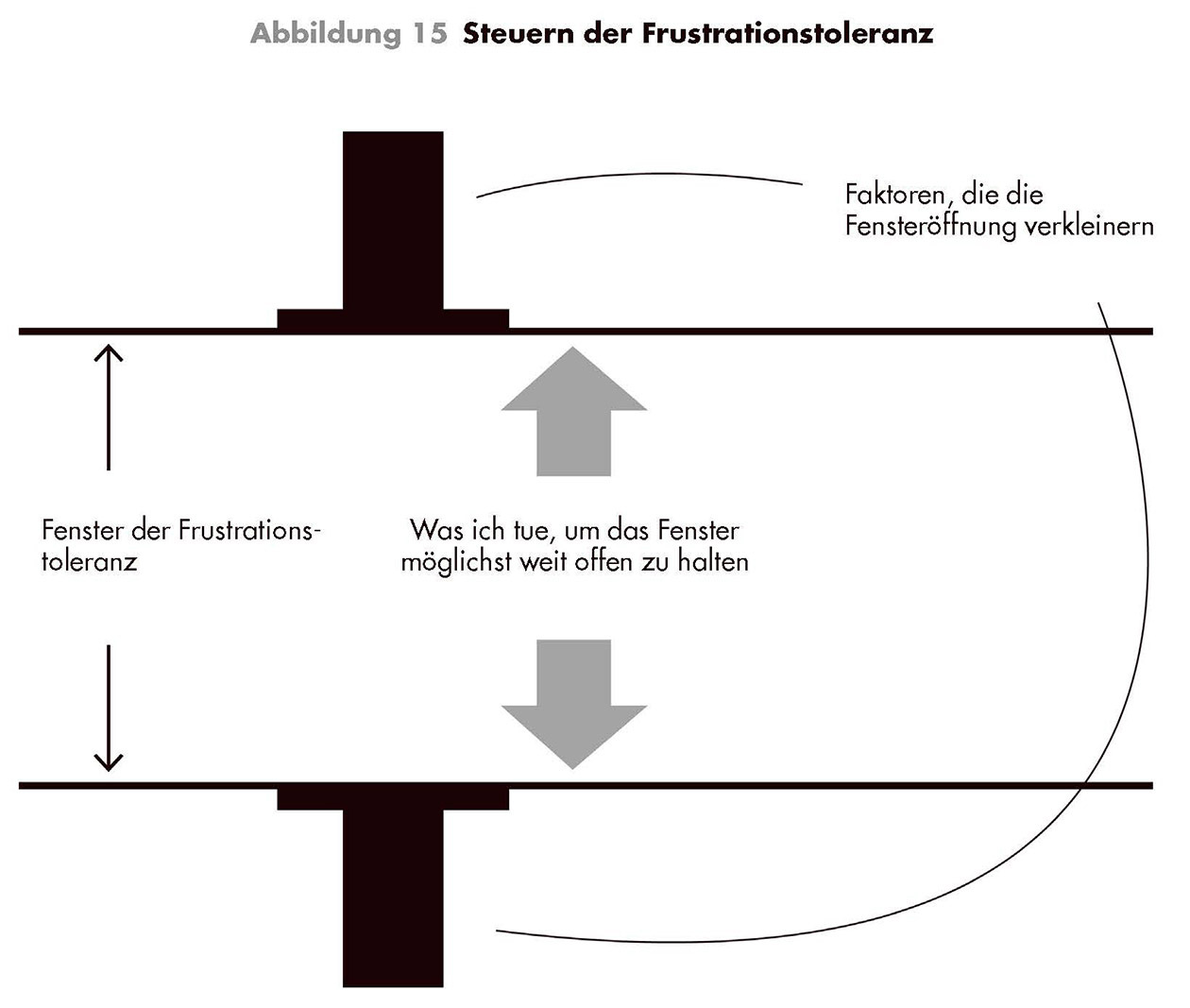
Die hier dargestellte »Fensteröffnung« oder Lücke illustriert, wie ich mir meine täglichen Bemühungen vorstelle, um meine Frustrationstoleranz zu wahren und zu stärken. Ich versuche, alles dafür zu tun, um das Fenster so weit wie möglich off en zu halten.
Das Fundament der DBT ist Achtsamkeit. Das war eines von diesen gefühlsduseligen Modewörtern, die ich immer verabscheute, bis ich begriff, dass sich dahinter tatsächlich ein ungeheuer wirksames Instrument verbarg, um eine Distanz zwischen meinen Gedanken und meinem Selbst zu schaffen, ja sogar ein bisschen Luft zwischen irgendeinem Reiz und meiner reflexartigen Reaktion darauf. Genau das brauchte ich.
Seit ich The Bridge verlassen hatte, hatte ich Achtsamkeitsmeditation praktiziert und dabei eher gemischte Resultate erzielt. Nun aber gelangen mir gelegentliche Blitze der Erkenntnis, Momente, in denen es mir gelang, mich von meinen Gedanken und Gefühlen zu lösen. Damit ist keine vollständige Distanzierung gemeint, in dem Sinne, dass man komplett abtaucht. Man versucht vielmehr, zwischen Reiz und Reaktion so viel Abstand herzustellen, dass man nicht reflexartig auf Ereignisse reagiert – etwa auf einen Autofahrer, der uns den Weg abschneidet, oder irgendeinen Ärger oder mögliche Sorgen. Dieser Abstand erlaubt es uns dann, ruhiger und rationaler mit der Situation umzugehen. Müssen wir wirklich hupen und fluchen und damit alles vielleicht noch schlimmer machen (selbst wenn der Typ es verdient hätte)? Oder sollte man einfach akzeptieren, was passiert ist, und weiterfahren? Beim Reframing hilft uns Achtsamkeit: Möglicherweise hat es der andere Fahrer ja eilig, weil er mit einem kranken Kind ins Krankenhaus will.
Achtsamkeit führt uns noch etwas anderes vor Augen: Wenn wir uns schlecht fühlen, hat das selten einen unmittelbaren realen Grund – wie etwa ein herabstürzender Felsbrocken, der genau in diesem Augenblick unser Bein zerschmettert. Viel häufiger liegt es daran, dass wir an ein schmerzliches Ereignis aus der Vergangenheit denken oder uns Sorgen machen, dass in Zukunft etwas Schlimmes geschieht. Auch das war für mich eine wahre Offenbarung. Einfach gesagt, empfinde ich weniger Schmerz, wenn ich erkenne, dass die Quelle des Schmerzes in meinem eigenen Kopf sitzt. Diese Erkenntnis war nicht neu, aber berührte mich tief. Rund 2500 Jahre vor mir hatte bereits Buddha gesagt: »Dein schlimmster Feind kann dir nicht so viel Schaden zufügen wie deine eigenen unkontrollierten Gedanken.« Im 1. Jahrhundert nach Christus setzte Seneca noch einen drauf: »Öfter leiden wir unter der Vorerwartung als unter der Wirklichkeit.« Und später, im 16. Jahrhundert, bemerkte Shakespeares Hamlet: »An sich ist nichts weder gut noch böse, das Denken macht es erst dazu.«
Das gilt offenkundig auch für die Art und Weise, wie wir über uns selber denken. Wie klingt unser innerer Dialog? Ist er freundlich, nachsichtig und weise oder harsch und verurteilend, wie mein innerer Bobby Knight? Eine der nachhaltigsten Übungen, die ich praktiziert habe, war schlicht, mir meine Selbstgespräche anzuhören. Immer wenn ich etwas getan hatte, was eine Selbstbewertung nach sich ziehen konnte, wie Bogenschießen oder ein Rennen in meinem Fahrsimulator oder auch nur die Zubereitung des Abendessens, nahm ich eine Sprachmemo an mich selbst auf und schickte sie meinem Therapeuten. In diesen Situationen war ich üblicherweise instinktiv versucht, mich anzuschreien, weil ich irgendwas falsch gemacht hatte. Mein Therapeut beim PCS sagte, ich solle mir vorstellen, dass nicht ich, sondern mein bester Freund genau das Gleiche getan hätte. Wie würde ich dann mit ihm reden? Würde ich ihn genauso beschimpfen, wie ich mich so oft abkanzelte? Natürlich nicht.
Das war ein etwas anderer Reframing-Ansatz, der mich zwang, aus mir selbst herauszutreten und das Missverhältnis zwischen meinen »Fehlern« (geringfügig) und der Art, wie ich mit mir selbst über diese Fehler sprach (brutal), unmittelbar zu beobachten. Das machte ich täglich unzählige Male etwa vier Monate lang. Sie können sich vorstellen, wie viel Speicherplatz das auf meinem Handy beanspruchte. Mit der Zeit wurde mein innerer Bobby Knight immer zahmer, und heute kann ich mich kaum noch daran erinnern, wie seine Stimme früher geklungen hatte.
Ein weiteres wichtiges Ziel der DBT ist die Unterstützung beim Regulieren der eigenen Emotionen. Als ich bei The Bridge ankam, war ich kaum in der Lage zu erkennen, wie ich mich fühlte, und erst recht nicht, meinen Gefühlszustand zu ändern oder zu beeinflussen. Alles, was ich wahrnahm, war überschäumende Wut. Das spitzte sich zu Beginn der Covid-Pandemie zu, als ich schließlich so überlastet und überfordert war, dass ich explodierte. Ich verlor komplett die Kontrolle über meine Gefühle. Mein guter Freund Jim Kochalka, ein klinischer Psychologe, bezeichnet diese Art von emotionaler Dysregulation als »Entzündung der Psyche«, was für mich sehr stimmig klingt.
Diese Wut hatte schon lange meine Beziehungen belastet, sogar innerhalb meiner Familie. Wie Terry Real schon viel früher hervorgehoben hatte, wurzelte die Wut in meiner Scham, doch sehr oft sorgte meine Wut ihrerseits dafür, dass die Scham noch größer wurde. Wenn ich beispielsweise meine Kinder anbrülle, vor allem, wenn ich mich eigentlich über etwas anderes aufrege, schäme ich mich. Diese Scham hindert mich dann daran, offen mit ihnen zu reden und mich zu entschuldigen, und dann schäme ich mich noch mehr. Es ist, als würde ich mir selbst ein immer tieferes Loch graben, und das geht mir nicht nur mit meinen Kindern so. Solange ich nicht zu einer Versöhnung fähig bin und mein Verhalten eingestehe, komme ich nicht weiter. Das war früher ein noch viel größeres Problem. Mittlerweile erkenne ich zumindest sofort die Gefahr, bevor das Loch zu tief wird.
Die DBT vermittelt vielerlei Techniken, um die Frustrationstoleranz aufrechtzuerhalten und zu verbessern sowie die eigenen Gefühle wahrzunehmen und sie in den Griff zu bekommen – statt von ihnen beherrscht zu werden, wie es bei mir so lange der Fall war. Eine einfache Taktik, die ich bei aufsteigendem inneren Aufruhr anwende, ist ein abrupter neuer Sinnesreiz – ich spritze mir meist Eiswasser ins Gesicht. Wenn es wirklich kritisch wird, nehme ich eine kalte Dusche oder steige in ein Eisbad. Diese simple Maßnahme stimuliert einen wichtigen Hirnnerv, den Vagusnerv, der dann dafür sorgt, dass sich Puls und Atemfrequenz verlangsamen, und uns in einen ruhigen, parasympathischen Modus versetzt (und aus dem sympathischen Kampf-oder-Flucht-Modus herausholt). Maßnahmen wie diese helfen häufig, sich neu zu fokussieren und eine Situation mit mehr Ruhe und eher konstruktiv zu betrachten. Eine weitere Technik, die ich mittlerweile sehr gerne anwende, ist langsames, tiefes Atmen – vier Sekunden einatmen, sechs Sekunden ausatmen, dann wiederholen. Mit der Atmung entspannt sich auch das Nervensystem.
Zudem ist wichtig festzuhalten, dass die DBT keine passive Therapie ist. Sie erfordert täglich bewusstes Denken und Handeln. Was ich als besonders hilfreich empfinde, ist opposite action, »entgegengesetztes Handeln«. Das bedeutet, wenn ich den Impuls verspüre, etwas Bestimmtes zu tun (im Allgemeinen nichts Sinnvolles oder Positives), zwinge ich mich, stattdessen genau das Gegenteil davon zu tun. Das bewirkt, dass sich auch meine zugrunde liegenden Gefühle ändern.
Die erste praktische Erfahrung damit machte ich an einem schönen Sonntagnachmittag kurz nach unserem Umzug nach Austin. Ich hatte meiner Frau versprochen, mir einen Tag in der Woche, wahrscheinlich Sonntag, freizunehmen, um ihn mit der Familie zu verbringen. Der Sonntag kam, und ich versank in Arbeit. Ich war total gestresst und mies drauf und wollte nichts und niemanden sehen oder hören. Ich wollte einfach nur in Ruhe weiterschuften. Jill, die mein selbstsüchtiges Verhalten nur zu gut kannte, erhob kaum Einwände, als ich sagte, ich hätte zu viel zu tun, um mit den Kindern zu einem nahe gelegenen kleinen Fluss zu fahren. Doch als ich zusah, wie sie die Kinder in den Minivan bugsierte, erkannte ich die perfekte Gelegenheit, Theorie in Praxis umzuwandeln. Ich rannte raus, sprang auf den Vordersitz und sagte: »Los geht’s!« Wir fuhren zum Barton Creek, wo wir nichts Spektakuläres unternahmen – wir wanderten umher, flitschten Steine übers Wasser und versuchten, von einem Felsbrocken zum anderen zu springen, ohne nass zu werden. Zu meiner großen Überraschung schlug meine Stimmung ins komplette Gegenteil um. Auf dem Rückweg bestand ich sogar darauf, bei einem Imbiss Burger und Pommes (!) zu essen.
Das sieht nach einer leichten Aufgabe aus. Wer würde nicht lieber mit seinen Kindern spielen, statt zu arbeiten? Aber für den alten Peter wäre das ein Ding der Unmöglichkeit gewesen. Diese kleine Lektion, die ich seitdem Tausende Male in die Tat umgesetzt habe, hat mir etwas sehr Wichtiges vor Augen geführt: Das eigene Verhalten zu ändern, kann auch die Laune ändern. Man muss nicht darauf warten, dass sich die eigene Stimmung hebt, um eine Verhaltensänderung herbeizuführen. Aus diesem Grund greifen kognitive Verhaltenstherapien mitunter zu kurz – nur über Probleme nachzudenken hilft vielleicht nicht, wenn unser Denken selbst gestört ist.
Sportliche Betätigung ist ein weiterer bedeutsamer Bestandteil meines seelischen Gesundheitsprogramms, vor allem das in Kapitel 12 beschriebene Rucking. Wenn ich mir Zeit nehme, mich in der Natur zu bewegen, einfach nur den Wind im Gesicht zu spüren und im Frühling den Duft der knospenden Blätter einzuatmen (und das alles mit einem schweren Rucksack auf dem Rücken), komme ich dem nahe, was Ryan Holiday als »Stille« beschreibt, die Fähigkeit, inmitten all der Ablenkungen, die die Welt uns bietet und die wir uns selber schaffen, innere Ruhe zu bewahren und fokussiert zu bleiben. Wenn meine Familie mitkommt, schweißt uns das ganz besonders eng zusammen. Wandere ich allein, dient Rucking mir als Achtsamkeitsübung, als eine Art Wandermeditation. Kein Handy, keine Musik, keine Podcasts. Nur die Geräusche der Natur und mein schweres Atmen. Auch auf diese Weise kann uns Aktivität in einen besseren geistigen Zustand überführen. Und wie Michael Easter mir erklärt hat, weisen Forschungen darauf hin, dass die fraktalen geometrischen Muster in der Natur physiologischen Stress abbauen helfen, was sich auch in einem EEG niederschlägt.[483]
Die bei Weitem wichtigste »Taktik« ist meine regelmäßige wöchentliche Therapiesitzung (als ich das PCS verließ, waren es noch drei oder vier pro Woche). Die ist nicht optional. Jede Sitzung beginnt mit einem körperlichen Check-in: Wie fühle ich mich? Wie habe ich geschlafen (wichtig!)? Habe ich körperliche Schmerzen? Gibt es Konflikte? Danach sezieren und diskutieren wir die Ereignisse und Probleme der vergangenen Woche in allen Einzelheiten. Kein Thema ist zu banal. Wenn ich mich zum Beispiel über eine Fernsehshow oder einen Film so richtig aufgeregt habe, sollten wir genauer hinschauen. Wir behandeln aber auch die großen, übergreifenden Probleme, die meine Krise überhaupt erst ausgelöst haben. Die Therapiesitzungen ergänze ich durch Einträge in mein Tagebuch, wobei ich üben kann, meine Gefühle zu artikulieren und zu verstehen, ohne mit etwas hinterm Berg zu halten. Ich bin fest davon überzeugt, dass diese Arbeit mit einem ausgebildeten Therapeuten durch nichts ersetzbar ist.
Meistens bemühe ich mich, all die genannten Verhaltensweisen zu üben, auch wenn ich keine große Lust dazu habe oder zu beschäftigt mit anderen Dingen bin. Jeden Tag mache ich Fehler und jeden Tag versuche ich, sie mir zu verzeihen. Manche Tage sind besser als andere, aber im Laufe der Zeit habe ich spürbare Fortschritte gemacht. Festzuhalten ist, dass die Aktivitäten und Verhaltensweisen, die mir helfen, für andere Personen vielleicht weniger geeignet sind, und selbst meine sehen heute anders aus als in den ersten sechs Monaten, nachdem ich das PCS verlassen hatte. In der DBT-Literatur heißt es, man müsse etwas finden, was Spaß macht und »mit den eigenen Werten übereinstimmt«. Jeder hat andere Probleme und eine andere geistige Verfassung, und jeder kann Lösungen finden, die zu ihm passen. Die Techniken der DBT sind anpassungsfähig und flexibel und darum für ganz verschiedene Menschen von Nutzen.
Zumindest eines sollte Ihnen meine Geschichte sagen: Wenn ich mich ändern kann, können Sie das auch. Der Ausgangspunkt von allem ist die schlichte Überzeugung, dass reale Veränderungen möglich sind. Das ist der wichtigste Schritt. Ich habe geglaubt, ich sei der grässlichste, unverbesserlichste, jämmerlichste Trottel der zivilisierten Welt. Solange ich zurückdenken kann, war ich der Meinung, ich sei durch und durch verkorkst und meine Fehler von Natur aus in mich einprogrammiert. Unwiderruflich. Erst als ich zumindest den Gedanken zuließ, dass ich vielleicht doch kein Monster bin, war ich in der Lage, das Bild von mir, das um ein Haar mein Leben und alle mir nahestehenden Menschen zerstört hätte, Stück für Stück neu zu gestalten.
Dies ist der entscheidende Schritt. Sie müssen daran glauben, dass Sie sich ändern können – und dass Sie ein besseres Leben verdienen.
Dieser Schritt fällt vielen Menschen jedoch aus ganz unterschiedlichen Gründen ungeheuer schwer – das soziale Stigma, das nach wie vor mit geistiger und seelischer Gesundheit verbunden ist, ist nur einer davon. Für viele Menschen, und zu ihnen zählte ich auch, ist es schwierig zu erkennen, dass sie ein Problem haben, zuzugeben, dass sie Hilfe brauchen, und dann aktiv zu werden – insbesondere wenn das bedeutet, offen mit anderen darüber sprechen zu müssen, sich eine berufliche Auszeit zu nehmen oder die Behandlungskosten zu tragen.
Doch diese und andere Einstellungen müssen sich ändern, wenn wir etwas gegen die Epidemie seelischer Gesundheitsstörungen unternehmen wollen, wie auch gegen Drogenkonsum, Alkoholmissbrauch, Essstörungen, Selbstmord und Gewalt, die damit einhergehen. Es muss okay sein, sich verletzlich zu zeigen, um Hilfe zu bitten und sie zu erhalten.
Ich habe mich ewig dagegen gewehrt, Hilfe zu suchen. Erst als ich mit unerträglichen Folgen konfrontiert wurde – meine Familie zu verlieren oder mich umzubringen –, war ich widerstrebend bereit, das zu tun, was ich schon viel eher hätte tun sollen, und auf meine seelische Gesundheit ebenso zu achten wie – schon immer – auf die körperliche.
Als ich in die nächste Phase meiner Genesung eintrat, wurde mir langsam etwas bewusst, was ich nie zuvor erlebt hatte: Ich fand es schöner, etwas zu sein, als etwas zu tun. Zum ersten Mal in meinem Leben hatte ich das Gefühl, dass ich ein guter Vater sein konnte. Ich konnte ein guter Ehemann sein. Ich konnte ein guter Mensch sein. Letzten Endes ist dies doch der eigentliche Sinn des Lebens. Und der eigentliche Grund, um länger besser zu leben.
Ich denke oft an ein Zitat von Paulo Coelho: »Vielleicht geht es auf deiner Reise gar nicht darum, irgendetwas zu werden. Vielleicht geht es darum, alles, was du nicht bist, abzustreifen, sodass du das sein kannst, wofür du bestimmt bist.«
Epilog
Erst nachdem ich sehr viel über alle meine Erlebnisse nachgedacht hatte, dämmerte mir, auf welche Weise die seelische Gesundheit mit Langlebigkeit zusammenhängt und inwiefern mir meine Reise geholfen hat, eine neue Perspektive zu finden.
Meine Herangehensweise an Langlebigkeit und Gesundheit war lange ein Ansatz à la Silicon Valley gewesen – ich glaubte, man könne unsere Biologie hacken, wieder und wieder, bis aus uns jene perfekten kleinen Humanoiden würden, die hundertzwanzig Jahre alt werden. Auf diesen Gedanken fuhr ich voll ab, bastelte und experimentierte ständig an neuen Fastenprotokollen oder Schlafgeräten herum, um meine Langlebigkeit zu maximieren. Alles in meinem Leben musste optimiert werden. Und Langlebigkeit war im Wesentlichen ein technisches Problem. So glaubte ich wenigstens.
Es brauchte fünf Jahre, zwei stationäre Behandlungen und den drohenden Verlust von Frau und Kindern, um mir die Augen zu öffnen. Was ich nach dieser langen und sehr schmerzlichen Reise endlich erkannte, war, dass Langlebigkeit sinnlos ist, wenn du ein mieses Leben führst. Oder wenn du keine engen Beziehungen aufbauen kannst. Nichts davon zählt, wenn deine Frau dich hasst. Nichts davon zählt, wenn du ein beschissener Vater bist oder Wut oder Sucht dich auffressen. Auch dein Lebenslauf spielt keine große Rolle, wenn die Zeit für deine Grabrede gekommen ist.
Um all das musst du dich kümmern, wenn es sich lohnen soll, länger zu leben – denn die wichtigste Größe in der Langlebigkeitsgleichung ist das Warum. Warum wollen wir länger leben? Für was? Für wen?
Eigentlich war ich von Langlebigkeit nur deshalb so besessen, weil ich Angst vor dem Sterben hatte. Und dass ich Kinder hatte, befeuerte diese Besessenheit noch. Ich rannte vor dem Tod davon, so schnell ich konnte. Doch zugleich verpasste ich es ironischerweise zu leben. Vielleicht hätte mir meine Taktik mit optimaler Glucoseregulation und einem idealen Lipoproteinspiegel tatsächlich ein längeres Leben beschert, aber die Enttäuschungen, die ich meiner Strategie verdankte, überwogen. Körperlich und geistig war ich großartig in Form, aber meine seelische Gesundheit lag am Boden.
Am meisten bedauere ich, dass so viel von dem Elend, das ich selbst erlebte, und dem Schmerz, den ich anderen Menschen zufügte, hätte vermieden werden können, wenn ich das alles früher, viel früher besser verstanden hätte. Das Traurigste ist, dass ich derart viel Zeit damit vergeudet habe, so distanziert, unglücklich und auf einem falschen Weg zu sein. So lange auf der Jagd nach einem sinnlosen Ziel.
Doch im Laufe meiner Genesung bemerkte ich, dass meine Gedanken nicht mehr unablässig ums Sterben kreisten. Meine Suche nach Langlebigkeit fühlte sich nicht mehr wie eine düstere, verzweifelte Aufgabe an. Nun empfand ich die Dinge, die ich täglich tat, als willkommen, als notwendig. Ich bereicherte mein Leben, und freute mich auf die Zukunft. Mein Ziel, länger gesund zu leben, lag klar und deutlich vor mir und hatte endlich Sinn und Zweck.
Ich fühlte mich an etwas erinnert, was mein lieber Freund Ric Elias einmal zu mir gesagt hatte. Ric war einer der 155 Menschen an Bord des US-Airways-Fluges gewesen, das im Januar 2009 auf dem Hudson River notwassern musste. Als das Flugzeug sich dem Boden näherte, waren Ric und die meisten anderen Passagiere sicher, dass sie sterben würden. Nur das Geschick des Flugkapitäns und eine Riesenportion Glück verhinderten eine Katastrophe. Wäre das Flugzeug nur ein wenig schräger oder schneller gewesen, wäre es beim Aufprall auf die Wasseroberfläche auseinandergebrochen; mit ein paar Knoten weniger wäre das Flugzeug mit der Nase voran im Fluss versunken. Einige winzige Kleinigkeiten entschieden darüber, ob alle Menschen an Bord überlebten oder ob viele oder die meisten (oder alle) starben.
Dieser Tag veränderte Rics Einstellung zur Langlebigkeit auf dieselbe Weise wie bei mir. All die Jahre war ich von Langlebigkeit aus dem falschen Grund besessen gewesen. Ich dachte nicht an ein langes, gesundes Leben, das vor mir liegen würde. Stattdessen betrauerte ich die Vergangenheit. Ich war gefangen in dem Schmerz, den mir meine Vergangenheit zugefügt hatte und immer noch zufügte. Ich glaube, ich wollte länger leben, weil ich tief in mir wusste, dass ich ein längeres Rollfeld brauchte, um die Dinge in Ordnung zu bringen. Doch ich schaute nicht nach vorne, sondern nur zurück.
»Ich glaube, man wird alt, wenn man nicht mehr über die Zukunft nachdenkt«, sagte Ric zu mir. »Wenn du wissen willst, wie alt jemand wirklich ist, hör ihm zu. Wenn er von der Vergangenheit spricht und von all den Dingen, die passiert sind und die er getan hat, ist er alt. Wenn er über seine Träume nachdenkt, über seine Ziele, über das, worauf er sich immer noch freut – dann ist er jung.«
Ein Hoch auf das Jungbleiben beim Älterwerden!
Dank
Um ein Haar hätte dieses Buch nie das Licht der Welt erblickt. Anfang 2020 zeigten mir mein Agent und mein Verlag die rote Karte, weil ich das Manuskript nach einem Jahr Verspätung immer noch nicht eingereicht hatte. Danach hatte ich keine Lust mehr, weitere Arbeit hineinzustecken, und beschloss, das ganze Projekt in den Wind zu schießen. Etwa neun Monate blieb der Entwurf unangetastet, bis mein Freund Michael Ovitz mich fragte, ob er ihn lesen dürfe. Einige Wochen später rief Michael mich an, weil er meinte, das Manuskript habe großes Potenzial und solle veröffentlicht werden. Er schlug meinem Co-Autor Bill Gifford und mir vor, eine korrigierte Fassung an seine Freundin Diana Baroni bei Penguin Random House zu schicken. Hätte sich Michael nicht dahintergeklemmt, mich mit Diana bekannt gemacht und den Vertrag mit Penguin Random House unter Dach und Fach gebracht, wäre Outlive vielleicht immer noch irgendein Google Doc, das außer Bill und mir nur eine Handvoll anderer Leute kennen würden. Ich danke Diana dafür, dass sie erkannte, was aus diesem leicht ramponierten Manuskript werden könnte, und noch mehr für ihre Anleitung auf dem Weg dorthin.
Ohne Bills Unterstützung wäre dieses Buch schon viel früher im Ansatz gescheitert. Mitte 2017, nachdem ich im Alleingang rund 30 000 Wörter zu Papier gebracht hatte, bescheinigte mir mein damaliger Verlag, der Entwurf sei zu technisch; ich als Person sei überhaupt nicht sichtbar, und man könne meinen Weg, auf dem ich nach und nach die Relevanz der Langlebigkeit erkannte, nicht nachvollziehen. Sie rieten mir, einen Co-Autor zu suchen, und so begann eine lange Suche, die schließlich zu Bill führte. Von ihm hatte ich bereits einen Artikel über Rapamycin gelesen, den er 2015 verfasst hatte, sowie sein Buch Spring Chicken (dt. »Jung bleiben«). Ich hatte das Gefühl, er sei der Richtige, um mir bei der Bewältigung einer richtig schweren Aufgabe zu helfen – dieses komplexe Thema korrekt sowie nuanciert und detailliert zu vermitteln, während es zugleich für ein breiteres Publikum leicht lesbar und zugänglich war. Er war, um es mit seinen eigenen Worten zu sagen, mein Übersetzer. Während unserer Zusammenarbeit wurden wir gute Freunde. Zuweilen sah er meine dunkelsten Seiten, aber auch die besten, wie ich hoffe.
Ich wüsste nicht, wie ich dieses Buch ohne die Unterstützung von Bob Kaplan zuwege gebracht hätte. Bob war von 2015 bis 2021 mein Forschungsleiter; er war unverzichtbar beim Zusammentragen und Durchforsten aller Studien, die Eingang in das Buch gefunden haben, aber auch beim Verwerfen von Ideen und indem er mich zwang, stringenter zu denken. Als sei das noch nicht genug, unterbrach Bob 2022 seinen Ruhestand und übernahm die Herkulesaufgabe, die Anmerkungen einzufügen. Gemeinsam mit Vin Miller erledigte Bob zudem großenteils den Faktencheck, während Rachel Harrus, Sam Lipman und Kathryn Birkenbach mich bei einigen Recherchen unterstützten.
Was mich in jener Zeit wirklich verblüffte, war die Großzügigkeit, mit der Leute mir ihre Zeit schenkten und mit mir ihr Wissen teilten. Viele Teile des Manuskripts schickte ich mit der Bitte um Feedback an einschlägige Experten. Ausnahmslos alle, die ich fragte, waren dazu bereit. Den folgenden Personen kann ich gar nicht genug danken: Kellyann Niotis und Richard Isaacson (neurodegenerative Erkrankungen), Matt Walker und Vik Jain (Schlaf), Lew Cantley und Keith Flaherty (Krebs), Layne Norton, David Allison und Kevin Bass (Ernährung), Steve Austad (Kalorienrestriktion), Nir Barzilai (Hundertjährige), Matt Kaeberlein und David Sabatini (Rapamycin, mTOR) sowie Beth Lewis, die mir eine große Hilfe war, als ich (immer und immer wieder) versuchte, etwas Sinnvolles über Stabilität zu schreiben.
Sehr viel, worüber ich hier geschrieben habe, geht auf den Austausch mit meinen Patienten und den Gästen in meinem Podcast zurück. Die Erfahrungen meiner Patienten waren die Grundlage, das Rohmaterial für dieses Buch, und sie halten mir stets vor Augen, dass man nie aufhören soll zu lernen. Aus diesem Grund gibt es meinen Podcast The Drive: Er zwingt mich und mein Team zum Lernen in halsbrecherischer Geschwindigkeit. Das Wissen, das ich mir Woche für Woche in den Interviews meiner Fachleute aneigne, ist auch in viele der vorangegangenen Kapitel eingeflossen.
Auch den brillanten Wissenschaftlern und Ärzten, die mir in meiner beruflichen Laufbahn zur Seite gestanden haben, bin ich zu Dank verpflichtet. Genauso dankbar, wenn nicht noch mehr, bin ich Paul Conti, der mich gedrängt hat, zu The Bridge zu gehen, und den Therapeuten, die mir das Leben gerettet haben: Esther Perel, Terry Real, Lorie Teagno, Katy Powell, Andy White, Jeff English und dem gesamten Team vom PCS.
Mehrere Freunde haben ebenfalls frühe Kapitelentwürfe gelesen und mir wertvolle Hinweise gegeben: Rosie Kurmaniak, Deb und Hugh Jackman, David Buttaro, Jason Fried und Judith Barker.
Vielleicht wissen Sie noch nicht (oder mittlerweile doch), dass ich ein wenig speziell bin. Darum war es nicht einfach, ein Cover zu gestalten, das wirklich »passte«. Wunderbarerweise waren Rodrigo Corral und sein Team zur Stelle, und Bill und ich waren uns einig, dass sie ein Cover designten, das den Inhalt des Buches treffend widerspiegelte. Sie bewiesen eine Engelsgeduld und ertrugen mein Mikromanagement bei allen Details ohne einen Muckser.
Eines der größten Probleme beim Schreiben des Buches war schlicht, Zeit dafür zu finden. Das klinische Team unseres Onlineprogramms Early Medical machte viele Überstunden, damit ich über längere Zeiträume ungestört arbeiten konnte. Lacey Stenson managt mein privates und berufliches Leben bis ins Kleinste und tat alles dafür, um das Buch zu realisieren. Ohne Lacey hätten alle Züge Verspätung. Nick Stenson betreut nicht nur jeden Aspekt unseres digitalen und Podcast-Contents – er war auch für die Markteinführungsstrategie für das Buch und ihre Realisierung verantwortlich, was sich als sehr viel komplexer erwies, als wir beide erwartet hatten.
Zuletzt und ganz besonders möchte ich Jill danken. Sie erlebte mit mir alle Höhen und Tiefen und unterstützte mich in jedem einzigen Augenblick, obwohl jeder andere vernünftige Mensch mich mit Fug und Recht in die Wüste geschickt hätte. Du hast das Seil nie losgelassen! Olivia, Reese und Ayrton sahen ihren Daddy abends und am Wochenende zu oft vor dem Computerbildschirm sitzen und baten mich immer wieder, weniger zu arbeiten. Nun, da das Buch geschrieben ist, kann ich ihnen endlich geben, was ihnen zusteht.
Bill Gifford
Ich möchte Martha McGraw für ihre Freundlichkeit danken und dafür, dass sie mir im Lauf dieses langen und zuweilen mühsamen Projekts mit Rat und Tat zur Seite gestanden hat. Ohne dich hätte ich es nicht geschafft. Danke auch an Bob Kaplan für die Unmengen an Recherchen und die Erläuterungen zu vielen komplexen Themen. Und an meinen Freund Stephen Dark für all die Spaziergänge.
Bibliografie
AAA Foundation. (2016). 2015 Traffic Safety Culture Index. https://aaafoundation.org/2015-traffic-safety-culture-index/
Abbasi, F., Chu, J. W., Lamendola, C., McLaughlin, T., Hayden, J., Reaven, G. M. and Reaven, P. D. (2004). Discrimination between obesity and insulin resistance in the relationship with adiponectin. Diabetes 53, 585–590. https://doi.org/10.2337/diabetes.53.3.585
Abdelhamid, A. S., Martin, N., Bridges, C., Brainard, J. S., Wang, X., Brown, T. J., Hanson, S., Jimoh, O. F., Ajabnoor, S. M., Deane, K. H. O. et al. (2018). Polyunsaturated fatty acids for the primary and secondary prevention of cardiovascular disease. Cochrane Database Syst. Rev. 11, CD012345. https://doi.org/10.1002/14651858.CD012345.pub3
ACS (American Cancer Society). (2022a). Breast Cancer Statistics | How common is breast cancer? Last revised January 12. https://www.cancer.org/cancer/breast-cancer/about/how-common-is-breast-cancer.html
ACS (American Cancer Society). (2022b). Colorectal cancer facts and figures, 2020–2022. https://www.cancer.org/content/dam/cancer-org/research/cancer-facts-and-statistics/colorectal-cancer-facts-and-figures/colorectal-cancer-facts-and-figures-2020-2022.pdf
ACS (American Cancer Society). (2022c). Eating well during treatment. March 16. https://www.cancer.org/treatment/survivorship-during-and-after-treatment/coping/nutrition/once-treatment-starts.html
ACSM (American College of Sports Medicine) (2017). ACSM’s guidelines for exercise testing and prescription. Philadelphia: Lippincott Williams and Wilkins
Alghamdi, B. S. (2018). The neuroprotective role of melatonin in neurological disorders. J. Neurosci. Res. 96, 1136–1149. https://doi.org/10.1002/jnr.24220
Allen, H., and Coggan, A. (2010). Training and racing with a power meter. Boulder, CO: VeloPress [(2012). Wattmessung im Radsport und Triathlon. Übers. von S. Kohler. Hamburg: Spomedis]
Anand, S. S., Tarnopolsky, M. A., Rashid, S., Schulze, K. M., Desai, D., Mente, A., Rao, S., Yusuf, S., Gerstein, H. C. und Sharma, A. M. (2011). Adipocyte hypertrophy, fatty liver and metabolic risk factors in South Asians: The Molecular Study of Health and Risk in Ethnic Groups (mol-SHARE). PLOS ONE 6, e22112. https://doi.org/10.1371/journal.pone.0022112
Ancoli-Israel, S., Palmer, B. W., Cooke, J. R., Corey-Bloom, J., Fiorentino, L., Natarajan, L., Liu, L., Ayalon, L., He, F. und Loredo, J. S. (2008). Cognitive effects of treating obstructive sleep apnea in Alzheimer’s disease: A randomized controlled study. J. Am. Geriatr. Soc. 56, 2076–2081. https://doi.org/10.1111/j.1532–5415.2008.01934.x
Andersson, C., Blennow, K., Almkvist, O., Andreasen, N., Engfeldt, P., Johansson, S.-E., Lindau, M. und Eriksdotter-Jönhagen, M. (2008). Increasing CSF phospho-tau levels during cognitive decline and progression to dementia. Neurobiol. Aging 29, 1466–1473. https://doi.org/10.1016/j.neurobiolaging.2007.03.027
Andreasen, N., Hesse, C., Davidsson, P., Minthon, L., Wallin, A., Winblad, B., Vanderstichele, H., Vanmechelen, E. und Blennow, K. (1999). Cerebrospinal fluid beta-amyloid(1–42) in Alzheimer’s disease: Differences between early-and late-onset Alzheimer’s disease and stability during the course of disease. Arch. Neurol. 56, 673–680. https://doi.org/10.1001/archneur.56.6.673
Andreasen, N., Vanmechelen, E., Van de Voorde, A., Davidsson, P., Hesse, C., Tarvonen, S., Räihä, I., Sourander, L., Winblad, B. und Blennow, K. (1998). Cerebrospinal fluid tau protein as a biochemical marker for Alzheimer’s disease: A community-based follow up study. J. Neurol. Neurosurg. Psychiatry 64, 298–305. https://doi.org/10.1136/jnnp.64.3.298
Andrieu, S., Guyonnet, S., Coley, N., Cantet, C., Bonnefoy, M., Bordes, S. et al. (2017). Effect of long-term omega 3 polyunsaturated fatty acid supplementation with or without multidomain intervention on cognitive function in elderly adults with memory complaints (MAPT): A randomised placebo-controlled trial. Lancet 16, 377–389. https://doi.org/10.1016/S1474-4422(17)30040-6
Araujo, C. G., Souza e Silva, C. G. de, Laukkanen, J. A., Singh, M. F., Kunutsor, S. K., Myers, J., Franca, J. F. und Castro, C. L. (2022). Successful 10-second one-legged stance performance predicts survival in middle-aged and older individuals. Br. J. Sports Med. 56, 975–980. https://doi.org/10.1136/bjsports-2021-105360
Araújo, J., Cai, J. und Stevens, J. (2019). Prevalence of optimal metabolic health in American adults: National Health and Nutrition Examination Survey 2009–2016. Metab. Syndr. Relat. Disord. 17, 46–52. https://doi.org/10.1089/met.2018.0105
Arbon, E. L., Knurowska, M. und Dijk, D.-J. (2015). Randomised clinical trial of the effects of prolonged-release melatonin, temazepam and zolpidem on slow-wave activity during sleep in healthy people. J. Psychopharmacol. 29, 764–776. https://doi.org/10.1177/0269881115581963
Artero, E. G., Lee, D. C., Ruiz, J. R. (2011). A prospective study of muscular strength and all-cause mortality in men with hypertension. J. Am. Coll. Cardiol. 57(18), 1831–1837. https://doi:10.1016/j.jacc.2010.12.025
Asarnow, J. R., Berk, M. S., Bedics, J., Adrian, M., Gallop, R., Cohen, J., Korslund, K., Hughes, J., Avina, C., Linehan, M. M. et al. (2021). Dialectical Behavior Therapy for suicidal self-harming youth: Emotion regulation, mechanisms, and mediators. J. Am. Acad. Child Adolesc. Psychiatry 60, 1105–1115.e4. https://doi.org/10.1016/j.jaac.2021.01.016
Atkins, M. B., Kunkel, L., Sznol, M. und Rosenberg, S. A. (2000). High-dose recombinant interleukin-2 therapy in patients with metastatic melanoma: Long-term survival update. Cancer J. Sci. Am. 6, Suppl 1, S11-14
Attia, P. (2018a). #09-David Sabatini, M. D., Ph. D.: Rapamycin and the discovery of mTOR–The nexus of aging and longevity? The Drive (Podcast), Episode 9, 13. August. https://peterattiamd.com/davidsabatini/
Attia, P. (2018b). #10-Matt Kaeberlein, Ph. D.: Rapamycin and dogs – man’s best friends? Living longer, healthier lives and turning back the clock on aging and age-related diseases. The Drive (Podcast), Episode 10, 20. August. https://peterattiamd.com/mattkaeberlein/
Attia, P. (2018c). #18-Richard Isaacson, M. D.: Alzheimer’s prevention. The Drive (Podcast), Episode 18, 1. Oktober. https://peterattiamd.com/richardisaacson/
Attia, P. (2019). #38-Francisco Gonzalez-Lima, Ph. D.: Advancing Alzheimer’ disease treatment and prevention: Is AD actually a vascular and metabolic disease? The Drive (Podcast), Episode 38, 28. Januar. https://peterattiamd.com/franciscogonzalezlima/
Attia, P. (2020a). Colorectal cancer screening. peterattiamd.com (Blog), 27. September. https://peterattiamd.com/colorectal-cancer-screening/
Attia, P. (2020b). The killer(s) on the road: Reducing your risk of automotive death. peterattiamd.com (Blog), 9. Februar. https://peterattiamd.com/the-killers-on-the-road-reducing-your-risk-of-automotive-death/
Attia, P. (2020c). Rick Johnson, M. D.: Metabolic effects of fructose. The Drive (Podcast), Episode 87, 6. Januar. https://peterattiamd.com/rickjohnson/
Attia, P. (2021a). Michael Rintala, D. C.: Principles of Dynamic Neuromuscular Stabilization (DNS). The Drive (Podcast), Episode 152, 8. März. https://peterattiamd.com/michaelrintala/
Attia, P. (2021b). Steven Rosenberg, M. D., Ph. D.: The development of cancer immunotherapy and its promise for treating advanced cancers. The Drive (Podcast), Episode 177, 27. September
Avgerinos, K. I., Spyrou, N., Mantzoros, C. S. und Dalamaga, M. (2019). Obesity and cancer risk: Emerging biological mechanisms and perspectives. Metabolism 92, 121–135. https://doi.org/10.1016/j.metabol.2018.11.001
Azad, M. B., Abou-Setta, A. M., Chauhan, B. F., Rabbani, R., Lys, J., Copstein, L., Mann, A., Jeyaraman, M. M., Reid, A. E., Fiander, M. et al. (2017). Nonnutritive sweeteners and cardiometabolic health: A systematic review and meta-analysis of randomized controlled trials and prospective cohort studies. CMAJ 189, E929-E939. https://doi.org/10.1503/cmaj.161390
Bagherniya, M., Butler, A. E., Barreto, G. E. und Sahebkar, A. (2018). The effect of fasting or calorie restriction on autophagy induction: A review of the literature. Ageing Res. Rev. 47, 183–197. https://doi.org/10.1016/j.arr.2018.08.004
Bannister, C. A., Holden, S. E., Jenkins-Jones, S., Morgan, C. L., Halcox, J. P., Schernthaner, G., Mukherjee, J. und Currie, C. J. (2014). Can people with type 2 diabetes live longer than those without? A comparison of mortality in people initiated with metformin or sulphonylurea monotherapy and matched, non-diabetic controls. Diabetes Obes. Metab. 16, 1165–1173. https://doi.org/10.1111/dom.12354
Bao, Y., Han, J., Hu, F. B., Giovannucci, E. L., Stampfer, M. J., Willett, W. C. und Fuchs, C. S. (2013). Association of nut consumption with total and cause-specific mortality. N. Engl. J. Med. 369, 2001–2011. https://doi.org/10.1056/NEJMoa1307352
Barnes, J. N. und Corkery, A. T. (2018). Exercise improves vascular function, but does this translate to the brain? Brain Plast. 4, 65–79. https://doi.org/10.3233/BPL-180075
Baum, J. I., Kim, I.-Y. und Wolfe, R. R. (2016). Protein consumption and the elderly: What is the optimal level of intake? Nutrients 8, 359. https://doi.org/10.3390/nu8060359
Baur, J. A., Pearson, K. J., Price, N. L., Jamieson, H. A., Lerin, C., Kalra, A., Prabhu, V. V., Allard, J. S., Lopez-Lluch, G., Lewis, K. et al. (2006). Resveratrol improves health and survival of mice on a high-calorie diet. Nature 444, 337–342. https://doi.org/10.1038/nature05354
Bautch, V. L. und Caron, K. M. (2015). Blood and lymphatic vessel formation. Cold Spring Harb. Perspect. Biol. 7, a008268. https://doi.org/10.1101/cshperspect.a008268
Beckett, L. A., Harvey, D. J., Gamst, A., Donohue, M., Kornak, J., Zhang, H., Kuo, J. H. und Alzheimer’s Disease Neuroimaging Initiative (2010). The Alzheimer’s Disease Neuroimaging Initiative: Annual change in biomarkers and clinical outcomes. Alzheimer’s & Dementia. 6, 257–264. https://doi.org/10.1016/j.jalz.2010.03.002
Belloy, M. E., Napolioni, V., Han, S. S., Le Guen, Y. und Greicius, M. D. (2020). Association of Klotho-VS heterozygosity with risk of Alzheimer disease in individuals who carry APOE4. JAMA Neurol. 77, 849–862. https://doi.org/10.1001/jamaneurol.2020.0414
Benito-León, J., Bermejo-Pareja, F., Vega, S. und Louis, E. D. (2009). Total daily sleep duration and the risk of dementia: A prospective population-based study. Eur. J. Neurol. 16, 990–997. https://doi.org/10.1111/j.1468-1331.2009.02618.x
Benn, M., Tybjærg-Hansen, A., Stender, S., Frikke-Schmidt, R. und Nordestgaard, B. G. (2011). Low-density lipoprotein cholesterol and the risk of cancer: A Mendelian randomization study. J. Natl. Cancer Inst. 103, 508–519. https://doi.org/10.1093/jnci/djr008
Biddinger, K. J., Emdin, C. A., Haas, M. E., Wang, M., Hindy, G., Ellinor, P. T., Kathiresan, S., Khera, A. V. und Aragam, K. G. (2022). Association of habitual alcohol intake with risk of cardiovascular disease. JAMA Netw. Open 5, e223849. https://doi.org/10.1001/jamanetworkopen.2022.3849
Billat, V., Dhonneur, G., Mille-Hamard, L., Le Moyec, L., Momken, I., Launay, T., Koralsztein, J. P. und Besse, S. (2017). Case studies in physiology: Maximal oxygen consumption and performance in a centenarian cyclist. J. Appl. Physiol. 122, 430–434. https://doi.org/10.1152/japplphysiol.00569.2016
Blackwell, D. L. und Clarke, T. C. (2018). State variation in meeting the 2008 federal guidelines for both aerobic and muscle-strengthening activities through leisure-time physical activity among adults aged 18–64: United States, 2010–2015. Natl. Health Stat. Rep. 112 (June), 1–22
Blasbalg, T. L., Hibbeln, J. R., Ramsden, C. E., Majchrzak, S. F. und Rawlings, R. R. (2011). Changes in consumption of omega-3 and omega-6 fatty acids in the United States during the 20th century. Am. J. Clin. Nutr. 93, 950–962. https://doi.org/10.3945/ajcn.110.006643
Blessed, G., Tomlinson, B. E. und Roth, M. (1968). The association between quantitative measures of dementia and of senile change in the cerebral grey matter of elderly subjects. Br. J. Psychiatry J. Ment. Sci. 114, 797–811. https://doi.org/10.1192/bjp.114.512.797
Boden, G., Sargrad, K., Homko, C., Mozzoli, M. und Stein, T. P. (2005). Effect of a low-carbohydrate diet on appetite, blood glucose levels, and insulin resistance in obese patients with type 2 diabetes. Ann. Intern. Med. 142, 403–411. https://doi.org/10.7326/0003-4819-142-6-200503150-00006
Bohannon, R. W. (2019). Grip strength: An indispensable biomarker for older adults. Clin. Interv. Aging 14, 1681–1691. https://doi.org/10.2147/CIA.S194543
Boneti Moreira, N., Vagetti, G. C., Oliveira, V. de und Campos, W. de (2014). Association between injury and quality of life in athletes: A systematic review, 1980–2013. Apunts Sports Med. 49, 123–138
Booth, F. W. und Zwetsloot, K. A. (2010). Basic concepts about genes, inactivity and aging. Scand. J. Med. Sci. Sports 20, 1–4. https://doi.org/10.1111/j.1600-0838.2009.00972.x
Børsheim, E., Bui, Q.-U.T., Tissier, S., Cree, M. G., Rønsen, O., Morio, B., Ferrando, A. A., Kobayashi, H., Newcomer, B. R. und Wolfe, R. R. (2009). Amino acid supplementation decreases plasma and liver triglycerides in elderly. Nutr. Burbank Los Angel. Cty. Calif. 25, 281–288. https://doi.org/10.1016/j.nut.2008.09.001
Bosy-Westphal, A., Hinrichs, S., Jauch-Chara, K., Hitze, B., Later, W., Wilms, B., Settler, U., Peters, A., Kiosz, D. und Müller, M. J. (2008). Influence of partial sleep deprivation on energy balance and insulin sensitivity in healthy women. Obes. Facts 1, 266–273. https://doi.org/10.1159/000158874
Bouwman, F. H., Flier, W. M. van der, Schoonenboom, N. S. M., Elk, E. J. van, Kok, A., Rijmen, F., Blankenstein, M. A. und Scheltens, P. (2007). Longitudinal changes of CSF biomarkers in memory clinic patients. Neurology 69, 1006–1011. https://doi.org/10.1212/01.wnl.0000271375.37131.04
Bradley, D. (2004). Biography of Lewis C. Cantley. Proc. Natl. Acad. Sci. 101, 3327–3328. https://doi.org/10.1073/pnas.0400872101
Branger, P., Arenaza-Urquijo, E. M., Tomadesso, C., Mézenge, F., André, C., de Flores, R., Mutlu, J., de La Sayette, V., Eustache, F., Chételat, G. et al. (2016). Relationships between sleep quality and brain volume, metabolism, and amyloid deposition in late adulthood. Neurobiol. Aging 41,107–114. https://doi.org/10.1016/j.neurobiolaging.2016.02.009
Brondel, L., Romer, M. A., Nougues, P. M., Touyarou, P. und Davenne, D. (2010). Acute partial sleep deprivation increases food intake in healthy men. Am. J. Clin. Nutr. 91, 1550–1559. https://doi.org/10.3945/ajcn.2009.28523
Brookmeyer, R., Abdalla, N., Kawas, C. H. und Corrada, M. M. (2018). Forecasting the prevalence of preclinical and clinical Alzheimer’s disease in the United States. Alzheimer’s & Dementia. 14, 121–129. https://doi.org/10.1016/j.jalz.2017.10.009
Brooks, D. (2016). The road to character. Farmington Hills, MI: Large Print Press [(2015). Charakter – Die Kunst, Haltung zu zeigen. Übers. von T. Schmidt. München, Kösel]
Broussard, J. L., Chapotot, F., Abraham, V., Day, A., Delebecque, F., Whitmore, H. R. und Tasali, E. (2015). Sleep restriction increases free fatty acids in healthy men. Diabetologia 58, 791–798. https://doi.org/10.1007/s00125-015-3500-4
Broussard, J. L., Ehrmann, D. A., Van Cauter, E., Tasali, E. und Brady, M. J. (2012). Impaired insulin signaling in human adipocytes after experimental sleep restriction. Ann. Intern. Med. 157, 549–557. https://doi.org/10.7326/0003-4819-157-8-201210160-00005
Broussard, J. L., Kilkus, J. M., Delebecque, F., Abraham, V., Day, A., Whitmore, H. R. und Tasali, E. (2016). Elevated ghrelin predicts food intake during experimental sleep restriction. Obesity 24, 132–138. https://doi.org/10.1002/oby.21321
Brown, B. M., Rainey-Smith, S. R., Villemagne, V. L., Weinborn, M., Bucks, R. S., Sohrabi, H. R., Laws, S. M., Taddei, K., Macaulay, S. L., Ames, D. et al. (2016). The relationship between sleep quality and brain amyloid burden. Sleep 39, 1063–1068. https://doi.org/10.5665/sleep.5756
Brown, E. J., Albers, M. W., Shin, T. B., Ichikawa, K., Keith, C. T., Lane, W. S. und Schreiber, S. L. (1994). A mammalian protein targeted by G1-arresting rapamycin-receptor complex. Nature 369, 756–758. https://doi.org/10.1038/369756a0
Brys, M., Pirraglia, E., Rich, K., Rolstad, S., Mosconi, L., Switalski, R., Glodzik-Sobanska, L., De Santi, S., Zinkowski, R., Mehta, P. et al. (2009). Prediction and longitudinal study of CSF biomarkers in mild cognitive impairment. Neurobiol. Aging 30, 682–690. https://doi.org/10.1016/j.neurobiolaging.2007.08.010
Bunout, D., Maza, M. P. de la, Barrera, G., Leiva, L. und Hirsch, S. (2011). Association between sarcopenia and mortality in healthy older people. Australas. J. Ageing 30, 89–92. https://doi.org/10.1111/j.1741-6612.2010.00448.x
Business Wire (2021). U. S. sleep aids market worth $ 30 billion as Americans battle insomnia, sleep disorders – ResearchAndMarkets.com, June 30. https://www.businesswire.com/news/home/20210630005428/en/U.S.-Sleep-Aids-Market-Worth-30-Billion-as-Americans-Battle-Insomnia-Sleep-Disorders---ResearchAndMarkets.com
Buxton, O. M., Pavlova, M., Reid, E. W., Wang, W., Simonson, D. C. und Adler, G. K. (2010). Sleep restriction for 1 week reduces insulin sensitivity in healthy men. Diabetes 59, 2126–2133. https://doi.org/10.2337/db09-0699
Buysse, D. J., Reynolds, C. F., Charles, F., Monk, T. H., Berman, S. R. und Kupfer, D. J. (1989). The Pittsburgh Sleep Quality Index: A new instrument for psychiatric practice and research. Psychiat. Res. 28(2), 193–213
Cacace, R., Sleegers, K. und Van Broeckhoven, C. (2016). Molecular genetics of early-onset Alzheimer’s disease revisited. Alzheimer’s & Dementia. 12, 733–748. https://doi.org/10.1016/j.jalz.2016.01.012
Calle, E. E., Rodriguez, C., Walker-Thurmond, K. und Thun, M. J. (2003). Overweight, obesity, and mortality from cancer in a prospectively studied cohort of U. S. adults. N. Engl. J. Med. 348, 1625. https://doi.org/10.1056/NEJMoa021423
Calvin, A. D., Carter, R. E., Adachi, T., Macedo, P. G., Albuquerque, F. N., van der Walt, C., Bukartyk, J., Davison, D. E., Levine, J. A. und Somers, V. K. (2013). Effects of experimental sleep restriction on caloric intake and activity energy expenditure. Chest 144, 79–86. https://doi.org/10.1378/chest.12-2829
Campbell, K. L., Winters-Stone, K., Wiskemann, J., May, A. M., Schwartz, A. L., Courneya, K. S., Zucker, D., Matthews, C., Ligibel, J., Gerber, L. et al. (2019). Exercise guidelines for cancer survivors: Consensus statement from International Multidisciplinary Roundtable. Med. Sci. Sports Exerc. 51, 2375–2390. https://doi.org/10.1249/MSS.0000000000002116
Campbell, W. W., Trappe, T. A., Wolfe, R. R. und Evans, W. J. (2001). The recommended dietary allowance for protein may not be adequate for older people to maintain skeletal muscle. J. Gerontol. A. Biol. Sci. Med. Sci. 56, M373-380. https://doi.org/10.1093/gerona/56.6.m373
Case, A. und Deaton, A. (2015). Rising morbidity and mortality in midlife among white non-Hispanic Americans in the 21st century. Proc. Natl. Acad. Sci. 112(49), 15078–15083. https://doi.org/10.1073/pnas.1518393112
Caselli, G. und Lipsi, R. M. (2006). Survival differences among the oldest old in Sardinia: Who, what, where, and why? Demogr. Res. 14, 267–294
Cavazzoni, A., Digiacomo, G., Alfieri, R., La Monica, S., Fumarola, C., Galetti, M., Bonelli, M., Cretella, D., Barili, V., Zecca, A. et al. (2020). Pemetrexed enhances membrane PD-L1 expression and potentiates T cell-mediated cytotoxicity by anti-PD-L1 antibody therapy in non-small-cell lung cancer. Cancers 12, E666. https://doi.org/10.3390/cancers12030666
CDC (Centers for Disease Control). (2020a). The influence of metabolic syndrome in predicting mortality risk among US adults: Importance of metabolic syndrome even in adults with normal weight. https://www.cdc.gov/pcd/issues/2020/20_0020.htm
CDC (Centers for Disease Control). (2020b). Diabetes. FastStats. https://www.cdc.gov/nchs/fastats/diabetes.htm
CDC (Centers for Disease Control). (2021). Facts about falls. Injury Center. https://www.cdc.gov/falls/facts.html
CDC (Centers for Disease Control). (2022a). Accidents or unintentional injuries. FastStats. https://www.cdc.gov/nchs/fastats/accidental-injury.htm
CDC (Centers for Disease Control). (2022b) Adult obesity facts. https://www.cdc.gov/obesity/data/adult.html
CDC (Centers for Disease Control). (2022c). Heart disease facts. https://www.cdc.gov/heartdisease/facts.htm
CDC (Centers for Disease Control). (2022d). Life expectancy in the U. S. dropped for the second year in a row in 2021. Press release, 31. August. https://www.cdc.gov/nchs/pressroom/nchs_press_releases/2022/20220831.htm
CDC (Centers for Disease Control). (2022e). National diabetes statistics report. https://www.cdc.gov/diabetes/data/statistics-report/index.html?ACSTrackingID=DM72996&ACSTrackingLabel=New%20Report%20Shares%20Latest%20Diabetes%20Stats%20&deliveryName=DM72996
CDC (Centers for Disease Control). (2022 f.). Ten leading causes of death and injury. https://www.cdc.gov/injury/wisqars/LeadingCauses_images.html
Cerri, S., Mus, L. und Blandini, F. (2019). Parkinson’s disease in women and men: What’s the difference? J. Parkinson’s Dis. 9(3), 501–515. https://doi.org/10.3233/JPD-191683
Chan, J. M., Rimm, E. B., Colditz, G. A., Stampfer, M. J. und Willett, W. C. (1994). Obesity, fat distribution, and weight gain as risk factors for clinical diabetes in men. Diabetes Care 17, 961–969. https://doi.org/10.2337/diacare.17.9.961
Chapman, C. D., Schiöth, H. B., Grillo, C. A. und Benedict, C. (2018). Intranasal insulin in Alzheimer’s disease: Food for thought. Neuropharmacology 136, 196–201. https://doi.org/10.1016/j.neuropharm.2017.11.037
Charante, E. van, Richard, E., Eurelings, L. S., Dalen, J-W. van, Ligthart, S. A., Bussel, E. F. van, Hoevenaar-Blom, M. P., Vermeulen, M. und Gool, W. A. van (2016). Effectiveness of a 6-year multidomain vascular care intervention to prevent dementia (preDIVA): A cluster-randomised controlled trial. Lancet 388, 797–805. https://doi.org/10.1016/S0140-6736(16)30950-3
Chen, D. L., Liess, C., Poljak, A., Xu, A., Zhang, J., Thoma, C., Trenell, M., Milner, B., Jenkins, A. B., Chisholm, D. J. et al. (2015). Phenotypic characterization of insulin-resistant and insulin-sensitive obesity. J. Clin. Endocrinol. Metab. 100, 4082–4091. https://doi.org/10.1210/jc.2015-2712
Chen, X., Dong, Z., Hubbell, E., Kurtzman, K. N., Oxnard, G. R., Venn, O., Melton, C., Clarke, C. A., Shaknovich, R., Ma, T. et al. (2021). Prognostic significance of blood-based multi-cancer detection in plasma cell-free DNA. Clin. Cancer Res. 27, 4221–4229. https://doi.org/10.1158/1078-0432.CCR-21-0417
Cholerton, B., Baker, L. D., Montine, T. J. und Craft, S. (2016). Type 2 diabetes, cognition, and dementia in older adults: Toward a precision health approach. Diabetes Spectr. 29, 210–219. https://doi.org/10.2337/ds16-0041
Christofferson, Travis (2017). Tripping Over the Truth: How the Metabolic Theory of Cancer Is Overturning One of Medicine’s Most Entrenched Paradigms. White River Junction: Chelsea Green Publishing [(2019). Über die Wahrheit stolpern. Die metabolische Theorie: eine neue und mächtige Waffe gegen den Krebs. Übers. von A. Kühn und M. Lebmann. Rottenburg: Kopp]
Cirelli, C. und Tononi, G. (2008). Is sleep essential? PLOS Biol. 6, e216. https://doi.org/10.1371/journal.pbio.0060216
Colman, R. J., Anderson, R. M., Johnson, S. C., Kastman, E. K., Kosmatka, K. J., Beasley, T. M., Allison, D. B., Cruzen, C., Simmons, H. A., Kemnitz, J. W. et al. (2009). Caloric restriction delays disease onset and mortality in rhesus monkeys. Science 325, 201–204. https://doi.org/10.1126/science.1173635
Copinschi, G. und Caufriez, A. (2013). Sleep and hormonal changes in aging. Endocrinol. Metab. Clin. North Am. 42, 371–389. https://doi.org/10.1016/j.ecl.2013.02.009
Cordain, L., Eaton, S. B., Miller, J. B., Mann, N. und Hill, K. (2002). The paradoxical nature of hunter-gatherer diets: Meat-based, yet non-atherogenic. Eur. J. Clin. Nutr. 56, S42-S52. https://doi.org/10.1038/sj.ejcn.1601353
Cordain, L., Miller, J. B., Eaton, S. B., Mann, N., Holt, S. H. und Speth, J. D. (2000). Plant-animal subsistence ratios and macronutrient energy estimations in worldwide hunter-gatherer diets. Am. J. Clin. Nutr. 71, 682–692. https://doi.org/10.1093/ajcn/71.3.682
Creevy, K. E., Akey, J. M., Kaeberlein, M. und Promislow, D. E. L. (2022). An open science study of ageing in companion dogs. Nature 602, 51–57. https://doi.org/10.1038/s41586-021-04282-9
Crispim, C. A., Zimberg, I. Z., Reis, B. G. dos, Diniz, R. M., Tufik, S. und Mello, M. T. de (2011). Relationship between food intake and sleep pattern in healthy individuals. J. Clin. Sleep Med. 7, 659–664. https://doi.org/10.5664/jcsm.1476
Crowe, K. (2018). University of Twitter? Scientists give impromptu lecture critiquing nutrition research. CBC Health, 5. Mai. https://www.cbc.ca/news/health/second-opinion-alcohol180505-1.4648331
Cruchaga, C., Chakraverty, S., Mayo, K., Vallania, F. L. M., Mitra, R. D., Faber, K., Williamson, J., Bird, T., Diaz-Arrastia, R. et al. (2012). Rare variants in APP, PSEN1 and PSEN2 increase risk for AD in late-onset Alzheimer’s disease families. PLOS ONE 7, e31039. https://doi.org/10.1371/journal.pone.0031039
Cruz-Jentoft, A. J., Bahat, G., Bauer, J., Boirie, Y., Bruyère, O., Cederholm, T., Cooper, C., Landi, F., Rolland, Y., Sayer, A. A. et al. (2019). Sarcopenia: Revised European consensus on definition and diagnosis. Age and Ageing 48, 16–31. https://doi.org/10.1093/ageing/afy169
Cullen, T., Thomas, G., Wadley, A. J. und Myers, T. (2019). The effects of a single night of complete and partial sleep deprivation on physical and cognitive performance: A Bayesian analysis. J. Sports Sci. 37, 2726–2734. https://doi.org/10.1080/02640414.2019.1662539
Cummings, J. L., Goldman, D. P., Simmons-Stern, N. R. und Ponton, E. (2022). The costs of developing treatments for Alzheimer’s disease: A retrospective exploration. Alzheimer’s & Dementia. 18, 469–477. https://doi.org/10.1002/alz.12450
Cuyvers, E. und Sleegers, K. (2016). Genetic variations underlying Alzheimer’s disease: Evidence from genome-wide association studies and beyond. Lancet Neurol. 15, 857–868. https://doi.org/10.1016/S1474-4422(16)00127-7
Daghlas, I., Dashti, H. S., Lane, J., Aragam, K. G., Rutter, M. K., Saxena, R. und Vetter, C. (2019). Sleep duration and myocardial infarction. J. Am. Coll. Cardiol. 74, 1304–1314. https://doi.org/10.1016/j.jacc.2019.07.022
Dahlhamer, J. (2018). Prevalence of chronic pain and high-impact chronic pain among adults – United States, 2016. MMWR 67. https://doi.org/10.15585/mmwr.mm6736a2
Danneskiold-Samsøe, B., Bartels, E. M., Bülow, P. M., Lund, H., Stockmarr, A., Holm, C. C., Wätjen, I., Appleyard, M. und Bliddal, H. (2009). Isokinetic and isometric muscle strength in a healthy population with special reference to age and gender. Acta Physiol. 197, 1–68. https://doi.org/10.1111/j.1748-1716.2009.02022.x
Dashti, H. S., Jones, S. E., Wood, A. R., Lane, J. M., van Hees, V. T., Wang, H., Rhodes, J. A., Song, Y., Patel, K., Anderson, S. G. et al. (2019). Genome-wide association study identifies genetic loci for self-reported habitual sleep duration supported by accelerometer-derived estimates. Nat. Commun. 10, 1100. https://doi.org/10.1038/s41467-019-08917-4
Daviglus, M. L., Bell, C. C., Berrettini, W., Bowen, P. E., Connolly, E. S., Cox, N. J., Dunbar-Jacob, J. M., Granieri, E. C., Hunt, G., McGarry, K. et al. (2010). NIH state-of-the-science conference statement: Preventing Alzheimer’s disease and cognitive decline. NIH Consens. State Sci. Statements 27, 1–30
Dawson, D. und Reid, K. (1997). Fatigue, alcohol and performance impairment. Nature 388, 235. https://doi.org/10.1038/40775
Dewasmes, G., Bothorel, B., Hoeft, A. und Candas, V. (1993). Regulation of local sweating in sleep-deprived exercising humans. Eur. J. Appl. Physiol. 66, 542–546. https://doi.org/10.1007/BF00634307
Diamond, J. (2003). The double puzzle of diabetes. Nature 423, 599–602. https://doi.org/10.1038/423599a
Diekelmann, S. und Born, J. (2010). The memory function of sleep. Nat. Rev. Neurosci. 11, 114–126. https://doi.org/10.1038/nrn2762
Dietary Guidelines Advisory Committee. (2015). Scientific report of the 2015 Dietary Guidelines Advisory Committee: Advisory report to the Secretary of Health and Human Services and the Secretary of Agriculture. Washington, D. C.: U. S. Department of Agriculture, Agricultural Research Service. https://health.gov/sites/default/files/2019-09/Scientific-Report-of-the-2015-Dietary-Guidelines-Advisory-Committee.pdf
Dietschy, J. M., Turley, S. D. und Spady, D. K. (1993). Role of liver in the maintenance of cholesterol and low density lipoprotein homeostasis in different animal species, including humans. J. Lipid Res. 34, 1637–1659
Dominy, S. S., Lynch, C., Ermini, F., Benedyk, M., Marczyk, A., Konradi, A., Nguyen, M., Haditsch, U., Raha, D., Griffin, C. et al. (2019). Porphyromonas gingivalis in Alzheimer’s disease brains: Evidence for disease causation and treatment with small-molecule inhibitors. Sci. Adv. 5, eaau3333. https://doi.org/10.1126/sciadv.aau3333
Dworak, M., Diel, P., Voss, S., Hollmann, W. und Strüder, H. K. (2007). Intense exercise increases adenosine concentrations in rat brain: Implications for a homeostatic sleep drive. Neuroscience 150, 789–795. https://doi.org/10.1016/j.neuroscience.2007.09.062
Dye, L. (1988). Nobel physicist R. P. Feynman of Caltech dies. Los Angeles Times, 16. Februar. https://www.latimes.com/archives/la-xpm-1988-02-16-mn-42968-story.html
Easter, M. (2021). The comfort crisis: Embrace discomfort to reclaim your wild, happy, healthy self. New York: Rodale Books
Ebrahim, I. O., Shapiro, C. M., Williams, A. J. und Fenwick, P. B. (2013). Alcohol and sleep I: Effects on normal sleep. Alcohol. Clin. Exp. Res. 37, 539–549. https://doi.org/10.1111/acer.12006
Echouffo-Tcheugui, J. B., Zhao, S., Brock, G., Matsouaka, R. A., Kline, D. und Joseph, J. J. (2019). Visit-to-visit glycemic variability and risks of cardiovascular events and all-cause mortality: The ALLHAT study. Diabetes Care 42, 486–493. https://doi.org/10.2337/dc18-1430
Ejima, K., Li, P., Smith, D. L., Nagy, T. R., Kadish, I., Groen, T. van, Dawson, J. A., Yang, Y., Patki, A. und Allison, D. B. (2016). Observational research rigor alone does not justify causal inference. Eur. J. Clin. Invest. 46, 985–993. https://doi.org/10.1111/eci.12681
Emamian, F., Khazaie, H., Tahmasian, M., Leschziner, G. D., Morrell, M. J., Hsiung, G.-Y.R., Rosenzweig, I. und Sepehry, A. A. (2016). The association between obstructive sleep apnea and Alzheimer’s disease: A meta-analysis perspective. Front. Aging Neurosci. 8, 78. https://doi.org/10.3389/fnagi.2016.00078
Esteban-Cornejo, I., Ho, F. K., Petermann-Rocha, F., Lyall, D. M., Martinez-Gomez, D., Cabanas-Sánchez, V., Ortega, F. B., Hillman, C. H., Gill, J. M. R., Quinn, T. J. et al. (2022). Handgrip strength and all-cause dementia incidence and mortality: Findings from the UK Biobank prospective cohort study. J. Cachexia Sarcopenia Muscle 13, 1514–1525. https://doi.org/10.1002/jcsm.12857
Estruch, R., Ros, E., Salas-Salvadó, J., Covas, M.-I., Corella, D., Arós, F., Gómez-Gracia, E., Ruiz-Gutiérrez, V., Fiol, M., Lapetra, J. et al. (2013). Primary prevention of cardiovascular disease with a Mediterranean diet. N. Engl. J. Med. 368, 1279–1290. https://doi.org/10.1056/NEJMoa1200303
Evert, J., Lawler, E., Bogan, H. und Perls, T. (2003). Morbidity profiles of centenarians: Survivors, delayers, and escapers. J. Gerontol. Ser. A 58, M232-M237. https://doi.org/10.1093/gerona/58.3.M232
Fagan, A. M., Mintun, M. A., Mach, R. H., Lee, S.-Y., Dence, C. S., Shah, A. R., LaRossa, G. N., Spinner, M. L., Klunk, W. E., Mathis, C. A. et al. (2006). Inverse relation between in vivo amyloid imaging load and cerebrospinal fluid Abeta42 in humans. Ann. Neurol. 59, 512–519. https://doi.org/10.1002/ana.20730
Fain, E. und Weatherford, C. (2016). Comparative study of millennials’ (age 20–34 years) grip and lateral pinch with the norms. J. Hand Ther. 29, 483–488. https://doi.org/10.1016/j.jht.2015.12.006
Fayek, S. A., Quintini, C., Chavin, K. D. und Marsh, C. L. (2016). The current state of liver transplantation in the United States. Am. J. Transplant. 16, 3093–3104. https://doi.org/10.1111/ajt.14017
Ference, B. A. (2015). Mendelian randomization studies: Using naturally randomized genetic data to fill evidence gaps. Curr. Opin. Lipidol. 26, 566–571. https://doi.org/10.1097/MOL.0000000000000247
Ference, B. A., Bhatt, D. L., Catapano, A. L., Packard, C. J., Graham, I., Kaptoge, S., Ference, T. B., Guo, Q., Laufs, U., Ruff, C. T. et al. (2019). Association of genetic variants related to combined exposure to lower low-density lipoproteins and lower systolic blood pressure with lifetime risk of cardiovascular disease. JAMA 322, 1381–1391. https://doi.org/10.1001/jama.2019.14120
Ferriss, T. (2018). LeBron James and his top-secret trainer, Mike Mancias (#349). Tim Ferriss Show (Podcast), Episode 349, 27. November
Fontana, L. und Partridge, L. (2015). Promoting health and longevity through diet: From model organisms to humans. Cell 161, 106–118. https://doi.org/10.1016/j.cell.2015.02.020
Forrester, J. S. (2010). Redefining normal low-density lipoprotein cholesterol: A strategy to unseat coronary disease as the nation’s leading killer. J. Am. Coll. Cardiol. 56, 630–636. https://doi.org/10.1016/j.jacc.2009.11.090
Frank, C., Kobesova, A. und Kolar, P. (2013). Dynamic neuromuscular stabilization and sports rehabilitation. Int. J. Sports Phys. Ther. 8, 62–73
Franz, M. J. (1997). Protein: Metabolism and effect on blood glucose levels. Diabetes Educ. 23, 643–646, 648, 650–651. https://doi.org/10.1177/014572179702300603
Frayn, K. (2019). Human metabolism: A regulatory perspective. 4th ed. New York: Wiley
Freiherr, J., Hallschmid, M., Frey, W. H., Brünner, Y. F., Chapman, C. D., Hölscher, C., Craft, S., De Felice, F. G. und Benedict, C. (2013). Intranasal insulin as a treatment for Alzheimer’ disease: A review of basic research and clinical evidence. CNS Drugs 27, 505–514. https://doi.org/10.1007/s40263-013-0076-8
Friend, T. (2003). Jumpers. The New Yorker, 13. Oktober. https://www.newyorker.com/magazine/2003/10/13/jumpers
Fruman, D. A., Chiu, H., Hopkins, B. D., Bagrodia, S., Cantley, L. C. und Abraham, R. T. (2017). The PI3K pathway in human disease. Cell 170, 605–635. https://doi.org/10.1016/j.cell.2017.07.029
Fryar, C. D., Kruszon-Moran, D., Gu, Q. und Ogden, C. L. (2018). Mean body weight, height, waist circumference, and body mass index among adults: United States, 1999–2000 through 2015–2016. Natl. Health Stat. Rep. 1–16
Fullagar, H. H. K., Skorski, S., Duffield, R., Hammes, D., Coutts, A. J. und Meyer, T. (2015). Sleep and athletic performance: The effects of sleep loss on exercise performance, and physiological and cognitive responses to exercise. Sports Med. Auckl. NZ 45, 161–186. https://doi.org/10.1007/s40279-014-0260-0
Gaskin, D. J. und Richard, P. (2012). The economic costs of pain in the United States. J. Pain 13, 715–724. https://doi.org/10.1016/j.jpain.2012.03.009
Gavrilova, O., Marcus-Samuels, B., Graham, D., Kim, J. K., Shulman, G. I., Castle, A. L., Vinson, C., Eckhaus, M. und Reitman, M. L. (2000). Surgical implantation of adipose tissue reverses diabetes in lipoatrophic mice. J. Clin. Invest. 105, 271–278
Gay, N. und Prasad, V. (2017). Few people actually benefit from »breakthrough« cancer immunotherapy. Stat News, 8. März. https://www.statnews.com/2017/03/08/immunotherapy-cancer-breakthrough/
Gibala, M. J., Little, J. P., Essen, M. van, Wilkin, G. P., Burgomaster, K. A., Safdar, A., Raha, S. und Tarnopolsky, M. A. (2006). Short-term sprint interval versus traditional endurance training: Similar initial adaptations in human skeletal muscle and exercise performance. J. Physiol. 575, 901–911. https://doi.org/10.1113/jphysiol.2006.112094
Gibson, A. A., Seimon, R. V., Lee, C. M. Y., Ayre, J., Franklin, J., Markovic, T. P., Caterson, I. D. und Sainsbury, A. (2015). Do ketogenic diets really suppress appetite? A systematic review and meta-analysis. Obes. Rev. 16, 64–76. https://doi.org/10.1111/obr.12230
Gillen, J. B., Percival, M. E., Skelly, L. E., Martin, B. J., Tan, R. B., Tarnopolsky, M. A. und Gibala, M. J. (2014). Three minutes of all-out intermittent exercise per week increases skeletal muscle oxidative capacity and improves cardiometabolic health. PLOS ONE 9, e111489. https://doi.org/10.1371/journal.pone.0111489
Goldin, A., Beckman, J. A., Schmidt, A. M. und Creager, M. A. (2006). Advanced glycation end products. Circulation 114, 597–605. https://doi.org/10.1161/CIRCULATIONAHA.106.621854
Goldstein, A. N. und Walker, M. P. (2014). The role of sleep in emotional brain function. Annu. Rev. Clin. Psychol. 10, 679–708. https://doi.org/10.1146/annurev-clinpsy-032813-153716
Goldstein-Piekarski, A. N., Greer, S. M., Saletin, J. M. und Walker, M. P. (2015). Sleep deprivation impairs the human central and peripheral nervous system discrimination of social threat. J. Neurosci. 35, 10135–10145. https://doi.org/10.1523/JNEUROSCI.5254-14.2015
Gordon, R. J. (2016). The rise and fall of American growth: The U. S. standard of living since the Civil War. Princeton, NJ: Princeton University Press
Gradisar, M., Wolfson, A. R., Harvey, A. G., Hale, L., Rosenberg, R. und Czeisler, C. A. (2013). The sleep and technology use of Americans: Findings from the National Sleep Foundation’s 2011 Sleep in America Poll. J. Clin. Sleep Med. 9, 1291–1299. https://doi.org/10.5664/jcsm.3272
Graeber, C. (2018). The breakthrough: Immunotherapy and the race to cure cancer. New York: Twelve
Grammatikopoulou, M. G., Goulis, D. G., Gkiouras, K., Theodoridis, X., Gkouskou, K. K., Evangeliou, A., Dardiotis, E. und Bogdanos, D. P. (2020). To keto or not to keto? A systematic review of randomized controlled trials assessing the effects of ketogenic therapy on Alzheimer disease. Adv. Nutr. 11, 1583–1602. https://doi.org/10.1093/advances/nmaa073
Grandner, M. A. und Drummond, S. P. A. (2007). Who are the long sleepers? Towards an understanding of the mortality relationship. Sleep Medicine Reviews, 11: 5, 341–360. https://doi.org/10.1016/j.smrv.2007.03.010
Grimmer, T., Riemenschneider, M., Förstl, H., Henriksen, G., Klunk, W. E., Mathis, C. A., Shiga, T., Wester, H.-J., Kurz, A. und Drzezga, A. (2009). Beta amyloid in Alzheimer’s disease: Increased deposition in brain is reflected in reduced concentration in cerebrospinal fluid. Biol. Psychiatry 65, 927–934. https://doi.org/10.1016/j.biopsych.2009.01.027
Groot, S. de, Lugtenberg, R. T., Cohen, D., Welters, M. J. P., Ehsan, I., Vreeswijk, M. P. G., Smit, V. T. H. B.M., de Graaf, H., Heijns, J. B., Portielje, J. E. A. et al. (2020). Fasting mimicking diet as an adjunct to neoadjuvant chemotherapy for breast cancer in the multicentre randomized phase 2 DIRECT trial. Nat. Commun. 11, 3083. https://doi.org/10.1038/s41467-020-16138-3
Gross, D. N., Heuvel, A. P. J. van den und Birnbaum, M. J. (2008). The role of FoxO in the regulation of metabolism. Oncogene 27, 2320–2336. https://doi.org/10.1038/onc.2008.25
Guyenet, S. J. und Carlson, S. E. (2015). Increase in adipose tissue linoleic acid of US adults in the last half century. Adv. Nutr. 6, 660–664. https://doi.org/10.3945/an.115.009944
Haase, C. L., Tybjærg-Hansen, A., Ali Qayyum, A., Schou, J., Nordestgaard, B. G. und Frikke-Schmidt, R. (2012). LCAT, HDL cholesterol and ischemic cardiovascular disease: A Mendelian randomization study of HDL cholesterol in 54,500 individuals. J. Clin. Endocrinol. Metab. 97, E248-E256. https://doi.org/10.1210/jc.2011-1846
Hafner, M., Stepanek, M., Taylor, J., Troxel, W. M. und Stolk, C. van (2017). Why sleep matters: The economic costs of insufficient sleep. Rand Health Q. 6, 11
Hagerhall, C. M., Laike, T., Taylor, R. P., Küller, M., Küller, R. und Martin, T. P. (2008). Investigations of human EEG response to viewing fractal patterns. Perception 37, 1488–1494. https://doi.org/10.1068/p5918
Hamer, M. und O’Donovan, G. (2017). Sarcopenic obesity, weight loss, and mortality: The English Longitudinal Study of Ageing. Am. J. Clin. Nutr. 106, 125–129. https://doi.org/10.3945/ajcn.117.152488
Hanahan, D. und Weinberg, R. A. (2011). Hallmarks of cancer: The next generation. Cell 144, 646–674. https://doi.org/10.1016/j.cell.2011.02.013
Hanefeld, M., Koehler, C., Schaper, F., Fuecker, K., Henkel, E. und Temelkova-Kurktschiev, T. (1999). Postprandial plasma glucose is an independent risk factor for increased carotid intima-media thickness in non-diabetic individuals. Atherosclerosis 144, 229–235. https://doi.org/10.1016/S0021-9150(99)00059-3
Hardeland, R. (2013). Chronobiology of melatonin beyond the feedback to the suprachiasmatic nucleus: Consequences to melatonin dysfunction. Int. J. Mol. Sci. 14, 5817–5841. https://doi.org/10.3390/ijms14035817
Hardie, D. G. (2011). AMP-activated protein kinase: An energy sensor that regulates all aspects of cell function. Genes Dev. 25, 1895–1908. https://doi.org/10.1101/gad.17420111
Harding, E. C., Franks, N. P. und Wisden, W. (2020). Sleep and thermoregulation. Curr. Opin. Physiol. 15, 7–13. https://doi.org/10.1016/j.cophys.2019.11.008
Harrison, D. E., Strong, R., Reifsnyder, P., Kumar, N., Fernandez, E., Flurkey, K., Javors, M. A., Lopez-Cruzan, M., Macchiarini, F., Nelson, J. F. et al. (2021). 17-a-estradiol late in life extends lifespan in aging UM-HET3 male mice; nicotinamide riboside and three other drugs do not affect lifespan in either sex. Aging Cell 20, e13328. https://doi.org/10.1111/acel.13328
Harrison, D. E., Strong, R., Sharp, Z. D., Nelson, J. F., Astle, C. M., Flurkey, K., Nadon, N. L., Wilkinson, J. E., Frenkel, K., Carter, C. S. et al. (2009). Rapamycin fed late in life extends lifespan in genetically heterogeneous mice. Nature 460, 392–395. https://doi.org/10.1038/nature08221
Harrison, S. A., Gawrieh, S., Roberts, K., Lisanti, C. J., Schwope, R. B., Cebe, K. M., Paradis, V., Bedossa, P., Aldridge Whitehead, J. M., Labourdette, A. et al. (2021). Prospective evaluation of the prevalence of non-alcoholic fatty liver disease and steatohepatitis in a large middle-aged US cohort. J. Hepatol. 75, 284–291. https://doi.org/10.1016/j.jhep.2021.02.034
Hatori, M., Vollmers, C., Zarrinpar, A., DiTacchio, L., Bushong, E. A., Gill, S., Leblanc, M., Chaix, A., Joens, M., Fitzpatrick, J. A. J. et al. (2012). Time restricted feeding without reducing caloric intake prevents metabolic diseases in mice fed a high fat diet. Cell Metab. 15, 848–860. https://doi.org/10.1016/j.cmet.2012.04.019
Heron, M. (2021). Deaths: Leading causes for 2018. Natl. Vital Stat. Rep. 70(4), 1–115
Herring, W. J., Connor, K. M., Ivgy-May, N., Snyder, E., Liu, K., Snavely, D. B., Krystal, A. D., Walsh, J. K., Benca, R. M., Rosenberg, R. et al. (2016). Suvorexant in patients with insomnia: Results from two 3-month randomized controlled clinical trials. Biol. Psychiatry 79, 136–148. https://doi.org/10.1016/j.biopsych.2014.10.003
HHS (US Department of Health and Human Services). (2018). Physical activity guidelines for Americans. 2. Aufl. https://health.gov/sites/default/files/2019-09/Physical_Activity_Guidelines_2nd_edition.pdf
Hill, A. B. (1965). The environment and disease: Association or causation? Proc. R. Soc. Med. 58, 295–300
Hines, L. und Rimm, E. (2001). Moderate alcohol consumption and coronary heart disease: A review. Postgrad. Med. J. 77, 747–752. https://doi.org/10.1136/pmj.77.914.747
Hirode, G. und Wong, R. J. (2020). Trends in the prevalence of metabolic syndrome in the United States, 2011–2016. JAMA 323, 2526–2528. https://doi.org/10.1001/jama.2020.4501
Hitchens, C. (2012). Mortality. New York: Twelve [(2013) Endlich. Mein Sterben. Übers. von J. Kalka. München: Pantheon]
Hitt, R., Young-Xu, Y., Silver, M. und Perls, T. (1999). Centenarians: The older you get, the healthier you have been. Lancet 354, 652
Hjelmborg, J., Iachine, I., Skytthe, A., Vaupel, J. W., McGue, M., Koskenvuo, M., Kaprio, J., Pedersen, N. L. und Christensen, K. (2006). Genetic influence on human lifespan and longevity. Hum. Genet. 119, 312–321. https://doi.org/10.1007/s00439-006-0144-y
Hofseth, L. J., Hebert, J. R., Chanda, A., Chen, H., Love, B. L., Pena, M. M., Murphy, E. A., Sajish, M., Sheth, A., Buckhaults, P. J. et al. (2020). Early-onset colorectal cancer: Initial clues and current views. Nat. Rev. Gastroenterol. Hepatol. 17, 352–364. https://doi.org/10.1038/s41575-019-0253-4
Hoglund, K., Thelen, K. M., Syversen, S., Sjogren, M., Bergmann, K. von, Wallin, A., Vanmechelen, E., Vanderstichele, H., Lutjohann, D. und Blennow, K. (2005). The effect of simvastatin treatment on the amyloid precursor protein and brain cholesterol metabolism in patients with Alzheimer’s disease. Dement. Geriatr. Cogn. Disord. 19, 256–265. https://doi.org/10.1159/000084550
Holt, S. H., Miller, J. C., Petocz, P. und Farmakalidis, E. (1995). A satiety index of common foods. Eur. J. Clin. Nutr. 49, 675–690
Hooper, L., Martin, N., Jimoh, O. F., Kirk, C., Foster, E. und Abdelhamid, A. S. (2020). Reduction in saturated fat intake for cardiovascular disease. Cochrane Database Syst. Rev. https://doi.org/10.1002/14651858.CD011737.pub3
Hopkins, B. D., Pauli, C., Du, X., Wang, D. G., Li, X., Wu, D., Amadiume, S. C., Goncalves, M. D., Hodakoski, C., Lundquist, M. R. et al. (2018). Suppression of insulin feedback enhances the efficacy of PI3K inhibitors. Nature 560, 499–503. https://doi.org/10.1038/s41586-018-0343-4
Houston, D. K., Nicklas, B. J., Ding, J., Harris, T. B., Tylavsky, F. A., Newman, A. B., Lee, J. S., Sahyoun, N. R., Visser, M., Kritchevsky, S. B. et al. (2008). Dietary protein intake is associated with lean mass change in older, community-dwelling adults: The Health, Aging, and Body Composition (Health ABC) Study. Am. J. Clin. Nutr. 87, 150–155. https://doi.org/10.1093/ajcn/87.1.150
Howard, B. V., Van Horn, L., Hsia, J., Manson, J. E., Stefanick, M. L., Wassertheil-Smoller, S., Kuller, L. H., LaCroix, A. Z., Langer, R. D., Lasser, N. L. et al. (2006). Low-fat dietary pattern and risk of cardiovascular disease: The Women’s Health Initiative Randomized Controlled Dietary Modification Trial. JAMA 295, 655–666. https://doi.org/10.1001/jama.295.6.655
Hughes, V. A., Frontera, W. R., Wood, M., Evans, W. J., Dallal, G. E., Roubenoff, R. und Singh, M. A. F. (2001). Longitudinal muscle strength changes in older adults: Influence of muscle mass, physical activity, and health. J. Gerontol. Ser. A 56, B209-B217. https://doi.org/10.1093/gerona/56.5.B209
Hutchison, I. C. und Rathore, S. (2015). The role of REM sleep theta activity in emotional memory. Front. Psychol. 6, 1439. https://doi.org/10.3389/fpsyg.2015.01439
Iftikhar, I. H., Donley, M. A., Mindel, J., Pleister, A., Soriano, S. und Magalang, U. J. (2015). Sleep duration and metabolic syndrome: An updated dose-risk metaanalysis. Ann. Am. Thorac. Soc. 12, 1364–1372. https://doi.org/10.1513/AnnalsATS.201504-190OC
Igwe, E., Azman, A. Z. F., Nordin, A. J. und Mohtarrudin, N. (2015). Association between HOMA-IR and cancer. Int. J. Public Health Clin. Sci. 2, 21
Iliff, J. J., Lee, H., Yu, M., Feng, T., Logan, J., Nedergaard, M. und Benveniste, H. (2013). Brain-wide pathway for waste clearance captured by contrast-enhanced MRI. J. Clin. Invest. 123, 1299–1309. https://doi.org/10.1172/JCI67677
IOM (Institute of Medicine). Committee on Military Nutrition Research. (2001). Caffeine for the sustainment of mental task performance: Formulations for military operations. Washington, DC: National Academies Press
Ioannidis, J. P. A. (2018). The challenge of reforming nutritional epidemiologic research. JAMA 320, 969–970. https://doi.org/10.1001/jama.2018.11025
Itani, O., Jike, M., Watanabe, N. und Kaneita, Y. (2017). Short sleep duration and health outcomes: A systematic review, meta-analysis, and meta-regression. Sleep Med. 32, 246–256. https://doi.org/10.1016/j.sleep.2016.08.006
Jack, C. R., Knopman, D. S., Jagust, W. J., Petersen, R. C., Weiner, M. W., Aisen, P. S., Shaw, L. M., Vemuri, P., Wiste, H. J., Weigand, S. D. et al. (2013). Update on hypothetical model of Alzheimer’s disease biomarkers. Lancet Neurol. 12, 207–216. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3622225/
Jackson, M. L., Croft, R. J., Kennedy, G. A., Owens, K. und Howard, M. E. (2013). Cognitive components of simulated driving performance: Sleep loss effects and predictors. Accid. Anal. Prev. 50, 438–444. https://doi.org/10.1016/j.aap.2012.05.020
Jakubowski, B., Shao, Y., McNeal, C., Xing, C. und Ahmad, Z. (2021). Monogenic and polygenic causes of low and extremely low LDL-C levels in patients referred to specialty lipid clinics: Genetics of low LDL-C. J. Clin. Lipidol. 15, 658–664. https://doi.org/10.1016/j.jacl.2021.07.003
Jamaspishvili, T., Berman, D. M., Ross, A. E., Scher, H. I., De Marzo, A. M., Squire, J. A. und Lotan, T. L. (2018). Clinical implications of PTEN loss in prostate cancer. Nat. Rev. Urol. 15, 222–234. https://doi.org/10.1038/nrurol.2018.9
Jamshed, H., Beyl, R. A., Della Manna, D. L., Yang, E. S., Ravussin, E. und Peterson, C. M. (2019). Early time-restricted feeding improves 24-hour glucose levels and affects markers of the circadian clock, aging, and autophagy in humans. Nutrients 11, 1234. https://doi.org/10.3390/nu11061234
Jensen, T. L., Kiersgaard, M. K., Sørensen, D. B. und Mikkelsen, L. F. (2013). Fasting of mice: A review. Lab. Anim. 47, 225–240. https://doi.org/10.1177/0023677213501659
Johnson, R. J. und Andrews, P. (2015). Ancient mutation in apes may explain human obesity and diabetes. Scientific American, 1. Oktober
Johnson, R. J., Sánchez-Lozada, L. G., Andrews, P. und Lanaspa, M. A. (2017). Perspective: A historical and scientific perspective of sugar and its relation with obesity and diabetes. Adv. Nutr. 8, 412–422. https://doi.org/10.3945/an.116.014654
Johnson, R. J., Stenvinkel, P., Andrews, P., Sánchez-Lozada, L. G., Nakagawa, T., Gaucher, E., Andres-Hernando, A., Rodriguez-Iturbe, B., Jimenez, C. R., Garcia, G. et al. (2020). Fructose metabolism as a common evolutionary pathway of survival associated with climate change, food shortage and droughts. J. Intern. Med. 287, 252–262. https://doi.org/10.1111/joim.12993
Johnson, S. (2021). Extra life: A short history of living longer. New York: Riverhead Books
Jones, K., Gordon-Weeks, A., Coleman, C. und Silva, M. (2017). Radiologically determined sarcopenia predicts morbidity and mortality following abdominal surgery: A systematic review and meta-analysis. World J. Surg. 41, 2266–2279. https://doi.org/10.1007/s00268-017-3999-2
Jose, J. (2016). Statins and its hepatic effects: Newer data, implications, and changing recommendations. J. Pharm. Bioallied Sci. 8, 23–28. https://doi.org/10.4103/0975-7406.171699
Joslin, E. P. (1940). The universality of diabetes: A survey of diabetic morbidity in Arizona. The Frank Billings Lecture. JAMA 115, 2033–2038. https://doi.org/10.1001/jama.1940.02810500001001
Ju, Y.-E.S., McLeland, J. S., Toedebusch, C. D., Xiong, C., Fagan, A. M., Duntley, S. P., Morris, J. C. und Holtzman, D. M. (2013). Sleep quality and preclinical Alzheimer disease. JAMA Neurol. 70, 587–593. https://doi.org/10.1001/jamaneurol.2013.2334
Kaivola, K., Shah, Z., Chia, R., International LBD Genomics Consortium und Scholz, S. W. (2022). Genetic evaluation of dementia with Lewy bodies implicates distinct disease subgroups. Brain 145(5), 1757–1762. https://doi.org/10.1093/brain/awab402
Kalmbach, D. A., Schneider, L. D., Cheung, J., Bertrand, S. J., Kariharan, T., Pack, A. I. und Gehrman, P. R. (2017). Genetic basis of chronotype in humans: Insights from three landmark GWAS. Sleep 40, zsw048. https://doi.org/10.1093/sleep/zsw048
Kanai, M., Matsubara, E., Isoe, K., Urakami, K., Nakashima, K., Arai, H., Sasaki, H., Abe, K., Iwatsubo, T., Kosaka, T. et al. (1998). Longitudinal study of cerebrospinal fluid levels of tau, A beta1–40, and A beta1–42(43) in Alzheimer’s disease: A study in Japan. Ann. Neurol. 44, 17–26. https://doi.org/10.1002/ana.410440108
Karagiannis, A. D., Mehta, A., Dhindsa, D. S., Virani, S. S., Orringer, C. E., Blumenthal, R. S., Stone, N. J. und Sperling, L. S. (2021). How low is safe? The frontier of very low (<30 mg/dL) LDL cholesterol. Eur. Heart J. 42, 2154–2169. https://doi.org/10.1093/eurheartj/ehaa1080
Karsli-Uzunbas, G., Guo, J. Y., Price, S., Teng, X., Laddha, S. V., Khor, S., Kalaany, N. Y., Jacks, T., Chan, C. S., Rabinowitz, J. D. et al. (2014). Autophagy is required for glucose homeostasis and lung tumor maintenance. Cancer Discov. 4, 914–927. https://doi.org/10.1158/2159-8290.CD-14-0363
Kawada, S. und Ishii, N. (2005). Skeletal muscle hypertrophy after chronic restriction of venous blood flow in rats. Med. Sci. Sports Exerc. 37, 1144–1150. https://doi.org/10.1249/01.mss.0000170097.59514.bb
Kawano, H., Motoyama, T., Hirashima, O., Hirai, N., Miyao, Y., Sakamoto, T., Kugiyama, K., Ogawa, H. und Yasue, H. (1999). Hyperglycemia rapidly suppresses flow-mediated endothelium-dependent vasodilation of brachial artery. J. Am. Coll. Cardiol. 34, 146–154. https://doi.org/10.1016/S0735-1097(99)00168-0
Keramidas, M. E. und Botonis, P. G. (2021). Short-term sleep deprivation and human thermoregulatory function during thermal challenges. Exp. Physiol. 106, 1139–1148. https://doi.org/10.1113/EP089467
Kerrouche, N., Herholz, K., Mielke, R., Holthoff, V. und Baron, J.-C. (2006). 18FDG PET in vascular dementia: Differentiation from Alzheimer’s diease using voxel-based multivariate analysis. J. Cereb. Blood Flow Metab. 26, 1213–1221. https://doi.org/10.1038/sj.jcbfm.9600296
Killgore, W. D. S. (2013). Self-reported sleep correlates with prefrontal-amygdala functional connectivity and emotional functioning. Sleep 36, 1597–1608. https://doi.org/10.5665/sleep.3106
Kim, C.-H., Wheatley, C. M., Behnia, M. und Johnson, B. D. (2016). The effect of aging on relationships between lean body mass and VO2max in rowers. PLOS ONE 11, e0160275. https://doi.org/10.1371/journal.pone.0160275
Kim, D.-Y., Hong, S.-H., Jang, S.-H., Park, S.-H., Noh, J.-H., Seok, J.-M., Jo, H.-J., Son, C.-G. und Lee, E.-J. (2022). Systematic review for the medical applications of meditation in randomized controlled trials. Int. J. Environ. Res. Public. Health 19, 1244. https://doi.org/10.3390/ijerph19031244
Kim, T. N. und Choi, K. M. (2013). Sarcopenia: Definition, epidemiology, and pathophysiology. J. Bone Metab. 20, 1–10. https://doi.org/10.11005/jbm.2013.20.1.1
Kim, Y., White, T., Wijndaele, K., Westgate, K., Sharp, S. J., Helge, J. W., Wareham, N. J. und Brage, S. (2018). The combination of cardiorespiratory fitness and muscle strength, and mortality risk. Eur. J. Epidemiol. 33, 953–964. https://doi.org/10.1007/s10654-018-0384-x
Kinsella, K. G. (1992). Changes in life expectancy, 1900–1990. Am. J. Clin. Nutr. 55, 1196S-1202S. https://doi.org/10.1093/ajcn/55.6.1196S
Kloske, C. M. und Wilcock, D. M. (2020). The important interface between apolipoprotein E and neuroinflammation in Alzheimer’s disease. Front. Immunol. 11, 754. https://doi.org/10.3389/fimmu.2020.00754
Kochenderfer, J. N., Wilson, W. H., Janik, J. E., Dudley, M. E., Stetler-Stevenson, M., Feldman, S. A., Maric, I., Raffeld, M., Nathan, D.-A.N., Lanier, B. J. et al. (2010). Eradication of B-lineage cells and regression of lymphoma in a patient treated with autologous T cells genetically engineered to recognize CD19. Blood 116, 4099–4102. https://doi.org/10.1182/blood-2010-04-281931
Kokkinos, P., Faselis, C., Babu, H. S. I., Pittaras, A., Doumas, M., Murphy, R., Heimall, M. S., Sui, X., Zhang, J. und Myers, J. (2022). Cardiorespiratory fitness and mortality risk across the spectra of age, race, and sex. J. Am. Coll. Cardiol. 80, 598–609
Kolata, G. (2012). Severe diet doesn’t prolong life, at least in monkeys. New York Times, 29. August 29 2012. https://www.nytimes.com/2012/08/30/science/low-calorie-diet-doesnt-prolong-life-study-of-monkeys-finds.html?action=click&module=RelatedCoverage&pgtype=Article®ion=Footer
Kolata, G. (2020). An Alzheimer’s treatment fails: »We don’t have anything now«. New York Times, 10. Februar. https://www.nytimes.com/2020/02/10/health/alzheimers-amyloid-drug.html
Kolka, M. A. und Stephenson, L. A. (1988). Exercise thermoregulation after prolonged wakefulness. J. Appl. Physiol. 64, 1575–1579. https://doi.org/10.1152/jappl.1988.64.4.1575
Konstantinos, I., Avgerinos, N. S., Mantzoros, C. S., Dalamaga, M. (2019). Obesity and cancer risk: Emerging biological mechanisms and perspectives. Metabolism 92, 121–135. https://doi.org/10.1016/j.metabol.2018.11.001
Kortebein, P., Ferrando, A., Lombeida, J., Wolfe, R. und Evans, W. J. (2007). Effect of 10 days of bed rest on skeletal muscle in healthy older adults. JAMA 297, 1769–1774. https://doi.org/10.1001/jama.297.16.1772-b
Kourtis, N. und Tavernarakis, N. (2009). Autophagy and cell death in model organisms. Cell Death Differ. 16, 21–30. https://doi.org/10.1038/cdd.2008.120
Krause, A. J., Simon, E. B., Mander, B. A., Greer, S. M., Saletin, J. M., Goldstein-Piekarski, A. N. und Walker, M. P. (2017). The sleep-deprived human brain. Nat. Rev. Neurosci. 18, 404–418. https://doi.org/10.1038/nrn.2017.55
Kuna, S. T., Maislin, G., Pack, F. M., Staley, B., Hachadoorian, R., Coccaro, E. F. und Pack, A. I. (2012). Heritability of performance deficit accumulation during acute sleep deprivation in twins. Sleep 35, 1223–1233. https://doi.org/10.5665/sleep.2074
Kuo, T., McQueen, A., Chen, T.-C. und Wang, J.-C. (2015). Regulation of glucose homeostasis by glucocorticoids. Adv. Exp. Med. Biol. 872, 99–126. https://doi.org/10.1007/978-1-4939-2895-8_5
Kwo, P. Y., Cohen, S. M. und Lim, J. K. (2017). ACG clinical guideline: Evaluation of abnormal liver chemistries. Am. J. Gastroenterol. 112, 18–35. https://doi.org/10.1038/ajg.2016.517
Kwok, C. S., Kontopantelis, E., Kuligowski, G., Gray, M., Muhyaldeen, A., Gale, C. P., Peat, G. M., Cleator, J., Chew-Graham, C., Loke, Y. K., Mamas, M. A. (2018). Self-reported sleep duration and quality and cardiovascular disease and mortality. JAHA, 7:15. https://doi.org/10.1161/JAHA.118.008552
Lammert, F. und Wang, D.Q.-H. (2005). New insights into the genetic regulation of intestinal cholesterol absorption. Gastroenterology 129, 718–734. https://doi.org/10.1053/j.gastro.2004.11.017
Lamond, N. und Dawson, D. (1999). Quantifying the performance impairment associated with fatigue. J. Sleep Res. 8, 255–262. https://doi.org/10.1046/j.1365-2869.1999.00167.x
Langa, K. M. und Levine, D. A. (2014). The diagnosis and management of mild cognitive impairment: A clinical review. JAMA 312, 2551–2561. https://doi.org/10.1001/jama.2014.13806
Laukkanen, T., Khan, H., Zaccardi, F. und Laukkanen, J. A. (2015). Association between sauna bathing and fatal cardiovascular and all-cause mortality events. JAMA Intern. Med. 175, 542–548. https://doi.org/10.1001/jamainternmed.2014.8187
Laukkanen, T., Kunutsor, S., Kauhanen, J. und Laukkanen, J. A. (2017). Sauna bathing is inversely associated with dementia and Alzheimer’s disease in middle-aged Finnish men. Age and Ageing 46, 245–249. https://doi.org/10.1093/ageing/afw212
Lawson, J. S. (2016). Multiple infectious agents and the origins of atherosclerotic coronary artery disease. Front. Cardiovasc. Med. 3, 30. https://doi.org/10.3389/fcvm.2016.00030
Le, D. T., Uram, J. N., Wang, H., Bartlett, B. R., Kemberling, H., Eyring, A. D., Skora, A. D., Luber, B. S., Azad, N. S., Laheru, D. et al. (2015). PD-1 blockade in tumors with mismatch-repair deficiency. N. Engl. J. Med. 372, 2509–2520. https://doi.org/10.1056/NEJMoa1500596
Le, R., Zhao, L. und Hegele, R. A. (2022). Forty year follow-up of three patients with complete absence of apolipoprotein B-containing lipoproteins. J. Clin. Lipidol. 16, 155–159. https://doi.org/10.1016/j.jacl.2022.02.003
Lee, I.-M. und Buchner, D. M. (2008). The importance of walking to public health. Med. Sci. Sports Exerc. 40, S512-518. https://doi.org/10.1249/MSS.0b013e31817c65d0
Lee, J. C., Kim, S. J., Hong, S. und Kim, Y. (2019). Diagnosis of Alzheimer’s disease utilizing amyloid and tau as fluid biomarkers. Exp. Mol. Med. 51, 1–10. https://doi.org/10.1038/s12276-019-0250-2
Lega, I. C. und Lipscombe, L. L. (2019). Review: diabetes, obesity, and cancer–pathophysiology and clinical implications. Endocr. Rev. 41(1), 33–52. https://doi.org/10.1210/endrev/bnz014
Lemasters, J. J. (2005). Selective mitochondrial autophagy, or mitophagy, as a targeted defense against oxidative stress, mitochondrial dysfunction, and aging. Rejuvenation Res. 8, 3–5. https://doi.org/10.1089/rej.2005.8.3
Lendner, J. D., Helfrich, R. F., Mander, B. A., Romundstad, L., Lin, J. J., Walker, M. P., Larsson, P. G. und Knight, R. T. (2020). An electrophysiological marker of arousal level in humans. ELife 9, e55092. https://doi.org/10.7554/eLife.55092
Leon, M. J. de, DeSanti, S., Zinkowski, R., Mehta, P. D., Pratico, D., Segal, S., Rusinek, H., Li, J., Tsui, W., Saint Louis, L. A. et al. (2006). Longitudinal CSF and MRI biomarkers improve the diagnosis of mild cognitive impairment. Neurobiol. Aging 27, 394–401. https://doi.org/10.1016/j.neurobiolaging.2005.07.003
Leproult, R., Holmbäck, U. und Van Cauter, E. (2014). Circadian misalignment augments markers of insulin resistance and inflammation, independently of sleep loss. Diabetes 63, 1860–1869. https://doi.org/10.2337/db13-1546
Leproult, R. und Van Cauter, E. (2010). Role of sleep and sleep loss in hormonal release and metabolism. Endocr. Dev. 17, 11–21. https://doi.org/10.1159/000262524
Lexell, J. (1995). Human aging, muscle mass, and fiber type composition. J. Gerontol. A. Biol. Sci. Med. Sci. 50 Spec No, 11–16. https://doi.org/10.1093/gerona/50a.special_issue.11
Li, R., Xia, J., Zhang, X., Gathirua-Mwangi, W. G., Guo, J., Li, Y., McKenzie, S. und Song, Y. (2018). Associations of muscle mass and strength with all-cause mortality among US older adults. Med. Sci. Sports Exerc. 50, 458–467. https://doi.org/10.1249/MSS.0000000000001448
Libby, P. (2021). The changing landscape of atherosclerosis. Nature 592, 524–533. https://doi.org/10.1038/s41586-021-03392-8
Libby, P. und Tokgözoğlu, L. (2022). Chasing LDL cholesterol to the bottom: PCSK9 in perspective. Nat. Cardiovasc. Res. 1, 554–561. https://doi.org/10.1038/s44161-022-00085-x
Liberti, M. V. und Locasale, J. W. (2016). The Warburg effect: How does it benefit cancer cells? Trends Biochem. Sci. 41, 211–218. https://doi.org/10.1016/j.tibs.2015.12.001
Lieberman, D. E., Kistner, T. M., Richard, D., Lee, I.-M. und Baggish, A. L. (2021). The active grandparent hypothesis: Physical activity and the evolution of extended human healthspans and lifespans. Proc. Natl. Acad. Sci. 118, e2107621118. https://doi.org/10.1073/pnas.2107621118
Liguori, G. (Hrsg.) (2020). ACSM’s guidelines for exercise testing and prescription. 10. Aufl. Philadelphia: Wolters Kluwer Health
Lim, A. S. P., Kowgier, M., Yu, L., Buchman, A. S. und Bennett, D. A. (2013a). Sleep fragmentation and the risk of incident Alzheimer’s disease and cognitive decline in older persons. Sleep 36, 1027–1032. https://doi.org/10.5665/sleep.2802
Lim, A. S. P., Yu, L., Kowgier, M., Schneider, J. A., Buchman, A. S. und Bennett, D. A. (2013b). Sleep modifies the relation of APOE to the risk of Alzheimer disease and neurofibrillary tangle pathology. JAMA Neurol. 70, 10.1001/jamaneurol.2013.4215. https://doi.org/10.1001/jamaneurol.2013.4215
Lim, J. und Dinges, D. F. (2008). Sleep deprivation and vigilant attention. Ann. N. Y. Acad. Sci. 1129, 305–322. https://doi.org/10.1196/annals.1417.002
Lin, H.-J., Lee, B.-C., Ho, Y.-L., Lin, Y.-H., Chen, C.-Y., Hsu, H.-C., Lin, M.-S., Chien, K.-L. und Chen, M.-F. (2009). Postprandial glucose improves the risk prediction of cardiovascular death beyond the metabolic syndrome in the nondiabetic population. Diabetes Care 32, 1721–1726. https://doi.org/10.2337/dc08-2337
Lin, H.-S., Watts, J. N., Peel, N. M. und Hubbard, R. E. (2016). Frailty and post-operative outcomes in older surgical patients: A systematic review. BMC Geriatr. 16, 157. https://doi.org/10.1186/s12877-016-0329-8
Lindle, R. S., Metter, E. J., Lynch, N. A., Fleg, J. L., Fozard, J. L., Tobin, J., Roy, T. A. und Hurley, B. F. (1997). Age and gender comparisons of muscle strength in 654 women and men aged 20–93 yr. J. Appl. Physiol. 83, 1581–1587. https://doi.org/10.1152/jappl.1997.83.5.1581
Linehan, M. M., Comtois, K. A., Murray, A. M., Brown, M. Z., Gallop, R. J., Heard, H. L., Korslund, K. E., Tutek, D. A., Reynolds, S. K. und Lindenboim, N. (2006). Two-year randomized controlled trial and follow-up of dialectical behavior therapy vs therapy by experts for suicidal behaviors and borderline personality disorder. Arch. Gen. Psychiatry 63, 757–766. https://doi.org/10.1001/archpsyc.63.7.757
Little, J. P., Gillen, J. B., Percival, M. E., Safdar, A., Tarnopolsky, M. A., Punthakee, Z., Jung, M. E. und Gibala, M. J. (2011). Low-volume high-intensity interval training reduces hyperglycemia and increases muscle mitochondrial capacity in patients with type 2 diabetes. J. Appl. Physiol. 111, 1554–1560. https://doi.org/10.1152/japplphysiol.00921.2011
Liu, D., Huang, Y., Huang, C., Yang, S., Wei, X., Zhang, P., Guo, D., Lin, J., Xu, B., Li, C. et al. (2022). Calorie restriction with or without time-restricted eating in weight loss. N. Engl. J. Med. 386, 1495–1504. https://doi.org/10.1056/NEJMoa2114833
Liu, G. Y. und Sabatini, D. M. (2020). mTOR at the nexus of nutrition, growth, ageing and disease. Nat. Rev. Mol. Cell Biol. 21, 183–203. https://doi.org/10.1038/s41580-019-0199-y
Livingston, G. (2019). On average, older adults spend over half their waking hours alone. Policy Commons, 3. Juli. https://policycommons.net/artifacts/616735/on-average-older-adults-spend-over-half-their-waking-hours-alone/1597428/
Lobo, A., López-Antón, R., de-la-Cámara, C., Quintanilla, M. A., Campayo, A., Saz, P. und ZARADEMP Workgroup (2008). Non-cognitive psychopathological symptoms associated with incident mild cognitive impairment and dementia, Alzheimer’s type. Neurotox. Res.14, 263–272. https://doi.org/10.1007/BF03033815
López-Otín, C., Blasco, M. A., Partridge, L., Serrano, M. und Kroemer, G. (2013). The hallmarks of aging. Cell 153, 1194–1217. https://doi.org/10.1016/j.cell.2013.05.039
Lowe, D. A., Wu, N., Rohdin-Bibby, L., Moore, A. H., Kelly, N., Liu, Y. E., Philip, E., Vittinghoff, E., Heymsfield, S. B., Olgin, J. E. et al. (2020). Effects of time-restricted eating on weight loss and other metabolic parameters in women and men with overweight and obesity: The TREAT randomized clinical trial. JAMA Intern. Med. 180, 1491–1499. https://doi.org/10.1001/jamainternmed.2020.4153
Lucey, B. P., McCullough, A., Landsness, E. C., Toedebusch, C. D., McLeland, J. S., Zaza, A. M., Fagan, A. M., McCue, L., Xiong, C., Morris, J. C. et al. (2019). Reduced non-rapid eye movement sleep is associated with tau pathology in early Alzheimer’s disease. Sci. Transl. Med. 11, eaau6550. https://doi.org/10.1126/scitranslmed.aau6550
Ludwig, J., Viggiano, T. R., McGill, D. B. und Oh, B. J. (1980). Nonalcoholic steatohepatitis: Mayo Clinic experiences with a hitherto unnamed disease. Mayo Clinic proceedings, 55(7), 434–438
Lüth, H.-J., Ogunlade, V., Kuhla, B., Kientsch-Engel, R., Stahl, P., Webster, J., Arendt, T. und Münch, G. (2005). Age-and stage-dependent accumulation of advanced glycation end products in intracellular deposits in normal and Alzheimer’s disease brains. Cereb. Cortex 15, 211–220. https://doi.org/10.1093/cercor/bhh123
Mach, F., Ray, K. K., Wiklund, O., Corsini, A., Catapano, A. L., Bruckert, E., De Backer, G., Hegele, R. A., Hovingh, G. K., Jacobson, T. A. et al. (2018). Adverse effects of statin therapy: perception vs. the evidence: Focus on glucose homeostasis, cognitive, renal and hepatic function, haemorrhagic stroke and cataract. Eur. Heart J. 39, 2526–2539. https://doi.org/10.1093/eurheartj/ehy182
Maddock, J., Cavadino, A., Power, C. und Hyppönen, E. (2015). 25-hydroxyvitamin D, APOE ε4 genotype and cognitive function: Findings from the 1958 British birth cohort. Eur. J. Clin. Nutr. 69, 505–508. https://doi.org/10.1038/ejcn.2014.201
Maeng, L. Y. und Milad, M. R. (2015). Sex differences in anxiety disorders: Interactions between fear, stress, and gonadal hormones. Horm. Behav. 76, 106–117. https://doi.org/10.1016/j.yhbeh.2015.04.002
Mah, C. D., Mah, K. E., Kezirian, E. J. und Dement, W. C. (2011). The effects of sleep extension on the athletic performance of collegiate basketball players. Sleep 34, 943–950. https://doi.org/10.5665/SLEEP.1132
Mandsager, K., Harb, S., Cremer, P., Phelan, D., Nissen, S. E. und Jaber, W. (2018). Association of cardiorespiratory fitness with long-term mortality among adults undergoing exercise treadmill testing. JAMA Netw. Open 1, e183605. https://doi.org/10.1001/jamanetworkopen.2018.3605
Mannick, J. B., Del Giudice, G., Lattanzi, M., Valiante, N. M., Praestgaard, J., Huang, B., Lonetto, M. A., Maecker, H. T., Kovarik, J., Carson, S. et al. (2014). mTOR inhibition improves immune function in the elderly. Sci. Transl. Med. 6, 268ra179. https://doi.org/10.1126/scitranslmed.3009892
Manson, J. E., Chlebowski, R. T., Stefanick, M. L., Aragaki, A. K., Rossouw, J. E., Prentice, R. L., Anderson, G., Howard, B. V., Thomson, C. A., LaCroix, A. Z. et al. (2013). The Women’s Health Initiative hormone therapy trials: Update and overview of health outcomes during the intervention and post-stopping phases. JAMA 310, 1353–1368
Mansukhani, M. P., Kolla, B. P., Surani, S., Varon, J. und Ramar, K. (2012). Sleep deprivation in resident physicians, work hour limitations, and related outcomes: A systematic review of the literature. Postgrad. Med. 124, 241–249. https://doi.org/10.3810/pgm.2012.07.2583
Marston, N. A., Giugliano, R. P., Melloni, G. E. M., Park, J.-G., Morrill, V., Blazing, M. A., Ference, B., Stein, E., Stroes, E. S., Braunwald, E. et al. (2022). Association of Apolipoprotein B-containing lipoproteins and risk of myocardial infarction in individuals with and without atherosclerosis: Distinguishing between particle concentration, type, and content. JAMA Cardiol. 7(3), 250–256. http://doi.org/10.1001/jamacardio.2021.5083
Martínez-Lapiscina, E. H., Clavero, P., Toledo, E., Estruch, R., Salas-Salvadó, J., Julián, B. S., Sanchez-Tainta, A., Ros, E., Valls-Pedret, C. und Martinez-Gonzalez, M. Á. (2013). Mediterranean diet improves cognition: The PREDIMED-NAVARRA randomised trial. J. Neurol. Neurosurg. Psychiatry 84, 1318–1325. https://doi.org/10.1136/jnnp-2012-304792
Masana, L., Girona, J., Ibarretxe, D., Rodríguez-Calvo, R., Rosales, R., Vallvé, J.-C., Rodríguez-Borjabad, C., Guardiola, M., Rodríguez, M., Guaita-Esteruelas, S. et al. (2018). Clinical and pathophysiological evidence supporting the safety of extremely low LDL levels: The zero-LDL hypothesis. J. Clin. Lipidol. 12, 292–299.e3. https://doi.org/10.1016/j.jacl.2017.12.018
Masters, C. L. und Selkoe, D. J. (2012). Biochemistry of amyloid β-protein and amyloid deposits in Alzheimer disease. Cold Spring Harb. Perspect. Med. 2, a006262. https://doi.org/10.1101/cshperspect.a006262
Matsuzaki, T., Sasaki, K., Tanizaki, Y., Hata, J., Fujimi, K., Matsui, Y., Sekita, A., Suzuki, S. O., Kanba, S., Kiyohara, Y., et al. (2010). Insulin resistance is associated with the pathology of Alzheimer disease: The Hisayama study. Neurology 75, 764–770. https://doi.org/10.1212/WNL.0b013e3181eee25f.
Mattison, J. A., Roth, G. S., Beasley, T. M., Tilmont, E. M., Handy, A. H., Herbert, R. L., Longo, D. L., Allison, D. B., Young, J. E., Bryant, M. et al. (2012). Impact of caloric restriction on health and survival in rhesus monkeys: The NIA study. Nature 489, https://doi.org/10.1038/nature11432
Maurer, L. F., Schneider, J., Miller, C. B., Espie, C. A. und Kyle, S. D. (2021). The clinical effects of sleep restriction therapy for insomnia: A meta-analysis of randomised controlled trials. Sleep Med. Rev. 58, 101493. https://doi.org/10.1016/j.smrv.2021.101493
McDonald, R. B. und Ramsey, J. J. (2010). Honoring Clive McCay and 75 years of calorie restriction research. J. Nutr. 140, 1205–1210. https://doi.org/10.3945/jn.110.122804
McLaughlin, T., Abbasi, F., Cheal, K., Chu, J., Lamendola, C. und Reaven, G. (2003). Use of metabolic markers to identify overweight individuals who are insulin resistant. Ann. Intern. Med. 139, 802–809. https://doi.org/10.7326/0003-4819-139-10-200311180-00007
McMillin, S. L., Schmidt, D. L., Kahn, B. B. und Witczak, C. A. (2017). GLUT4 is not necessary for overload-induced glucose uptake or hypertrophic growth in mouse skeletal muscle. Diabetes 66, 1491–1500. https://doi.org/10.2337/db16-1075
McNamara, D. J. (2015). The fifty year rehabilitation of the egg. Nutrients 7, 8716–8722. https://doi.org/10.3390/nu7105429
Melov, S., Tarnopolsky, M. A., Beckman, K., Felkey, K. und Hubbard, A. (2007). Resistance exercise reverses aging in human skeletal muscle. PLOS ONE 2, e465. https://doi.org/10.1371/journal.pone.0000465
Mensah, G. A., Wei, G. S., Sorlie, P. D., Fine, L. J., Rosenberg, Y., Kaufmann, P. G., Mussolino, M. E., Hsu, L. L., Addou, E., Engelgau, M. M. und Gordon, D. (2017). Decline in Cardiovascular Mortality: Possible Causes and Implications. Circulation research, 120(2), 366–380. https://doi.org/10.1161/CIRCRESAHA.116.309115
Mensink, R. P. und Katan, M. B. (1992). Effect of dietary fatty acids on serum lipids and lipoproteins. A meta-analysis of 27 trials. Arterioscler. Thromb. J. Vasc. Biol. 12, 911–919. https://doi.org/10.1161/01.atv.12.8.911
Mercken, E. M., Crosby, S. D., Lamming, D. W., JeBailey, L., Krzysik-Walker, S., Villareal, D. T., Capri, M., Franceschi, C., Zhang, Y., Becker, K. et al. (2013). Calorie restriction in humans inhibits the PI3K/AKT pathway and induces a younger transcription profile. Aging Cell 12, 645–651. https://doi.org/10.1111/acel.12088
Michaelson, D. M. (2014). APOE ε4: The most prevalent yet understudied risk factor for Alzheimer’s disease. Alzheimer’s & Dementia. 10, 861–868. https://doi.org/10.1016/j.jalz.2014.06.015
Milewski, M. D., Skaggs, D. L., Bishop, G. A., Pace, J. L., Ibrahim, D. A., Wren, T. A. L. und Barzdukas, A. (2014). Chronic lack of sleep is associated with increased sports injuries in adolescent athletes. J. Pediatr. Orthop. 34, 129–133. https://doi.org/10.1097/BPO.0000000000000151
Miller, R. A., Harrison, D. E., Astle, C. M., Baur, J. A., Boyd, A. R., Cabo, R. de, Fernandez, E., Flurkey, K., Javors, M. A., Nelson, J. F. et al. (2011). Rapamycin, but not resveratrol or simvastatin, extends life span of genetically heterogeneous mice. J. Gerontol. Ser. A 66 A, 191–201. https://doi.org/10.1093/gerona/glq178
Mitter, S. S., Oriá, R. B., Kvalsund, M. P., Pamplona, P., Joventino, E. S., Mota, R. M. S., Gonçalves, D. C., Patrick, P. D., Guerrant, R. L. und Lima, A. A. M. (2012). Apolipoprotein E4 influences growth and cognitive responses to micronutrient supplementation in shantytown children from northeast Brazil. Clinics 67, 11–18. https://doi.org/10.6061/clinics/2012(01)03
Moco, S., Bino, R. J., Vorst, O., Verhoeven, H. A., Groot, J. de, Beek, T. A. van, Vervoort, J. und Vos, C. H. R. de (2006). A liquid chromatography-mass spectrometry-based metabolome database for tomato. Plant Physiol. 141, 1205–1218. https://doi.org/10.1104/pp.106.078428
Mollenhauer, B., Bibl, M., Trenkwalder, C., Stiens, G., Cepek, L., Steinacker, P., Ciesielczyk, B., Neubert, K., Wiltfang, J., Kretzschmar, H. A. et al. (2005). Follow-up investigations in cerebrospinal fluid of patients with dementia with Lewy bodies and Alzheimer’s disease. J. Neural Transm. 112, 933–948. https://doi.org/10.1007/s00702-004-0235-7
Montagne, A., Nation, D. A., Sagare, A. P., Barisano, G., Sweeney, M. D., Chakhoyan, A., Pachicano, M., Joe, E., Nelson, A. R., D’Orazio, L. M. et al. (2020). APOE4 leads to blood-brain barrier dysfunction predicting cognitive decline. Nature 581, 71–76. https://doi.org/10.1038/s41586-020-2247-3
Moraes, W. A. dos S., Poyares, D. R., Guilleminault, C., Ramos, L. R., Bertolucci, P. H. F. und Tufik, S. (2006). The effect of donepezil on sleep and REM sleep EEG in patients with Alzheimer disease: A double-blind placebo-controlled study. Sleep 29, 199–205. https://doi.org/10.1093/sleep/29.2.199
Mosconi, L., Rahman, A., Diaz, I., Wu, X., Scheyer, O., Hristov, H. W., Vallabhajosula, S., Isaacson, R. S., de Leon, M. J. und Brinton, R. D. (2018). Increased Alzheimer’s risk during the menopause transition: A 3-year longitudinal brain imaging study. PLOS ONE 13, e0207885. https://doi.org/10.1371/journal.pone.0207885
Motomura, Y., Kitamura, S., Oba, K., Terasawa, Y., Enomoto, M., Katayose, Y., Hida, A., Moriguchi, Y., Higuchi, S. und Mishima, K. (2013). Sleep debt elicits negative emotional reaction through diminished amygdala-anterior cingulate functional connectivity. PLOS ONE 8, e56578. https://doi.org/10.1371/journal.pone.0056578
Mukherjee, S. (2011). The emperor of all maladies: A biography of cancer. New York: Scribner [(2022). Der König aller Krankheiten. Krebs – eine Biographie. Übers. von B. Schaden. Berlin: Ullstein]
Mullane, K. und Williams, M. (2020). Alzheimer’s disease beyond amyloid: Can the repetitive failures of amyloid-targeted therapeutics inform future approaches to dementia drug discovery? Biochem. Pharmacol. 177, 113945. https://doi.org/10.1016/j.bcp.2020.113945
Müller, U., Winter, P. und Graeber, M. B. (2013). A presenilin 1 mutation in the first case of Alzheimer’s disease. Lancet Neurol. 12, 129–130. https://doi.org/10.1016/S1474-4422(12)70307-1
Naci, H. und Ioannidis, J. P. A. (2015). Comparative effectiveness of exercise and drug interventions on mortality outcomes: Metaepidemiological study. Br. J. Sports Med. 49, 1414–1422. https://doi.org/10.1136/bjsports-2015-f5577rep
Naghshi, S., Sadeghian, M., Nasiri, M., Mobarak, S., Asadi, M. und Sadeghi, O. (2020). Association of total nut, tree nut, peanut, and peanut butter consumption with cancer incidence and mortality: A comprehensive systematic review and dose-response meta-analysis of observational studies. Adv. Nutr. 12, 793–808. https://doi.org/10.1093/advances/nmaa152
Naimi, T. S., Stockwell, T., Zhao, J., Xuan, Z., Dangardt, F., Saitz, R., Liang, W. und Chikritzhs, T. (2017). Selection biases in observational studies affect associations between »moderate« alcohol consumption and mortality. Addiction 112, 207–214. https://doi.org/10.1111/add.13451
Nakamura, T., Shoji, M., Harigaya, Y., Watanabe, M., Hosoda, K., Cheung, T. T., Shaffer, L. M., Golde, T. E., Younkin, L. H. und Younkin, S. G. (1994). Amyloid beta protein levels in cerebrospinal fluid are elevated in early-onset Alzheimer’s disease. Ann. Neurol. 36, 903–911. https://doi.org/10.1002/ana.410360616
Nasir, K., Cainzos-Achirica, M., Valero-Elizondo, J., Ali, S. S., Havistin, R., Lakshman, S., Blaha, M. J., Blankstein, R., Shapiro, M. D., Arias, L. et al. (2022). Coronary atherosclerosis in an asymptomatic U. S. population. JACC Cardiovasc. Imaging 15(9), 1619–1621. https://doi.org/10.1016/j.jcmg.2022.03.010
NCI (National Cancer Institute, 2015). Risk factors: Age. https://www.cancer.gov/about-cancer/causes-prevention/risk/age
NCI (National Cancer Institute, 2021). Risk factors: Age. https://www.cancer.gov/about-cancer/causes-prevention/risk/age
NCI (National Cancer Institute, 2022b). SEER survival statistics – SEER Cancer Query Systems. https://seer.cancer.gov/canques/survival.html
Nedeltcheva, A. V., Kessler, L., Imperial, J. und Penev, P. D. (2009). Exposure to recurrent sleep restriction in the setting of high caloric intake and physical inactivity results in increased insulin resistance and reduced glucose tolerance. J. Clin. Endocrinol. Metab. 94, 3242–3250. https://doi.org/10.1210/jc.2009-0483
Neth, B. J. und Craft, S. (2017). Insulin resistance and Alzheimer’s disease: Bioenergetic linkages. Front. Aging Neurosci. 9, 345. https://doi.org/10.3389/fnagi.2017.00345
Neu, S. C., Pa, J., Kukull, W., Beekly, D., Kuzma, A., Gangadharan, P., Wang, L.-S., Romero, K., Arneric, S. P., Redolfi, A. et al. (2017). Apolipoprotein E genotype and sex risk factors for Alzheimer disease: A meta-analysis. JAMA Neurol. 74, 1178–1189. https://doi.org/10.1001/jamaneurol.2017.2188
Newman, A. B., Kupelian, V., Visser, M., Simonsick, E. M., Goodpaster, B. H., Kritchevsky, S. B., Tylavsky, F. A., Rubin, S. M. und Harris, T. B. (2006). Strength, but not muscle mass, is associated with mortality in the Health, Aging and Body Composition Study cohort. J. Gerontol. Ser. A 61, 72–77. https://doi.org/10.1093/gerona/61.1.72
Newman, C. B., Preiss, D., Tobert, J. A., Jacobson, T. A., Page, R. L., Goldstein, L. B., Chin, C., Tannock, L. R., Miller, M., Raghuveer, G. et al. (2019). Statin safety and associated adverse events: A scientific statement from the American Heart Association. Arterioscler. Thromb. Vasc. Biol. 39, e38-e81. https://doi.org/10.1161/ATV.0000000000000073
New York Times. (1985). New evidence, old debate. 12. September. https://www.nytimes.com/1985/09/12/us/new-evidence-old-debate.html
Ngandu, T., Lehtisalo, J., Solomon, A., Levälahti, E., Ahtiluoto, S., Antikainen, R., Bäckman, L., Hänninen, T., Jula, A., Laatikainen, T. et al. (2015). A 2 year multidomain intervention of diet, exercise, cognitive training, and vascular risk monitoring versus control to prevent cognitive decline in at-risk elderly people (FINGER): A randomised controlled trial. Lancet 385, 2255–2263. https://doi.org/10.1016/S0140-6736(15)60461-5
NHTSA (National Highway Traffic Safety Administration). (2022a). Early estimates of motor vehicle traffic fatalities and fatality rate by sub-categories in 2021. Traffic Safety Facts, May. https://crashstats.nhtsa.dot.gov/Api/Public/ViewPublication/813298
NHTSA (National Highway Traffic Safety Administration). (2022b). Fatality and Injury Reporting System Tool (FIRST). https://cdan.dot.gov/query
Nicklas, B. J., Chmelo, E., Delbono, O., Carr, J. J., Lyles, M. F. und Marsh, A. P. (2015). Effects of resistance training with and without caloric restriction on physical function and mobility in overweight and obese older adults: A randomized controlled trial. Am. J. Clin. Nutr. 101, 991–999. https://doi.org/10.3945/ajcn.114.105270
NIDDK (National Institute of Diabetes and Digestive and Kidney Diseases). (2018). Diabetes in America. 3. Aufl. Bethesda, MD: NIDDK.
Ninonuevo, M. R., Park, Y., Yin, H., Zhang, J., Ward, R. E., Clowers, B. H., German, J. B., Freeman, S. L., Killeen, K., Grimm, R. et al. (2006). A strategy for annotating the human milk glycome. J. Agric. Food Chem. 54, 7471–7480. https://doi.org/10.1021/jf0615810
Nuttall, F. Q. und Gannon, M. C. (2006). The metabolic response to a high-protein, low-carbohydrate diet in men with type 2 diabetes mellitus. Metabolism 55, 243–251. https://doi.org/10.1016/j.metabol.2005.08.027
Nymo, S., Coutinho, S. R., Jørgensen, J., Rehfeld, J. F., Truby, H., Kulseng, B. und Martins, C. (2017). Timeline of changes in appetite during weight loss with a ketogenic diet. Int. J. Obes. 41, 1224–1231. https://doi.org/10.1038/ijo.2017.96
O’Donoghue, M. L., Fazio, S., Giugliano, R. P. et al. (2019). Lipoprotein(a), PCSK9 inhibition, and cardiovascular risk. Circulation, 139(12): 1483–1492. doi.org/10.1161/CIRCULATIONAHA.118.037184
Ogden, C. L., Fryar, C. D., Carroll, M. D. und Flegal, K. M. (2004). Mean body weight, height, and body mass index, United States 1960–2002. Adv. Data 1–17
Ohayon, M. M., Carskadon, M. A., Guilleminault, C. und Vitiello, M. V. (2004). Meta-analysis of quantitative sleep parameters from childhood to old age in healthy individuals: Developing normative sleep values across the human lifespan. Sleep 27, 1255–1273. https://doi.org/10.1093/sleep/27.7.1255
O’Keefe, J. H., Cordain, L., Harris, W. H., Moe, R. M. und Vogel, R. (2004). Optimal low-density lipoprotein is 50 to 70 mg/dl: Lower is better and physiologically normal. J. Am. Coll. Cardiol. 43, 2142–2146. https://doi.org/10.1016/j.jacc.2004.03.046
Oliveira, C., Cotrim, H. und Arrese, M. (2019). Nonalcoholic fatty liver disease risk factors in Latin American populations: Current scenario and perspectives. Clin. Liver Dis. 13, 39–42. https://doi.org/10.1002/cld.759
Oriá, R. B., Patrick, P. D., Blackman, J. A., Lima, A. A. M. und Guerrant, R. L. (2007). Role of apolipoprotein E4 in protecting children against early childhood diarrhea outcomes and implications for later development. Med. Hypotheses 68, 1099–1107. https://doi.org/10.1016/j.mehy.2006.09.036
Orphanet (2022). Orphanet: 3 hydroxyisobutyric aciduria. https://www.orpha.net/consor/cgi-bin/OC_Exp.php?Lng=EN&Expert=939
Osorio, R. S., Pirraglia, E., Agüera-Ortiz, L. F., During, E. H., Sacks, H., Ayappa, I., Walsleben, J., Mooney, A., Hussain, A., Glodzik, L. et al. (2011). Greater risk of Alzheimer’s disease in older adults with insomnia. J. Am. Geriatr. Soc. 59, 559–562. https://doi.org/10.1111/j.1532-5415.2010.03288.x
Oulhaj, A., Jernerén, F., Refsum, H., Smith, A. D. und de Jager, C. A. (2016). Omega-3 fatty acid status enhances the prevention of cognitive decline by B vitamins in mild cognitive impairment. J. Alzheimers Dis. 50, 547–557. https://doi.org/10.3233/JAD-150777
Oyetakin-White, P., Suggs, A., Koo, B., Matsui, M. S., Yarosh, D., Cooper, K. D. und Baron, E. D. (2015). Does poor sleep quality affect skin ageing? Clin. Exp. Dermatol. 40, 17–22. https://doi.org/10.1111/ced.12455
Patel, A. K., Reddy, V., Shumway, K. R. und Araujo, J. F. (2022). Physiology, sleep stages. Treasure Island, FL: StatPearls
Patel, D., Steinberg, J. und Patel, P. (2018). Insomnia in the elderly: A review. J. Clin. Sleep Med. 14, 1017–1024. https://doi.org/10.5664/jcsm.7172
Peng, B., Yang, Q., B Joshi, R., Liu, Y., Akbar, M., Song, B.-J., Zhou, S. und Wang, X. (2020). Role of alcohol drinking in Alzheimer’s disease, Parkinson’s disease, and amyotrophic lateral sclerosis. Int. J. Mol. Sci. 21, 2316. https://doi.org/10.3390/ijms21072316
Perls, T. T. (2017). Male centenarians: How and why are they different from their female counterparts? J. Am. Geriatr. Soc. 65, 1904–1906. https://doi.org/10.1111/jgs.14978
Pesch, B., Kendzia, B., Gustavsson, P., Jöckel, K.-H., Johnen, G., Pohlabeln, H., Olsson, A., Ahrens, W., Gross, I. M., Brüske, I. et al. (2012). Cigarette smoking and lung cancer-relative risk estimates for the major histological types from a pooled analysis of case-control studies. Int. J. Cancer 131, 1210–1219. https://doi.org/10.1002/ijc.27339
Petersen, K. F., Dufour, S., Savage, D. B., Bilz, S., Solomon, G., Yonemitsu, S., Cline, G. W., Befroy, D., Zemany, L., Kahn, B. B. et al. (2007). The role of skeletal muscle insulin resistance in the pathogenesis of the metabolic syndrome. Proc. Natl. Acad. Sci. 104, 12587–12594. https://doi.org/10.1073/pnas.0705408104
Petersen, M. C. und Shulman, G. I. (2018). Mechanisms of insulin action and insulin resistance. Physiol. Rev. 98, 2133–2223. https://doi.org/10.1152/physrev.00063.2017
Pfister, R., Sharp, S. J., Luben, R., Khaw, K.-T. und Wareham, N. J. (2011). No evidence of an increased mortality risk associated with low levels of glycated haemoglobin in a non-diabetic UK population. Diabetologia 54, 2025–2032. https://doi.org/10.1007/s00125-011-2162-0
Phinney, S. und Volek, J. (2018). The science of nutritional ketosis and appetite. Virta (Blog), 25. Juli. https://www.virtahealth.com/blog/ketosis-appetite-hunger
Picard, C. (2018). The secrets to living to 100 (according to people who’ve done it). Good Housekeeping
Picton, J. D., Marino, A. B. und Nealy, K. L. (2018). Benzodiazepine use and cognitive decline in the elderly. Am. J. Health. Syst. Pharm. 75, e6-e12. https://doi.org/10.2146/ajhp160381
Pollack, A. (2005). Huge genome project is proposed to fight cancer. New York Times, 28. März. https://www.nytimes.com/2005/03/28/health/huge-genome-project-is-proposed-to-fight-cancer.html
Pontzer, H., Wood, B. M. und Raichlen, D. A. (2018). Hunter-gatherers as models in public health. Obes. Rev. 19, 24–35. https://doi.org/10.1111/obr.12785
Potvin, O., Lorrain, D., Forget, H., Dubé, M., Grenier, S., Préville, M. und Hudon, C. (2012). Sleep quality and 1-year incident cognitive impairment in community-dwelling older adults. Sleep 35, 491–499. https://doi.org/10.5665/sleep.1732
Powell-Wiley, T. M., Poirier, P., Burke, L. E., Després, J.-P., Gordon-Larsen, P., Lavie, C. J., Lear, S. A., Ndumele, C. E., Neeland, I. J., Sanders, P. et al. (2021). Obesity and cardiovascular disease: A scientific statement from the American Heart Association. Circulation 143, e984-e1010. https://doi.org/10.1161/CIR.0000000000000973
Prather, A. A., Bogdan, R. und Hariri, A. R. (2013). Impact of sleep quality on amygdala reactivity, negative affect, and perceived stress. Psychosom. Med. 75, 350–358. https://doi.org/10.1097/PSY.0b013e31828ef15b
Prati, D., Taioli, E., Zanella, A., Della Torre, E., Butelli, S., Del Vecchio, E., Vianello, L., Zanuso, F., Mozzi, F., Milani, S. et al. (2002). Updated definitions of healthy ranges for serum alanine aminotransferase levels. Ann. Intern. Med. 137, 1–10. https://doi.org/10.7326/0003-4819-137-1-200207020-00006
Proctor, R. N. (1995). Cancer wars: How politics shapes what we know and don’t know about cancer. New York: Basic Books
Proctor, R. N. (2001). Tobacco and the global lung cancer epidemic. Nat. Rev. Cancer 1, 82–86. https://doi.org/10.1038/35094091
Rabinovici, G. D., Gatsonis, C., Apgar, C., Chaudhary, K., Gareen, I., Hanna, L., Hendrix, J., Hillner, B. E., Olson, C., Lesman-Segev, O. H. et al. (2019). Association of amyloid positron emission tomography with subsequent change in clinical management among medicare beneficiaries with mild cognitive impairment or dementia. JAMA 321, 1286–1294. https://doi.org/10.1001/jama.2019.2000
Rahman, A., Schelbaum, E., Hoffman, K., Diaz, I., Hristov, H., Andrews, R., Jett, S., Jackson, H., Lee, A., Sarva, H. et al. (2020). Sex-driven modifiers of Alzheimer risk: A multimodality brain imaging study. Neurology 95, e166-e178. https://doi.org/10.1212/WNL.0000000000009781
Raichle, M. E. und Gusnard, D. A. (2002). Appraising the brain’s energy budget. Proc. Natl. Acad. Sci. 99, 10237–10239. https://doi.org/10.1073/pnas.172399499
Rajpathak, S. N., Liu, Y., Ben-David, O., Reddy, S., Atzmon, G., Crandall, J. und Barzilai, N. (2011). Lifestyle factors of people with exceptional longevity. J. Am. Geriatr. Soc. 59, 1509–1512. https://doi.org/10.1111/j.1532-5415.2011.03498.x
Rao, M. N., Neylan, T. C., Grunfeld, C., Mulligan, K., Schambelan, M. und Schwarz, J.-M. (2015). Subchronic sleep restriction causes tissue-specific insulin resistance. J. Clin. Endocrinol. Metab. 100, 1664–1671. https://doi.org/10.1210/jc.2014-3911
Raskind, M. A., Peskind, E. R., Hoff, D. J., Hart, K. L., Holmes, H. A., Warren, D., Shofer, J., O’Connell, J., Taylor, F., Gross, C. et al. (2007). A parallel group placebo controlled study of prazosin for trauma nightmares and sleep disturbance in combat veterans with post-traumatic stress disorder. Biol. Psychiatry 61, 928–934. https://doi.org/10.1016/j.biopsych.2006.06.032
Raskind, M. A., Peskind, E. R., Kanter, E. D., Petrie, E. C., Radant, A., Thompson, C. E., Dobie, D. J., Hoff, D., Rein, R. J., Straits-Tröster, K. et al. (2003). Reduction of nightmares and other PTSD symptoms in combat veterans by prazosin: A placebo-controlled study. Am. J. Psychiatry 160, 371–373. https://doi.org/10.1176/appi.ajp.160.2.371
Ratnakumar, A., Zimmerman, S. E., Jordan, B. A. und Mar, J. C. (2019). Estrogen activates Alzheimer’s disease genes. Alzheimer’s & Dementia. 5, 906–917. https://doi.org/10.1016/j.trci.2019.09.004
Real, T. (1998). I don’t want to talk about it: Overcoming the secret legacy of male depression. New York: Scribner [(1999). Mir geht’s doch gut. Männliche Depressionen – warum sie so oft verborgen bleiben, woran man sie erkennt und wie man sie heilen kann. Übers. von C. Strüh. Bern: Scherz]
Reddy, O. C. und van der Werf, Y. D. (2020). The sleeping brain: Harnessing the power of the glymphatic system through lifestyle choices. Brain Sci. 10, 868. https://doi.org/10.3390/brainsci10110868
Reiman, E. M., Arboleda-Velasquez, J. F., Quiroz, Y. T., Huentelman, M. J., Beach, T. G., Caselli, R. J., Chen, Y., Su, Y., Myers, A. J., Hardy, J. et al. (2020). Exceptionally low likelihood of Alzheimer’s dementia in APOE2 homozygotes from a 5,000-person neuropathological study. Nat. Commun. 11, 667. https://doi.org/10.1038/s41467-019-14279-8
Reiman, E. M., Caselli, R. J., Yun, L. S., Chen, K., Bandy, D., Minoshima, S., Thibodeau, S. N. und Osborne, D. (1996). Preclinical evidence of Alzheimer’s disease in persons homozygous for the epsilon 4 allele for apolipoprotein E. N. Engl. J. Med. 334, 752–758. https://doi.org/10.1056/NEJM199603213341202
Reimers, C. D., Knapp, G., und Reimers, A. K. (2012). Does physical activity increase life expectancy? A review of the literature. J. Aging Res. 2012, 243958. https://doi.org/10.1155/2012/243958
Repantis, D., Wermuth, K., Tsamitros, N., Danker-Hopfe, H., Bublitz, J. C., Kühn, S. und Dresler, M. (2020). REM sleep in acutely traumatized individuals and interventions for the secondary prevention of post-traumatic stress disorder. Eur. J. Psychotraumatology 11, 1740492. https://doi.org/10.1080/20008198.2020.1740492
Reutrakul, S. und Van Cauter, E. (2018). Sleep influences on obesity, insulin resistance, and risk of type 2 diabetes. Metabolism 84, 56–66. https://doi.org/10.1016/j.metabol.2018.02.010
Revelas, M., Thalamuthu, A., Oldmeadow, C., Evans, T.-J., Armstrong, N. J., Kwok, J. B., Brodaty, H., Schofield, P. R., Scott, R. J., Sachdev, P. S. et al. (2018). Review and meta-analysis of genetic polymorphisms associated with exceptional human longevity. Mech. Ageing Dev. 175, 24–34. https://doi.org/10.1016/j.mad.2018.06.002
Richter, E. A. (2021). Is GLUT4 translocation the answer to exercise-stimulated muscle glucose uptake? Am. J. Physiol.-Endocrinol. Metab. 320, E240-E243. https://doi.org/10.1152/ajpendo.00503.2020
Riis, J. A. (1901). The making of an American. United States: Aegypan
Ritchie, H. und Roser, M. (2018). Causes of death. Our World in Data. https://ourworldindata.org/causes-of-death
Rosenberg, A., Mangialasche, F., Ngandu, T., Solomon, A. und Kivipelto, M. (2020). Multidomain interventions to prevent cognitive impairment, Alzheimer’s disease, and dementia: From FINGER to world-wide FINGERS. J. Prev. Alzheimers Dis. 7(1): 29–36. https://doi.org/10.14283/jpad.2019.41
Rosenberg, S. A. und Barry, J. B. (1992). The Transformed Cell. Unlocking the Mysteries of Cancer. New York: Putnam [(1992). Die veränderte Zelle. Die Rosenberg-Story: Das Rätsel Krebs und seine Entschlüsselung. Übers. von S. Vogel. München: Goldmann]
Roy, J. und Forest, G. (2018). Greater circadian disadvantage during evening games for the National Basketball Association (NBA), National Hockey League (NHL) and National Football League (NFL) teams travelling westward. J. Sleep Res. 27, 86–89. https://doi.org/10.1111/jsr.12565
Rozentryt, P., Haehling, S. von, Lainscak, M., Nowak, J. U., Kalantar-Zadeh, K., Polonski, L. und Anker, S. D. (2010). The effects of a high-caloric protein-rich oral nutritional supplement in patients with chronic heart failure and cachexia on quality of life, body composition, and inflammation markers: A randomized, double-blind pilot study. J. Cachexia Sarcopenia Muscle 1, 35–42. https://doi.org/10.1007/s13539-010-0008-0
Rupp, T. L., Wesensten, N. J. und Balkin, T. J. (2012). Trait-like vulnerability to total and partial sleep loss. Sleep 35, 1163–1172. https://doi.org/10.5665/sleep.2010
Sabatini, D. M., Erdjument-Bromage, H., Lui, M., Tempst, P. und Snyder, S. H. (1994). RAFT1: A mammalian protein that binds to FKBP12 in a rapamycin-dependent fashion and is homologous to yeast TORs. Cell 78, 35–43. https://doi.org/10.1016/0092-8674(94)90570-3
Samra, R. A. (2010). Fats and satiety. In Montmayeur, J.-P. und Coutre, J. le (Hrsg.) Fat detection: Taste, texture, and post ingestive effects. Boca Raton, FL: CRC Press/Taylor and Francis
San Millán, I. und Brooks, G. A. (2018). Assessment of metabolic flexibility by means of measuring blood lactate, fat, and carbohydrate oxidation responses to exercise in professional endurance athletes and less-fit individuals. Sports Med. Auckl. NZ 48, 467–479. https://doi.org/10.1007/s40279-017-0751-x
Sasco, A. J., Secretan, M. B. und Straif, K. (2004). Tobacco smoking and cancer: A brief review of recent epidemiological evidence. Lung Cancer Amst. Neth. 45, Suppl 2, S3-9. https://doi.org/10.1016/j.lungcan.2004.07.998
Saul, S. (2006). Record sales of sleeping pills are causing worries. New York Times, 7. Februar. https://www.nytimes.com/2006/02/07/business/record-sales-of-sleeping-pills-are-causing-worries.html
Sawka, M. N., Gonzalez, R. R. und Pandolf, K. B. (1984). Effects of sleep deprivation on thermoregulation during exercise. Am. J. Physiol. 246, R72-77. https://doi.org/10.1152/ajpregu.1984.246.1.R72
Schoenfeld, B. J. und Aragon, A. A. (2018). How much protein can the body use in a single meal for muscle-building? Implications for daily protein distribution. J. Int. Soc. Sports Nutr. 15, 10. https://doi.org/10.1186/s12970-018-0215-1
Schwingshackl, L., Schwedhelm, C., Hoffmann, G., Knüppel, S., Laure Preterre, A., Iqbal, K., Bechthold, A., De Henauw, S., Michels, N., Devleesschauwer, B. et al. (2018). Food groups and risk of colorectal cancer. Int. J. Cancer 142, 1748–1758. https://doi.org/10.1002/ijc.31198
Schwingshackl, L., Zähringer, J., Beyerbach, J., Werner, S., Heseker, H., Koletzko, B. und Meerpoh, J. Total dietary fat intake, fat quality, and health outcomes: A scoping review of systematic reviews of prospective studies. Ann. Nutr. Metab. 77(1), 4–15. https://doi.org/10.1159/000515058
Sebastiani, P., Gurinovich, A., Nygaard, M., Sasaki, T., Sweigart, B., Bae, H., Andersen, S. L., Villa, F., Atzmon, G., Christensen, K. et al. (2019). APOE alleles and extreme human longevity. J. Gerontol. Ser. A 74, 44–51. https://doi.org/10.1093/gerona/gly174
Sebastiani, P., Nussbaum, L., Andersen, S. L., Black, M. J. und Perls, T. T. (2016). Increasing sibling relative risk of survival to older and older ages and the importance of precise definitions of »aging,« »life span,« and »longevity«. J. Gerontol. A. Biol. Sci. Med. Sci. 71, 340–346. https://doi.org/10.1093/gerona/glv020
Seidelin, K. N. (1995). Fatty acid composition of adipose tissue in humans. Implications for the dietary fat-serum cholesterol-CHD issue. Prog. Lipid Res. 34, 199–217. https://doi.org/10.1016/0163-7827(95)00004-J
Seifert, T., Brassard, P., Wissenberg, M., Rasmussen, P., Nordby, P., Stallknecht, B., Adser, H., Jakobsen, A. H., Pilegaard, H., Nielsen, H. B. et al. (2010). Endurance training enhances BDNF release from the human brain. Am. J. Physiol. Regul. Integr. Comp. Physiol. 298, R372-377. https://doi.org/10.1152/ajpregu.00525.2009
Selvarani, R., Mohammed, S. und Richardson, A. (2021). Effect of rapamycin on aging and age-related diseases–past and future. GeroScience 43, 1135–1158. https://doi.org/10.1007/s11357-020-00274-1
Serna, E., Gambini, J., Borras, C., Abdelaziz, K. M., Mohammed, K., Belenguer, A., Sanchis, P., Avellana, J. A., Rodriguez-Mañas, L. und Viña, J. (2012). Centenarians, but not octogenarians, up-regulate the expression of microRNAs. Sci. Rep. 2, 961. https://doi.org/10.1038/srep00961
Shahid, A., Wilkinson, K., Marcu, S. und Shapiro, C. M. (2011). Insomnia Severity Index (ISI). In: STOP, THAT and one hundred other sleep scales, ed. A. Shahid, K. Wilkinson, S. Marcu und C. M. Shapiro, 191–193. New York: Springer
Shan, Z., Ma, H., Xie, M., Yan, P., Guo, Y., Bao, W., Rong, Y., Jackson, C. L., Hu, F. B. und Liu, L. (2015). Sleep duration and risk of type 2 diabetes: A meta-analysis of prospective studies. Diabetes Care 38, 529–537. https://doi.org/10.2337/dc14-2073
Shephard, R. J. (2009). Maximal oxygen intake and independence in old age. Br. J. Sports Med. 43, 342–346. https://doi.org/10.1136/bjsm.2007.044800
Shmagel, A., Ngo, L., Ensrud, K. und Foley, R. (2018). Prescription medication use among community-based US adults with chronic low back pain: A cross-sectional population based study. J. Pain 19, 1104–1112. https://doi.org/10.1016/j.jpain.2018.04.004
Siegel, R. L., Miller, K. D., Fuchs, H. E. und Jemal, A. (2021). Cancer statistics, 2021. CA. Cancer J. Clin. 71, 7–33. https://doi.org/10.3322/caac.21654
Slayday, R. E., Gustavson, D. E., Elman, J. A., Beck, A., McEvoy, L. K., Tu, X. M., Fang, B., Hauger, R. L., Lyons, M. J., McKenzie, R. E. et al. (2021). Interaction between alcohol consumption and apolipoprotein E (ApoE) genotype with cognition in middle-aged men. J. Int. Neuropsychol. Soc. 27, 56–68. https://doi.org/10.1017/S1355617720000570
Sleeman, J. und Steeg, P. S. (2010). Cancer metastasis as a therapeutic target. Eur. J. Cancer 46, 1177–1180. https://doi.org/10.1016/j.ejca.2010.02.039
Small, G. W., Ercoli, L. M., Silverman, D. H. S., Huang, S.-C., Komo, S., Bookheimer, S. Y., Lavretsky, H., Miller, K., Siddarth, P., Rasgon, N. L. et al. (2000). Cerebral metabolic and cognitive decline in persons at genetic risk for Alzheimer’s disease. Proc. Natl. Acad. Sci. 97, 6037–6042
Smith, A. D., Smith, S. M., de Jager, C. A., Whitbread, P., Johnston, C., Agacinski, G., Oulhaj, A., Bradley, K. M., Jacoby, R. und Refsum, H. (2010). Homocysteine-lowering by B vitamins slows the rate of accelerated brain atrophy in mild cognitive impairment: A randomized controlled trial. PLOS ONE 5, e12244. https://doi.org/10.1371/journal.pone.0012244
Smith, C. und Lapp, L. (1991). Increases in number of REMS and REM density in humans following an intensive learning period. Sleep 14, 325–330. https://doi.org/10.1093/sleep/14.4.325
Smith, C. und Smith, D. (2003). Ingestion of ethanol just prior to sleep onset impairs memory for procedural but not declarative tasks. Sleep 26, 185–191
Sniderman, A. D., Bhopal, R., Prabhakaran, D., Sarrafzadegan, N. und Tchernof, A. (2007). Why might South Asians be so susceptible to central obesity and its atherogenic consequences? The adipose tissue overflow hypothesis. Int. J. Epidemiol. 36, 220–225. https://doi.org/10.1093/ije/dyl245
Sniderman, A. D., Thanassoulis, G., Williams, K. und Pencina, M. (2016). Risk of premature cardiovascular disease vs the number of premature cardiovascular events. JAMA Cardiol. 1, 492–494. https://doi.org/10.1001/jamacardio.2016.0991
Sokol, D. K. (2013). »First do no harm« revisited. BMJ 347, f6426. https://doi.org/10.1136/bmj.f6426
Soran, H., Ho, J. H. und Durrington, P. N. (2018). Acquired low cholesterol: Diagnosis and relevance to safety of low LDL therapeutic targets. Curr. Opin. Lipidol. 29, 318–326. https://doi.org/10.1097/MOL.0000000000000526
Souich, P. du, Roederer, G. und Dufour, R. (2017). Myotoxicity of statins: Mechanism of action. Pharmacol. Ther. 175, 1–16. https://doi.org/10.1016/j.pharmthera.2017.02.029
Spaeth, A. M., Dinges, D. F. und Goel, N. (2015). Resting metabolic rate varies by race and by sleep duration. Obesity 23, 2349–2356. https://doi.org/10.1002/oby.21198
Spencer, C. (2005). Genes, aging and immortality. Upper Saddle River, NJ: Pearson
Sperling, R. A., Aisen, P. S., Beckett, L. A., Bennett, D. A., Craft, S., Fagan, A. M., Iwatsubo, T., Jack, C. R., Kaye, J., Montine, T. J. et al. (2011). Toward defining the preclinical stages of Alzheimer’s disease: Recommendations from the National Institute on Aging-Alzheimer’s Association workgroups on diagnostic guidelines for Alzheimer’s disease. Alzheimer’s & Dementia. 7, 280–292. https://doi.org/10.1016/j.jalz.2011.03.003
Spiegel, K., Leproult, R., L’Hermite-Balériaux, M., Copinschi, G., Penev, P. D. und Van Cauter, E. (2004b). Leptin levels are dependent on sleep duration: Relationships with sympathovagal balance, carbohydrate regulation, cortisol, and thyrotropin. J. Clin. Endocrinol. Metab. 89, 5762–5771.
Spiegel, K., Leproult, R. und Van Cauter, E. (1999). Impact of sleep debt on metabolic and endocrine function. Lancet 354, 1435–1439. https://doi.org/10.1016/S0140-6736(99)01376-8
Spiegel, K., Tasali, E., Penev, P. und Van Cauter, E. (2004a). Brief communication: Sleep curtailment in healthy young men is associated with decreased leptin levels, elevated ghrelin levels, and increased hunger and appetite. Ann. Intern. Med. 141, 846–850. https://doi.org/10.7326/0003-4819-141-11-200412070-00008
Spillane, S., Shiels, M. S., Best, A. F., Haozous, E. A., Withrow, D. R., Chen, Y., Berrington de González, A. und Freedman, N. D. (2020). Trends in alcohol-induced deaths in the United States, 2000–2016. JAMA Netw. Open 3, e1921451. https://doi.org/10.1001/jamanetworkopen.2019.21451
Spira, A. P., Gamaldo, A. A., An, Y., Wu, M. N., Simonsick, E. M., Bilgel, M., Zhou, Y., Wong, D. F., Ferrucci, L. und Resnick, S. M. (2013). Self-reported sleep and β-amyloid deposition in community-dwelling older adults. JAMA Neurol. 70, 1537–1543. https://doi.org/10.1001/jamaneurol.2013.4258
Sprecher, K. E., Bendlin, B. B., Racine, A. M., Okonkwo, O. C., Christian, B. T., Koscik, R. L., Sager, M. A., Asthana, S., Johnson, S. C. und Benca, R. M. (2015). Amyloid burden is associated with self-reported sleep in non-demented late middle-aged adults. Neurobiol. Aging 36, 2568–2576. https://doi.org/10.1016/j.neurobiolaging.2015.05.004
Stamatakis, K. A. und Punjabi, N. M. (2010). Effects of sleep fragmentation on glucose metabolism in normal subjects. Chest 137, 95–101. https://doi.org/10.1378/chest.09-0791
Standl, E., Schnell, O. und Ceriello, A. (2011). Postprandial hyperglycemia and glycemic variability: Should we care? Diabetes Care 34, Suppl 2, S120-127. https://doi.org/10.2337/dc11-s206
Stary, H. C. (2003). Atlas of atherosclerosis: progression and regression. Boca Raton, FL: CRC Press
Stefan, N., Schick, F. und Häring, H.-U. (2017). Causes, characteristics, and consequences of metabolically unhealthy normal weight in humans. Cell Metab. 26, 292–300. https://doi.org/10.1016/j.cmet.2017.07.008
Stickgold, R., Whidbee, D., Schirmer, B., Patel, V. und Hobson, J. A. (2000). Visual discrimination task improvement: A multi-step process occurring during sleep. J. Cogn. Neurosci. 12, 246–254. https://doi.org/10.1162/089892900562075
Stobbe, M. (2021). U. S. overdose deaths topped 100,000 in one year, officials say. AP News, 17. November. https://apnews.com/article/overdodse-deaths-fentanayl-health-f34b022d75a1eb9776e27903ab40670f.
Stomrud, E., Hansson, O., Zetterberg, H., Blennow, K., Minthon, L. und Londos, E. (2010). Correlation of longitudinal cerebrospinal fluid biomarkers with cognitive decline in healthy older adults. Arch. Neurol. 67, 217–223. https://doi.org/10.1001/archneurol.2009.316
Stroes, E. S., Thompson, P. D., Corsini, A., Vladutiu, G. D., Raal, F. J., Ray, K. K., Roden, M., Stein, E., Tokgözoğlu, L., Nordestgaard, B. G. et al. (2015). Statin-associated muscle symptoms: impact on statin therapy–European Atherosclerosis Society Consensus Panel Statement on Assessment, Aetiology and Management. Eur. Heart J. 36, 1012–1022. https://doi.org/10.1093/eurheartj/ehv043
Strong, R., Miller, R. A., Astle, C. M., Baur, J. A., Cabo, R. de, Fernandez, E., Guo, W., Javors, M., Kirkland, J. L., Nelson, J. F. et al. (2013). Evaluation of resveratrol, green tea extract, curcumin, oxaloacetic acid, and medium-chain triglyceride oil on life span of genetically heterogeneous mice. J. Gerontol. Ser. A 68, 6–16. https://doi.org/10.1093/gerona/gls070
Strozyk, D., Blennow, K., White, L. R. und Launer, L. J. (2003). CSF Abeta 42 levels correlate with amyloid-neuropathology in a population-based autopsy study. Neurology 60, 652–656.
Sudimac, S., Sale, V. und Kühn, S. (2022). How nature nurtures: Amygdala activity decreases as the result of a one-hour walk in nature. Mol Psychiatry. https://doi.org/10.1038/s41380-022-01720-6
Sumithran, P., Prendergast, L. A., Delbridge, E., Purcell, K., Shulkes, A., Kriketos, A. und Proietto, J. (2013). Ketosis and appetite-mediating nutrients and hormones after weight loss. Eur. J. Clin. Nutr. 67, 759–764. https://doi.org/10.1038/ejcn.2013.90
Suzuki, K., Elkind, M. S., Boden-Albala, B., Jin, Z., Berry, G., Di Tullio, M. R., Sacco, R. L. und Homma, S. (2009). Moderate alcohol consumption is associated with better endothelial function: A cross sectional study. BMC Cardiovasc. Disord. 9, 8. https://doi.org/10.1186/1471-2261-9-8
Tabata, I., Nishimura, K., Kouzaki, M., Hirai, Y., Ogita, F., Miyachi, M. und Yamamoto, K. (1996). Effects of moderate-intensity endurance and high-intensity intermittent training on anaerobic capacity and VO2max. Med. Sci. Sports Exerc. 28, 1327–1330. https://doi.org/10.1097/00005768-199610000-00018
Taieb, J. und Gallois, C. (2020). Adjuvant chemotherapy for stage III colon cancer. Cancers, 12(9), 2679. https://doi.org/10.3390/cancers12092679
Tang, C., Liu, C., Fang, P., Xiang, Y. und Min, R. (2019). Work-related accumulated fatigue among doctors in tertiary hospitals: A cross-sectional survey in six provinces of China. Int. J. Environ. Res. Public. Health 16, E3049. https://doi.org/10.3390/ijerph16173049
Tanweer, S. A. W. (2021). How smart phones effects health. Tech neck: Causes and preventions. Pak. J. Phys. Ther. 02-02.
Tapiola, T., Pirttilä, T., Mikkonen, M., Mehta, P. D., Alafuzoff, I., Koivisto, K. und Soininen, H. (2000). Three-year follow-up of cerebrospinal fluid tau, beta-amyloid 42 and 40 concentrations in Alzheimer’s disease. Neurosci. Lett. 280, 119–122. https://doi.org/10.1016/s0304-3940(00)00767-9
Tapiola, T., Alafuzoff, I., Herukka, S.-K., Parkkinen, L., Hartikainen, P., Soininen, H. und Pirttilä, T. (2009). Cerebrospinal fluid β-amyloid 42 and tau proteins as biomarkers of Alzheimer-type pathologic changes in the brain. Arch. Neurol. 66, 382–389. https://doi.org/10.1001/archneurol.2008.596
Tasali, E., Leproult, R., Ehrmann, D. A. und Van Cauter, E. (2008). Slow-wave sleep and the risk of type 2 diabetes in humans. Proc. Natl. Acad. Sci. 105, 1044–1049. https://doi.org/10.1073/pnas.0706446105
Tatebe, H. und Shiozaki, K. (2017). Evolutionary conservation of the components in the TOR signaling pathways. Biomolecules 7, 77. https://doi.org/10.3390/biom7040077
Taylor, J. (2009). »Cigarettes, whisky, and wild, wild women.« Independent, June 20. https://www.independent.co.uk/life-style/health-and-families/health-news/cigarettes-whisky-and-wild-wild-women-1710744.html
Tchernof, A. und Després, J.-P. (2013). Pathophysiology of human visceral obesity: An update. Physiol. Rev. 93, 359–404. https://doi.org/10.1152/physrev.00033.2011
Templeman, I., Smith, H. A., Chowdhury, E., Chen, Y.-C., Carroll, H., Johnson-Bonson, D., Hengist, A., Smith, R., Creighton, J., Clayton, D. et al. (2021). A randomized controlled trial to isolate the effects of fasting and energy restriction on weight loss and metabolic health in lean adults. Sci. Transl. Med. 13, eabd8034. https://doi.org/10.1126/scitranslmed.abd8034
Thanassoulis, G., Sniderman, A. D. und Pencina, M. J. (2018). A long-term benefit approach vs standard risk-based approaches for statin eligibility in primary prevention. JAMA Cardiol. 3, 1090–1095. https://doi.org/10.1001/jamacardio.2018.3476
Tieland, M., Dirks, M. L., Zwaluw, N. van der, Verdijk, L. B., Rest, O. van de, Groot, L. C. P. G.M. de und Loon, L. J. C. van (2012a). Protein supplementation increases muscle mass gain during prolonged resistance-type exercise training in frail elderly people: A randomized, double-blind, placebo-controlled trial. J. Am. Med. Dir. Assoc. 13, 713–719. https://doi.org/10.1016/j.jamda.2012.05.020
Tieland, M., Rest, O. van de, Dirks, M. L., Zwaluw, N. van der, Mensink, M., Loon, L. J. C. van und Groot, L. C. P. G.M. de (2012b). Protein supplementation improves physical performance in frail elderly people: A randomized, double-blind, placebo-controlled trial. J. Am. Med. Dir. Assoc. 13, 720–726. https://doi.org/10.1016/j.jamda.2012.07.005
Tolboom, N., Flier, W. M. van der, Yaqub, M., Boellaard, R., Verwey, N. A., Blankenstein, M. A., Windhorst, A. D., Scheltens, P., Lammertsma, A. A. und Berckel, B. N. M. van (2009). Relationship of cerebrospinal fluid markers to 11C-PiB and 18 F-FDDNP binding. J. Nucl. Med. 50, 1464–1470. https://doi.org/10.2967/jnumed.109.064360
Torre, J. de la (2016). Alzheimer’s turning point: A vascular approach to clinical prevention. Cham: Springer International, 169–183
Torre, J. de la (2018). The vascular hypothesis of Alzheimer’s disease: A key to preclinical prediction of dementia using neuroimaging. J. Alzheimer’s Dis. 63, 35–52. https://doi.org/10.3233/JAD-180004
Trappe, S., Hayes, E., Galpin, A., Kaminsky, L., Jemiolo, B., Fink, W., Trappe, T., Jansson, A., Gustafsson, T. und Tesch, P. (2013). New records in aerobic power among octogenarian lifelong endurance athletes. J. Appl. Physiol. 114, 3–10. https://doi.org/10.1152/japplphysiol.01107.2012
Trumble, B. C. und Finch, C. E. (2019). The exposome in human evolution: From dust to diesel. Q. Rev. Biol. 94, 333–394. https://doi.org/10.1086/706768
Tsimikas, S., Fazio, S., Ferdinand, K. C., Ginsberg, H. N., Koschinsky, M. L., Santica, M., Moriarity, P. M., Rader, D. J., Remaley, A. T., Reyes-Soffer, G. et al. (2018). NHLBI Working Group recommendations to reduce lipoprotein(a)-mediated risk of cardiovascular disease and aortic stenosis. J. Am. Coll. Cardiol. 71(2), 177–192
Tuchman, A. (2009). Diabetes and the public’s health. Lancet 374, 1140–1141. https://doi.org/10.1016/S0140-6736(09)61730-X
United States Census Bureau. (2022). National population by characteristics: 2020–2021 tables>median age and age by sex>annual estimates of the resident population by single year of age and sex for the United States: 1. April 2020 bis 1. Juli 2021 (NC-EST2021-SYASEX) [inzwischen aktualisiert bis 1. Juli 2022]
Uretsky, S., Rozanski, A., Singh, P., Supariwala, A., Atluri, P., Bangalore, S., Pappas, T. W., Fisher, E. A. und Peters, M. R. (2011). The presence, characterization and prognosis of coronary plaques among patients with zero coronary calcium scores. Int. J. Cardiovasc. Imaging 27, 805–812. https://doi.org/10.1007/s10554-010-9730-0
Urfer, S. R., Kaeberlein, T. L., Mailheau, S., Bergman, P. J., Creevy, K. E., Promislow, D. E. L. und Kaeberlein, M. (2017). A randomized controlled trial to establish effects of short-term rapamycin treatment in 24 middle-aged companion dogs. GeroScience 39, 117–127. https://doi.org/10.1007/s11357-017-9972-z
Urry, E. und Landolt, H.-P. (2015). Adenosine, caffeine, and performance: From cognitive neuroscience of sleep to sleep pharmacogenetics. In: Sleep, neuronal plasticity and brain function, ed. P. Meerlo, R. M. Benca und T. Abel, 331–366. Berlin: Springer
Van Ancum, J. M., Pijnappels, M., Jonkman, N. H., Scheerman, K., Verlaan, S., Meskers, C. G. M. und Maier, A. B. (2018). Muscle mass and muscle strength are associated with pre- and post-hospitalization falls in older male inpatients: a longitudinal cohort study. BMC Geriatr. 18, 116. https://doi.org/10.1186/s12877-018-0812-5
Van Cauter, E., Caufriez, A., Kerkhofs, M., Van Onderbergen, A., Thorner, M. O. und Copinschi, G. (1992). Sleep, awakenings, and insulin-like growth factor-I modulate the growth hormone (GH) secretory response to GH-releasing hormone. J. Clin. Endocrinol. Metab. 74, 1451–1459. https://doi.org/10.1210/jcem.74.6.1592893
Vander Heiden, M. G., Cantley, L. C. und Thompson, C. B. (2009). Understanding the Warburg effect: The metabolic requirements of cell proliferation. Science 324, 1029–1033. https://doi.org/10.1126/science.1160809
Van Dongen, H. P. A., Baynard, M. D., Maislin, G. und Dinges, D. F. (2004). Systematic interindividual differences in neurobehavioral impairment from sleep loss: Evidence of trait-like differential vulnerability. Sleep 27, 423–433
Van Dongen, H. P. A., Maislin, G., Mullington, J. M. und Dinges, D. F. (2003). The cumulative cost of additional wakefulness: Dose-response effects on neurobehavioral functions and sleep physiology from chronic sleep restriction and total sleep deprivation. Sleep 26, 117–126. https://doi.org/10.1093/sleep/26.2.117
Varady, K. A. und Gabel, K. (2019). Safety and efficacy of alternate day fasting. Nat. Rev. Endocrinol. 15, 686–687. https://doi.org/10.1038/s41574-019-0270-y
Vendelbo, M. H., Møller, A. B., Christensen, B., Nellemann, B., Clasen, B. F. F., Nair, K. S., Jørgensen, J. O. L., Jessen, N. und Møller, N. (2014). Fasting increases human skeletal muscle net phenylalanine release and this is associated with decreased mTOR signaling. PLOS ONE 9, e102031. https://doi.org/10.1371/journal.pone.0102031
Veronese, N., Koyanagi, A., Cereda, E., Maggi, S., Barbagallo, M., Dominguez, L. J. und Smith, L. (2022). Sarcopenia reduces quality of life in the long-term: Longitudinal analyses from the English longitudinal study of ageing. Eur. Geriatr. Med. 13, 633–639. https://doi.org/10.1007/s41999-022-00627-3
Voight, B. F., Peloso, G. M., Orho-Melander, M., Frikke-Schmidt, R., Barbalic, M., Jensen, M. K., Hindy, G., Hólm, H., Ding, E. L., Johnson, T. et al. (2012). Plasma HDL cholesterol and risk of myocardial infarction: A Mendelian randomisation study. Lancet 380, 572–580. https://doi.org/10.1016/S0140-6736(12)60312-2
Voulgari, C., Tentolouris, N., Dilaveris, P., Tousoulis, D., Katsilambros, N. und Stefanadis, C. (2011). Increased heart failure risk in normal-weight people with metabolic syndrome compared with metabolically healthy obese individuals. J. Am. Coll. Cardiol. 58, 1343–1350. https://doi.org/10.1016/j.jacc.2011.04.047
Wade, N. (2009). Dieting monkeys offer hope for living longer. New York Times, 9. Juli. https://www.nytimes.com/2009/07/10/science/10aging.html
Wahlund, L.-O. und Blennow, K. (2003). Cerebrospinal fluid biomarkers for disease stage and intensity in cognitively impaired patients. Neurosci. Lett. 339, 99–102. https://doi.org/10.1016/s0304-3940(02)01483-0
Waks, A. G. und Winer, E. P. (2019). Breast cancer treatment: A review. JAMA, 321(3), 288–300. https://doi.org/10.1001/jama.2018.19323
Walker, M. P. (2009). The role of slow wave sleep in memory processing. J. Clin. Sleep Med. 5, S20-S26
Walker, M. P. (2017). Why we sleep: Unlocking the power of sleep and dreams. New York: Scribner. [(2018). Das große Buch vom Schlaf – Die enorme Bedeutung des Schlafs. 3. Aufl. Übers. von A. Tschöpe. München: Goldmann]
Walker, M. P. und Helm, E. van der (2009). Overnight therapy? The role of sleep in emotional brain processing. Psychol. Bull. 135, 731–748. https://doi.org/10.1037/a0016570
Wallace, D. F. (2009). This is water: Some thoughts, delivered on a significant occasion, about living a compassionate life. New York: Little, Brown [(2012). Das hier ist Wasser. Gedanken zu einer Lebensführung der Anteilnahme vorgebracht bei einem wichtigen Anlass. Übers. von U. Blumenbach. Frankfurt am Main: Büchergilde Gutenberg]
Wang, C. und Holtzman, D. M. (2020). Bidirectional relationship between sleep and Alzheimer’s disease: Role of amyloid, tau, and other factors. Neuropsychopharmacology 45, 104–120. https://doi.org/10.1038/s41386-019-0478-5
Wang, N., Fulcher, J., Abeysuriya, N., Park, L., Kumar, S., Di Tanna, G. L., Wilcox, I., Keech, A., Rodgers, A. und Lal, S. (2020). Intensive LDL cholesterol-lowering treatment beyond current recommendations for the prevention of major vascular events: A systematic review and meta-analysis of randomised trials including 327 037 participants. Lancet Diabetes Endocrinol. 8, 36–49. https://doi.org/10.1016/S2213-8587(19)30388-2
Wang, Y. und Brinton, R. D. (2016). Triad of risk for late onset Alzheimer’s: Mitochondrial haplotype, APOE genotype and chromosomal sex. Front. Aging Neurosci. 8, 232. https://doi.org/10.3389/fnagi.2016.00232
Wang, Y., Jones, B. F. und Wang, D. (2019). Early-career setback and future career impact. Nat. Commun. 10, 4331. https://doi.org/10.1038/s41467-019-12189-3
Warburg, O. (1956). On the origin of cancer cells. Science 123, 309–314. https://doi.org/10.1126/science.123.3191.309
Warburg, O., Posener, K. und Negelein, E. (1924). Über den Stoffwechsel der Carcinomzelle. Biochemische Zeitschrift 152, 309–344
Watanabe, K., Oba, K., Suzuki, T., Ouchi, M., Suzuki, K., Futami-Suda, S., Sekimizu, K., Yamamoto, N. und Nakano, H. (2011). Oral glucose loading attenuates endothelial function in normal individual. Eur. J. Clin. Invest. 41, 465–473. https://doi.org/10.1111/j.1365-2362.2010.02424.x
Watson, A. M. (2017). Sleep and athletic performance. Curr. Sports Med. Rep. 16, 413–418. https://doi.org/10.1249/JSR.0000000000000418
Watson, J. D. (2009). Opinion | To fight cancer, know the enemy. New York Times, 5. August. https://www.nytimes.com/2009/08/06/opinion/06watson.html
Wen, C. P., Wai, J. P. M., Tsai, M. K., Yang, Y. C., Cheng, T. Y. D., Lee, M.-C., Chan, H. T., Tsao, C. K., Tsai, S. P. und Wu, X. (2011). Minimum amount of physical activity for reduced mortality and extended life expectancy: a prospective cohort study. Lancet 378, 1244–1253. https://doi.org/10.1016/S0140-6736(11)60749-6
Westerterp, K. R., Yamada, Y., Sagayama, H., Ainslie, P. N., Andersen, L. F., Anderson, L. J., Arab, L., Baddou, I., Bedu-Addo, K., Blaak, E. E. et al. (2021). Physical activity and fat-free mass during growth and in later life. Am. J. Clin. Nutr. 114, 1583–1589. https://doi.org/10.1093/ajcn/nqab260
WHI (Women’s Health Initiative). (o. J.) About WHI: Dietary Modification Trial. Zugegriffen 7. September 2023. https://sp.whi.org/about/SitePages/Dietary%20Trial.aspx
WHO (World Health Organization). (2019). Global health estimates: Leading causes of death. https://www.who.int/data/gho/data/themes/mortality-and-global-health-estimates/ghe-leading-causes-of-death
Willcox, B. J., Donlon, T. A., He, Q., Chen, R., Grove, J. S., Yano, K., Masaki, K. H., Willcox, D. C., Rodriguez, B. und Curb, J. D. (2008). FOXO3 A genotype is strongly associated with human longevity. Proc. Natl. Acad. Sci. 105, 13987–13992. https://doi.org/10.1073/pnas.0801030105
Wilson, M. A. und McNaughton, B. L. (1994). Reactivation of hippocampal ensemble memories during sleep. Science 265, 676–679. https://doi.org/10.1126/science.8036517
Winer, J. R., Mander, B. A., Helfrich, R. F., Maass, A., Harrison, T. M., Baker, S. L., Knight, R. T., Jagust, W. J. und Walker, M. P. (2019). Sleep as a potential biomarker of tau and β-amyloid burden in the human brain. J. Neurosci. 39, 6315–6324. https://doi.org/10.1523/JNEUROSCI.0503-19.2019
Wishart, D. S., Tzur, D., Knox, C., Eisner, R., Guo, A. C., Young, N., Cheng, D., Jewell, K., Arndt, D., Sawhney, S. et al. (2007). HMDB: The Human Metabolome Database. Nucleic Acids Res. 35, D521-526. https://doi.org/10.1093/nar/gkl923
Wolters, F. J. und Ikram, M. A. (2019). Epidemiology of vascular dementia. Arterioscler. Thromb. Vasc. Biol. 39, 1542–1549. https://doi.org/10.1161/ATVBAHA.119.311908
Wu, G. (2016). Dietary protein intake and human health. Food Funct. 7, 1251–1265. https://doi.org/10.1039/c5fo01530h
Xu, J. (2016). Mortality among centenarians in the United States, 2000–2014. NCHS Data Brief 233. https://www.cdc.gov/nchs/products/databriefs.htm
Xue, Q.-L. (2011). The frailty syndrome: Definition and natural history. Clin. Geriatr. Med. 27, 1–15. https://doi.org/10.1016/j.cger.2010.08.009
Yamamoto, T., Yagi, S., Kinoshita, H., Sakamoto, Y., Okada, K., Uryuhara, K., Morimoto, T., Kaihara, S. und Hosotani, R. (2015). Long-term survival after resection of pancreatic cancer: A single-center retrospective analysis. World J. Gastroenterol. 21, 262–268. https://doi.org/10.3748/wjg.v21.i1.262
Yamazaki, R., Toda, H., Libourel, P.-A., Hayashi, Y., Vogt, K. E. und Sakurai, T. (2020). Evolutionary origin of distinct NREM and REM sleep. Front. Psychol. 11, 567618. https://doi.org/10.3389/fpsyg.2020.567618
Yan, Y., Wang, X., Chaput, D., Shin, M. K., Koh, Y., Gan, L., Pieper, A. A., Woo, J. A. A. und Kang, D. E. (2022). X-linked ubiquitin-specific peptidase 11 increases tauopathy vulnerability in women. Cell 185(21), 3913–3930.e19. https://doi.org/10.1016/j.cell.2022.09.002
Yassine, H. N., Braskie, M. N., Mack, W. J., Castor, K. J., Fonteh, A. N., Schneider, L. S., Harrington, M. G. und Chui, H. C. (2017). Association of docosahexaenoic acid supplementation with Alzheimer disease stage in apolipoprotein E ε4 carriers. JAMA Neurol. 74, 339–347. https://doi.org/10.1001/jamaneurol.2016.4899
Yasuno, F., Minami, H., Hattori, H. und Alzheimer’s Disease Neuroimaging Initiative (2020). Interaction effect of Alzheimer’ disease pathology and education, occupation, and socioeconomic status as a proxy for cognitive reserve on cognitive performance: in vivo positron emission tomography study. Psychogeriatr. 20, 585–593. https://doi.org/10.1111/psyg.12552
Yin, J., Jin, X., Shan, Z., Li, S., Huang, H., Li, P., Peng, X., Peng, Z., Yu, K., Bao, W., Yang, W., Chen, X. und Liu, L. (2017). Relationship of sleep duration with all-cause mortality and cardiovascular events. JAHA 117. https://www.ahajournals.org/doi/full/10.1161/JAHA.117.005947
Yoo, S.-S., Gujar, N., Hu, P., Jolesz, F. A. und Walker, M. P. (2007). The human emotional brain without sleep: A prefrontal amygdala disconnect. Curr. Biol. 17, R877-878. https://doi.org/10.1016/j.cub.2007.08.007
Youlden, D. R., Cramb, S. M. und Baade, P. D. (2008). The international epidemiology of lung cancer: Geographical distribution and secular trends. J. Thorac. Oncol. 3, 819–831. https://doi.org/10.1097/JTO.0b013e31818020eb
Youngstedt, S. D., O’Connor, P. J., Crabbe, J. B. und Dishman, R. K. (2000). The influence of acute exercise on sleep following high caffeine intake. Physiol. Behav. 68, 563–570. https://doi.org/10.1016/S0031-9384(99)00213-9
Zambotti, M. de, Colrain, I. M. und Baker, F. C. (2015). Interaction between reproductive hormones and physiological sleep in women. J. Clin. Endocrinol. Metab. 100, 1426–1433. https://doi.org/10.1210/jc.2014-3892
Zelman, S. (1952). The liver in obesity. Arch. Intern. Med. 90, 141–156. https://doi.org/10.1001/archinte.1952.00240080007002
Zethelius, B. und Cederholm, J. (2015). Comparison between indexes of insulin resistance for risk prediction of cardiovascular diseases or development of diabetes. Diabetes Res. Clin. Pract. 110, 183–192. https://doi.org/10.1016/j.diabres.2015.09.003
Zhang, Y., Zhang, Y., Du, S., Wang, Q., Xia, H. und Sun, R. (2020). Exercise interventions for improving physical function, daily living activities and quality of life in community-dwelling frail older adults: A systematic review and meta-analysis of randomized controlled trials. Geriatr. Nur. 41, 261–273. https://doi.org/10.1016/j.gerinurse.2019.10.006
Zheng, Y., Fan, S., Liao, W., Fang, W., Xiao, S. und Liu, J. (2017). Hearing impairment and risk of Alzheimer’s disease: a meta-analysis of prospective cohort studies. Neurol. Sci. 38, 233–239. https://doi.org/10.1007/s10072-016-2779-3
Zheng, Y., Lv, T., Wu, J. und Lyu, Y. (2022). Trazodone changed the polysomnographic sleep architecture in insomnia disorder: a systematic review and meta-analysis. Scientific reports, 12(1), 14453. https://doi.org/10.1038/s41598-022-18776-7
Zhou, C., Wu, Q., Wang, Z., Wang, Q., Liang, Y. und Liu, S. (2020). The effect of hormone replacement therapy on cognitive function in female patients with Alzheimer’s disease: A meta-analysis. Am. J. Alzheimer’s Dis. Other Demen. 35, 1533317520938585. https://doi.org/10.1177/1533317520938585
Ziemichód, W., Grabowska, K., Kurowska, A. und Biała, G. (2022). A comprehensive review of daridorexant, a dual-orexin receptor antagonist as new approach for the treatment of insomnia. Molecules 27(18), 6041. https://doi.org/10.3390/molecules27186041
Zuccarelli, L., Galasso, L., Turner, R., Coffey, E. J. B., Bessone, L. und Strapazzon, G. (2019). Human physiology during exposure to the cave environment: A systematic review with implications for aerospace medicine. Front. Physiol. 10, 442
Anmerkungen
Yamamoto et al. (2015) ↑
Kinsella (1992) ↑
Mensah et al. (2017) ↑
Siegel et al. (2021) ↑
Der HbA1c-Wert misst die Menge des glykolisierten Hämoglobins im Blut, aufgrund dessen sich der durchschnittliche Blutzuckerspiegel des Patienten über die letzten rund 90 Tage schätzen lässt. ↑
Tatsächlich hatte ich die Strecke schon zum zweiten Mal bewältigt. Einige Jahre zuvor war ich von Catalina nach L. A. geschwommen, aber wegen der Strömung brauchte ich für die Gegenrichtung vier Stunden länger. ↑
»Outlive« bedeutet »überdauern«, »(jemanden) überleben« im Sinne von »länger leben als andere«. (Anm. d. Übs.) ↑
Hypotheken für Kreditnehmer mit der höchsten Bonität bzw. dem geringsten Risikopotenzial (Anm. d. Übs.) ↑
Sokol (2013) ↑
Die Worte »Vor allem schade nicht« kommen in keiner von Hippokrates’ Schriften vor. Er mahnte Ärzte, »zwei Dinge im Umgang mit Krankheiten zu beachten: entweder hilf oder schade dem Kranken nicht«. Das wurde im 19. Jahrhundert von dem britischen Chirurgen Thomas Inman zu »Vor allem schade nicht« umformuliert. Ansonsten war Inman berühmt für – nichts. Irgendwie wurde der Spruch dann zum ewig gültigen, sakrosankten Motto des Ärztestandes. ↑
Pasteur entdeckte das Vorkommen von durch die Luft übertragenen Krankheitserregern und Bakterien, die Fäulnis von Nahrungsmitteln bewirken, und Impfstoffe, etwa gegen Tollwut. Lister entwickelte antiseptische chirurgische Verfahren. Koch entdeckte die Erreger von Tuberkulose und Cholera. ↑
S. Johnson (2021) ↑
Gordon (2016) ↑
Manson et al. (2013) ↑
Eine genauere Betrachtung der Daten legt nahe, dass der verschwindend geringe Anstieg des Brustkrebsrisikos sehr wahrscheinlich auf die Art des in der Studie verwendeten synthetischen Progesterons zurückzuführen war und nicht auf das Östrogen. Der Teufel steckt immer im Detail. ↑
New York Times (1985) ↑
Wobei es zweifellos eine gute Idee ist, Sonnenbrand zu vermeiden, weil er die Haut schneller altern lässt, vom Risiko, an schwarzem Hautkrebs zu erkranken, ganz zu schweigen. ↑
López-Otín et al. (2013) ↑
Für einen reibungslosen Ablauf der MR müssen spezielle Bedingungen erfüllt sein. Erstens muss eine Verbindung zwischen der betreffenden Genvariante (oder Genvarianten) und dem zu untersuchenden Risikofaktor bestehen (Relevanz). Zweitens darf die Genvariante keine gemeinsame Ursache mit dem Ergebnis haben (Unabhängigkeit). Und drittens darf die Genvariante das Ergebnis nur über den Risikofaktor beeinflussen (Ausschließlichkeit). ↑
Benn et al. (2011) ↑
Ference (2015) ↑
Taylor (2009) ↑
Spencer (2005) ↑
Picard (2018) ↑
Rajpathak et al. (2011) ↑
United States Census Bureau (2022) ↑
Hjelmborg et al. (2006) ↑
Sebastiani, Nussbaum et al. (2016) ↑
Xu (2016) ↑
Evert et al. (2003) ↑
Perls (2017) ↑
Hitt et al. (1999) ↑
Michaelson (2014) ↑
Sebastiani, Gurinovich et al. (2019) ↑
Willcox et al. (2008) ↑
Revelas et al. (2018) ↑
Serna et al. (2012) ↑
Melov et al. (2007) ↑
Ein Analogon ist ein Wirkstoff, der nicht exakt dieselbe, aber eine sehr ähnliche chemische Struktur hat. ↑
E. J. Brown et al. (1994); Sabatini et al. (1994) ↑
Hier ist die Nomenklatur etwas verwirrend. Kurz gesagt, blockiert (inhibiert) das Rapamycin-Molekül die Aktivität von mTOR, dem in der Zelle entdeckten Proteinkomplex. Die Verwirrung rührt daher, dass das m in mTOR ursprünglich für mammalian (Säugetier-) stand, um es von TOR zu unterscheiden, einer Version dieses Proteinkomplexes, die man zuvor in Hefen gefunden hatte. Doch TOR und mTOR sind mehr oder weniger identisch, was bedeutet, dass dieser grundlegende Mechanismus im Stammbaum des Lebens von ganz unten bis ganz oben vorkommt und sich somit über Milliarden von Jahren erhalten hat. ↑
Tatebe und Shiozaki (2017) ↑
G. Y. Liu und Sabatini (2020) ↑
Attia (2018a) ↑
Attia (2018a) ↑
D. E. Harrison, Strong, Sharp et al. (2009) ↑
Selvarani, Mohammed und Richardson (2021) ↑
Baur et al. (2006) ↑
Miller et al. (2011); Strong et al. (2013) ↑
D. E. Harrison, Strong, Reifsnyder et al. (2021) ↑
Selvarani, Mohammed und Richardson (2021) ↑
Fontana und Partridge (2015) ↑
Alvise Cornaro: Vom maßvollen Leben oder die Kunst alt zu werden. Hrsg. u. eingel. von Klaus Bergoldt; nach der Übersetzung von M. Christian Ludovici (1707). Regenbrecht Verlag 2022 ↑
McDonald und Ramsey (2010) ↑
Hardie (2011) ↑
Kourtis und Tavernarakis (2009) ↑
Karsli-Uzunbas et al. (2014) ↑
Mannick et al. (2014) ↑
Creevy et al. (2022) ↑
Urfer et al. (2017) ↑
Attia (2018b) ↑
Bannister et al. (2014) ↑
Bevor wir Rapa Nui verließen, schworen wir vier, die gestohlene Gedenktafel für die Entdeckung des Rapamycins zu ersetzen. Die neue soll zum einen den einzigartigen Beitrag der Insel zur Molekularbiologie würdigen und zum anderen den von Suren Sehgal zur Rettung und zur Aufklärung der Bedeutung dieses Moleküls. ↑
Zelman (1952) ↑
Ludwig et al. (1980) ↑
S. A. Harrison (2021) ↑
In der Regel versteht man unter »normal« alles, was zwischen der 2,5. und der 97,5. Perzentile liegt, eine sehr große Spanne. ↑
Fryar et al. (2018); Ogden et al. (2004) ↑
Kwo, Cohen und Lim (2017) ↑
Prati et al. (2002) ↑
Fayek et al. (2016) ↑
Der sogenannte Body-Mass-Index (BMI) ist als Maßzahl alles andere als perfekt, da er das Verhältnis von Fett- zu Muskelmasse nicht berücksichtigt, aber für unsere Zwecke hier ist er gut genug. ↑
CDC (2022b) ↑
Hirode und Wong (2020) ↑
Araújo, Cai und Stevens (2019) ↑
Stefan, Schick und Häring (2017) ↑
Gavrilova et al. (2000) ↑
Tchernof und Després (2013) ↑
Anand et al. (2011); Sniderman, Bhopal et al. (2007) ↑
Ahima und Lazar (2013) ↑
M. C. Petersen und Shulman (2018) ↑
Ein Enzym, das in Fettzellen gebildet wird und das dabei hilft, die gespeicherten Triglyceride in freie Fettsäuren umzuwandeln. ↑
Frayn (2019) ↑
Tuchmann (2009) ↑
Diamond (2003) ↑
Joslin (1940) ↑
NIDDK (2018) ↑
CDC (2022e) ↑
CDC (2020) ↑
R. J. Johnson, Stenvinkel et al. (2020) ↑
Attia (2020c) ↑
R. J. Johnson und Andrews (2015) ↑
Auch wenn es gerade en vogue ist, High Fructose Corn Syrup (der zu 55 Prozent aus Fructose und zu 45 Prozent aus Glucose besteht) zu verteufeln, sei der Hinweis erlaubt, dass unser guter alter Haushaltszucker (Saccharose) zu je 50 Prozent aus Fructose und Glucose besteht. Der Unterschied ist also wirklich nicht groß. ↑
R. J. Johnson, Sánchez-Lozada et al. (2017) ↑
Das rasche Absinken des ATP-Spiegels ruft ein Enzym namens AMP-Desaminase, kurz AMPD, auf den Plan, das so eine Art böser Zwilling des Enzyms AMPK ist, das wir im vorigen Kapitel als Warnlämpchen der Tankanzeige kennengelernt haben. Wenn AMPK aktiviert wird, setzt sie alle möglichen Überlebensprogramme für Zellen in Gang, unter anderem das Verbrennen von gespeichertem Fett, das dem Organismus hilft, ohne Nahrung zu überleben. Wenn Fructose umgekehrt AMPD aktiviert, bringt uns das auf den Weg zur Fetteinlagerung. (Diese Reaktionsfolge löst auch Hungergefühle aus, indem sie das Sättigungshormon Leptin blockiert.) ↑
Zum Vergleich: Eine normale Coca-Cola mit 12 Unzen (etwa 360 Milliliter) enthält 39 Gramm High Fructose Corn Syrup, der zur Hälfte aus Glucose und zur Hälfte aus Fructose besteht. ↑
Igwe et al. (2015); Matsuzaki et al. (2010); Zethelius und Cederholm (2015) ↑
CDC (2022c) ↑
Caselli und Lipsi (2006) ↑
Bautch und Caron (2015) ↑
Außerdem gibt es noch very-low-density lipoproteins (Lipoproteine sehr niedriger Dichte, VLDL), die wir im vorigen Kapitel erwähnt haben, und d ACS (2022a); Heron (2021)ie intermediate-density lipoproteins (IDL), eine Zwischenstufe zwischen VLDL und LDL. Sie transportieren sogar noch mehr Fett als die LDLs, das meiste in Form von Triglyceriden, und sie sind ebenfalls mit ApoB verpackt. Wichtig: Während HDL-Partikel viele ApoAs haben können, ist jedes LDL (oder VLDL oder IDL) nur mit jeweils einem ApoB-Molekül versehen, dadurch lässt sich ihre Konzentration relativ leicht messen. ↑
McNamara (2015) ↑
Mensink und Katan (1992) ↑
Lammert und Wang (2005) ↑
Jaret (1997) ↑
Dietary Guidelines Advisory Committee (2015) ↑
Sniderman, Thanassoulis et al. (2016) ↑
Stary (2003) ↑
Der wissenschaftliche Begriff dafür lautet stochastisch, das bedeutet, es handelt sich um von einander unabhängige Zufallsereignisse. ↑
Thanassoulis, Sniderman und Pencina (2018) ↑
Nur kurz zur Nomenklatur: Mit LDL und HDL sind normalerweise die Partikel gemeint. Die Abkürzungen LDL-C und HDL-C dagegen bezeichnen die Konzentration des Cholesterins in diesen Partikeln, die bei den Laboruntersuchungen ermittelt wird. ↑
Das CT-Angiogramm kostet zwar mehr, erfordert die Gabe von Kontrastmittel und setzt den Patienten einer etwas höheren Strahlung aus, aber ich finde trotzdem kaum Argumente gegen seine Verwendung. Bei etwa 15 Prozent der Patienten mit einem normalen Calcium-Score (0) sind auf dem Angiogramm dennoch weiche Plaques oder sogar kleine Verkalkungen zu sehen, und bei 2–3 Prozent der Patienten mit Calcium-Score 0 werden auf dem CT-Angiogramm Hochrisiko-Plaques entdeckt (Nazir et al. (2022); Uretsky et al. (2011). Aus diesem Grund rate ich meinen Patienten immer zu einem CT-Angiogramm statt einem Calcium-Scan, wenn wir mit bildgebenden Verfahren nach Hinweisen für die Erkrankung suchen. ↑
Marston (2022) ↑
Tsimikas et al. (2018) ↑
O’Donoghue et al. (2019) ↑
Im Augenblick wird eine neue Wirkstoffklasse, die sogenannten Antisense-Oligonukleotide (ASO), in klinischen Studien getestet; mit ihrer Hilfe soll Lp(a) buchstäblich aus dem Blutkreislauf verschwinden. Bis jetzt sehen die Ergebnisse recht vielversprechend aus, denn sie senken die Lp(a)-Konzentration dramatisch, aber es ist noch zu früh, um etwas darüber zu sagen, wie gut sie darin sind, was wirklich zählt: die kardiovaskulären Ereignisse zu vermindern. ↑
Grund dafür ist, dass die absolute Zahl von LDL-Partikeln wesentlich größer ist als die von Lp(a)-Partikeln, dass Lp(a) jedoch selbst in relativ kleiner Zahl enorme Schäden verursachen kann. ↑
Libby (2021) ↑
Orphanet (2022) ↑
Ritchie und Roser (2018) ↑
Dietschy, Turley und Spady (1993); Ference et al. (2019); Forrester (2010); Jakubowski et al. (2021); Karagiannis et al. (2021); R. Le, Zahao und Hegele (2022); Libby und Tokgözoğlu (2022); Masana et al. (2018); O’Keefe et al. (2004); Soran, Ho und Durrington (2018); N. Wang et al. (2020) ↑
Homocystein wird von B-Vitaminen abgebaut, aus diesem Grund kann ein Mangel an B-Vitaminen oder Mutationen in Enzymen, die in deren Stoffwechsel eine Rolle spielen (z. B. Methylentetrahydrofolat-Reduktase, MTHFR), den Homocystein-Spiegel steigen lassen. ↑
Haase et al. (2012) ↑
Voight et al. (2012) ↑
Dafür gibt es mindestens zwei Gründe: Erstens scheinen die gesättigten Fette direkt zu einer verstärkten Cholesterinsynthese beizutragen. Zweitens, und das ist wichtiger, veranlassen die überschüssigen gesättigten Fette die Leber, die Expression der LDL-Rezeptoren zurückzufahren, dadurch verringert sich die LDL-Menge, die aus dem Blut entfernt wird. ↑
du Souich, Roederer und Dufour (2017); Stroes et al. (2015) ↑
Mach et al. (2018); C. B. Newman et al. (2019) ↑
Jose (2016) ↑
Der einzige Unterschied war, dass mir der Test von 2016 einen Calcium-Score von 0 gab, während der von 2022 bei 2 lag und der allererste Scan dieselbe kleine Plaque mit 6 bewertet hatte. Das bestärkt mich in der Überzeugung, dass Calcium-Scores zwar nützlich sind, für sich allein aber auf keinen Fall ausreichen. ↑
Thanassoulis, Sniderman und Pencina (2018) ↑
Nicht das Cholesterin, das Sie mit der Nahrung zu sich nehmen, das wird sowieso nicht aufgenommen. Es geht um das Cholesterin, das Ihr Körper selbst produziert und mithilfe von Leber und Galle recycelt. ↑
Rosenberg und Barry (1992), Die veränderte Zelle, S. 29 ↑
NCI (2022b) ↑
NCI (2021) ↑
NCI (2021) ↑
Jamaspishvili et al. (2018) ↑
Pollack (2005) ↑
Sleeman und Steeg (2010) ↑
Hitchens (2013), S. 31 ↑
Hitchens (2013), S. 92 f. ↑
Hanahan und Weinberg (2011) ↑
Warburg (1924, 1956) ↑
Liberti und Locasale (2016) ↑
Christofferson (2017) ↑
J. D. Watson (2009) ↑
Vander Heiden, Cantley und Thompson (2009) ↑
Eine Krebszelle kann auf noch andere Weise vom Warburg-Effekt profitieren. Eine weitere Theorie besagt, dass er den Tumor vor Immunzellen schützt, indem er durch die Erzeugung von Milchsäure und reaktiven Sauerstoffspezies für einen niedrigen pH-Wert im Tumormikromilieu sorgt, was für die Immunzellen nicht günstig ist. Einen ausgezeichneten Überblick über diese Thematik bieten Liberti und Locasale (2016). ↑
Avgerinos et al. (2019) ↑
Lega et al. (2019) ↑
Bradley (2004); Fruman et al. (2017) ↑
Mercken et al. (2013) ↑
Mukherjee (2011) ↑
Hopkins et al. (2018) ↑
de Groot et al. (2020) ↑
ACS (2022c) ↑
Damals war nicht ersichtlich, warum das so war, aber heute weiß man, dass der Ansatz funktionierte, weil diese beiden Krebsarten mit zahlreichen Genmutationen einhergehen, was bedeutet, dass das Immunsystem eine größere Chance hat, die Krebszellen als schädlich zu erkennen und anzugreifen. ↑
Kochenderfer et al. (2010) ↑
Wenn Sie mehr über die Geschichte der Immuntherapie erfahren möchten, lesen Sie Charles Graebers Buch The Breakthrough aus dem Jahr 2018, das Jim Allisons Arbeit an Checkpoint-Inhibitoren ausführlich beschreibt. ↑
D. T. Le et al. (2015) ↑
Gay und Prasad (2017) ↑
Cavazzoni et al. (2020) ↑
Attia (2021b) ↑
Beispielsweise steht per definitionem bereits fest, dass TILs auf die Bekämpfung des Tumors programmiert sind. Wenn man sie aber vervielfacht, können sie »altern« (Zellen »altern« bei jeder Zellteilung) und etwas von ihrer Wirksamkeit einbüßen. Umgekehrt sind genmodifizierte T-Zellen gemeinhin jünger und lassen sich leichter vermehren, verfügen aber nicht zwangsläufig über die gleiche Kapazität wie TILs, Tumoren zu vernichten. ↑
Atkins et al. (2000) ↑
Für 95 Prozent der Patienten mit metastasiertem Dickdarmkrebs. ↑
Taieb und Gallois (2020) ↑
Damit ist die Expression des humanen epidermalen Wachstumsfaktor-Rezeptors 2 gemeint. Dies ist ein Rezeptor an der Oberfläche von Brustkrebszellen, der ihr Wachstum fördert. Bei etwa 30 Prozent der Brustkrebsfälle ist er überexprimiert, also stark erhöht. ↑
Waks und Winer. (2019) ↑
Es gibt verschiedene Verfahren des Darmkrebs-Screenings, die sich in zwei Gruppen einteilen lassen: stuhlbasierte Tests und Darmspiegelungen. Stuhlbasierte Tests sind im Grunde ein Screeningtest für einen Screeningtest – ein positiver stuhlbasierter Test gibt Anlass zu einer Darmspiegelung. Durchgeführt werden entweder eine flexible Sigmoidoskopie, die allerdings nur die Untersuchung des unteren Dickdarmabschnitts (einschließlich des Colon sigmoideum und des absteigenden Dickdarms) erlaubt und daher nicht ausschließen kann, dass der obere Abschnitt von Krebs befallen ist, oder eine herkömmliche Koloskopie, bei der der gesamte Dickdarm untersucht wird. Meiner Ansicht nach kommt keiner der anderen Tests an die Koloskopie heran. ↑
Hofseth et al. (2020) ↑
ACS (2022b) ↑
Laut einer Studie von 2022 wurde das Darmkrebsrisiko bei Personen, denen man eine Koloskopie in einem Turnus von zehn Jahren empfahl, gegenüber Personen ohne eine solche Empfehlung um nur 18 Prozent (relativ) und 0,22 Prozent (absolut) gesenkt. Allerdings ließen sich nur 42 Prozent derjenigen, die die Empfehlung erhalten hatten, tatsächlich untersuchen, und zwar nur einmal in dem von der Studie erfassten Zeitraum. Ich würde behaupten, dass damit nicht die Wirksamkeit häufiger Koloskopien zur Prävention von Darmkrebs getestet wurde, sondern vielmehr, wie effektiv man den Leuten geraten hatte, sich (sporadisch) untersuchen zu lassen. ↑
Für diejenigen, die sich detailliertere Informationen wünschen, zitiere ich hier aus einem Blogpost über Darmkrebs-Screening, den ich vor einigen Jahren (Attia 2020a) verfasst habe: »Vor Ihrer ersten Koloskopie können Sie einiges tun, um Ihr Risiko-Nutzen-Verhältnis zu verbessern. Sie sollten sich nach der Adenom-Erkennungsrate (adenoma detection rate, ADR) Ihres Endoskopikers erkundigen. Die ADR gibt den Anteil der untersuchten Personen an, bei denen ein oder mehrere Adenome (Dickdarmpolypen) entdeckt wurden. Die Richtwerte für ADR liegen bei über 30 Prozent bei Männern und bei über 20 Prozent bei Frauen. Außerdem sollten Sie gezielt danach fragen, wie häufig es dort (bei einem routinemäßigen Screening) zu Perforationen sowie zu anderen schweren Komplikationen wie einer schwerwiegenden Darmblutung gekommen ist. Überdies sollten Sie die Rückzugszeit erfragen. Damit ist gemeint, wie viel Zeit bei der Koloskopie dafür aufgewendet wird, die Darmwand beim Rückzug des Endoskops genau zu betrachten. Eine längere Rückzugszeit spricht für eine gründlichere Untersuchung. Die derzeit standardmäßige Rückzugszeit beträgt sechs Minuten.« ↑
Die Spezifität der MRT leidet insbesondere bei Drüsengewebe. Beim Entdecken von Drüsenkrebs ist die MRT so gut, dass sie signifikant oft übers Ziel hinausschießt. Besonders problematisch ist hier wohl die Schilddrüse. ↑
Man spricht von Flüssigbiopsien, um sie von den herkömmlichen Biopsien von festem Gewebe zu unterscheiden. ↑
X. Chen et al. (2021) ↑
Bezeichnung für US-Amerikaner, die etwa zwischen 1901 und 1927 geboren wurden, die Große Depression durchlebten und im Zweiten Weltkrieg kämpften. Auch »G. I. Generation« oder »World War II Generation« genannt. (Anm. d. Übs.) ↑
Reiman, Arboleda-Velasquez et al. (2020) ↑
Belloy et al. (2020) ↑
Cacace, Sleegers und Van Broeckhoven (2016); Cruchaga et al. (2012); Cuyvers und Sleegers (2016) ↑
Cummings et al. (2022) ↑
Kolata (2020) ↑
Blessed, Tomlinson und Roth (1968) ↑
Rabinovici et al. (2019) ↑
Müller, Winter und Graeber (2013) ↑
Kaivola et al. (2022) ↑
Doogie Howser ist der Protagonist einer amerikanischen Fernsehserie, der als Wunderkind mit zehn Jahren sein Medizinexamen in Princeton gemacht hat und nun im Teenageralter als Arzt praktiziert. (Anm. d. Übs.) ↑
Attia (2018c) ↑
Daviglus et al. (2010) ↑
Ngandu et al. (2015) ↑
Rosenberg et al. (2020); Andrieu et al. (2017); van Charante et al. (2016) ↑
Mosconi et al. (2018); Rahman et al. (2020); Ratnakumar et al. (2019); Zhou et al. (2020) ↑
Yan et al. (2022) ↑
Cerri et al. (2019) ↑
Langa und Levine (2014) ↑
Brookmeyer et al. (2018) ↑
Attia (2019) ↑
Yasuno et al. (2020) ↑
Aus Kapitel 7 haben Sie vielleicht noch in Erinnerung, dass Verkalkungen der Reparatur von Blutgefäßen dienen sollen, die durch Atherosklerose geschädigt wurden. ↑
Blessed, Tomlinson und Roth (1968) ↑
Raichle und Gusnard (2002) ↑
de la Torre (2016) ↑
de la Torre (2018) ↑
Wolters und Ikram (2019) ↑
Cholerton et al. (2016) ↑
Neth und Craft (2017) ↑
Freiherr et al. (2013) ↑
Chapman et al. (2018) ↑
Kerrouche et al. (2006) ↑
Reiman, Caselli et al. (1996); Small et al. (2000); Sperling et al. (2011) ↑
Kerrouche et al. (2006) ↑
Neu et al. (2017) ↑
Montagne et al. (2020) ↑
Trumble und Finch (2019) ↑
Mitter et al. (2012); Oriá et al. (2007) ↑
Kloske und Wilcock (2020) ↑
Yassine et al. (2017) ↑
Grammatikopoulou et al. (2020) ↑
Slayday et al. (2021) ↑
Maeng und Milad (2015) ↑
Esteban-Cornejo et al. (2022) ↑
C. Wang und Holtzman (2020) ↑
Zheng et al. (2017) ↑
Dominy et al. (2019) ↑
Laukkanen et al. (2017) ↑
Laukkanen et al. (2015) ↑
A. Smith et al. (2010) ↑
Oulhaj et al. (2016) ↑
Maddock et al. (2015) ↑
Proctor (1995) ↑
Kurzfristig ist unsere Nahrungsversorgung sicherer als je zuvor – dank Kühlung und Fortschritten in der Verarbeitung sowie Vorschriften, die die Verwendung von giftigen Substanzen untersagen. Langfristig ist das weniger der Fall (siehe Kapitel 15). ↑
NHTSA (2022a) ↑
NHTSA (2022b); Attia (2020b) ↑
Wenn Ihnen das Buch gefällt, danken Sie also John Griffin. Wenn nicht, geben Sie mir die Schuld. ↑
Blackwell und Clarke (2018) ↑
Wen et al. (2011) ↑
Reimers, Knapp und Reimers (2012) ↑
Booth und Zwetsloot (2010) ↑
I.-M. Lee und Buchner (2008) ↑
HHS (2018) ↑
Mandsager et al. (2018) ↑
Die Mehrheit der besten Fahrer der Tour de France hat einen VO2max-Wert von um die 80. Der höchste je gemessene VO2max-Wert lag bei absolut unglaublichen 97,5 mg/kg/min. ↑
Mandsager et al. (2018) ↑
Mandsager et al. (2018) ↑
Mandsager et al. (2018) ↑
Kokkinos et al. (2022) ↑
Diese Faktoren entsprechen fünf der neun Kriterien, die in den Dreißigerjahren des 20. Jahrhunderts von Austin Bradford Hill formuliert wurden, dem Gottvater der wissenschaftlichen Methodik. Sie sollten als Werkzeug für die Evaluation epidemiologischer und im Labor ermittelter Befunde dienen. Mehr zu Bradford Hill in den Kapiteln zur Ernährung. ↑
Mandsager et al. (2018) ↑
Li et al. (2018) ↑
Artero et al. (2011) ↑
Die kardiorespiratorische Fitness wurde auf dem Laufband mittels modifiziertem Balke-Protokoll ermittelt, die Kraft als One-Repetition-Maximum (One-Rep-Max oder 1RM) beim Bankdrücken und Beinstrecken. ↑
Naci und Ioannidis (2015) ↑
Eine Ausnahme bildete bei Ioannidis’ Analyse das Herzversagen, das besser auf eine medikamentöse Behandlung mit Diuretika (Medikamente zur Entwässerung) ansprach als auf eine Sporttherapie. ↑
Seifert et al. (2010) ↑
Barnes und Corkery (2018) ↑
Westerterp et al. (2021) ↑
Bunout et al. (2011) ↑
Jones et al. (2017) ↑
Van Ancum et al. (2018) ↑
CDC (2021) ↑
H.-S. Lin et al. (2016) ↑
Veronese et al. (2022) ↑
Nicklas et al. (2015) ↑
K. L. Campbell et al. (2019) ↑
Zhang et al. (2020) ↑
Danneskiold-Samsøe et al. (2009); Hughes et al. (2001); Lindle et al. (1997) ↑
Allen und Coggan (2010) ↑
San Millán und Brooks (2018) ↑
Dies liegt daran, dass das Wasserstoffion die Entspannung der Aktin- und Myosinfilamente in unseren Muskeln verhindert, was zu schmerzhaften Versteifungen im Muskel führt. ↑
Personen, die mit einer Chemotherapie gegen Krebs behandelt werden, zeigen oft eine ähnliche Beeinträchtigung der mitochondrialen Effizienz. Es gibt zudem Vermutungen, dass dies auch bei Long-Covid-Patienten der Fall ist; einiges spricht durchaus dafür. ↑
Lemasters (2005) ↑
Kawada und Ishii (2005) ↑
Richter (2021) ↑
McMillin et al. (2017) ↑
Seifert et al. (2010) ↑
Mandsager et al. (2018) ↑
C.-H. Kim et al. (2016) ↑
Shephard (2009) ↑
Trappe et al. (2013) ↑
Zwei der alternden Athleten hatten VO2max-Werte von über 40, und der älteste Teilnehmer, ein einundneunzigjähriger ehemaliger Olympionike, kam diesem mit 36 ziemlich nahe. Damit wäre er in der Altersgruppe der Sechzigjährigen im obersten Quartil gelandet. ↑
Shephard (2009) ↑
Shephard et al. (2009) ↑
Booth und Zwetsloot (2010); Mandsager et al. (2018) ↑
Billat et al. (2017) ↑
Ich habe für mich herausgefunden, dass mein ideales VO2max-Tempo ungefähr ein Drittel höher und kraftvoller ist als mein Zone-2-Tempo, wenn ich vier Wechselintervalle absolviere. Entspricht also Ihr Zone-2-Tempo einem Output von 150 Watt, sollte Ihre VO2max-Trainingsintensität für vier Minuten bei etwa 200 Watt liegen, gefolgt von vier Ruheminuten. Besser noch, wenn Sie Ihre funktionelle Leistungsschwelle (functional threshold power, FTP) kennen, also die höchste Leistung, die Sie eine Stunde lang durchhalten können, sollten Sie 120 Prozent davon für Drei-Minuten-Intervalle und 106 Prozent davon für Acht-Minuten-Intervalle anstreben und alles dazwischen entsprechend anpassen. ↑
Lexell (1995) ↑
Kortebein et al. (2007) ↑
T. N. Kim und Choi (2013) ↑
Xue (2011) ↑
Tieland, Dirks et al. (2012) ↑
Easter (2021) ↑
Die Definition für Sarkopenie, auf die man sich geeinigt hat, beinhaltet eine geringe Skelettmuskelmasse und entweder eine geringe Muskelkraft (z. B. Handkraft) oder schlechte körperliche Leistungsfähigkeit (z. B. geringes Gehtempo). ↑
Cruz-Jentoft et al. (2019) ↑
Bohannon (2019); Hamer und O’Donovan (2017); Y. Kim et al. (2018); A. B. Newman et al. (2006) ↑
Fain und Weatherford (2016) ↑
Dahlhamer (2018) ↑
Shmagel et al. (2018) ↑
Gaskin und Richard (2012) ↑
Boneti Moreira et al. (2014) ↑
Ein Riss der Knorpellippe des Schultergelenks (Labrum glenoidale) ist eine recht häufige Verletzung, doch viele Menschen lassen diese nie operativ behandeln. Obwohl das endlose Schwimmen die Sache verschlimmert hatte, lag die Ursache der Verletzung in den häufigen Subluxationen oder leichten Dislokationen des Gelenks, die ich als Heranwachsender erlitten hatte. Jedes Mal, wenn das Schultergelenk so unvollständig ausgerenkt wird, schädigt dies die Knorpellippe und erhöht das Risiko späterer Schulterinstabilität und -schmerzen. ↑
Frank, Kobesova und Kolar (2013) ↑
Attia (2021a) ↑
Als ich noch jede Woche geflogen bin, probierte ich erstmals einen guten Trick aus, den mir Michael Rintala gezeigt hatte: Ich stecke zwei Tennisbälle in eine Sportsocke, im Abstand von etwa 10 bis 15 Zentimetern, und positioniere sie ungefähr auf Höhe meiner Nieren, also im Übergang von der Brust- in die Lendenwirbelsäule. Bei jedem Atemzug versuche ich dann, meinen Rumpf so weit auszudehnen, dass ich beide Tennisbälle spüre. Dahinter steckt der Gedanke, bewusst zu atmen. Dieser Trick bewirkte, dass ich mich nach einem Fünf-Stunden-Flug fühlte, als hätte ich nicht länger als fünf Minuten gesessen. (Außerdem hielt er meine Sitznachbarn davon ab, sich mit mir zu unterhalten, während ich zu arbeiten versuchte.) Es lohnt sich, ihn auf einem langen Flug oder bei einer langen Autofahrt auszuprobieren. ↑
Wenn Sie es mit dem Zehenyoga ernst meinen, schaffen Sie sich ein paar orthopädische Zehenspreizer an, die die Zehen in eine natürlichere, gespreiztere Position bringen, besonders bei Personen mit Hallux valgus (Ballenzeh) und anderen schuhbedingten Problemen. Ich trage sie oft zu Hause, auch gerade jetzt, während ich diese Zeilen schreibe. Meine Kinder ziehen mich dauernd damit auf. ↑
Araujo et al. (2022) ↑
Tanweer (2021) ↑
Manche der grundlegenden Gleichgewichtsbewegungen der DNS, die ich hier beschreibe, haben Entsprechungen in klassischen Yoga-Positionen, und ein guter Yogalehrer kann Ihnen dabei helfen, die neuromuskuläre Kontrolle und Achtsamkeit, die für eine gute Stabilität essenziell sind, zu entwickeln. Die meisten Yogakurse gehen dafür aber nach meinem Empfinden nicht genug in die Tiefe. ↑
Dye (1988) ↑
Naghshi et al. (2020) ↑
Damals, im Jahr 1775, wies mit Percival Pott, einem englischen Chirurgen, erstmals jemand nach, dass Krebs durch einen Umweltfaktor (heute als Karzinogen bezeichnet) ausgelöst werden kann. Pott bemerkte eine Zunahme der Fälle von »Warzen« am Hodensack von jungen Schornsteinfegern, die sich durch Schornsteine zwängen mussten, um Asche und Ruß zu entfernen. Seine Untersuchungen brachten ihn zu dem Schluss, dass Rußteilchen, die in die Hautfalten des Hodensacks geraten waren, die Ursache für diese Krebserkrankung (ein Plattenepithelkarzinom der Haut) waren. ↑
Einer im Jahr 2013 erschienenen Studie zufolge (Bao et al., 2013) sank das Risiko von Menschen, in den nächsten 30 Jahren zu sterben, um 20 Prozent, wenn sie täglich zwölf Haselnüsse aßen. (Kein Wort zum Mechanismus hinter diesem wunderbaren Ergebnis.) ↑
Azad et al. (2017) ↑
Hill (1965) ↑
Das sind die Bradford-Hill-Kriterien: (1) Stärke des Zusammenhangs (z. B. die Größe des Effekts), (2) Konsistenz (z. B. Wiederholbarkeit), (3) Spezifität (z. B., wenn eine Krankheit bei einer bestimmten Bevölkerungsgruppe an einem bestimmten Ort beobachtet wird und es keine andere wahrscheinliche Erklärung gibt), (4) zeitliche Beziehung (die Ursache muss der Folge vorausgehen), (5) Dosis-Wirkungs-Beziehung (z. B., wenn der Effekt mit höherer Dosis stärker wird), (6) Plausibilität (das Geschehen ist logisch, nachvollziehbar), (7) Stimmigkeit (z. B. Übereinstimmung der Daten mit denen aus kontrollierten Studien an Tieren), (8) Experiment (z. B. die Existenz experimentell gewonnener Daten, die die eigenen Befunde stützen) und (9) Analogie (ähnliche Effekte wurden bereits mit ähnlichen Faktoren erzielt). ↑
Schwingshackl, Schwedhelm et al. (2017) ↑
Pesch et al. (2012); Proctor (2001); Sasco, Secretan und Straif (2004); Youlden, Cramb und Baade (2008) ↑
Wenn Sie es selbst mal ausprobieren wollen, geben Sie »Food Frequency Questionnaire« in die Suchmaschine ein – und dann viel Glück. ↑
Ioannidis (2018); Moco et al. (2006); Ninonuevo et al. (2006); Wishart et al. (2007) ↑
Crowe (2018) ↑
Ejima et al. (2016) ↑
Meiner Meinung nach ist der healthy user bias auch der größte einzelne Störfaktor in der Literatur zur Epidemiologie des Sports. Gesunde Menschen treiben häufig auch deshalb mehr Sport, weil sie gesund sind. ↑
Naimi et al. (2017) ↑
Biddinger et al. (2022) ↑
WHI (o. D.) ↑
Howard et al. (2006) ↑
Diese Studie konnte zwar keinen statistisch signifikanten Unterschied beim Tod aufgrund von Brustkrebs feststellen, weder nach 8,5 noch nach 16,5 Jahren Nachverfolgung, doch sie fand bei Frauen mit einer Brustkrebsdiagnose eine statistisch signifikante Verringerung der Gesamtmortalität; allerdings war der Unterschied beim absoluten Risiko nicht signifikant. Die Verringerung der Gesamtsterblichkeit betrug nach 8,5 Jahren 0,013 Prozent und nach 16,5 Jahren gerade einmal 0,025 Prozent. ↑
Primärprävention heißt, dass die betreffende Gruppe bislang kein »Ereignis« erlebt und keine klinische Diagnose erhalten hatte. In der Sekundärprävention wiesen die Statine eine etwas niedrigere number needed to treat auf. Die PREDiMED-Studie wurde später zurückgezogen und noch einmal neu analysiert, um Fehler bei der Randomisierung zu korrigieren (das heißt, die Teilnehmer waren nicht wirklich zufällig den einzelnen Interventionsgruppen zugeordnet worden); aber die neue Analyse änderte die Schlussfolgerungen der Studie nicht wesentlich. Meiner Meinung nach war das größte Problem bei der PREDIMED-Studie der sogeannte performance bias (in etwa: Verzerrung während der Durchführung), das heißt, es könnte zu einer Verzerrung gekommen sein, weil die Teilnehmer der Nuss- und der Öl-Gruppe ihr Verhalten vielleicht geändert hatten, da sie häufiger mit den Forschern in Kontakt kamen als die fettarme Kontrollgruppe. ↑
Estruch et al. (2013) ↑
Martínez-Lapiscina et al. (2013) ↑
Anm. d. Übers.: Im EU-Durchschnitt sind 60 Prozent der Männer und 46 Prozent der Frauen übergewichtig. (Statistisches Bundesamt, https://www.destatis.de/Europa/DE/Thema/Bevoelkerung-Arbeit-Soziales/Gesundheit/Uebergewicht.html) ↑
Colman et al. (2009) ↑
Wade (2009) ↑
Mattison et al. (2012) ↑
Kolata (2012) ↑
In Wisconsin suchten die Forscher nach Diabetesmarkern wie Insulinresistenz, während die Forscher des NIH lediglich die Diagnose Diabetes protokollierten. ↑
Cordain, Miller et al. (2000) ↑
Cordain, Eaton et al. (2002); Pontzer et al. (2018) ↑
Gibson et al. (2015); Nymo et al. (2017); Phinney und Volek (2018); Sumithran et al. (2013) ↑
Oliveira, Cotrim und Arrese (2019) ↑
Peng et al. (2020) ↑
C. Wang und Holtzman (2020) ↑
Hines und Rimm (2001); Suzuki et al. (2009) ↑
Biddinger et al. (2022) ↑
Hanefeld et al. (1999); Kawano et al. (1999); H.-J. Lin et al. (2009); Standl, Schnell und Ceriello (2011); Watanabe et al. (2011) ↑
Offenlegung möglicher Interessenkonflikte: Ich verwende CGM seit 2015 regelmäßig, im Jahr 2021 war ich bezahlter Berater für ein Unternehmen (Dexcom), das Geräte zur CGM produziert und verkauft, wenn sich meine Tätigkeit für das Unternehmen auch auf andere Analyten als Glucose bezog. ↑
Der Sensorfaden hat keinen Kontakt zum Blut des Patienten, er misst die Glucosekonzentration in der Interstitialflüssigkeit und rechnet daraus den Blutzucker hoch. ↑
Bis es so weit ist, können Sie sich auch ein konventionelles Blutzuckermessgerät kaufen (Apotheke, Drogeriemarkt, Onlinehandel) und einfach jede Stunde eine Messung vornehmen und die Ergebnisse notieren (ebenso die Uhrzeiten, wann Sie etwas gegessen haben). Es ist auch sehr aufschlussreich, die Blutzuckermessung vor und nach einer Mahlzeit vorzunehmen, in Abständen von 30 Minuten bis zwei Stunden nach dem Essen. Auf diese Weise kann man schön sehen, wie sich unterschiedliche Nahrungsmittel(-kombinationen) auf die Blutzuckerkurve auswirken. ↑
Pfister et al. (2011) ↑
Echouffo-Tcheugui et al. (2019) ↑
Die Standardabweichung ist eine statistische Größe, die angibt, wie stark die Schwankungsbreite (Variation) innerhalb einer Gruppe (oder eines Individuums) ist. Sie gibt uns eine Vorstellung davon, wie stark die Blutzuckerspiegel eines Patienten um den Durchschnittswert schwanken, und kann deshalb auch als grobe Abschätzung für die Insulinausschüttung des Patienten dienen, die anschließend für die Verwertung der Glucose sorgen soll. Eine hohe Standardabweichung zeigt an, dass es größere Schwankungen gibt und dass vermutlich mehr Insulin gebraucht wird, um die Glucosemengen unter Kontrolle zu bringen. Für mich ist das ein wichtiges Frühwarnsignal für Hyperinsulinämie. ↑
Wie wir in einem der vorherigen Kapitel gesehen haben, kann die Glucoseverwertung mit und ohne Insulin stattfinden. ↑
Franz (1997) ↑
Ähnliche Ergebnisse wurden in zahlreichen anderen Studien erzielt, obwohl es weiterhin unklar ist, ob die Protein-Supplementierung auch hilft, die Muskelkraft zu erhöhen, oder ob sie nur die Muskelmasse vermehrt. ↑
Die Leber kann zwar Aminosäuren in Glucose verwandeln (über einen Prozess, der als Gluconeogenese bezeichnet wird), doch das ist weder eine primäre Glucosequelle noch eine bevorzugte Verwendung für Proteine. ↑
Anm. d. Übers.: Die von den Fachgesellschaften Deutschlands, Österreichs und der Schweiz herausgegebenen D-A-CH-Referenzwerte für die Nährstoffzufuhr sehen für Erwachsene bis 65 Jahre die gleiche Menge vor. (Quelle: https://www.dge.de/wissenschaft/referenzwerte/protein) ↑
W. Campbell et al. (2001) ↑
Wu (2016) ↑
Baum, Kim und Wolfe (2016) ↑
Schoenfeld und Aragon (2018) ↑
Baum, Kim und Wolfe (2016) ↑
Houston et al. (2008) ↑
Rozentryt et al. (2012) ↑
Tieland, van de Rest et al. (2012) ↑
Børsheim et al. (2009) ↑
Nuttall und Gannon (2006) ↑
Boden et al. (2005); Holt et al. (1995); Samra (2010) ↑
Darüber hinaus gibt es noch die gefürchteten Transfette, aber die sind weitgehend aus unserer Ernährung verschwunden, darum gehe ich hier nicht weiter auf sie ein. ↑
Die Unterschiede zwischen den Fett-Typen haben mit organischer Chemie zu tun. Fettsäuren sind im Prinzip Kohlenstoffketten unterschiedlicher Länge. Darum sprechen wir manchmal auch von langkettigen Fettsäuren oder mittellangkettigen Fettsäuren. Eine gesättigte Fettsäure heißt so, weil ihre Kohlenstoffkette vollständig mit Wasserstoffatomen »abgesättigt« ist. Eine einfach ungesättigte Fettsäure enthält zwei Wasserstoffatome weniger und dafür eine Doppelbindung statt einer Einfachbindung zwischen zwei Kohlenstoffatomen. Bei mehrfach ungesättigten Fettsäuren finden wir mehr als eine Doppelbindung und entsprechend weniger Wasserstoffatome. Die Doppelbindungen führen zum Abknicken der Kohlenstoffkette und dazu, dass die Fettsäure leichter oxidiert. Gesättigte Fette sind stabiler und reagieren nicht so leicht mit anderen Molekülen. Da die Kohlenstoffketten von gesättigten Fetten gerade (nicht geknickt) sind, können sie dichter gepackt werden und sind bei Zimmertemperatur mehr oder weniger fest. Umgekehrt sind ungesättigte Fette wegen der Knicke in der Kohlenstoffkette bei Zimmertemperatur eher flüssig. ↑
Die Plus-Version dieses Tests kann außerdem das Verhältnis von Omega-6- zu Omega-3-Fettsäuren im Blut der Patienten bestimmen sowie die Konzentration aller Fettsäuren. ↑
Interessanterweise besteht das menschliche Fettgewebe aus etwa 55 Prozent einfach ungesättigten, 30 Prozent gesättigten und 15 Prozent mehrfach gesättigten Fetten (Seidelin 1995) und deckt sich damit mit der Zusammensetzung der Nahrungsfette, die sich bei den meisten meiner Patienten bewährt hat. ↑
Blasbalg et al. (2011) ↑
Anm. d. Übers.: In der EU gilt für Transfette in Lebensmitteln ein Grenzwert von 2 Gramm pro 100 Gramm Fett. ↑
Abdelhamid et al. (2018) ↑
Hooper et al. (2020) ↑
Schwingshackl, Zähringer et al. (2021) ↑
Als ich noch meine ketogene Diät hielt, konnte ich 250 bis 300 Gramm Fett pro Tag zu mir nehmen, davon gut 40 bis 50 Prozent als gesättigte Fette, und meine Lipidwerte waren trotzdem völlig in Ordnung, ich hatte keine messbaren Entzündungsmarker. Ich habe keine Ahnung, warum das so war, außer vielleicht, dass ich zu der Zeit auch drei bis vier Stunden am Tag Sport trieb. ↑
Vendelbo et al. (2014) ↑
Bagherniya et al. (2018) ↑
Gross, van den Heuvel und Birnbaum (2008) ↑
Hatori et al. (2012) ↑
Jensen et al. (2013) ↑
Lowe et al. (2020) ↑
Jamshed et al. (2019); D. Liu et al. (2022) ↑
Varady und Gabel (2019) ↑
Templeman et al. (2021) ↑
Etwas Ähnliches habe ich in der Zeit erlebt, als ich noch viel Rad gefahren bin. In meinen Spitzenzeiten praktizierte ich ein striktes Intervallfasten im Modus 20/4 täglich. Das Mittagessen bestand im Wesentlichen aus einem Hähnchensalat um 14 Uhr und einem normal dimensionierten Abendessen um 18 Uhr; zu der Zeit war ich 10 Kilo leichter als heute – vor allem, weil ich weniger Muskelmasse hatte. Für das Radfahren war das toll, hier ist ein geringes Gewicht von Vorteil, aber für die Oberkörpermuskulatur war es schlecht. ↑
Dawson und Reid (1997); Lamond und Dawson (1999) ↑
Mansukhani et al. (2012); Tang et al. (2019) ↑
Iftikhar et al. (2015) ↑
Shan et al. (2015) ↑
Leproult und Van Cauter (2010); Reutrakul und Van Cauter (2018); de Zambotti, Colrain und Baker (2015) ↑
Goldstein und Walker (2014); Killgore (2013); Krause et al. (2017); Motomura et al. (2013); Prather, Bogdan und Hariri (2013); Rupp, Wesensten und Balkin (2012); Van Dongen, Maislin et al. (2003); Van Dongen, Baynard et al. (2004); Yoo et al. (2007) ↑
Reddy und van der Werf (2020) ↑
C. Wang und Holtzman (2020) ↑
Walker (2018), S. 463 ↑
Cirelli und Tononi (2008) ↑
Zuccarelli et al. (2019). ↑
Cullen et al. (2019); Fullagar et al. (2015) ↑
Dewasmes et al. (1993); Kolka und Stephenson (1988); Sawka, Gonzalez und Pandolf (1984) ↑
Milewski et al. (2014) ↑
Mah et al. (2011) ↑
Allerdings geht es nicht nur darum, genug zu schlafen – für die Fitness spielt auch das Timing eine Rolle. Mehrere Studien haben die Siegesraten von Basketball-, Football- und Eishockeyteams untersucht und festgestellt, dass diejenigen Teams, die in den Westen der USA reisen mussten, klar benachteiligt waren, weil durch die Zeitverschiebung ihre innere Uhr aus dem Takt geriet (Roy und Forest, 2018). ↑
Ferriss (2018) ↑
Jackson et al. (2013) ↑
AAA Foundation (2016) ↑
Hafner et al. (2017); Killgore (2013); Krause et al. (2017); J. Lim und Dinges (2008); Van Dongen, Maislin et al. (2003) ↑
Oyetakin-White et al. (2015) ↑
Broussard, Ehrmann et al. (2012) ↑
Broussard, Ehrmann et al. (2012); Broussard, Chapotot et al. (2015); Buxton et al. (2010); Leproult, Holmbäck und Van Cauter (2014); Nedeltcheva et al. (2009); Rao et al. (2015); Spiegel, Leproult und Van Cauter (1999); Stamatakis und Punjabi (2010); Tasali et al. (2008) ↑
Iftikhar et al. (2015); Itani et al. (2017); Shan et al. (2015) ↑
Itani et al. (2017) ↑
Kuo et al. (2015) ↑
Spiegel, Tasali et al. (2004); Spiegel, Leproult, L’hermite-Balériaux et al. (2004) ↑
Bosy-Westphal et al. (2008); Brondel et al. (2010); Broussard, Kilkus et al. (2016); Calvin et al. (2013); Spaeth, Dinges und Goel (2015) ↑
Itani et al. (2017); Yin et al. (2017) ↑
Dashti et al. (2019) ↑
Daghlas et al. (2019) ↑
C. Wang und Holtzman (2020) ↑
Lendner et al. (2020) ↑
Diekelmann und Born (2010); Wilson und McNaughton (1994) ↑
Walker (2009) ↑
A. K. Patel, Reddy, Shumway und Araujo (2022) ↑
C. Smith und Lapp (1991); Stickgold et al. (2000) ↑
Walker und van der Helm (2009); Hutchison und Rathore (2015) ↑
Repantis et al. (2020) ↑
Goldstein-Piekarski et al. (2015) ↑
Der Noradrenalinspiegel lässt sich mit dem Blutdruckmittel Prazosin senken. ↑
Raskind et al. (2007) ↑
Der REM-Schlaf erschien interessanterweise erst relativ spät auf der Bühne der Evolution. Bei allen Tieren ist NREM-Schlaf zu beobachten, REM-Schlaf hingegen nur bei Vögeln und nicht im Wasser lebenden Säugetieren. Neuere Studien lassen jedoch vermuten, dass bei nicht vogelartigen Reptilien ein Zustand auftritt, der dem REM-Schlaf ähnelt. (Meeressäuger müssen in regelmäßigen Abständen zum Atmen an die Wasseroberfläche kommen, sodass sie nicht tief schlafen können.) ↑
Yamazaki et al. (2020) ↑
Iliff et al. (2013) ↑
Lucey, McCullough et al. (2019) ↑
Branger et al. (2016); B. M. Brown et al. (2016); Ju et al. (2013); Spira et al. (2013); Sprecher et al. (2015) ↑
C. Wang und Holtzman (2020) ↑
Emamian et al. (2016) ↑
Benito-León et al. (2009); Jack et al. (2013); A. S. P. Lim, Kowgier et al. (2013); A. S. P. Lim, Yu et al. (2013); Lobo et al. (2008); Osorio et al. (2011) ↑
Potvin et al. (2012) ↑
A. S. P. Lim, Kowgier et al. (2013); A. S. P. Lim, Yu et al. (2013) ↑
Ancoli-Israel et al. (2008); Moraes et al. (2006) ↑
Winer et al. (2019) ↑
Saul (2006) ↑
Business Wire (2021) ↑
Arbon, Knurowska und Dijk (2015) ↑
Herring et al. (2016) ↑
Ziemichód et al. (2022) ↑
Picton, Marino und Nealy (2018) ↑
Zheng et al. (2022) ↑
Mittlerweile wird Trazodon zunehmend häufig bei Schlafstörungen verordnet, doch die FDA erkennt darin weiterhin einen »Off-Label-Use«, also eine zulassungsüberschreitende Anwendung. Trazodon scheint insbesondere das Durchschlafen zu fördern. ↑
Shahid et al. (2011) ↑
Der Fragebogen Pittsburgh Sleep Quality Index ist zu finden auf www.sleep.pitt.edu/instruments/#psqi. Eine detaillierte Anleitung zur Auswertung bietet Buysse et al. (1989). ↑
Die Epsworth Sleepiness Scale mit Auswertung findet sich auf www.cdc.gov/niosh/emres/longhourstraining/scale.html. ↑
Der Insomnia Severity Index und Informationen zu Auswertung und Interpretation finden sich auf www.ons.org/sites/default/files/InsomniaSeverityIndex_ISI.pdf. ↑
Zur Ermittlung Ihres Chronotyps hilft Ihnen der Morningness/Eveningness Questionnaire (MEQ) auf https://reference.medscape.com/calculator/829/morningness-eveningness-questionnaire-meq. ↑
Kalmbach et al. (2017) ↑
Der STOP-BANG-Fragebogen findet sich auf www.stopbang.ca/osa/screening.php. ↑
Hardeland (2013) ↑
Gradisar et al. (2013) ↑
Gradisar et al. (2013) ↑
Harding, Franks und Wisden (2020) ↑
Ebrahim et al. (2013) ↑
C. Smith und Smith (2003) ↑
Urry und Landolt (2015) ↑
IOM (2001) ↑
Maurer et al. (2021) ↑
Dworak et al. (2007); Youngstedt et al. (2000) ↑
D. Kim et al. (2022) ↑
CDC (2022f) ↑
Friend (2003) ↑
Spillane et al. (2020) ↑
Stobbe (2021) ↑
CDC (2022a) ↑
Case und Deaton (2015) ↑
CDC (2022d) ↑
Case und Deaton (2015) ↑
Livingston (2019) ↑
Real (1998) ↑
Real (1999), S. 247 ↑
Wallace (2012), S. 12 f. ↑
Brooks (2016) ↑
Riis (1901) ↑
Asarnow et al. (2021); Linehan et al. (2006) ↑
Hagerhall (2008)
Eine aktualisierte Liste meiner Offenlegungen findet sich unter
https://peterattiamd.com/about/ unter der Überschrift »Disclosures«. ↑
Besuchen Sie uns auf
 |
 |
Bleiben Sie informiert!
 | Melden Sie sich jetzt für unseren Newsletter an und erhalten Sie monatlich Informationen zu unseren Neuerscheinungen sowie Neuigkeiten, Tipps und mehr. |

Lebe unbeschwert
Singer, Michael A.
9783843730631
272 Seiten
Der neue Bestseller von einem der wichtigsten spirituellen Lehrer weltweit
Die Menschen sind immer auf der Suche nach mehr Freude, Liebe, Inspiration und Sinn – doch wie kann man das Leben genießen, wenn man sich ständig Sorgen macht und darum kämpft, dass alles so läuft, wie man es haben will?
Der weltweit geachtete spirituelle Lehrer Michael A. Singer knüpft in seinem neuen Buch an seinen Bestseller Die Seele will frei sein an. Er ruft die wichtigsten Erkenntnisse in Erinnerung, und erforscht gemeinsam mit den Leser:innen, wie sich die Welt um uns herum bildet und wie wir sie wahrnehmen. Er zeigt anschaulich, wie wir Denkmuster durchbrechen und Blockaden auflösen, um so zu einem Zustand der Akzeptanz und des Loslassens zu gelangen, der unserem Selbst entspricht und uns unabhängig von äußeren Ereignissen werden lässt.

Kinderklinik Weißensee – Geteilte Träume
Blum, Antonia
9783843728744
512 Seiten
Der langersehnte vierte Band der Kinderklinik Weißensee
Berlin-Weißensee, 1948: Elisabeth "Lissi" Vogel kann es kaum erwarten, als Assistenzärztin an der Kinderklinik Weißensee endlich in die Fußstapfen ihrer Tante Marlene zu treten. Doch der Klinikdirektor schätzt die begabte, junge Frau wegen ihres steifen Beines, das von einer überstandenen Kinderlähmung herrührt, gering. Außerdem legt er ihr immer neue Steine in den Weg. Aber Lissi lässt sich so schnell nicht einschüchtern, genauso wie ihre Tante Marlene. Die musste in einer Nacht- und Nebelaktion nach West-Berlin fliehen und dort von Null anfangen. Als sich in Berlin Fälle von Kinderlähmung häufen, wird die frisch verliebte Lissi plötzlich mit ihrer größten Angst konfrontiert und verliert den Mut, für ihre kleinen Patienten und für den Mann ihres Herzens zu kämpfen.

In ewiger Freundschaft
Neuhaus, Nele
9783843726375
480 Seiten
Ein tödliches Geheimnis – in Blut geschrieben
Der neue Krimi von Nr.1-Bestsellerautorin Nele Neuhaus!
Eine Frau wird vermisst. Im Obergeschoss ihres Hauses in Bad Soden findet die Polizei den dementen Vater, verwirrt und dehydriert. Und in der Küche Spuren eines Blutbads. Die Ermittlungen führen Pia Sander und Oliver von Bodenstein zum renommierten Frankfurter Literaturverlag Winterscheid, wo die Vermisste Programmleiterin war. Ihr wurde nach über dreißig Jahren gekündigt, woraufhin sie einen ihrer Autoren wegen Plagiats ans Messer lieferte – ein Skandal und vielleicht ein Mordmotiv? Als die Leiche der Frau gefunden wird und ein weiterer Mord geschieht, stoßen Pia und Bodenstein auf ein gut gehütetes Geheimnis. Beide Opfer kannten es. Das war ihr Todesurteil. Wer muss als nächstes sterben? Pia und Bodenstein jagen einen Täter, der ihnen immer einen Schritt voraus zu sein scheint ...

Wer länger liest, ist später tot
Auerbach & Auerbach
9783843730808
Lesen oder sterben, das ist hier die Frage
Pippa hütet ein einsam an der englischen Südküste gelegenes Bücherhaus, in dem ein Lesefest abgehalten werden soll. Doch die dafür gebuchte Liebesromanautorin Julia Timmings wird überfallen und schwer misshandelt. Für sie springt ihr Ex-Mann und Thrillerautor Jem ein, der aufgrund seiner Hardboiled-Bücher als gewaltaffin eingestuft wird. Bald gibt es erste Gerüchte: Hat er Julia aus dem Weg geräumt, um selbst auf dem beliebten Fest lesen zu können? Er avanciert zum Tatverdächtigen, doch Pippa Bolle ahnt, dass der Fall nicht so einfach zu lösen ist.
Liest du noch, oder stirbst du schon?
Ihr könnt von Pippa Bolle nicht genug bekommen?
Fall 1: Unter allen Beeten ist Ruh
Fall 2: Dinner for one, Murder for two
Fall 3: Tote Fische beißen nicht
Fall 4: Ins Gras gebissen
Fall 5: Tote trinken keinen Whisky
Fall 6: Des Katers Kern
Fall 7: Tödlicher Bienenstich
Fall 8: Viele Erben verderben das Sterben

Blutmond
Nesbø, Jo
9783843728775
544 Seiten
Harry Hole – unerbittlich wie nie.
Harry Hole hat alle Brücken hinter sich abgebrochen. In Los Angeles trinkt er sich als einer der zahllosen Obdachlosen fast zu Tode. Hin und wieder hilft er Lucille, einer älteren Filmdiva, die einem Drogenkartell eine Million Dollar schuldet.
Zur gleichen Zeit werden in Oslo zwei Mädchen ermordet. Beide feierten auf der Yacht eines stadtbekannten Immobilienmaklers. Kommissarin Katrine Bratt fordert Harry Hole an, doch die Führungsetage der Polizei hat kein Interesse an dem Spezialisten für Mordserien. Der Makler hat weniger Skrupel und bietet Hole als privatem Ermittler ein Vermögen, um seinen Ruf zu schützen.
Hole willigt ein, denn er sieht eine Chance, Lucille freizukaufen, und sucht sich ein Team, bestehend aus einem Kokain-dealendem Schulfreund, einem korrupten Polizisten und einem schwer an Krebs erkrankten Psychologen. Die Zeit läuft, während über Oslo ein Blutmond aufzieht.
Der neue Bestseller aus Skandinavien, der Sie zum Schaudern bringt.
Settings
Theme
Ask about this document
Ask anything about this document.

